Биология / Физиология растений / Фотосинтез. Физиология растений фотосинтез
Физиология растений. Фотосинтез
Фотосинтез – это процесс трансформации поглощенной растением электромагнитной энергии солнечного света в химическую энергию органических соединений. Чтобы свет мог быть использованным в процессе фотосинтеза, необходимо его поглощение фоторецепторами – пигментами. Пигменты
Хлорофиллы
У всех высших растений, водорослей и цианобактерий содержится хлорофилл a, хлорофилл b имеется у высших растений и зеленых водорослей. Хлорофилл с, лишенный фитола, содержится в бурых и диатомовых водорослях, хлорофилл d – в красных водорослях. Фотосинтезирующие зеленые бактерии имеют бактериохлорофиллы c и d, пурпурные бактерии – бактериохлорофиллы a и b.
У хлорофилла а четыре пиррольных кольца соединены между собой метиновыми мостиками (=СН-), образуя порфириновое кольцо. Кроме того, атомы азота пиррольных колец связаны с атомом магния. С порфириновым ядром соединено циклопентановое кольцо, образованное остатком кетопропионовой кислоты и содержащее активные карбонильную (С=О) и метилированную карбоксильную (О=С-О-СН3) группы. Структура, состоящая из порфиринового ядра и циклопентанового кольца, называется форбином. Боковая цепь, состоящая из пропионовой кислоты и непредельного спирта фитола, связана с атомом углерода IV пиррольного кольца. Хлорофилл, лишенный фитола, называется хлорофиллидом. Если атом магния замещен протоном, то такое соединение носит название феофитина. Активность хлорофиллов, также как и других пигментов, обусловлена наличием большого количества двойных связей с делокализованными электронами.
Хлорофиллы хорошо растворимы в органических растворителях (этиловом эфире, бензоле, хлороформе, ацетоне, этиловом спирте) и нерастворимы в воде. Хлорофиллы имеют максимумы поглощения света в красной и синей частях спектра. Растворы хлорофиллов обладают флуоресценцией и фосфоресценцией.
Каротиноиды
Каротиноиды – жирорастворимые пигменты, присутствующие в хлоропластах всех растений. Они входят в состав хромопластов в незеленых частях растений, например, корнеплодов моркови. К каротиноидам относят 3 группы соединений: 1) оранжевые или красные каротины, 2) желтые ксантофиллы, 3) каротиноидные кислоты. Каротины и ксантофиллы состоят из 8 остатков изопрена, которые образуют цепь конъюгированных двойных связей. Основные каротиноиды – b-каротин, лютеин, виолаксантин и неоксантин.
Каротины и ксантофиллы растворимы в хлороформе, бензоле, сероуглероде, ацетоне. Каротины хорошо растворяются в эфирах, но плохо в спиртах, а ксантофиллы наоборот. Каротиноиды имеют максимумы поглощения в фиолетово-синей и синей частях спектра света. Они не способны к флуоресценции.
Главные функции каротиноидов: поглощение света в качестве дополнительных пигментов, защита молекул хлорофиллов от необратимого фотоокисления, тушение активных радикалов, участие в фототропизме, так как способствуют определению направления роста побега.
Фикобилины
Сине-зеленые и красные водоросли помимо хлорофилла а и каротиноидов содержат пигменты фикобилины. Их молекула состоит из 4 последовательных пиррольных колец. Фикобилины являются хромофорными группами глобулиновых белков фикобилипротеинов. Они делятся на 3 группы: 1) фикоэритрины – белки красного цвета, 2) фикоцианины – сине-голубые белки и 3) аллофикоцианины – синие белки. Все они обладают флуоресценцией и растворимы в воде.
Фикобилины имеют максимумы поглощения в оранжевой, желтой и зеленой частях спектра света. Это позволяет водорослям полнее использовать свет, проникающий в воду. Вода обладает светопоглощающей способностью. На глубине около 30 м полностью исчезают красные лучи, около 180 м – желтые, 320 м – зеленые, а на глубину более 500 м не проникают синие и фиолетовые лучи. Фикобилины – это дополнительные пигменты, участвующие в светособирающем комплексе. Около 90 % энергии света, поглощенного фикобилинами, передается на хлорофилл а.
У растений имеется фикобилин фитохром. Он не участвует в фотосинтезе, но является фоторецептором красного и дальнего красного света и выполняет регуляторные функции в клетках растений.
Световая фаза фотосинтеза
Фотосинтез имеет две фазы – световую и темновую. В световой фазе молекулы пигментов поглощают фотоны, передают поглощенную энергию молекулам хлорофилла а, происходит трансформация энергии света в химическую энергию АТФ и восстановленного НАДФН, выделяется кислород в результате фоторазложения воды. Все эти процессы происходят на мембранах хлоропластов. При темновой фазе фотосинтеза в строме хлоропластов восстанавливается поглощенный СО2 с образованием углеводов и других органических соединений.
Поглощение света и возбуждение хлорофилла
Электрон представляет собой заряженную частицу, которая движется по орбите вокруг ядра атома. Электрон обладает вектором магнитного момента – спином, который отражает направление вращения электрона вокруг своей оси. В стабильном состоянии валентные электроны занимают самые низкие энергетические уровни и распределены по ним согласно принципу Паули: два электрона с антипараллельными спинами на каждой орбитали. Такое состояние молекулы называют основным синглетным состоянием S0. При поглощении молекулой пигмента фотона электрон переходит на более высокую орбиталь за счет энергии фотона. Если у возбужденного электрона сохраняется направление спина, то считают, что молекула находится в синглетном возбужденном состоянии S*. Если возбужденный электрон меняет спин, то такое возбужденное состояние называется триплетным Т*.
Поглощение молекулой хлорофилла кванта красного света приводит к синглетному возбужденному состоянию S*1. При поглощении кванта синего цвета с более высоким уровнем энергии электрон переходит на более высокую орбиталь S*2. Время жизни электрона на S*2 составляет не более 10-12 секунды. За такое короткое время энергия электронного возбуждения не может быть использована и электрон возвращается на S*1, потеряв немного энергии в виде тепла. Время жизни электрона в состоянии S*1 равно 10-9. Если молекула пигмента не участвует в фотохимической реакции, то электрон возвращается в стабильное состояние. При этом часть энергии теряется в виде тепла и излучается квант света с большей по сравнению с поглощенным фотоном длиной волны – явление флуоресценции.
Время жизни электрона в состоянии Т* равно 10-4-10-2 секунды. Из триплетного возбужденного состояния молекула может вернуться в стабильное состояние, излучив кроме тепла еще более длинноволновый, чем при флуоресценции, квант света. Это слабое свечение называют фосфоресценцией. Если молекула в возбужденном состоянии участвует в фотохимических реакциях с передачей электрона акцептору, то флуоресценции и фосфоресценции не происходит.
Для более полного использования падающего на листья света энергия фотонов улавливается 200-400 молекулами пигментов светособирающего (антенного) комплекса и передается к одной молекуле хлорофилла а, являющейся реакционным центром, которая и участвует в фотохимических реакциях. Передача энергии молекулами пигментов происходит по принципу индуктивного резонанса. Молекула пигмента, поглотившая фотон, создает переменное электрическое поле, которое усиливает колебания электрона в соседней молекуле. Это происходит из-за перекрытия частот колебаний и очень маленького расстояния между молекулами пигментов. Тем более, что при освещении листьев тилакоиды и граны сдвигаются и уплотняются, поэтому хлоропласты уменьшаются в объеме. Передача энергии молекулами пигментов идет с большой эффективностью. Так, от хлорофилла b к хлорофиллу а передается примерно 90 %, а от каротиноидов к хлорофиллу а – 40 % поглощенной энергии.
Совокупность молекул светособирающего комплекса и реакционного центра составляет фотосистему. Предположение о существовании в хлоропластах двух фотосистем высказал Р. Эмерсон в 1957 г, изучая влияние света на квантовый выход фотосинтеза у водоросли хлореллы. Квантовый выход фотосинтеза – это количество выделившегося кислорода или связанного углекислого газа на 1 квант поглощенной энергии. Он установил, что при одновременном освещении хлореллы коротковолновым (650 нм) и длинноволновым (700 нм) красным светом эффект выше, чем суммарный квантовый выход при воздействии красным светом этих длин в отдельности. Это явление получило название эффекта усиления Эмерсона. Позже предположение Р. Эмерсона о наличии двух фотосистем получило экспериментальное подтверждение.
Нециклический и циклический транспорт электронов
В фотосистеме II реакционный центр, состоящий из димера хлорофилла а с максимумом поглощения при 680 нм (П680), последовательно поглотив энергию, равную 2 квантам коротковолнового красного света, и перейдя в синглетное возбужденное состояние, передает 2 электрона феофитину. От феофитина электроны последовательно передаются на пластохиноны QA и QB, расположенные на другой стороне мембраны тилакоида, затем на две липидорастворимые молекулы пластохинона PQ. Он является переносчиком протонов и электронов, выполняющего в мембране роль челнока. Принимая 2 электрона и захватывая из стромы 2 Н+, 2 молекулы PQh3 диффундируют через липидную фазу мембраны. Электроны от 2 PQh3 поступают в цепь: железосерный белок FeSr® цитохром f ® Cu-содержащий белок пластоцианин ® П700, а протоны попадают в полость тилакоида.
Вакантные места в П+680 заполняются 2 электронами из содержащего Mn переносчика электронов, который восстанавливается с участием белкового комплекса S. Окисленный комплекс S связывает воду и восстанавливается за счет электронов воды. При фотоокислении воды комплексом S вторая пара протонов освобождается в полость тилакоида, а атом кислорода диффундирует из хлоропласта.
После возбуждения реакционного центра фотосистемы I – молекулы хлорофилла а с максимумом поглощения при 700 нм (П700), 2 квантами длинноволного красного света 2 электрона передаются мономерной форме хлорофилла а – А1 и затем переносчикам электронoв железосерным белкам А2 и АВ, ферредоксину на наружной стороне мембраны тилакоида, НАДФ-редуктазе. Этот фермент восстанавливает НАДФ в НАДФН. На вакантные места в П+700 переходят электроны с пластоцианина и нециклическая цепь транспорта электронов замыкается.
В мембранах хлоропластов может функционировать циклический транспорт электронов, когда действует только фотосистема I. Возбужденные молекулы П700 передают электроны на А1, железосерные белки А2 и АВ, переносящие электроны на другую сторону мембраны, ферредоксин, пластохинон, цитохром b6, железосерный белок FeSr, цитохром f, пластоцианин и П700. Энергия, освобождающаяся при транспорте электронов, используется для фосфорилирования АДФ.
Механизм фотофосфорилирования АДФ объясняет теория П. Митчелла. Согласно этой теории, трансмембранный перенос пластохинонами электронов и протонов в одну сторону чередуется с переносом цитохромной системой в обратную сторону электронов. Поэтому по одну сторону мембраны накапливается избыток протонов и возникает электрохимический мембранный потенциал. Его энергия используется для синтеза АТФ при разрядке мембраны в результате транспорта протонов через мембрану посредством Н+-АТФазы, которая действует как АТФсинтетаза. Этот фермент выглядит как грибовидная частица на поверхности мембраны тилакоидов. Его молекула состоит из двух частей: головки, выступающей с наружной стороны мембраны и содержащей активный центр фермента, и ножки, погруженной в мембрану и представляющей канал, через который передвигаются протоны.
Темновая фаза фотосинтеза
С3-путь фотосинтеза или цикл Кальвина
Этот путь ассимиляции СО2 обнаружен у всех фотосинтезирующих растений. Он был назван циклом Кальвина в честь американского биохимика М. Кальвина, который с сотрудниками открыл и изучил его в 1946-1956 годах с помощью метода меченых атомов и хроматографии. Растения разное время подкармливали 14СО2 и хроматографировали экстракты. Радиоактивные изотопы по химическим свойствам не отличаются от стабильных. Принимая участие в реакциях, они помечают те соединения, в которые входят. Цикл состоит из трех этапов: карбоксилирования, восстановления, регенерации первичного акцептора СО2 и синтеза конечного продукта фотосинтеза.
1 – фосфорибулокиназа, 2 – рибулозодифосфаткарбоксилаза, 3 – фофсфоглицераткиназа, 4 – триозофосфатдегидрогеназа, 5 – триозофосфатизомераза, 6 – альдолаза, 7 – фосфатаза, 8 – транскетолаза, 9 – альдолаза, 10 – фосфатаза, 11 – транскетолаза, 12 – рибозофосфатизомераза, 13 – фосфокетопентоэпимераза (по В. В. Полевому).
1. Карбоксилирование. Фосфорибулокиназа фосфорилирует при участии АТФ рибулозо-5-фосфат с образованием АДФ и рибулозо-1,5-дифосфата. Последний является акцептором СО2 и под действием рибулозодифосфаткарбоксилазы присоединяет СО2. В результате образуются 2 молекулы 3-фосфоглицериновой кислоты (3-ФГК).
2. Восстановление. Фосфоглицераткиназа при участии АТФ фосфорилирует 3-ФГК и образовавшаяся 1,3-дифосфоглицериновая кислота восстанавливается с помощью НАДФН и дегидрогеназы фосфоглицеринового альдегида до 3-фосфоглицеринового альдегида (3-ФГА).
3. Регенерация. После фиксации трех молекул СО2 и образования шести молекул 3-ФГА пять из них используются для синтеза рибулозо-5-фосфата, а одна молекула 3-ФГА – для образования глюкозы.
Триозофосфатизомераза превращает 3-ФГА в фосфодиоксиацетон. Затем альдолаза образует из 3-ФГА и фосфодиоксиацетона фруктозо-1,6-дифосфат. Он теряет один остаток фосфорной кислоты под влиянием фруктозо-1,6-дифосфатазы и превращается во фруктозо-6-фосфат. Транскетолаза переносит гликолевый альдегид от фруктозо-6-фосфата на 3-ФГА с образованием эритрозо-4-фосфата и ксилулозо-5-фосфата. Альдолаза присоединяет фосфодиоксиацетон к эритрозо-4-фосфату с образованием седогептулозо-1,7-дифосфата. Он дефосфорилируется фосфатазой и под влиянием транскетолазы соединяется с 3-ФГА. Продуктами этой реакции являются ксилулозо-5-фосфат и рибозо-5-фосфат. Две молекулы ксилулозо-5-фосфата при участии рибулозофосфатэпимеразы и одна молекула рибозо-5-фосфата под действием рибозофосфатизомеразы превращаются в три молекулы рибулозо-5-фосфата.
Шестая молекула 3-ФГА используется для синтеза фруктозо-1,6-дифосфата при повторении цикла. Из двух молекул фруктозо-1,6-дифосфата образуются фруктозо-6-фосфат и глюкозо-1-фосфат. Последний, взаимодействуя с уридинтрифосфатом, дает уридинфосфоглюкозу. Она и фруктозо-6-фосфат образуют сахарозофосфат, который после дефосфорилирования превращается в сахарозу. Следовательно, для образования одной молекулы сахарозы необходимо прохождение четырех циклов Кальвина. Крахмал синтезируется из уридинфосфоглюкозы под влиянием амилосинтетазы.
Среди продуктов фотосинтеза обнаружены аминокислоты. При недостатке НАДФН 3-ФГК превращается не в 3-ФГА, а в пировиноградную кислоту. Она, присоединяя аммиак, образует аланин. Из пировиноградной кислоты в цикле Кребса образуются органические кислоты, которые в ходе реакций аминирования и переаминирования дают аминокислоты.
С4-путь фотосинтеза или цикл Хетча-Слэка
Австралийскими учеными М. Хетчем и К. Слэком был описан С4-путь фотосинтеза, характерный для тропических и субтропических растений (сахарный тростник, кукуруза и др.). Листья этих растений содержат хлоропласты двух типов: обычные в клетках мезофилла и крупные хлоропласты, не имеющие гран и фотосистемы II, в клетках обкладки, окружающих проводящие пучки.
В цитоплазме клеток мезофилла фосфоэнолпируваткарбоксилаза присоединяет СО2 к фосфоэнолпировиноградной кислоте, образуя щавелевоуксусную кислоту. Она транспортируется в хлоропласты, где восстанавливается до яблочной кислоты при участии НАДФН. В присутствии ионов аммония щавелевоуксусная кислота превращается в аспарагиновую кислоту. Яблочная и (или) аспарагиновая кислоты переходят в хлоропласты клеток обкладки, декарбоксилируются до пировиноградной кислоты и СО2. СО2 включается в цикл Кальвина, а пировиноградная кислота переносится в клетки мезофилла, где превращается в фосфоэнолпировиноградную кислоту. Такой механизм позволяет растениям фотосинтезировать при закрытых из-за высокой температуры устьицах. Кроме того, продукты цикла Кальвина образуются в хлоропластах клеток обкладки, окружающих проводящие пучки. Это способствует быстрому оттоку фотоассимилятов и тем самым повышает интенсивность фотосинтеза.
КС – клеточная стенка (по В. В. Полевому).
Фотосинтез по типу толстянковых (суккулентов)
У суккулентов (кактусов и растений сем. толстянковых (Crassulaceae) процессы фотосинтеза разделены не в пространстве, как у других С4-растений, а во времени. Этот тип фотосинтеза получил название CAM (crassulation acid metabolism)-путь. Устьица днем обычно закрыты, что предотвращает потерю воды в ходе транспирации, и открыты ночью. В темноте СО2 поступает в листья, где фосфоэнолпируваткарбоксилаза присоединяет его к фосфоэнолпировиноградной кислоте, образуя щавелевоуксусную кислоту. Она восстанавливается НАДФН-зависимой малатдегидрогеназой до яблочной кислоты, которая накапливается в вакуолях. Днем яблочная кислота переходит из вакуоли в цитоплазму, где декарбоксилируется с образованием СО2 и пировиноградной кислоты. СО2 диффундирует в хлоропласты и включается в цикл Кальвина.
Фотодыхание
Фотодыхание – это активируемый светом процесс выделения СО2 и поглощения О2. Так как первичным продуктом фотодыхания является гликолевая кислота, оно еще называется гликолатным путем. Фотодыхание усиливается при низком содержании СО2 и высокой концентрации О2 в воздухе. В этих условиях рибулозодисфаткарбоксилаза хлоропластов катализирует не карбоксилирование рибулозо-1,5-дифосфата, а его расщепление на 3-фосфоглицериновую и 2-фосфогликолевую кислоты. Последняя дефосфорилируется с образованием гликолевой кислоты.
Гликолевая кислота из хлоропласта переходит в пероксисому, где окисляется гликолатоксидазой до глиоксиловой кислоты. Образующаяся при этом перекись водорода разлагается каталазой, присутствующей в пероксисоме. Глиоксиловая кислота аминируется, превращаясь в глицин. Глицин транспортируется в митохондрию, где из двух молекул глицина синтезируется серин и освобождается СО2.
Серин может поступать в пероксисому и под действием аминотрансферазы передает аминогруппу на пировиноградную кислоту с образованием аланина, а сам превращается в гидроксипировиноградную кислоту. Последняя при участии НАДФН восстанавливается в глицериновую кислоту. Она переходит в хлоропласты, где включается в цикл Кальвина.
У растений С4-типа выделяющийся при фотодыхании углекислый газ реагирует в клетках мезофилла с фосфоэнолпировиноградной кислотой с образованием щавелевоуксусной и яблочной кислот. Яблочная кислота переходит в клетки обкладки, где служит донором СО2.
Влияние внутренних и внешних факторов на фотосинтез
Фотосинтез осуществляется в полуавтономных органеллах – хлоропластах. Однако он в значительной мере контролируется процессами, происходящими в растении, и факторами внешней среды.
Отток ассимилятов. Накопление фотоассимилятов в хлоропластах и в околопластидном пространстве приводит к ингибированию ферментов, участвующих в фотосинтезе.
Содержание хлорофилла. С увеличением содержания в клетке хлорофилла увеличивается интенсивность фотосинтеза.
Возраст листа и растения. В ходе роста листа интенсивность фотосинтеза увеличивается. После окончания роста листа она постепенно снижается. У многих однолетних растений интенсивность фотосинтеза достигает максимума в фазу бутонизации и цветения, а затем снижается.
Свет. Имеется нижний порог освещенности, при котором растения начинают фотосинтезировать. Затем зависимость интенсивности фотосинтеза от освещенности имеет логарифмический характер с последующим выходом на плато. Угол наклона кривой зависимости интенсивности фотосинтеза от освещенности зависит от влияния других факторов. Так, у светолюбивых растений она выходит на плато при значительно более высокой освещенности, чем у теневыносливых растений. Уровень освещения, при котором поглощение СО2 в ходе фотосинтеза равно выделению СО2 в процессе дыхания, называется компенсационным пунктом.
Важен и спектральный состав света. При освещении красным светом образуются преимущественно углеводы, синим – амино- и органические кислоты.
Температура. При низкой освещенности фотосинтез идет с одинаковой скоростью при 15 и 25оС. Это объясняется тем, что при низкой освещенности интенсивность фотосинтеза зависит от скорости световых реакций. При высокой освещенности интенсивность фотосинтеза лимитируется скоростью темновых реакций и Q10 примерно равен 2. Для большинства растения С3-типа оптимальная температура 20-25оС, для растений С4-типа она равна 25-40оС. При температуре выше оптимальной интенсивность фотосинтеза снижается из-за инактивации хлоропластов и закрытия устьиц.
Содержание СО2 в воздухе. Повышение содержания СО2 с 0,03 % до 0,3 % вызывает увеличение интенсивности фотосинтеза. Дальнейшее возрастание концентрации СО2 до 1 % не сказывается на фотосинтезе, но более высокий уровень СО2 в воздухе приводит к депрессии фотосинтеза. Высокие концентрации СО2 особенно неблагоприятны при высокой освещенности, так как происходит ингибирование темновых реакций. Влияние содержания углекислого газа на фотосинтез зависит от вида растения.
Снабжение водой. При большом водном дефиците интенсивность фотосинтеза снижается из-за закрытия устьиц, что уменьшает поступление СО2 в листья, снижает транспирацию и приводит к повышению температуры листа. Кроме того, обезвоживание изменяет конформацию и, следовательно, активность ферментов.
Содержание кислорода в воздухе, в среднем, равно 21 %. Повышение концентрации или отсутствие кислорода для фотосинтеза неблагоприятны. Кислород снижает активность рибулозодифосфаткарбоксилазы.
Минеральное питание. Исключение любого элемента минерального питания отрицательно сказывается на фотосинтезе. Особенно важны такие элементы как фосфор, магний, железо, марганец, медь, калий и азот. На всех этапах фотосинтеза участвуют фосфорилированные соединения. Калий активирует процессы фосфорилирования и участвует в открывании устьиц. Магний входит в состав хлорофиллов, активирует реакции карбоксилирования и восстановления НАДФ. Железо необходимо для синтеза хлорофиллов. Марганец участвует в фоторазложении воды. Медь входит в состав пластоцианина. Азот необходим для формирования хлоропластов и образования пигментов.
Значение фотосинтезирующих организмов для биосферы
Выделяют пять основных аспектов планетарной роли фотосинтезирующих организмов.
Накопление органической массы. В процессе фотосинтеза наземные растения образуют до 170 млрд. тонн, а растения мирового океана – до 70 млрд. тонн биомассы в год в пересчете на сухое вещество, используемой гетеротрофными организмами.
Обеспечение постоянства содержания СО2 в воздухе. Связывание СО2 в ходе фотосинтеза в значительной мере компенсирует его выделение в результате других процессов (дыхание, брожение, деятельность вулканов, производственная деятельность человечества).
Препятствие развитию парникового эффекта. Часть солнечного света отражается от поверхности Земли в виде тепловых инфракрасных лучей. СО2 поглощает инфракрасное излучение и тем самым сохраняет тепло на Земле. Повышение содержания СО2 в атмосфере может способствовать увеличению температуры, то есть создавать парниковый эффект. Это приведет к затоплению прибрежных зон из-за поднятия уровня мирового океана в результате таяния ледников в горах и на полюсах. Однако высокое содержание СО2 в воздухе активирует фотосинтез и, следовательно, концентрация СО2 в воздухе опять уменьшится.
Накопление кислорода в атмосфере. Первоначально в атмосфере Земли кислорода было очень мало. Сейчас его содержание составляет 21 % по объему воздуха. В основном, этот кислород является продуктом фотосинтеза. Ежегодно растения и другие фотосинтезирующие организмы поставляют в атмосферу примерно 120 млрд. тонн кислорода.
Озоновый экран. Озон (О3) образуется в результате фотодиссоциации молекул кислорода под действием солнечной радиации на высоте около 25 км. Озон задерживает большую часть ультрафиолетовых лучей, губительных для всего живого.
irk-florist.ru
Фотосинтез растений
Фотосинтез
Процесс образования органических веществ из неорганических элементов и соединений окружающей среды при участии света и хлорофилла называется фотосинтезом.
Фотосинтез может осуществляться высшими растениями, водорослями и некоторыми бактериями.
Началом экспериментального открытия фотосинтеза принято считать 1771г. и связывают его с именем английского ученого Дж. Пристли, который провел большое количество опытов с целью изучения условий, при которых воздух, «испорченный» горением или жизнедеятельностью животных, обновляет свои первоначальные свойства. Успех был достигнут после выращивания под стеклянным колпаком зеленых растений.
В 1779 году английский врач Я. Ингенхауз установил связь между светом и способностью растений обновлять (очищать) воздух, а в 1782г. произошло новое открытие швейцарца Ж. Сенебье, который констатировал выделение кислорода растением только при поглощении им углекислого газа. Великий вклад в теорию фотосинтеза внес в 1875г. К. А. Тимирязев, который обоснованно развил учение о космической роли растений как посредников между Солнцем и жизнью нашей планеты, довел, что процесс фотосинтеза подчиняется первому закону термодинамики - закону сохранения и преобразования энергии.
Общую формулу фотосинтеза принято изображать уравнением:
6 СО2 + 6 Н2О -------------- С6Н12О6 + 6 О2 (на свету и в хлоропластах при наличии хлорофилла)
Количество органического вещества, которое образуется ежегодно в процессе фотосинтеза, составляет приблизительно 200 млрд. тонн. Оно также является основой питания всех гетеротрофных организмов, а также основным источником органических ресурсов на Земле. 95% энергетических потребностей человечество обеспечивает за счет сжигания продуктов фотосинтеза (уголь, газ, нефть, лес) и только 5% - за счет энергии гидро – и атомных электростанций.
Благодаря побочному продукту фотосинтеза – кислорода - обеспечивается дыхание живых организмов, формирование озонового слоя атмосферы, который защищает весь растительный и животный мир от губительного жестокого космического излучения.
ФИЗИКО-ХИМИЧЕСКАЯ СУЩНОСТЬ
Вопрос о природе основных реакций фотосинтеза имеет большое значение не только для познавания сути этого процесса, но и для выяснения его зависимости от внешних и внутренних факторов, изучения путей управления им, а также и продуктивностью растений.
Процессы фотосинтеза подчинены 3 основным принципам фотохимии: химическое изменение может быть вызвано только поглощенным светом.
2. каждый поглощенный фотон активизирует только 1 молекулу, 3. вся энергия поглощенного кванта передается только 1 электрону, который вследствие чего переходит на более высокий энергетический уровень. В результате чего, фотохимический эффект пропорционален количеству поглощенной энергии.
Продуктивность фотохимического процесса определяется числом квантов.
В процессах фотосинтеза роль фотосенсибилизатора, т. е вещества, которое поглощает свет, играет хлорофилл. Поглотивши свет, он приобретает качества активного окислителя, способного окислять некоторые вещества путем отсоединения электронов или Н+.
ЛИСТ, КАК ОРГАН ФОТОСИНТЕЗА
Лист является наиважнейшим фотосинтетическим органом высших зеленых растений. Именно этой функции, а также газообмену и транспирации подчинено его морфологическое и анатомическое строение. Пластинка листа имеет дорсовентральное строение, и поэтому ее поверхность больше, чем объем. Благодаря этому обстоятельству лист отличается высокой интенсивностью газообмена. Этому способствуют также многочисленные устьица, система дыхательных пространств и межклетников.
Мезофилл листа состоит из 2 типов основной ткани.
Под верхним эпидермисом располагается палисадная ткань, которую образуют длинные цилиндрические клетки, размещенные перпендикулярно к поверхности листа. Эти клетки плотно прилегают одна к другой и содержат большое количество хлоропластов. Нижняя часть мезофилла имеет другое строение и называется губчатой паренхимой. Эта рыхлая ткань с клетками разной формы, между которыми находится много воздушных пустот над многочисленными устьицами в нижнем эпидермисе.
Палисадные клетки содержат большую часть общего количества хлоропластов и делают основной взнос в процесс ассимиляции углекислого газа, который поступает в фотоминтезирующие клетки через устьица путем диффузии по градиенту концентрации.
Транспортную роль в листовой пластинке выполняет система из многочисленных жилок. Движение веществ в листу происходит по ксилеме и флоэме.
ПЕРВИЧНЫЕ ПРОЦЕССЫ ФОТОСИНТЕЗА. СВЕТОВАЯ СТАДИЯ
Система первичных процессов световой фазы фотосинтеза состоит из 4 последовательных этапов: 1). Поглощение квантов света молекулой пигмента и ее возбуждение, 2). Энергия возбужденного электрона молекулы пигмента рассылается при флюоресценции или мигрирует к другой молекуле хлорофилла, 3). Возбужденная молекула передает 1 из электронов на первичный акцептор и переходит в окисленное состояние, 4). Переданный электрон движется по электротранспортной цепи, отдавая энергию для синтеза АТФ.
Для понятия механизмов поглощения кванта света молекулой пигмента и последующей трансформации энергии необходимо знакомство со строением молекулы и физико-химическими свойствами фотосинтетических пигментов.
ФОТОСИНТЕТИЧЕСКИЕ ПИГМЕНТЫ
Изучение физико-химических свойств пигментов началось в 19в. Ж. Пельтье и Ж. Каванту в 1818г. получили из листьев спиртовой раствор растительных пигментов и назвали его хлорофиллом.
М. С Цвет (1901-1903), используя хроматографический метод анализа, разделили смесь пигментов на хлорофил а и в и каратиноиды. В растениях могут быть фотосинтетические пигменты 3 групп: хлорофиллы, фикобилины, каратиноиды.
У большинства растений хлорофилл существует в 2 формах: сине-зеленый хлорофилл (а) и желто-зеленый хлорофилл (в). Основой структуры молекулы хлорофилла является магниевый комплекс порфириного ядра.
Спектры поглощения хлорофиллов а и в имеют 2 четких максимума : в красной части спектра - 660 и 640нм, сине-фиолетовый -430-450нм. Возбужденные под влиянием света молекулы хлорофиллов после прекращения его действия возвращаются в исходное состояние. Этот переход сопровождается потерей энергии в виде излучения света – флуоресценция.
В растительных клетках хлорофилл содержится в хлоропластах. В них постоянно происходит распад старых и синтез новых молекул хлорофилла.
Главное условие образования хлорофилла - наличие света и хлоропластов, способных к позеленению. Хлоропласт формируется, растет, стареет и отмирает. При старении листьев они меняют окраску желтого цвета от наличия в них каратиноидов.
КСАНТОФИЛЛЫ – это каратиноиды, содержащие кислород. Они поглощают свет в сине-фиолетовой части спектра.
КАРАТИНОИДЫ играют роль вспомогательных пигментов. Они передают энергию поглощенных квантов молекулам хлорофилла и этим способствуют более полному использованию солнечной энергии видимой части спектра света, которую не поглощает хлорофилл.
ФИКОБИЛИНЫ - пигменты красных и сине-зеленых водорослей. К ним относятся: фикоциан и фикоэритрин.
Флавоноиды это водорастворимые растительные пигменты. Размещаются в вакуолях, но могут встречаться и в хромопластах и хлоропластах. Их подразделяют на антоцианы, флавоны, флавоноли. Антоцианы содержит – свекла столовая, капуста краснокочанная. Другие 2 группы окрашивают клеточный сок растений в желтую окраску.
На фоне хлорофилла они незаметны (только осенью их видно при изменении окраски). Они стабилизируют процесс фотосинтеза, защищая хлорофилл от самоокисления. Растения растут и в темноте (этиолированные побеги – бледно-зеленой окраски).
Хлороз – разрушение хлорофилла в зеленом растении (железный хлороз).
Суть световой стадии фотосинтеза состоит в преобразовании энергии квантов света в энергию химических лабильных высокореактивных соединений – АТФ и НАДФ - Н2. Образование их происходит последовательно во время фотофизического и фотохимического этапов.
ФОТОФИЗИЧЕСКИЙ ЭТАП – это этап, на котором энергия светового излучения преобразуется в энергию возбужденного электрона молекулы хлорофилла реакционного центра (реакционный центр – группа молекул хлорофилла, которые преобразовывают энергию света в АТФ и НАДФ-Н2).
При ясной солнечной погоде молекула хлорофилла поглощает всего лишь 1 квант за 0,1 секунды, а при пасмурной погоде за более длительный период.
Эффективность фотофизического этапа определяется энергией кванта света, поглощенного молекулой хлорофилла реакционного центра. При поглощении света молекула переходит в возбужденное состояние, т. е. 1 из ее электронов попадает на более высокий энергетический уровень.
На фотохимическом этапе энергия возбужденного электрона преобразовывается в химическую связанную энергию соединений АТФ и НАДФ-Н2. Процесс происходит в такой последовательности:
А). ФОТОЛИЗ ВОДЫ – расщепление Н2О, индуктированное хлорофиллом, окисленным под действием света.
В).ФОТОСИНТЕТИЧЕСКОЕ ФОСФОРИЛЛИРОВАНИЕ – процесс образования высокоэнергетических соединений путем трансформации энергии электрона. Оно бывает 2 видов: циклическое и нециклическое.
ФОТОЛИЗ ВОДЫ – это реакция расщепления воды, которая наблюдается при осветлении хлоропластов. В ее осуществлении непосредственное участие принимает хлорофилл. Впервые выявлено Р. Хиллом в 1937г. При осветлении суспензий хлоропластов в присутствии акцептора электронов (А) выделяется кислород. Выделенный кислород является кислородом воды, а не СО2, как считали раньше.
ТЕМНОВАЯ СТАДИЯ
Образование углерода до углеводов происходит при помощи энергии АТФ и «обновляющей силы» - НАДФ-Н2, без прямого участия солнечного света и называется темновой стадией фотосинтеза.
ЦИКЛ КАЛЬВИНА. С3 – путь фотосинтеза
Эта стадия была подробно изучена в 1946-1956гг. американским биохимиком М. Кальвином и называется циклом Кальвина.
Первый этап состоит в присоединении СО2 к акцептору при участии фермента рибулозо- 1,5-бифосфаткарбоксилазы. В результате образуется нестойкая шестиуглеродное соединение, которая мгновенно гидролизуется дна 2 молекулы фосфоглицериновой кислоты (ФГК).
На 2 стадии темновой фазы при участии энергии АТР и «обновительной силы» - НАДФ-Н2 – образуется глюкоза, а именно: к каждой из 2 молекул ФГК при помощи фермента фосфоглицеринкиназы присоединяется по 1 остатку ортофосфорной кислоты, в результате чего, образуется дифосфоглицериновая кислота, которая под действием фермента дегидрогеназы и НАДФ-Н2 обновляется до фосфоглицеринового альдегида (ФГА). Фиксация СО2 происходит в пентозофосфатном цикле.
В цикле Кальвина происходит преобразование триоз, поэтому растения с таким циклом фотосинтеза, называются С3- растениями, а путь фотосинтеза – С3- путем. С3- способ ассимиляции СО2, который напоминает обратный пентозофосфатный цикл, конечным продуктом которого является глюкоза.
С3- растения – это наиболее распространенные растения в зоне умеренного климата, оптимальная дневная температура для фиксации СО2 у них составляет от 15 до 25 градусов.
ЦИКЛ ХЕТЧА-СЛЕКА. С4- путь фотосинтеза
Кроме фиксации СО2 в пентофозофосфатном цикле (цикл Кальвина), процесс карбоксилирования осуществляется и при взаимодействии углекислоты с монокарбоновыми кислотами путем образования дикарбоновых кислот.
При изучении кинетики и продуктов фотосинтеза у растений тропического происхождения (кукуруза, сорго, сахарный тростник) и растения тостолистных выявлен другой тип фиксации углекислого газа.
Установлено, что в хлоропластах клеток оболочки проводящих пучков в первую секунду осветления фиксация и преобразование СО2 осуществляются по циклу Кельвина с образованием триоз, а в хлоропластах мезофильной ткани первичными продуктами фотосинтеза являются четырехуглеродные соединения – малат и аспартат.
Этот тип фотосинтеза был изучен австралийскими учеными М. Д. ХЕТЧЕМ и К. Р. СЛЕКОМ и получил соответствующее название. Растения с таким типом фотосинтеза называются С4- растениями. Они распространены в засушливых местностях и в жарком климате (кукуруза, сорго, разные виды проса). Эти растения эффективнее используют высокую интенсивность осветления и более урожайные в засушливых условиях.
С4 –путь фотосинтеза включает в себя 2 реакции карбоксилирования, которые пространственно разделены.
Первая стадия карбоксилирования – заканчивается образованием яблочной или аспарагиновой кислоты (протекает в клетках мезофилла). Во время следующей стадии декарбоксилирования яблочная кислота разлагается на пировиноградную кислоту и СО2. Образованный СО2, вступает в карбоксилирование в цикле Кальвина.
Установлено, что световые и темновые реакции разделены во времени: сначала происходят световые реакции, а затем их продукты - АТФ и НАДФ-Н2 используются в светонезависимых биохимических реакциях преобразования СО2 в углеводы.
ЗАВИСИМОСТЬ ИНТЕНСИВНОСТИ ФОТОСИНТЕЗА ОТ ВНЕШНИХ УСЛОВИЙ
Интенсивность фотосинтеза – количество углекислоты, которое усваивается единицей листовой поверхности за единицу времени.
Фотосинтез возможен при минимальном осветлении. У большинства растений интенсивность фотосинтеза возрастает при увеличении осветления до1\3 полного солнечного света, после чего настает световое насыщение.
Зеленое растение имеет большую пластичность к интенсивности света.
Кроме интенсивности большое значение для фотосинтеза имеет спектральный состав света. Видимую часть солнечного спектра (380-720нм) принято относить до ФАР, которая состоит из прямого и рассеянного света.
Листья растений могут размещаться в пространстве так, чтобы использовать как прямой, так и рассеянный свет.
Скорость фотосинтеза на разных делянках спектра разная. Большая часть приходится на красную часть спектра. Утром преобладает рассеянный свет.
ЧИСТАЯ ПРОДУКТИВНОСТЬ ФОТОСИНТЕЗА – отношение прироста сухой массы растения в граммах за определенное время (сутки) к единице листовой поверхности (м2), определяется г\м2.
Продуктивность фотосинтеза зависит от факторов внешней среды:
Интенсивности и качественного состава света,
Концентрации углекислого газа и кислорода,
Температуры,
Водного режима тканей листа,
Минерального питания.
Листья растений поглощают в среднем 80-86% энергии ФАР (фотосинтетически активная радиация) и 25% инфракрасных лучей. На фотосинтез затрачивается от 1 до 3% поглощенной энергии.
Освещенность, при которой интенсивность достигает максимальной величины, у светолюбивых растений наступает от 10 до 40 тыс. люкс, у теневыносливых растений – при 1тыс. лк. Хлорофиллом поглощаются красные и синие лучи. Под влиянием синих лучей больше образуется аминокислот и белков, а красные лучи способствуют образованию и отложению углеводов.
Повышение интенсивности фотосинтеза в результате обогащения атмосферы СО2, приводит к увеличению общей и хозяйственной продуктивности растений. Органические удобрения способствуют увеличению количества СО2 в воздухе. При повышении температуры на 10градусов увеличивается в 2-3 раза скорость реакций.
po-teme.com.ua
фотосинтез, хлорофилл, хлоропласты и производительность растений — Сириус агро плант
ФОТОСИНТЕЗ
Фотосинтез является единственным механизмом получения энергии для биосферы (за исключением процессов, происходящих у некоторых хемосинтезирующих бактерий, которые получают энергию от окисления неорганических субстратов). Фотосинтез включает в себя окислительно-восстановительные реакции. В общем, в процессе окисления молекулы воды высвобождаются электроны с выделением кислорода и восстановлением диоксида углерода с образованием углеводов (Salisbury и Ross, 1994).
Фотосинтез важен для человека, среди прочего, потому что через него производится пища и кислород (Barcelo и др., 1983). Кроме того, он прямо или косвенно кормит почти весь живой мир на планете (Campbell и Reece, 2005).
Первые организмы-фотосинтезаторы, вероятно, появились 3 миллиарда или 3,5 миллиардов лет назад. По мере их распространения они устанавливали взаимозависимости и отношения, которые не только трансформировали их, но и изменили внешний облик планеты. Древние организмы жили в среде без свободного кислорода в атмосфере, в состав которой входил большой процент водорода. Кислород, даже был токсичным для этих примитивных организмов, так же, как в настоящее время для анаэробов. Энергия приобреталась такими процессами, как ферментация или гликолиз, что должно было привести к постепенному накоплению углекислого газа в ранней атмосфере. Если бы живые существа использовали сразу солнечную энергию, используя углекислый газ и выделяя кислород, они, безусловно, более эффективно использовали бы ресурсы своей окружающей среды, отметив веху в истории и эволюции жизни на планете. Условием фотосинтеза является поглощение фотонов, квантовых частиц определенными пигментами (Curtis и Barnes, 2001).
Фотосинтез представляет собой эндергонический процесс, потому что необходимо участие энергии солнечного излучения, чтобы начать цепные реакции, которые приводят к образованию органических соединений, которые накапливает организм.
Общая реакция фотосинтеза:

(Ch3O)n- это сокращенная форма представления крахмала или других углеводов по эмпирической формуле. Крахмал является наиболее распространенным продуктом фотосинтеза. Фотосинтез зависит от различных факторов окружающей среды, таких как интенсивность и качество освещения, влажность воздуха, температура, наличие воды, минеральных веществ и углекислого газа. Фотосинтез одного листа опирается на более, чем 50 индивидуальных реакций, каждая из которых зависят от параметров окружающей среды (Cogua, 2011).
Способность растений компенсировать воздействия окружающей среды зависит от их производительности и выживания в конкретной среде. Скорость фотосинтеза может измениться в течение следующих десятилетий в зависимости от приспособительных реакций к изменению уровней CO2, начиная от прямых реакций собственно на CO2, вплоть до косвенных реакций в связи с изменением температуры и водного режима, которые могут произойти в будущем (Cogua, 2011).
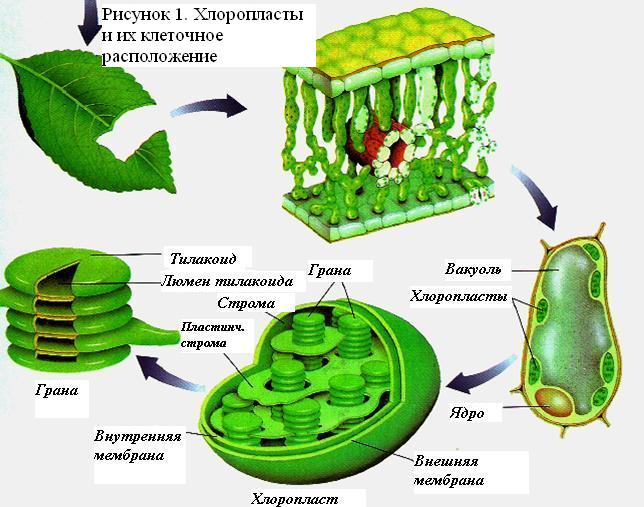
Хлоропласты
Клеточными органеллами, в которых происходит фотосинтез, являются хлоропласты.
Размер и форма хлоропластов изменчивы; они происходят из структур, известных как протопластиды (молодые хлоропласты), которые делятся по мере развития эмбриона. Хлоропласты окружены двойным набором мембран, контролирующих движение наружу и внутрь молекул. Внутренне они состоят из студенистого материала, богатого ферментами, называемого строма. Здесь происходит реакция превращения диоксида углерода в углеводы. Хлоропласты имеют пластинчатые мембраны и плоские закрытые «мешочки», похожие на пузырьки, называемые тилакоидами. Тилакоиды образуют стопки, называемые гранами, которые соединены между собой другими тилакоидами более вытянутой формы. В тилакоидных мембранах находятся хлорофиллы и другие пигменты, которые участвуют в поглощении света, ферменты для переноса электронов и фактор связи для образования АТФ (ATP). Основные пигменты, присутствующие в тилакоидных мембранах — хлорофилл a и хлорофилл b. В свою очередь, там найдены и другие пигменты, называемые каротинами и ксантофиллами (Salisbury и Росс, 1994).
Пигменты фотосинтеза
Чтобы световая энергия могла быть использована живыми существами, она должна быть поглощена фотосинтезирующими пигментами. Эти пигменты представляют собой вещества, способные поглощать свет на определенных длинах волн, например, хлорофилл – пигмент, который придает растениям характерный зеленый цвет, поглощает свет на длинах волн, соответствующих фиолетовому, синему и красному цвету, отражая зеленый цвет (Azcon и Talon, 1993).
Хлорофилл
Структура молекулы хлорофилла
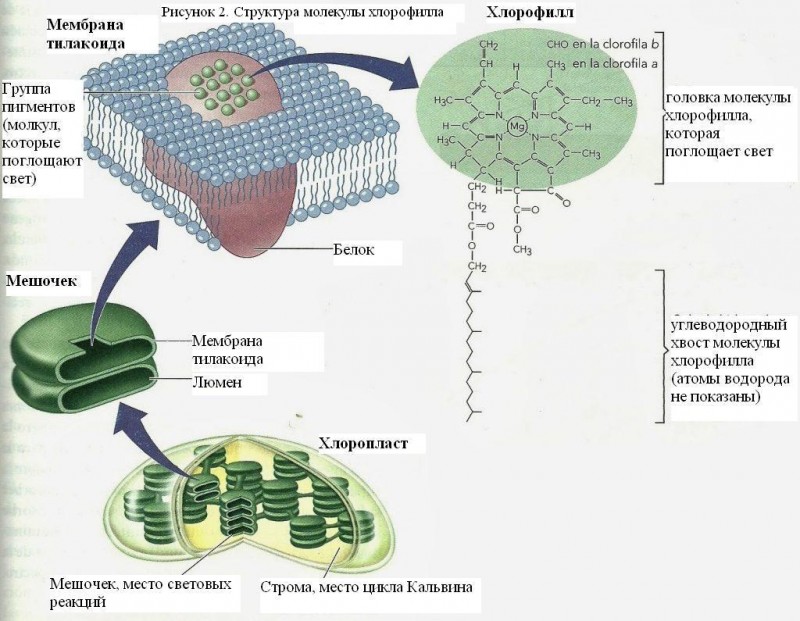
Хлорофилл является тетрапиррольным соединением, т.е. состоит из четырех пиррольных колец, соединенных метильными мостиками, которые образуют порфирин. Тетрапиррол является основной структурой порфирина, который, как и в хлорофилле, является частью гемоглобина и цитохрома.
В центре структуры находится металл (магний). Кольцо IV этерифицируется спиртом (фитолом), состоящим из серии из двадцати атомов углерода с двойной связью. Это «хвост» восковой природы, который приводит к тому, что пигмент является нерастворимым в воде, но растворим в некоторых органических растворителях. Отсюда и двойственная природа хлорофилла с центром гидрофильного порфирина и гидрофобным фитолом (Azcon и Talon, 1993).

Хлорофиллы a и b
Как упоминалось выше, хлорофилл a – это пигмент, непосредственно связанный с превращением световой энергии в химическую. Тем не менее, существует еще один тип хлорофилла, хлорофилл b, и пигменты, называемые каротиноидами, которые бывают красными, оранжевыми или желтыми, и которые в зеленых листьях маскируются обилием хлорофиллов. Эти дополнительные пигменты хлорофилла позволяют растениям поглощать более широкий диапазон спектра света, доступного для фотосинтеза, действуя в качестве рецепторов, которые передают энергию. Также существует хлорофилл с, найденный в бурых водорослях. В красных водорослях найден хлорофилл d. Наконец, существует тип хлорофилла (бактериохлорофилл), который является пигментом фототрофных бактерий (Cogua, 2011).
Каротиноиды
Желтые и красные пигменты, известные как каротиноиды, имеют систему сопряженных двойных связей, образованных атомами углерода, являются соединениями, нерастворимыми в воде, но растворимы в жировых растворителях. Они разделены на ненасыщенные углеводороды или каротины и кислородсодержащие производные, называемые ксантофиллами. В растениях каротиноид называется бета-каротином. Это пигменты красного, оранжевого или желтого цвета (Curtis и Barnes, 2001). Каротиноиды, участвующие в процессе фотосинтеза, называются первичными, в отличие от тех, которые находятся в цветах и плодах, формируя хромопласты, и в гетеротрофах, таких как бактерии, дрожжи и грибы (Cogua, 2011).
Организация пигментов в тилакоидах
Как отмечено выше, структурные единицы фотосинтеза у эукариот представляют собой хлоропласты, расположенные преимущественно в листьях. Внутренние ткани каждого листа покрыты эпидермальными клетками, покрытыми кутикулой, восковым слоем. Кислород и углекислый газ проникают в листья через специальные поры, называемые устьицами. Высокий процент фотосинтеза происходит в клетках палисадной паренхимы, которые расположены под эпидермисом и образуют мезофилл. Хлоропласты ориентированы внутри клеток, чтобы облегчить поглощение света тилакоидными мембранами (Curtis and Barnes, 2001).
Стадии фотосинтеза
Английский физиолог Ф. Блэкмэн (F. F. Blackman) после проведения различных экспериментов предположил, что в процессе фотосинтеза существует, по крайней мере, два ограничивающих фактора: интенсивность света и температура. Поэтому существует группа реакций, которые зависят от света, но не зависят от температуры, как видно из общей схемы фотосинтеза (Рисунок 3) (Curtis and Barnes, 2001).
В опытах Блэкмэна скорость реакций, которые зависят от температуры, увеличивалась лишь около 30°С. Затем скорость уменьшалась. На основании экспериментальных данных он сделал вывод, что эти реакции контролировались ферментами, так как это способ, по которому ферменты предположительно реагируют на температуру. Это способствовало дифференциации стадии световых реакций, зависящей от света и ферментативной стадии, не зависящей от света, или «темновых» реакций. Эти последние реакции нуждаются в химических веществах, синтезированных в «световых» реакциях, но они могут происходить и в светлых, и в темных условиях (Curtis и Barnes 2001).
Общая схема фотосинтеза

Поглощение света
Световые реакции можно резюмировать следующим образом. Светопоглощающие пигменты делятся на две группы: те, которые поглощают и передают энергию к реакционному центру, и те, которые образуют этот реакционный центр, представляющий собой определенный тип молекул хлорофилла (хлорофилл a P680 и Р700) и осуществляют фотохимическую реакцию.
Для обеспечения фотосинтеза требуется сотрудничество двух типов фотосистем, называемых I и II (PS I и PS II). В PS II вода используется в качестве донора электронов, выделяя кислород в качестве побочного продукта. В PS I восстанавливается терминальный акцептор, отдавая электрон ферредоксину, чтобы с его помощью восстановить НАДФ (NADP), которая, наконец, используется для превращения CO2 в углеводы (Melgarejo, 2010).
Фотосистемы I и II работают вместе, хотя в то же время фотосистема I может работать независимо, как это описано на рисунке.

В данной модели энергия света достигает фотосистемы II, где она захватывается молекулой хлорофилла a P680. Электрон молекулы Р680 высвобождается на более высоком энергетическом уровне, из которого он передается к молекуле первичного акцептора электронов. Электрон проходит вниз на фотосистему I вдоль цепи переноса электронов. В результате потока электронов вдоль транспортной цепи устанавливается протонный градиент по всей тилакоидной мембране; потенциальная энергия этого электрохимического градиента используется для формирования АТФ (ATP) из АДФ (ADP) – хемиосмотического процесса, аналогичного процессу у митохондрий. Этот процесс известен как фотофосфорилирование (Curtis и Barnes, 2001).
Одновременно выделяются три других действия:
1. Молекула хлорофилла P680, теряя свой электрон, ищет замену. Она находит ее в молекуле воды, которая, будучи прикрепленной к молекуле, содержащей марганец, лишается электрона, а затем распадается на протоны и газообразный кислород.
2. Дополнительно световая энергия захватывается в реактивной молекуле хлорофилла Р700 фотосистемы I. Молекула окисляется, и электрон высвобождается в первичный акцептор электронов, из которого он перемещается вниз по направлению к НАДФ+ (NADP+).
3. Электрон, удаленный из молекулы P700 фотосистемы I, замещается электроном, который перемещался вниз от первичного акцептора электронов фотосистемы II. Таким образом, на свету происходит непрерывный поток электронов от воды к фотосистеме II, к фотосистеме I, к НАДФ+ (CURTIS, Helena, BARNES, Sue, 2001). Энергия, восстановленная на этих этапах, представлена молекулой АТФ (ATP) (образование которой высвобождает молекулу воды) и НАДФH (NADPH), которые затем преобразуются в основные источники энергии для восстановления углекислого газа. Для генерации одной молекулы НАДФН необходимо поглотить 4 протона: 2 фотосистемой II и 2 фотосистемой I (Curtis и Barnes, 2001).
Восстановление и фиксация CO2
На второй стадии фотосинтеза энергия используется для восстановления углерода. Углерод доступен для фотосинтезирующих клеток в форме диоксида углерода. У растений двуокись углерода достигает фотосинтезирующих клеток через специализированные отверстия листьев и зеленых стеблей, называемые устьицами (Curtis и Barnes 2001).
На этой второй стадии фотосинтеза, АТФ и НАДФН, сформированные на первой стадии, используются для восстановления углерода из диоксида углерода до простого сахара. Затем химическая энергия, временно хранящаяся в молекулах АТФ и НАДФН, передается соответствующим молекулам для транспортировки и хранения энергии в клетках водорослей или органов растений. Результатом этого процесса является формирование углеродного скелета, из которого затем могут быть построены и другие органические молекулы (Cogua, 2011).
Реакции фиксации углерода проходят в условиях, которые не требуют света, но некоторые ферменты регулируются им и производятся в строме посредством цикла Кальвина (Рисунок 5). НАДФ и АТФ, образованные в реакциях, которые поглощают световую энергию, используются для восстановления углекислого газа. Цикл производит глицеральдегид фосфат, из которого может быть сформирована глюкоза и другие органические соединения (Cogua, 2011).
Цикл Кальвина

Это преобразование происходит в строме хлоропластов. CO2 поступает в хлоропласт, проходя через клеточные мембраны органеллы по определенным каналам. Этот газ поступает в тело растения, благодаря устьичному отверстию, которое в то же время облегчает выделение водяного пара в процессе, известном как транспирация (Cogua, 2011). Цикл Кальвина представляет собой центральный путь восстановления СО2 до органических молекул. Он начинается, когда фермент рибулоза 1,5 бифосфат карбоксилаза оксигеназа (Rubisco) выполняет карбоксилирование СО2 и дает начало двум молекулам из трех атомов углерода (Melgarejo, 2010). Чтобы выяснить это, было проведено несколько экспериментов, которые были успешными, благодаря использованию радиоизотопов в зеленых водорослях Chlorella pyrenoidosa и Scenedesmus obliquus. После получения 14СО2 в течение 60 секунд в культурах вышеупомянутых водорослей появляется несколько меченых соединений; фосфаты сахаров, органические кислоты и аминокислоты. Сокращая время применения С14О2 шаг за шагом, удалось восстановить образованные меченые продукты. Менее чем за 2 секунды появляется только одно меченое соединение, 3-фосфоглицериновая кислота (3-PGA), состоящая из трех атомов углерода. Таким образом, первая стадия восстановления СО2 состоит в карбоксилировании, в ходе которого СО2 включается в молекулу акцептора, имеющую 5 атомов углерода, рибулозо-1,5-дифосфат, расщепление которого приводит к образованию двух молекул 3-PGA. Механизм восстановления СО2 является циклическим процессом из нескольких частичных ферментативных стадий (Мельгарехо, 2010).
Метаболизм Хэтча/Слэка

Существуют и другие адаптивные процессы у различных типов растений, например, некоторые растения присоединяют диоксид углерода к первому соединению, известному как фосфоенолпировиноградная кислота или фосфоенолпируват (РЕР) с образованием соединения из четырех атомов углерода, щавелевоуксусной кислоты (промежуточное соединение в цикле Кребса). Среди других растений, которые имеют этот тип метаболизма, кукуруза и сорго. У них диоксид углерода, включенный в щавелевоуксусную кислоту, окончательно переносится в RuBP и входит в цикл Кальвина, но только после прохождения ряда реакций, которые транспортируют его в более глубокие участки внутри листа. Эти реакции протекают в клетках мезофилла, где хлоропласты характеризуются наличием обширной сети тилакоидов, организованных в хорошо развитые граны. Яблочная или аспарагиновая кислота, в зависимости от вида, транспортируются к клеткам обкладки сосудистого пучка, благодаря сети плазмодесм. Хлоропласты этих клеток, которые образуют плотные оболочки вокруг сосудистых пучков листа, имеют неразвитые граны и часто содержат граны крахмала. Растения, использующие этот путь, или путь Хэтча-Слэка, обычно называют C4-растениями, благодаря 4-углеродному соединению, которое служит в качестве акцептора СО2 (Cogua, 2011).
Кислотный метаболизм Толстянковых или растения MAC (CAM)

Существуют некоторые виды растений сухого климата, которые имеют толстые листы, с низким соотношением поверхности к объему, толстой кутикулой и низкой скоростью транспирации. Такие растения называются суккулентами. Как правило, фотосинтезирующие клетки листьев или стебля у них представлены в губчатом мезофилле. У некоторых суккулентов метаболизм CO2 необычен, первоначально исследован у членов семейства Толстянковых, поэтому его называют Кислотный метаболизм Толстянковых (Crasulaceae Acid Metabolism (CAM или MAC) по-английски).
Новый фотосинтетический путь, упомянутый выше, был найден у некоторых растений суккулентов или полусуккулентов из родов Бриофи́ллум, Каланхоэ, Седум, Клейния, Толстянка, Опунция (Salisbury и Ross, 1994). MAC или CAM растения поглощают диоксид углерода в течение ночи, фиксируя в органических кислотах, которые подкисляют среду и высвобождают его в течение дня, чтобы сразу же использовать в цикле Кальвина. Этот тип метаболизма уменьшает потери воды, связанные с открытием устьиц. (Cogua, 2011).
Факторы окружающей среды и фотосинтез
Подсчитано, что количество углерода, который фиксируется каждый год на планете, колеблется от 70000 до 120000 млн. тонн или эквивалентно около 170 – 290 гигатоннам сухого вещества, с минимальной формулой 0. Эта огромная производительность имеет место, несмотря на низкую концентрацию в атмосфере. Более 13% атмосферного углерода используется каждый год в процессе фотосинтеза, и почти равное количество обменивается при растворении в океанах. На фотосинтез оказывают влияние такие факторы, как вода, концентрация СО2, свет, питательные вещества и температура, а также возраст и генетика растений (Salisbury и Ross, 1994).
CO2
Количество СО2 является фактором, определяющим производительность, тем не менее некоторые реакции фотосинтеза могут быть осуществлены в его отсутствие. Однако, без этого газа не будет синтеза углеводов. Концентрация CO2 в атмосфере не является оптимальной для фотосинтеза, в сельскохозяйственной практике используется искусственное добавление газообразного СО2 в условиях постоянного освещения, для увеличения фотосинтетической скорости и урожайности при производстве биологического материала (Salisbury и Ross, 1994). CO2, как известно, производит немедленное увеличение скорости фотосинтеза, особенно у C3-растений. Однако, когда растения растут непрерывно с повышенным уровнем СО2, происходят биохимические изменения, которые снижают фотосинтетическую способность листьев, поэтому большой начальный рост фотосинтеза при высокой концентрации СО2 обычно не сохраняется таким же высоким, когда проходят несколько недель или месяцев. Это явление известно как акклиматизация фотосинтеза (Cogua, 2011).
Вода
Внеклеточно у высших растений вода транспортирует такие материалы, как соли, которые перемещаются от корней ко всем частям растения. Помимо того, что она является сырьем в процессе фотосинтеза, вода способствует в качестве реагента нескольким метаболическим реакциям. Ионы, образующие молекулу воды (Н) и (ОН) собираются и рекомбинируются в новые молекулы воды (Cogua, 2011).
Свет
Нет света, нет фотосинтеза, растения нуждаются в свете с точки зрения интенсивности и качества излучения. С увеличением интенсивности света увеличивается фотосинтетическая интенсивность вначале по линейной зависимости, а затем плавно уменьшается и, наконец, достигает постоянного значения, т.е. фотосинтетическая способность насыщается светом. Это значение насыщения достигается различными видами с разной скоростью. У светолюбивых растений это происходит после достижения высокой интенсивности излучения, а у тенелюбивых растений это насыщение достигается быстро, то есть требуется низкая интенсивность света (Cogua, 2011).
Температура
Зависимость фотосинтеза от факторов света и температуры позволяет сделать вывод, что фотосинтез не является непрерывным процессом, а состоит из множества фотохимических реакций, которые зависят от света и серии ферментативных реакций, зависящих от температуры. Последние очевидны в состоянии насыщения света, точке, в которой повышение температуры увеличивает фотосинтетическую интенсивность (Cogua, 2011). Транспорт, промышленность, вырубка лесов, сельское хозяйство и другие виды деятельности человека вызывают увеличение концентрации CO2 и других газов в атмосфере, таких как метан. Скопление этих газов имеет тенденцию к нагреву атмосферы, что может привести к региональным или глобальным изменениям, которые повлияют на такие параметры, как температура, осадки, влажность почвы и уровень моря, все они связаны с фотосинтезом и, следовательно, с самой жизнью на планете. (Cogua, 2011).
Инга Костенко, Mivena,Украина
Анна Устименко, Клуб Sirius Agro Plant
Universidad Nacional de Colombia
siriusap.com
Физиология растений и фотосинтез — КиберПедия
Получены доказательства обратимости стресс-индуцированного формирования водосберегающего типа фотосинтеза у растений, представляющего собой высоко эффективный механизм выживания в условиях жесткого водного дефицита. Полученные данные имеют важное значение для понимания механизмов специализированной адаптации растений к экстремальным условиям. (ИФР РАН)
Показано участие тирозинового типа фосфорилирования белков в ранней ответной реакции тканей растений на действие брассиностероидов и олигохитозанов. (КИББ КазНЦ РАН)
Установлено, что цитокинины участвуют в дифференциальной регуляции транскрипции хлоропластных генов. (ИФР РАН)
Показано, что в процессе фотоинактивации изолированных мембран и клеток Synechocystis sp. PCC 6803 образуется промежуточная форма фотосистемы 2, способная к темновому восстановлению фотохимической активности без синтеза белка de novo. (ИФПБ РАН)
Показано, что в протопластах клеток листа табака (Nicotiana rustika L.) имеется три относительно независимых системы актинового цитоскелета: а) мощная, равномерно распределенная сеть в субкортикальном слое цитоплазмы; б) филаменты, соединяющие между собой отдельные хлоропласты в единую систему (на поверхности хлоропластов показано присутствие F-актина) и в) структурные элементы в виде плоских лент, ассоциированных с ядром клетки. (ИБФРМ РАН)
Установлено, что одной из ранних ответных реакций при взаимодействии микоплазм с клетками растений является усиление теплопродукции. (КИББ КазНЦ РАН)
Показано, что в отсутствие функционально-активных хлоропластов сохраняется система рецепции и трансдукции цитокининового сигнала. (ИФР РАН)
Показано, что ризоид ламинариевых является не только органом прикрепления таллома к субстрату, но и принимает активное участие в метаболизме водорослей. (ММБИ КНЦ РАН)
При изучении функциональных характеристик природной флоры Приполярного Урала и Кольского п-ова выявлена тесная связь дыхательной активности листьев с составом биомассы и, в первую очередь, содержанием азота. (ИБ КомиНЦ УрО РАН)
Из погребенных льдов внутренних районов Антарктиды с глубины 14,5 м и 14,9 м выделены в альгологически чистых культурах древние жизнеспособные зеленые водоросли, идентифицированные как Chlorococcum sp. и Chlorella sp., и изучены их спектральные особенности. Клетки выделенных водорослей характеризуются низким содержанием хлорофилла а, высоким содержанием хлорофилла б и каротиноидов по отношению к хлорофиллу а и более сложным составом каротиноидов по сравнению с лабораторной культурой Chl. vulgaris, культивируемой в одинаковых с древними водорослями условиях. (ИФПБ РАН)
Обнаружена способность экзогенных замещенных хинонов в окисленном состоянии влиять на перенос электрона в фотосистеме 2 изолированных тилакоидов как фотохимически, акцептируя электроны от пула пластохинонов, так и нефотохимически – посредством тушения возбужденных синглетных состояний хлорофилла в антенне этой фотосистемы.
Получена принципиально новая информация о вовлечении элементов цитоскелета в стимуляцию водонагнетающей деятельности корня фитогормонами, нейромедиаторами и ионами кальция. Установлено, что восприятие указанных сигнальных молекул микрофиламентами и микротрубочками может носить как непосредственный, так и опосредованный характер. (ИФР РАН)
Исследованы мутанты галобактерий с различным значением рК для протонного акцептора Асп-85 в бактериородопсине. Получены кинетические и термодинамические параметры векторного внутрибелкового протонирования Асп-85. (МГУ)
Исследованы антиоксидантные системы растений галофитов, способствующие поддержанию окислительного гомеостаза и выживанию растений в условиях экстремально высокого засоления, основанные на активации прооксидантных свойств полиаминов, функционировании супероксиддис-мутаз, гваяколовых пероксидаз и генетически детерминированной способности растений к образованию и аккумуляции ферритина. (ИФР РАН)
Биологическая физика
Показано, что стабильный комплекс молекулярного шаперонина GroEL с ненативными белковыми мишенями ослабляется в результате присоединения ко-шаперонина GroES. Это свидетельствует о том, что ненативная белковая мишень не может удерживаться во внутренней полости GroEL под «крышкой» GroES, как то предполагалось ранее в моделях шаперонин-ассистируемого сворачивания белков. (ИБ РАН)
Показано, что одним из основных факторов, определяющих высокую эффективность и направленность первичного разделения зарядов в реакционных центрах пурпурных бактерий, является сочетание когерентного переноса электрона от возбужденного первичного донора электрона Р к первичному акцептору ВА и некогерентного изменения ядерных координат за счет переориентации гидроксильной группы тирозина М210. (ИФПБ РАН)
В клетках асцитной карциномы Эрлиха открыто влияние импульсной секреции АТФ, вызываемой как активацией АТФ-рецептора, так и неспецифическими воздействиями разной природы. Секретируемый АТФ взаимодействует с рецепторами на поверхности соседних клеток и клеток-индукторов, активизируя в них секрецию АТФ. Этот сигнал в виде «АТФ-волны» эстафетно передается от клетки к клетке. Установлены две функции внутриклеточного АТФ: с одной стороны, АТФ выступает как индуктор и усилитель процесса секреции, а с другой, как межклеточный трансмиттер.
Показано, что при механических и термических травмах кожи в первую неделю после нанесения травмы образуются молодые фибробласты, которые экспрессируют и секретируют пероксиредоксин VI. Установлено, что этот белок активно участвует в заживлении раны и ускоряет процесс в несколько раз за счет антиоксидантного механизма действия.
Получены новые данные, свидетельствующие о том, что конформационная подвижность заряженных и полярных аминокислотных остатков и образование альтернативных водородных связей составляют основу механизма регуляции термостабильности глобулярных белков. (ИБК РАН)
Показано, что фазовая скорость акустических волн, распространяющихся по поверхности мягких биологических тканей, существенно зависит от расстояния до источника возмущения. Изучена зависимость средней скорости распространения акустических волн в ближней зоне от упругих свойств среды. Полученные результаты могут служить основой системы диагностики состояния ткани. (ИМПБ РАН)
Обнаружены изоформы легких цепей миозина, характерные для предсердия (ЛЦ1п), в миозине желудочка сердца у больных в начальной стадии дилатационной кардиомиопатии (ДКМП), нехарактерные для этого отдела сердца в норме. На конечной стадии болезни ЛЦ1п исчезают. Повышенная сократительная активность миозина и появление в желудочке ЛЦ1п указывает на их компенсаторную роль при ДКМП, а исчезновение ЛЦ1п - на конечную стадию развития болезни. Создана основа для разработки нового прогностического показателя развития ДКМП. (ИТЭБ РАН)
cyberpedia.su
Физиология растений и фотосинтез
Получены доказательства обратимости стресс-индуцированного формирования водосберегающего типа фотосинтеза у растений, представляющего собой высоко эффективный механизм выживания в условиях жесткого водного дефицита. Полученные данные имеют важное значение для понимания механизмов специализированной адаптации растений к экстремальным условиям. (ИФР РАН)
Показано участие тирозинового типа фосфорилирования белков в ранней ответной реакции тканей растений на действие брассиностероидов и олигохитозанов. (КИББ КазНЦ РАН)
Установлено, что цитокинины участвуют в дифференциальной регуляции транскрипции хлоропластных генов. (ИФР РАН)
Показано, что в процессе фотоинактивации изолированных мембран и клеток Synechocystissp. PCC 6803 образуется промежуточная форма фотосистемы 2, способная к темновому восстановлению фотохимической активности без синтеза белкаde novo. (ИФПБ РАН)
Показано, что в протопластах клеток листа табака (Nicotiana rustikaL.) имеется три относительно независимых системы актинового цитоскелета: а) мощная, равномерно распределенная сеть в субкортикальном слое цитоплазмы; б) филаменты, соединяющие между собой отдельные хлоропласты в единую систему (на поверхности хлоропластов показано присутствие F-актина) и в) структурные элементы в виде плоских лент, ассоциированных с ядром клетки. (ИБФРМ РАН)
Установлено, что одной из ранних ответных реакций при взаимодействии микоплазм с клетками растений является усиление теплопродукции. (КИББ КазНЦ РАН)
Показано, что в отсутствие функционально-активных хлоропластов сохраняется система рецепции и трансдукции цитокининового сигнала. (ИФР РАН)
Показано, что ризоид ламинариевых является не только органом прикрепления таллома к субстрату, но и принимает активное участие в метаболизме водорослей. (ММБИ КНЦ РАН)
При изучении функциональных характеристик природной флоры Приполярного Урала и Кольского п-ова выявлена тесная связь дыхательной активности листьев с составом биомассы и, в первую очередь, содержанием азота. (ИБ КомиНЦ УрО РАН)
Из погребенных льдов внутренних районов Антарктиды с глубины 14,5 м и 14,9 м выделены в альгологически чистых культурах древние жизнеспособные зеленые водоросли, идентифицированные как Chlorococcum sp. и Chlorella sp., и изучены их спектральные особенности. Клетки выделенных водорослей характеризуются низким содержанием хлорофилла а, высоким содержанием хлорофилла б и каротиноидов по отношению к хлорофиллу а и более сложным составом каротиноидов по сравнению с лабораторной культурой Chl. vulgaris, культивируемой в одинаковых с древними водорослями условиях. (ИФПБ РАН)
Обнаружена способность экзогенных замещенных хинонов в окисленном состоянии влиять на перенос электрона в фотосистеме 2 изолированных тилакоидов как фотохимически, акцептируя электроны от пула пластохинонов, так и нефотохимически – посредством тушения возбужденных синглетных состояний хлорофилла в антенне этой фотосистемы.
Получена принципиально новая информация о вовлечении элементов цитоскелета в стимуляцию водонагнетающей деятельности корня фитогормонами, нейромедиаторами и ионами кальция. Установлено, что восприятие указанных сигнальных молекул микрофиламентами и микротрубочками может носить как непосредственный, так и опосредованный характер. (ИФР РАН)
Исследованы мутанты галобактерий с различным значением рК для протонного акцептора Асп-85 в бактериородопсине. Получены кинетические и термодинамические параметры векторного внутрибелкового протонирования Асп-85. (МГУ)
Исследованы антиоксидантные системы растений галофитов, способствующие поддержанию окислительного гомеостаза и выживанию растений в условиях экстремально высокого засоления, основанные на активации прооксидантных свойств полиаминов, функционировании супероксиддис-мутаз, гваяколовых пероксидаз и генетически детерминированной способности растений к образованию и аккумуляции ферритина. (ИФР РАН)
studfiles.net
Биология / Физиология растений / Фотосинтез.

Обратная связь
ПОЗНАВАТЕЛЬНОЕ
Сила воли ведет к действию, а позитивные действия формируют позитивное отношение
Как определить диапазон голоса - ваш вокал
Как цель узнает о ваших желаниях прежде, чем вы начнете действовать. Как компании прогнозируют привычки и манипулируют ими
Целительная привычка
Как самому избавиться от обидчивости
Противоречивые взгляды на качества, присущие мужчинам
Тренинг уверенности в себе
Вкуснейший "Салат из свеклы с чесноком"
Натюрморт и его изобразительные возможности
Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д.
Как научиться брать на себя ответственность
Зачем нужны границы в отношениях с детьми?
Световозвращающие элементы на детской одежде
Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия
Как слышать голос Бога
Классификация ожирения по ИМТ (ВОЗ)
Глава 3. Завет мужчины с женщиной

Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
 Отёска стен и прирубка косяков - Когда на доме не достаёт окон и дверей, красивое высокое крыльцо ещё только в воображении, приходится подниматься с улицы в дом по трапу.
Отёска стен и прирубка косяков - Когда на доме не достаёт окон и дверей, красивое высокое крыльцо ещё только в воображении, приходится подниматься с улицы в дом по трапу.
 Дифференциальные уравнения второго порядка (модель рынка с прогнозируемыми ценами) - В простых моделях рынка спрос и предложение обычно полагают зависящими только от текущей цены на товар.
Дифференциальные уравнения второго порядка (модель рынка с прогнозируемыми ценами) - В простых моделях рынка спрос и предложение обычно полагают зависящими только от текущей цены на товар.
Страница 7
П = Q -R - Тп + Rп
где П - поглощенная посевом радиация, Q - суммарная радиация, падающая на посев, R - радиация, отраженная от посева и вышедшая за пределы его верхней границы, Тп - радиация, проникшая к почве, Rп - радиация, отраженная от почвы под растительностью.
Коэффициент поглощения энергии ФАР (Qп) посевом определяют делением обеих частей формулы на Q:
Qп = П/ Q = 1 - R/Q - Тп/Q +Rп/ Q,где R/
Q -альбедо посева, показывающее, какая доля падающей радиации отражается посевом, Тп/ Q- коэффициент пропускания, показывающий, какая доля падающей радиации (Q) достигает почвы под растительностью, Rп/
Q -альбедо почвы под растительностью.
Эффективность фотосинтеза можно характеризовать коэффициентом полезного действия, который определяют по формуле:
Е% (КПД) = В.100/А,
где А - количество энергии , поступившей за период вегетации на 1 га посева, или энергии, которая была поглощена посевом, в кДж, В - количество энергии, накопившейся в органической массе урожая (биологического или хозяйственного), в кДж.
Доказано, что для образования продуктов фотосинтеза при всех благоприятных условиях (орошение, высокая концентрация СО2) солнечная энергия используется только на 2%. В среднем КПД фотосинтеза сельскохозяйственных растений в реальных условиях составляет около 0,5-1% (то есть около 16 кДж/м2 в час
), теоретически же возможно повышение уровня этого показателя до 4-6%. Одной из самых насущных задач, стоящих перед практическим сельскохозяйственным производством, и является повышение эффективности фотосинтеза.
Условия, влияющие на интенсивность и продуктивность фотосинтеза.
На основные показатели фотосинтеза влияют как внутренние факторы, так и внешние абиотические факторы.
К внутренним факторам - то есть к эндогенным механизмам регуляции фотосинтеза у растений - относятся:
проводимость листа,
фотохимическое лимитирование фотосинтеза,
биохимическое лимитирование фотосинтеза,
гормональное воздействие,
донорно-акцепторные отношения,
накопление углеводов,
возраст листа или растения.
Проводимость листа
бывает устьичная и остаточная. Она измеряется в сантиметрах в секунду и является величиной, обратной сопротивлению листа, колеблется от 1 см/с при открытых устьицах до 0,02 см/с при закрытых устьицах, показывает скорость прохождения углекислого газа по тканям листа.
Фотохимическое лимитирование фотосинтеза
происходит при недостатке поступления энергии из световой фазы фотосинтеза, то есть при недостатке освещенности.
Биохимическое лимитирование фотосинтеза
определяется недостаточным количеством необходимых для фотосинтеза ферментов, в частности рибулезодифосфаткарбоксилазы/оксигеназы, или недостатком собственно субстрата - рибулезодифосфата.
Гормональное воздействие
проявляется в действии ингибиторов роста, например, АБК, повышение концентрации которой приводит к закрытию устьиц и к снижению интенсивности фотосинтеза.
Донорно-акцепторные отношения
проявляются в том, что если
у растения уменьшается число акцепторов продуктов фотосинтеза
(число клубней, плодов), то интенсивность фотосинтеза снижается
, если
же уменьшается число доноров продуктов фотосинтеза
(листьев) (например в результате повреждения вредителями, искусственная частичная дефолиация), то интенсивность фотосинтеза у оставшихся листьев увеличивается.
Накопление углеводов
(крахмала) может вызвать снижение
интенсивности фотосинтеза, хотя вопрос остается до конца не изученным.
Возраст листа (растения)
определяет повышение интенсивности
фотосинтеза у завершившего рост листа и постепенное снижение интенсивности
фотосинтеза у стареющего листа за счет деградации хлоропластов.
На показатели фотосинтеза значительно влияют такие абиотические факторы, как:
освещенность,
температура,
водный режим,
минеральное питание,
Троение хлоропласта
- двойная мембрана, отделяющая хлоропласт от цитоплазмы, фотосинтетические мембраны - тилакоиды стромы и тилакоиды гран, наличие участков ДНК, способность к цитоплазматическому наследованию. Внутренние части полости тилакоидов гран и межгранальные тилакоиды - это единая замкнутая фотосинтетическая внутримембранная полость, объединенная в единую фотоэнергетическую систему хлоропласта.
Грана хлоропласта состоит из 10-30 тилакоидов, а всего в хлоропласте 100-150 гран, таким образом поверхность фотосинтетических мембран тилакоидов в 10 раз превышает поверхность самого хлоропласта.
Особая роль отводится концевым тилакоидам граны, которые, будучи селективным фильтром, предохраняют грану от излишнего облучения или подают сигнал на изменение ориентации оси граны. При оптимальных условиях освещения оси гран обычно направлены радиально к более выпуклой стороне хлоропласта.
Функция хлоропласта
- осуществление процесса световой фазы фотосинтеза и накопление энергии в виде макроэргических молекул (АТФ и НАДФ восстановленного).
Свойства хлоропластов
- способность к перемещению внутри клетки под воздействием условий освещенности и концентрации углекислого газа. Передвижение хлоропластов по клетке называется фототаксисом или хемотаксисом хлоропластов
в зависимости от причины , вызывающей это передвижение. При умеренном освещении хлоропласты выстраиваются таким образом, чтобы на них попадало максимальное количество света, а при избыточном освещении выстраиваются вдоль падающих солнечных лучей. Такое расположение хлоропластов называется парастрофией
. Ночью хлоропласты выстраиваются в положении апострофии
.
Хромопластыпридают желтую, оранжевую, красную окраску лепесткам, плодам, листьям, так как содержат большое количество специфических каротиноидов, обладающих тем или иным оттенком окраски. Хромопласты функционально дополняют деятельность хлоропластов, кроме того выполняют функцию привлечения насекомых-опылителей, животных-распространителей семян.
В состав фотосинтетических мембран (тилакоидов) входят специфические фотосинтетические пигменты - хлорофиллы и каротиноиды - погруженные в эти мембраны.
Хлорофиллыделятся на четыре разновидности: а, b, c, d. Это органические соединения, содержащие 4 пиррольных кольца, связанных атомами магния и имеющими зеленую окраску. Отличаются между собой хлорофиллы по молекулярной массе:
а - имеет молекулярную массу 893 и включает фитоловый и метиловый остаток,
b - имеет молекулярную массу 907 и включает фитоловый и метиловый остаток,
с - включает только метиловый остаток,
d - имеет молекулярную массу 891 и близок к протохлорофиллу.
У высших растений встречаются в основном хлорофиллы а и b, а у водорослей - а и с или а и d.
Хлорофилл впервые был выделен в 1818 году, к 1940 году была расшифрована его структура, а в 1960 году осуществили синтез хлорофилла. Хлорофиллы - это сложные эфиры дикарбоновой хлорофиллиновой кислоты с двумя спиртами (фитолом и метанолом). В карбоксильных группах хлорофиллиновой кислоты водород замещен остатками метилового и фитолового спиртов. Наличие в порфириновом ядре хлорофилла коньюгированной по кругу системы десяти двойных связей и магния обуславливает характерный для хлорофилла зеленый цвет. Хлорофиллу а
присущ темно-зеленый цвет, а хлорофиллу b
- светло-зеленый цвет. Остаток фитола придает хлорофиллу липоидные свойства, то есть он может растворяться в жировых растворителях.
Хлорофиллам свойственна флуоресценция - т.е. свойство под влиянием падающего света, в свою очередь, излучать свет, при этом длина волны излучаемого света обычно больше длины волны возбуждающего света. В проходящих лучах цвет хлорофилла - изумрудно-зеленый, а в лучах отраженного света хлорофилл приобретает красный цвет, то есть длина волны, отражаемой хлорофиллом, больше, чем длина волны света, возбуждающего излучение хлорофилла.
Хлорофиллы различаются по спектрам поглощения, при этом у хлорофилла bпо сравнению с хлорофиллом а
полоса поглощения в красной области спектра несколько смещена в сторону коротковолновых лучей, а в сине-фиолетовой области максимум поглощения смещен в сторону длинноволновых (красных) лучей.
В хлоропластах листьев хлорофиллов в три раза больше, чем каротиноидов, а в плодах, лепестках, зернах, корнеплодах - наоборот.
Каротиноиды являются непременными спутниками хлорофиллов. Они подразделяются на бескислородные (каротины и ликопины, имеющие оранжевую и красную окраску - общая формула - С40Н56) и окисленные (ксантофиллы - общая формула - С40Н56О2).
megapredmet.ru
Физиология растений
Физиология растений - наука об организации и координации функциональных систем зеленого растения. Физико-химический, экологический и эволюционный аспекты физиологии растений. Ее задача - познание закономерностей жизнедеятельности растений, раскрытие молекулярных основ сложных функций и механизмов их регуляции в системе целого организма. Методологические основы фитофизиологии. Редукционизм, органицизм и интегратизм как подходы к изучению живых систем. Сочетание различных уровней исследования (субклеточный, клеточный, организменный, биоценотический) как необходимое условие прогресса физиологии растений. Специфические методы фитофизиологии как науки.
Объект физиологии растений - эукариотный организм, осуществляющий фототрофный образ жизни. Специфика обмена зеленых растений по сравнению с другими объектами, характеризующимися фототрофным образом жизни. Космическая роль зеленого растения.
Этапы развития физиологии растений, их связь с общим развитием биологии и с практикой. Отечественные школы физиологов растений. Физиология растений - теоретическая основа растениеводства и новых отраслей биотехнологии. Физиологические основы продуктивности растений. Главные проблемы современной фитофизиологии.
Программа обучения по специальности
Особенности структуры и метаболизма растений по сравнению с животными. Синтетические способности растений. Физиология растительной клетки. Симбиотическая теория происхождения пластид и митохондрий. Уникальная роль процесса фотосинтеза на Земле. Образование энергии при фотофизических и фотохимических процессах фотосинтеза. Ассимиляция СО2 в цикле Кальвина. Подача СО2 у С3и С4растений и образование метаболитов. Дыхание растений как источник энергии и ассимилятов. Водный режим клетки и целого растения. Минеральное питание. Поглотительная проводящая и синтетическая роль корневой системы. Передвижение веществ. Донорно-акцепторные взаимоотношения и транспорт ассимилятов. Физиология роста. Меристемы. Фитогормоны. Периодичность роста. Покой. Движение растений. Физиология развития: механизмы прорастания семян, перехода к цветению, старению, опаданию. Явление яровизации, фотопериодизма. Фитохромная система. Устойчивость растений к неблагоприятным условиям. Интеграция физиологических процессов и ее связь с продуктивностью растений. Культура тканей и клеток. Использование ее в селекции и биотехнологии. Гибридизация клеток. Генная инженерия.
Теоретические вопросы:
1. Водный обмен у растений. Значение водного обмена. Основные этапы водного обмена. Механизмы процессов водного обмена.
2. Фотосинтез (определение и общее уравнение). Световая фаза: фотофизический и фотохимический этап. Фосфорилирование и его виды.
3. Темновая фаза фотосинтеза (С3 и С4 – пути фотосинтеза). Влияние внешних условий на фотосинтез. Космическая роль фотосинтеза.
4. Дыхание (определение дыхания, общее уравнение). Дыхание и брожение, сходство и отличие. Анаэробный этап дыхания растений.
5. Аэробное дыхание растений. Цикл Кребса и ЭТЦ. Энергетический выход дыхания.
6. Минеральное питание растений. Механизмы поглощения минеральных элементов корневой системой. Корень как орган поглощения минеральных ионов и воды.
Содержание ответов на теоретические вопросы:
| 1 вопрос: Определение водного обмена. Значение водного обмена. Поглощение воды клетками. Осмотические явления в клетках. Состояние воды в клетках: свободная и связанная вода. Поглощение воды корнем (корневое давление, плач, гуттация). Нижний концевой двигатель. Передвижение воды по стеблю. Верхний концевой двигатель. Транспирация, виды транспирации. Влияние внешних условий на транспирации. Водный режим растений разных экологических групп и жизненных форм. |
| Вопрос 2 Определение фотосинтеза. Общее уравнение фотосинтеза. Пигменты фотосинтеза, понятие о двух фотосистемах. Световая фаза фотосинтеза. Фотофизический этап. Поглощение и передача энергии между молекулами пигментов. Фотохимические процессы фотосинтеза. Z – схема. Фотосинтетическое фосфорилирование, общее понятие и виды (схема). |
| Вопрос 3 Темновая фаза фотосинтеза, общее понятие, локализация в структурах хлорапласта. Цикл Кальвина (С-3 - путь). Этапы цикла: карбоксилирование, восстановление, регенерация. Цикл Хэча – Слэка. Анатомическая структура листьев. Влияние внешних условий на фотосинтез. Космическая роль фотосинтеза. |
| Вопрос 4 Дыхание, определение дыхания, общее уравнение. Локализация процесса дыхания в клетке. Дыхание и брожение, сходство и отличие. Гликолиз, этапы гликолиза. Энергетический выход гликолиза |
| Вопрос 5 Аэробное дыхание, основные этапы, и их локализация в клетке. Митохондрии, их структура и функции. Цикл трикарбоновых кислот и его сущность. ЭТЦ, ее структура и особенности. Окислительное фосфорилирование, общий энергетический выход дыхания. |
| Вопрос 6 Элементарный состав растений. Зольные элементы и их значение. Механизм поглощения минеральных элементов, виды транспорта. Роль разных тканей корня в поглощении минеральных ионов и их транспорте. Понятие об азотном обмене растений, пути ассимиляции нитратов и аммиака в растении. |
Программа дисциплины "Физиология растений"
читайте далее
Физиология растительной клетки
Клетка как организм и как элементарная структура многоклеточного организма - сравнение функций. Специфические особенности растительной и животной клеток. Автотрофность и гетеротрофность.
Структурная организация клетки - основа ее биохимической активности и функционирования как целостной живой системы. Эволюция клеточной организации на примере сравнения прокариотной и эукариотной клетки.
Мембранные системы клетки и мембранный принцип ее организации. Структура и свойства биологических мембран, их роль в клетке (проницаемость, системы активного транспорта, биосинтезов и процессинга макромолекул). Модели структурно-функциональной организации мембран. Биохимическая и функциональная разнокачественность мембран.
Основные структурные элементы эукариотной клетки.
Ядро, его организация и функционирование. Генетический аппарат растительной клетки. Пластиды и митохондрии. Гипотезы происхождения клеточных органелл. Взаимодействие ядерного, митохондриального и хлоропластного геномов. Двойной генетический контроль за синтезом белков в хлоропластах и митохондриях.
Плазмалемма. Эндоплазматическая сеть, аппарат Гольджи, микротела (пероксисомы, глиоксисомы, лизосомы и др.), вакуоли, их строение и основные функции.
Цитоскелет, особенности его строения в связи с биологическими функциями.
Строение клеточной стенки, ее химический состав и основные функции (защитная, опорная, функции в морфогенезе, транспорте и др.).
Физико-химические свойства протоплазмы и их изменения в жизненном цикле клетки.
Функциональные взаимодействия различных органоидов клетки, их изменения в клеточном цикле и при ее дифференциации. Регуляторные системы клетки. Внутриклеточные факторы регуляции обмена: биохимические, генетические, мембранные. Регуляция с участием вторичных мессенджеров. Компартментация каталитических систем и метаболических фондов как один из механизмов регуляции клеточного метаболизма.
Дыхание
Фиологическая роль дыхания. Специфика дыхания у растений.
Развитие представлений о природе механизмов и о путях окислительно-восстановительных превращений в клетке. Каталитические системы дыхания (дегидрогеназы, оксидазы, оксигеназы, карбоксилазы, трансферазы и др.). Механизмы активации водорода субстрата и молекулярного кислорода.
Митохондрии. Их структура и функции. Изменение ультраструктуры митохондрий в зависимости от функционального состояния организма.
Пути окисления органических веществ в клетке. Унификация субстратов дыхания. Механизм активации дыхательных субстратов, пути их включения в процессы биологического окисления.
Основные пути диссимиляции углеводов. Пентозомонофосфатный путь окисления глюкозы и его роль в конструктивном обмене клетки. Гликолитический путь окисления; основные стадии. Гликолиз. Цикл Кребса. Глиоксалатный цикл. Механизмы регуляции циклов.
Электронтранспортная цепь митохондрий: структурная организация, основные компоненты, их окислительно-восстановительные потенциалы. Комплексы переносчиков электронов. Альтернативность каталитических механизмов биологического окисления.
Окислительное фосфорилирование. Единство элементарных энергетических процессов в живой природе. Фосфорилирование на уровне субстрата и фосфорилирование в дыхательной цепи. Основные положения хемиосмотической теории сопряжения Митчела. Мембраны как структурная основа биоэнергетических процессов. Трансформация энергии на сопрягающих мембранах. Электро-химический потенциал - движущая сила фосфорилирования. Регуляция электронного транспорта и фосфорилирования.
Дыхание как центральное звено обмена веществ. Значение дыхания в конструктивном метаболизме. Связь с другими функциями клетки. Дыхание роста и дыхание поддержания.
Количественные показатели газообмена (поглощение кислорода, выделение углекислоты, дыхательный коэффициент и др.).
Регуляция дыхания. Зависимость дыхания от внешних и внутренних факторов.
Фотосинтез
Развитие учения о фотосинтезе. Историческое значение работ К.А.Тимирязева.
Сущность и значение фотосинтеза. Общее уравнение фотосинтеза, его компоненты. Роль фотосинтеза в процессах энергетического и пластического обмена растительного организма. Фотосинтез как процесс трансформации энергии света в энергию химических связей. Масштабы фотосинтетической деятельности в биосфере.
Эволюция биосферы и фотосинтез.
Структурная организация фотосинтетического аппарата. Строение листа как органа фотосинтеза, изменения в онтогенезе. Хлоропласты. Основные элементы структуры хлоропластов (двойная мембрана, матрикс, тилакоиды, граны). Онтогенез хлоропластов.
Эволюция структуры фотосинтетического аппарата.
Пигментные системы фотосинтезирующих организмов. Хлорофиллы. Химическая структура, спектральные свойства. Отдельные представители группы хлорофиллов. Распространение хлорофиллов среди различных групп организмов. Функции хлорофиллов. Основные этапы биосинтеза молекулы хлорофилла. Хлорофилл-белковые комплексы.
Фикобилины. Распространение, химическое строение, спектральные свойства. Роль в фотосинтезе.
Каротиноиды. Химическое строение, свойства. Спектры поглощения. Функции в фотосинтезе.
Регуляция биосинтеза пигментов. Зависимость биосинтеза пигментов от интенсивности и качества света, снабжения СО2 02 и минеральными элементами. Явление хроматической адаптации.
Функциональное и экологическое значение спектрально-различных форм пигментов у фотосинтезирующих организмов.
Первичные процессы фотосинтеза. Электронно-возбужденные состояния пигментов (синглетное, триплетное). Типы дезактивации возбужденных состояний. Флуоресценция. Механизмы миграции энергии в системе фотосинтетических пигментов.
Представление о фотосинтетической единице. Антенные комплексы. Реакционные центры, модели их структурной организации. Преобразование энергии в реакционном центре. Окислительно-восстановительные превращения хлорофилла реакционного центра.
Электрон-транспортная цепь фотосинтеза, природа ее основных компонентов. Представление о совместном функционировании двух фотосистем. Эффекты Эмерсона. Основные функциональные комплексы электронтранспортной цепи - ФС1, ФС2, цитохром b6/f комплекс; их структура и функции. Образование соединений с высоким восстановительным потенциалом. Системы фотоокисления воды и выделения кислорода при фотосинтезе. Участие хинонов, цитохромов, Cuи Fe-протеидов в реакциях транспорта электронов. Циклические и нециклические потоки электронов, системы регуляции.
Фотофосфорилирование. Характеристика основных типов фотофосфорилирования - циклического, нециклического, псевдоциклического. Механизм сопряжения электронного транспорта и образования АТФ.
Темновая стадия фотосинтеза. Связь фотосинтетической ассимиляции СО2 с фотохимическими реакциями. Природа первичного акцептора углекислоты. Химизм реакций цикла Кальвина, его ключевые ферменты. Первичные продукты фотосинтеза, их превращения. Регенерация акцепторов СО2. Первичный синтез углеводов. Фотодыхание. Цикл Хэтча-Слэка-Карпилова. Особенности С3и С4растений и САМ-тип метаболизма.
Взаимосвязь фотосинтеза и процессов усвоения азота. Функциональная роль хлоропласта. Потоки метаболитов в хлоропласт и из него.
Экология фотосинтеза. Зависимость фотосинтеза от внешних условий и состояния организма. Влияние на фотосинтез температуры, условий освещения, содержания углекислоты, условий минерального питания, водоснабжения. Компенсационная точка при фотосинтезе и ее зависимость от особенностей организма. Ассимиляционное число.
Фотосинтез и общая продуктивность растительных организмов и их сообществ. Фотосинтез в онтогенезе растения. Теория фотосинтетической продуктивности.
Культура растений в условиях искусственного освещения и при повышении концентрации СО_42_0. Фотосинтез в условиях промышленной фитотроники и в замкнутых системах жизнеобеспечения.
Эволюция фотосинтеза. Хемосинтез. Бактериальный фотосинтез.
Физиология водообмена растений
Значение воды в жизнедеятельности растений. Растения и круговорот воды на Земле.
Молекулярная структура и физические свойства воды. Взаимодействие молекул воды и биополимеров, гидратация. Свободная и связанная вода. Физиологическое значение различных фракций воды в растении.
Основные закономерности поглощения воды клеткой. Набухание биоколлоидов, осмос - явления, лежащие в основе поступления воды в растение. Термодинамические показатели, определяющие поведение воды: активность воды, химический потенциал, водный потенциал. Составляющие водного потенциала: осмотический потенциал, матричный потенциал, потенциал давления. Градиент водного потенциала как движущая сила поступления и передвижения воды в системе "почва-растение-атмосфера", в клетках, тканях и целом растении.
Механизм передвижения воды по растению. Пути ближнего и дальнего транспорта. Движущие силы восходящего тока воды в растении. Верхний и нижний концевые двигатели. Корневое давление, механизм его развития и значение в жизни растений. Натяжение воды в сосудах; значение сил молекулярного сцепления.
Выделение воды растением. Гуттация, транспирация. Физиологическое значение этих процессов. Количественные показатели транспирации: интенсивность, продуктивность, транспирационный коэффициент. Устьичная и кутикулярная транспирация. Строение устьиц и механизмы их движений, влияние света. Устьичное и внеустьичное регулирование транспирации. Влияние внешних факторов (света, температуры, влажности воздуха и почвы и др.) на интенсивность транспирации. Суточный ход транспирации.
Экология водообмена растений. Особенности водообмена у растений разных экологических групп (ксерофитов, мезофитов, гигрофитов, галофитов) и пути адаптации растений к водному дефициту.
Физиология минерального питания
Роль растений в круговороте минеральных элементов в биосфере. Потребность растений в элементах минерального питания. Содержание и соотношение минеральных элементов в почве и в растениях и факторы, их определяющие. Классификации элементов, необходимых для растений. Основная функция ионов в метаболизме: структурная и каталитическая.
Почва как источник минеральных элементов. Твердая фаза почвы, почвенный раствор, состав и структура почвенного поглощающего комплекса.
Корень как орган поглощения минеральных элементов и воды, а также место специфических синтезов. Система взаимодействия "корень-почва". Рост корня как основа поступления минеральных элементов.
Ближний транспорт ионов в тканях корня. Симпластический и апопластический пути. Дальний транспорт. Восходящее передвижение веществ по растению: пути и механизмы. Перераспределение и реутилизация ионов в растении. Поступление и превращения ионов и дыхание. Взаимосвязь минерального питания с процессами роста и развития растений.
Механизм поглощения ионов. Роль процессов диффузии и адсорбции, их характеристика. Понятия водного свободного пространства и Доннановского свободного пространства. Транспорт ионов через плазматическую мембрану. Пассивный перенос. Активный транспорт ионов (первичный и вторичный активный транспорт). Уравнение Нернста. Движущие силы транспорта ионов и формы потребляемой энергии. Механизмы транспорта ионов через мембраны: АТФазы, редокс-цепи, ионные каналы, портерные системы (симпорт, антипорт, унипорт).
Кинетика процессов поглощения. Участие мембранных структур клетки в поглощении и компартментации ионов. Роль вакуоли. Пиноцитоз. Взаимосвязь процессов поглощения веществ корнем с другими функциями растения (дыханием, фотосинтезом, водообменом, биосинтезами, ростом и др.).
Физиологическая и биохимическая роль основных элементов питания
Азот и его значение в жизни растений. Круговорот азота в природе. Источники азота для растений. Симбиотическая фиксация молекулярного азота. Структурная и функциональная характеристика нитрогеназы. Минеральные формы азота, используемые растением. Ферментные системы, участвующие в усвоении нитратов, регуляция их синтеза и активности. Биохимические пути ассимиляции аммиака в растении. Синтез аминокислот, амидов, реакции переаминирования. Запасные и транспортные формы минерального и органического азота, накопление нитратов в тканях. Круговорот азота по растению.
Азотный обмен и дыхание. Азотный обмен и фотосинтез: взаимодействие азотного и углеродного потоков; роль первичных реакций фотосинтеза в усвоении окисленного азота.
Сера. Основные соединения серы в растении, их роль в структурной организации клетки, участие в окислительно-восстановительных реакциях. Источники серы для растения. Механизм восстановления сульфатов, отдельные этапы процесса, ферментные системы.
Фосфор. Значение разных типов фосфорсодержащих соединений в клетке. Поступление фосфора в клетку, пути его включения в обмен. Участие соединений, содержащих фосфор, в образовании клеточных структур, ферментных систем. Макроэргические соединения фосфора, их роль в энергетическом обмене.
Калий, его значение в обмене растительного организма. Влияние калия на физические свойства протоплазмы, на ферменты углеводного обмена, синтез белков и др. Роль калия в поддержании ионного баланса в тканях, в процессах осморегуляции.
Кальций. Структурообразовательная роль кальция. Участие в образовании клеточной стенки, поддержании структурной целостности мембран и регуляции их проницаемости. Регуляторная роль кальция.
Магний. Формы участия магния в метаболизме. Магний в составе хлорофилла. Участие в реакциях переноса фосфатных групп, в формировании функционально-активных клеточных структур.
Микроэлементы. Представления о роли микроэлементов в метаболизме растений. Металлы как компоненты простетических групп и как активаторы ферментных систем. Особенности поступления микроэлементов в растения. Физиологическая роль железа, меди, марганца, молибдена, цинка, бора и других микроэлементов. Участие микроэлементов в формировании и функционировании электронтранспортных цепей фотосинтеза и дыхания, в азотном и углеводном обмене, в ростовых процессах и других реакциях метаболизма.
Водная, песчаная и почвенная культуры, их применение в физиологии растений. Питательные смеси. Физиологически кислые и физиологически основные соли. Взаимодействие ионов (антагонизм, синергизм, аддитивность). Физиологические основы применения удобрений. Гидропоника. Значение работ Д.Н.Прянишникова, Д.А.Сабинина в создании теории минерального питания.
Корневое питание как важнейший фактор управления продуктивностью и качеством урожая. Генотипические различия в минеральном питании разных видов и сортов.
Транспорт веществ в растении
Понятие о восходящем и нисходящем токах веществ в растении. Передвижение органических веществ. Ближний и дальний (флоэмный) транспорт ассимилятов.
Транспортные формы веществ. Возможный механизм и регуляция флоэмного транспорта. Зависимость транспорта веществ от температуры, водного режима, минерального питания.
Донорно-акцепторные взаимодействия и роль транспортных систем в интеграции физиологических функций целого растения.
Физиология роста и развития растений
Определение понятий "рост" и "развитие" растений. Проблема роста и развития на клеточном и молекулярном уровнях. Существование организма как развертывание во времени генетической программы. Воздействие на этот процесс внутренних и внешних факторов.
Общие закономерности роста, типы роста у растений. Организация меристем корня и стебля. Рост и деятельность меристем. Кинетика ростовых процессов и их свойства. Ритмика, биологические часы. Корреляции. Полярность. Регенерация.
Рост растений и среда. Влияние температуры, света, воды, газового состава атмосферы, элементов минерального питания на ростовые процессы.
Клеточные основы роста. Фазы роста клеток и их характеристики. Изменения морфологии и метаболизма при прохождении каждой фазы. Понятие о клеточном цикле, влияние различных факторов на деление клеток. Рост клетки в фазе растяжения, механизм действия ауксина на этот процесс.
Дифференцировка клеток и тканей; компетенция и детерминация. Дифференциальная экспрессия генома как фактор реализации генетических программ развития. Тотипотентность растительной клетки.
Системы регуляции функций целого растения: трофическая, гормональная, электрическая. Доминирующие центры и физиологические градиенты. Системы восприятия и передачи сигналов. Системы связей и регуляторных контуров. Элементы теории сложных систем и их приложение к анализу систем регуляции в растении.
Механизм регуляции ростовых процессов. Фитогормоны (ауксины, гиббереллины, цитокинины, абсцизовая кислота, этилен, брассиностероиды), их строение, биосинтез, транспорт, физиологическое действие. Молекулярные основы действия гормонов и ингибиторов роста растений. Взаимодействие между различными гормонами. Синтетические регуляторы и ингибиторы роста (гербициды, ретарданты, морфактины), их практическое применение.
Ростовые и тургорные движения растений. Тропизмы (фото-, гео-, электро-, термотропизмы). Гормональная природа тропизмов. Настии. Сейсмонастические движения.Раздражимость; фитохромная и криптохромная системы; электрофизиологические процессы.
Жизненный цикл высших растений. Основные этапы онтогенеза (эмбриональный, ювенильный, репродуктивный, зрелости, старения), их морфологические, физиологические и метаболические особенности. Состояние покоя у растений. Типы покоя и их значение для жизнедеятельности растений.
Механизмы морфогенеза растений. Индукция генетических программ, морфогенетические градиенты и ориентация клеток в пространстве. Целостность и коррелятивное взаимодействие органов. Физиологические и молекулярные основы эмбриогенеза растений. Созревание и прорастание семян как фазы морфогенеза.
Внутренние и внешние факторы, определяющие переход растений от вегетативного развития к генеративному. Индукция цветения. Яровизация. Фотопериодизм. Роль фитохромной системы в фотопериодических реакциях. Типы фотопериодической реакции. Природа флорального стимула. Гипотезы о бикомпонентной природе флоригена, о многокомпонентном контроле цветения. Цветение как многоступенчатый процесс. Эвокация цветения и ее регуляция. Модель переключения генной активности. Закладка и рост соцветий и цветка. Оплодотворение.
Детерминация пола. Генетические, фенотипические и гормональные факторы, определяющие пол у растений.
Физиология вегетативного размножения. Размножение клубнями, луковицами, корневищами, усами, отводками и черенками.
Культура изолированных зародышей, органов, тканей, клеток, протопластов как модель для изучения процессов роста и развития. Биология изолированных клеток и тканей, клеточная биотехнология. Использование метода культуры клеток для изучения биологии клетки и понимания взаимоотношений части и целого при функционировании клеток в растительном организме.
Пути практического использования культуры растительных клеток (освобождение от вирусных инфекций, массовое размножение, сохранение генофонда редких видов, получение биомассы клеток-продуцентов практически важных веществ.
Устойчивость растений к неблагоприятным факторам
Устойчивость как приспособление растений к условиям существования. Ответные реакции растений на действие неблагоприятных факторов. Общие принципы адаптивных реакций растений на экологический стресс (изменение экспрессии генов и включение синтеза стрессовых, мембранных, структурных белков; перестройки мембранных систем и физиологических процессов; синтез протекторных соединений и др.). Биохимическая адаптация. Пути повышения устойчивости растений.
Реакция растений на температуру. Влияние низких положи тельных температур (холодоустойчивость растений), низких отрицательных температур (морозоустойчивость растений) и почвенно-климатических факторов (зимостойкость растений), высоких положительных температур (жароустойчивость растений). Закаливание растений.
Реакция растений на водный дефицит (засухоустойчивость растений). Атмосферная и почвенная засуха. Приспособление различных ксерофитных форм и мезофитных растений к низкому водному потенциалу и гигрофитов - к гипоксии. Пути адаптации растений к гипои аноксии.
Реакция растений на высокое содержание солей в почве (солеустойчивость растений). Типы засоления почв. Классификация растений по отношению к засолению почв. Механизмы адаптации галофитных организмов к солям. Особенности загрязнения почв тяжелыми металлами. Токсичность их для высших растений.
Радиоустойчивость растений и ее механизмы.
Загрязнение атмосферы сернистым газом, оксидами азота и углерода, соединениями фтора и др. Токсичность их действия на растения. Формирование устойчивости к газам (регулирование их поступления, поддержание внутриклеточного гомеостаза, детоксикация образующихся ядов).
Физиологические и биохимические основы устойчивости высших растений к патогенным микроорганизмам и другим биотическим факторам. Конституционные и индуцированные защитные свойства. Приобретенный (индуцированный) иммунитет.
www.berl.ru











