Учебно- исследовательская работа "Исследование влияния пигментов на окрас растений". Пигменты растений таблица
Изучение растительных пигментов в рамках школьной программы изучения биологии
Введение
Природа обладает удивительным многоцветием. Мы не устаем восхищаться красотой окружающего растительного мира. Весной мы с надеждой смотрим на нежно-зеленые молодые листочки деревьев, а желто-оранжевая цветовая гамма осеннего леса навевает грусть и печаль по ушедшему лету. Кто не восхищался красками цветущего луга, лесной опушки, осенней листвы, даров сада и огорода? Я думаю, что каждый ребенок, как только он начинает изучать окружающий мир, задает себе вопросы: «Почему листья зеленые? Почему они осенью желтеют или краснеют? Почему лепестки ромашки белые, а розы - красные? Почему окружающие растения окрашены именно так, а не иначе, как возникает такое богатство цветов и оттенков? Что для природы значат эти цвета?». Меня заинтересовали эти вопросы, надеюсь, что моя работа поможет на них ответить.
Цель моей работы – выяснить, от чего зависит цвет растения.
Задачи, которые я перед собой поставила:
Изучить литературу с целью выяснить, какие вещества придают органам растения различную окраску.
Провести несколько практических опытов с целью выявления особенностей этих веществ.
Что такое «пигмент»? Какие бывают пигменты?
Изучив специальную литературу, я выяснила, что окраску различным органам растений придают особые вещества – пигменты. Это органические соединения, присутствующие в клетках и тканях растений и окрашивающие их.Многие из них важны для фотосинтеза. Расположены пигменты в пластидах клетки – хлоропластах и хромопластах, некоторые находятся в клеточном соке растений.
Существует несколько основных групп растительных пигментов:
Самыми распространенным растительным пигментом является хлорофилл. Это одно из самых важных на Земле красящих веществ. Название хлорофилла идет от греческих слов «хлорос» - зеленый и «филлон» - лист. Хлорофилловые пластиды зеленые. Зеленый цвет – цвет жизни. Зеленые «фабрики» вокруг нас поддерживают жизнь. Хлорофилл обладает жизненно важной функций: перехват солнечных лучей и преобразование полученной энергии в питательные вещества — простые сахара, которые получаются из воды и углекислого газа. Эти сахара являются основой питания растений — источниками углеводов, необходимых для роста и развития. Во время процесса производства питательных веществ хлорофилл разрушается, так как непрерывно используется. Несмотря на это, в течение сезона роста, растения снова и снова восстанавливают запасы хлорофилла. Большой запас хлорофилла позволяет листьям оставаться зелёными.Возрастные изменения хлоропластов сопровождаются изменением окраски – от салатно-зеленого, разной интенсивности зеленого, до желто-зеленого. Когда он в большом количестве содержится в клетках, что происходит во время периода роста, зелёный цвет хлорофилла преобладает, затмевая цвета любых других пигментов, которые могут содержаться в листе. Поэтому листья летом имеют характерный зелёный цвет.
Флавоны и флавонолы – одни из самых распространенных растительных пигментов. Нет растения, где бы они ни были обнаружены. Долгое время считалось, что эти пигменты характерны только для растительного царства, однако в 90-х годах прошлого века некоторые флавоны были обнаружены и в грибах. На латинском языке «flavus» означает «желтый». В природе флавоны и флавонолы являются основными пигментами, обеспечивающими желтую цветовую гамму плодов и цветов. Много этих красителей и в других органах растений, хотя там желтая окраска маскируется другими пигментами. Разнообразие оттенков желтого цвета достигается как изменением концентрации флавонов и флавонолов, так и присутствием в соке растений солей кальция и магния, увеличивающих интенсивность окраски.
Близки к флавонам по строению другие красители желтого цвета – халконы и ауроны. Встречаются они значительно реже. Среди известных нам растений эти пигменты можно обнаружить в листьях и цветах кислицы, кореопсиса и львиного зева. Как и некоторые люди, эти красители совершенно не переносят курильщиков и краснеют, если их окуривать сигаретным дымом. Отдельного упоминания заслуживают халконы еще и потому, что во многих случаях именно из них в процессе биосинтеза в растениях образуются флавоны, флавонолы и ауроны. Подражая природе, химики применяют халконы для получения разнообразных растительных и искусственных пигментов в лабораторных условиях.
Еще одна группа пигментов, родственная флавонам и флавонолам, носит название антоцианов. Антоцианы, которые ответственны за красные цвета в листьях, не присутствуют в листьях до тех пор, пока в листьях не начнёт снижаться уровень хлорофиллов. Раньше предполагали, что антоцианы просто результат разрушения зелёного хлорофилла, но эта теория уже не считается общепризнанной. Антоциановые пигменты, вызывающие розовую, красную и пурпурную осеннюю окраску листьев, связаны с веществом - углевод (или сахара, крахмала). Так накопление углеводов способствует образованию клеточного сока с пигментами антацина. Антоцианы растворимы в воде и обычно встречаются в клеточном соке.
Каротиноиды – пигменты, которые имеют преимущественно жёлтый или оранжевый цвет. Они всегда присутствуют в листьях, но перекрываются зелёным цветом хлорофилла. Название пигментам этого типа дал ученый М. С. Цвет. В честь одного из пигментов, содержащегося в оранжевых корнях моркови, он назвал весь этот класс красителей каротиноидами («carotte» – морковь).Каротиноиды придают желтый цвет цветам и листьям растений. Желтая, оранжевая и красная окраска кукурузы, тыквы, кабачков и перезрелых огурцов, баклажанов, паслена, помидора, дыни, а также многих цитрусовых обусловлена присутствием в них разнообразных каротиноидных пигментов. Рекордсменом по числу каротиноидных пигментов является стручковый красный перец.
Какие пигменты составляют окраску листа?
Первый опыт проведем с целью выяснить, какие пигменты обеспечивают листьям растения зеленую окраску.Оборудование, необходимое для проведения опыта: свежие листья комнатных растений, 95% -ый этиловый спирт, бензин, ступка фарфоровая, пробирка, воронка, ножницы, фильтровальная бумага.
Ход опыта. Прежде всего, получим вытяжку пигментов. Лучше, если вытяжка будет концентрированной, темно-зеленой. Можно использовать листья любых травянистых растений, а лучше всего теневыносливых комнатных растений - они мяче, легче растираются, содержат больше хлорофилла. К измельченным листьям добавим 5-10 мл этилового спирта, на кончике ножа мел для нейтрализации кислот клеточного сока и разотрем их в фарфоровой ступке до однородной зеленой массы. Подольем еще этилового спирта и осторожно продолжаем растирание, пока спирт не окрасится в интенсивный зеленый цвет. Полученную спиртовую вытяжку отфильтруем в чистую сухую пробирку или колбу.Убедимся в том, что спиртовая вытяжка пигментов помимо зеленых содержит еще и желтые пигменты. Для этого на фильтровальную бумагу нанесем стеклянной палочкой каплю спиртовой вытяжки пигментов листа. Через 3-5 мин на бумаге образуются цветные концентрические круги: в центре зеленый (хлорофилл), снаружи - желтый (каротиноиды) (Приложение 1).
Вывод. Разделение пигментов обусловлено их различной адсорбцией (поглощением в поверхностном слое) на фильтровальной бумаге и неодинаковой растворимостью в растворителе, в данном случае - этиловом спирте. Каротиноиды хуже, по сравнению с хлорофиллом, адсорбируются на бумаге, больше растворимы в спирте, поэтому передвигаются по фильтровальной бумаге дольше хлорофилла.Таким образом, в создании цвета листа участвуют две группы пигментов - зеленые и желтые. Содержание хлорофилла в сформировавшихся листьях примерно в 3 раза выше, чем каротиноидов, поэтому желтый цвет каротиноидов маскируется зеленым цветом хлорофилла. Количественное соотношение хлорофилла и каротиноидов не постоянно, оно зависит от возраста листа, физиологического состояния растения. Если содержание хлорофилла уменьшается, листья приобретают желто-зеленый или желтый цвет.
При каком освещении желтеют листья?
Различные факторы внешней среды (освещенность растений, температура воздуха, водоснабжение) оказывают влияние на окраску листьев. Например, в зависимости от погодных условий цвет листьев клена меняется от желтого до пурпурно-красного.
Цель этого опыта –установить устойчивость хлорофилла в листьях растений без освещения.
Оборудование: для опыта нужны листья любого растения, которые уже закончили рост, но еще не имеют внешних признаков старения, стакан, черный лист бумаги.
Ход опыта. Половину листовой пластинки закрываем с двух сторон черной бумагой. Лист помещаем в стакан с водой и ставим в хорошо освещенное место. Спустя 4-5 дней снимем бумагу, сравним цвет половинок листа. Хорошо заметны различия в окраске: освещенная часть зеленая, а затемненная - желтая.
Вывод: Результаты опыта свидетельствуют, что снижение интенсивности и продолжительности освещения листьев ускоряет распад молекул хлорофилла в хлоропластах. Мы сравнили устойчивость хлорофилла в листьях бадана и традесканции. Самый неустойчивый пигмент в листьях традесканции, он разрушается за 20 дней, а самый устойчивый у фикуса, разрушается через 40 - 50 дней.(Приложение 1)
Необходимость кислорода для разрушения хлорофилла.
Для разрушения хлорофилла необходимо еще одно условие – кислород. Проводимый опыт ставит своей целью доказать, что без кислорода хлорофилл не разрушается или разрушается медленнее.
Оборудование: стакан c водой, лист плотной бумаги, зеленые листья растения.
Ход опыта: Стареющий, но еще сохранивший зеленый цвет лист любого светолюбивого растения опустим в стакан с водой так, чтобы только половина листа его находилась под водой. Для этого закрепим лист в прорези укрывающей стакан плотной бумаги. Стакан поставим в темное место.
Вывод: Через 3 - 5 дней станут заметны различия в окраске листа: находившаяся в воде часть сохранит зеленый цвет, другая - пожелтеет. Уменьшение скорости распада хлорофилла в той части листа, которая находилась в воде, свидетельствует, что в разрушении хлорофилла важную роль играет процесс дыхания. Содержание кислорода в воде намного ниже, чем в воздухе.(Приложение 2)
Влияние на хлорофилл химических веществ.
Как органическое вещество, пигмент хлорофилл должен разрушаться от воздействия различных химических веществ. Цель этого опыта – проверить, как воздействует на хлорофилл соляная кислота.
Оборудование: Для опыта нужны "чернила" - 10%-ая соляная кислота, листья растений, палочка.
Ход опыта: Заостренный конец палочки смочим в соляной кислоте и нанесем на лист рисунок (в нашем случае это смайлик и звездочка). На зеленом фоне листа бегонии постепенно появляется рисунок звездочки бурого цвета. На листе монстеры был нарисован смайлик, но картинка не появилась, бурое пятно было маленьким, размером с копеечную монету. Значит, скорость изменения цвета в месте нанесения кислоты зависит от плотности покровов листа. Появление бурой окраски обусловлено проникновением кислоты внутрь клеток и образованием в них особого вещества - феофитина.
Вывод: Хлорофилл разрушается при воздействии на него соляной кислоты, а значит, и других кислот. Следовательно, газообразные выделения промышленных предприятий, которые часто содержат в себе химические вещества (например, сернистый ангидрит), которые, проникая через устьица в листья, растворяются в цитоплазме клеток и образуют кислоту. Накопление ее в больших количествах в цитоплазме вызывает разнообразные нарушения обмена веществ в клетках, в том числе и разрушение хлорофилла. Внешне такие повреждения могут выражаться в появлении на листьях бурых пятен.(Приложение 3)
Воздействие на пигмент хлорофилл высокой температуры.
Образование феофитина в листьях многих растений может происходить также и при нагревании листа выше 70 - 80 С. Цель данного опыта –показать, что разрушение хлорофилла и образование феофитина в листьях растений возможно и при воздействии на клетки листьев высокой температуры.
Оборудование: Для опыта нужны зеленые листья различных растений, спиртовка, стеклянная палочка.
Ход опыта: Прикоснемся к листу концом сильно нагретой стеклянной палочки или проколем его раскаленной препаровальной иглой. Во всех случаях возникают своеобразные изменения окраски листа: зеленые круги с неровными бурыми кольцами.
Вывод: Появление бурых колец обусловлено поступлением кислот клеточного сока из вакуолей в цитоплазму, а затем в хлоропласты. Под действием температуры раскаленной стеклянной палочки происходит разрушение молекул хлорофилла, образование феофитина и появление бурого окрашивания. Поскольку химический состав листьев различных растений имеет свои особенности, можно получить различные картины колец отмирания. Желтые, коричневые пятна отмирания появляются на листьях и в природных условиях под влиянием сильного перегрева, засухи.(Приложение 5)
Выводы.
Исследовав вопрос о растительных пигментах, я узнала, что пигменты играют очень значительную роль в природе и имеют огромное значение для жизни на Земле. Многие природные пигменты принимают участие в важных метаболических или физиологических процессах. Особенно детально изучено значение хлорофилла и других пигментов в фотосинтезе. Во многих случаях, однако, единственной известной функцией пигмента является то, что он придает окраску организму или той его части, которая содержит данный пигмент. В растительном царстве ярко окрашенные цветки и плоды, контрастно выделяющиеся на общем фоне зеленой окраски листвы, привлекают внимание насекомых и других животных. Благодаря этому растения извлекают для себя пользу при опылении и распространении семян. По итогам работы были установлены следующие выводы:
В создании цвета листа участвуют различные группы пигментов.
Снижение интенсивности и продолжительности освещения листьев ускоряет распад молекул хлорофилла в хлоропластах.
Уменьшение скорости распада хлорофилла в той части листа, которая находилась в воде, свидетельствует, что в разрушении хлорофилла важную роль играет процесс дыхания.
Хлорофилл разрушается при воздействии на него кислоты
Под действием температуры происходит разрушение молекул хлорофилла и появление бурого окрашивания.
Список литературы и Интернет-ресурсов.
Энциклопедия для детей. Биология; "Аванта +", М., 1993.
Биология. Первое сентября. № 44, 45, 46, 1999.
http://ru.wikipedia.org – Википедия.
http://lib.e- science.ru – Портал Естественных наук.
Приложения.
Приложение 1. Какие пигменты составляют окраску листа?






Приложение 2.При каком освещении желтеют листья?


Приложение 3. Необходимость кислорода для разрушения хлорофилла.



Приложение 4. Письмо на зеленом листе.






Приложение 5. Образование колец отмирания на листьях.



xn--j1ahfl.xn--p1ai
| Пигменты — органические соединения, присутствующие в клетках и тканях растений и окрашивающие их.Расположены пигменты в ХЛОРОПЛАСТАХ и хромопластах. Известно более 150 стойких пигментов. Многие из них важны для ФОТОСИНТЕЗА и являются источником витамина А. Аротиноиды- окрашивают растения в желтый, оранжевый или красный цвет. Флавоны и флавонолы – одни из самых распространенных растительных пигментов. Нет растения, где бы они ни были обнаружены.В природе флавоны и флавонолы являются основными пигментами, обеспечивающими желтую цветовую гамму плодов и цветов. Много этих красителей и в других органах растений, хотя там желтая окраска маскируется другими пигментами. Разнообразие оттенков желтого цвета достигается как изменением концентрации флавонов и флавонолов, так и присутствием в соке растений солей кальция и магния, увеличивающих интенсивность окраски. Халконы и ауроны- другие красители желтого цвета – близки по строению к флавонам. Встречаются они значительно реже. Среди известных нам растений эти пигменты можно обнаружить в листьях и цветах кислицы, кореопсиса и львиного зева. Как и некоторые люди, эти красители совершенно не переносят курильщиков и краснеют, если их окуривать сигаретным дымом. Отдельного упоминания заслуживают халконы еще и потому, что во многих случаях именно из них в процессе биосинтеза в растениях образуются флавоны, флавонолы и ауроны. Меланин — пигмент, встречающийся как в клетках растений, так и животных. В частности, он придаёт чёрный и коричневый цвет волосам. Отсутствие меланина в клетках делает животных и человека альбиносами. Структура молекул меланина жидкокристаллическая. Пигмент является сильным антиоксидантом. Синтетически продуцированный меланин в водных растворах оказывает на растение удивительные свойства — ускоряет рост и созревание плодов, редуцирует деятельность камбия, ускоряет прорастание семян. В организме животных меланин обладает иммуномодулированием и генопротекторной защитой. В растениях содержится в кожуре красных сортов винограда, лепестках некоторых цветков. Фитохром- голубой растительный пигмент белкового строения, контролирует процессы цветения и прорастания семян. У одних растений ускоряя цветение, у других — задерживая. Фитохром играет роль «биологических часов» растения, механизм действия пока не изучен. Известно, что строение пигмента меняется в зависимости от светлого и тёмного времени суток, сигнализируя об этом растению. Phyton — от греческого растение, сhrom — цвет, краска. Обнаружил меланин американский учёный — биохимик У. Батлер в проросшем в темноте турнепсе, в его семядолях. Это вåщество регулирует синтез белковых молекул (ДНК, РНК), образование хлорофилла, каротиноидов, антоцианов, органических фосфатов, витаминов. Если хлорофилл можно сравнить со схожими по строению клетками крови — эритроцитами, то фитохром подлежит образному сравнению с мозгом и памятью растения. Фитохром связан с клеточными мембранами и встречается практически во всех органах растения. Антоцианы — придают растениям окраску в диапазоне от розовой, красной, сиреневой, до синей и тёмно-фиолетовой. Антоцианы образуются в процессах гидролиза крахмала и по своему происхождению являются безазотистыми соединениями, близким к глюкозидам — соединениям сахара с неуглеводной частью. Усиленное образование антоцианов в клетках растения происходит при снижениях температур окружающей среды, при остановках синтеза хлорофилла, при интенсивном освещении УФ-лучами, при недостатке фосфора, необходимого для ввязывания гидролизованных крахмалом сахаров. При этом окраска листьев растений изменяется от зелёных до красных и синих цветов. Антоцианы хорошо растворимы в воде и присутствуют в соке вакуолей. Диапазон цветов изменяется благодаря наличию в растении всего трёх моделей антоцианов, различных между собой числом гидроксильных групп. Вариации в пропорциях этих пигментов в растениях дают разную окраску лепестков. В зависимости от кислотности (рН) среды сока вакуолей, антоциан придаёт ту или иную окраcку. В кислой среде он обычно имеет красные тона, например, у герани, гортензии, фиалок. В щелочной эти растения приобретают сине-голубые тона. Если же к синему или фиолетовому раствору антоциана прибавить кислоту, раствор снова станет розовым. Опытным путём это легко проверить на растениях, подбирая в качестве подкормок те или иные микроэлементы, изменяющие кислотность жидкости вакуолей. Если к нейтральному раствору антоциана добавить очень слабый щелочной раствор — получается голубое окрашивание, при более концентрированном растворе щелочи окрашивание перейдёт в жёлто-зелёное. Красная окраска — у маков, роз, герани, синяя — у васильков, голубая — у колокольчиков обусловлена наличием пигмента антоциана. Плоды винограда, слив, терна, краснокочанной капусты, свеклы окрашены антоцианом. Считается, что антоциан защищает растения от низких температур, от вредного воздействия солнечного цвета на цитоплазму. Антохлор — пигмент жёлтого цвета. Встречается в клетках кожици лепестков первоцвета (баранчики, примула), льнянки, жёлтого мака, георгины, в плодах лимонов и других растениях. Антофеин — редко встречающийся пигмент тёмного цвета. Вызывает окраску пятен на крыльях венчика у русских бобов (Faba vulgaris). Каротиноиды — содержатся в растениях, устойчивых к пониженным температурам. Когда хлорофилл исчерпывается в холодное время года, листья приобретают заметную жёлтую или оранжевую окраску за счёт пролонгированного действия пигмента каротиноида. Каротиноиды защищают растения от пагубного действия солнечного света, принимая УФ-излучения солнца на себя, трансформируя в энергию и передавая её хлорофиллу. С помощью такой передачи хлорофилл регулирует процессы фотосинтеза. В доказательство того, что каротиноиды присутствуют в листьях постоянно наравне с хлорофиллом, послужит следующий эксперимент: к спиртовой вытяжке хлорофилла прилить бензина 1:1, взболтать смесь и дать отстояться, смесь расслоится. Нижний слой из спирта имеет жёлтую окраску и содержит жёлтый пигмент ксантофилл. Верхний бензиновый слой зелёного цвета и содержит хлорофилл и каротин. Оранжево-красный цвет растениям даёт пигмент каротин, жёлтую — ксантофилл. Эти пигменты имеют белково-липоидную основу. Эти пигменты обнаружены в плодах помидоров, апельсинов, мандаринов, в корне моркови. Основная роль этих пигментов- придать растениям яркую привлекательную окраску, привлекая птиц и животных для разнесения семян. Цветы с оранжево-жёлтой окраской — лютик, настурция. Эфирные масла растений — представляют собой чаще бесцветные или желтоватые прозрачные жидкости, чуть реже — темно-коричневые, красные, зеленые или синие, зеленовато-синие. Запах эфирных масел всегда специфический и ароматный. Вкус у эфирных масел — пряный, острый, жгучийи зависит от растения, из которого они получены. Плотность большинства эфирных масел меньше единицы, а некоторые, например, гвоздичное масло тяжелее воды. Эфирные масла практически не растворимы в воде. Если взбалтать эфирное масло с водой образуется эмульсия, и вода приобретает специфический запах и вкус эфирного масла. Почти все эфирные масла хорошо растворимы в спирте, в жирных маслах, в минеральных маслах и смешиваются во всех пропорциях с хлороформом, эфиром. Реактив Судан III окрашиваетэфирные масла растений в оранжевый цвет. Температура кипения эфирных масел составляет от 40 0С, причем фракция монотерпенов кипит при 150-190 0С, фракция сесквитерпенов при 230-300 0С. Эфирные масла растений оптически активны. Реакция масел нейтральная или слегка кислая. Эфирные масла растений перегоняются с водяным паром, причем монотерпены перегоняются хорошо, сесквитерпены – хуже. При охлаждении эфирных масел некоторые компоненты выкристаллизовываются (ментол, тимол, камфора). Твердую часть эфирного масла называют стеароптен, жидкую – элеоптен. |
www.ronl.ru
Пигменты окраски листьев растений
«Лес, точно терем расписной, лиловый, золотой, багряный»
Изменение окраски листьев – одна из первых примет осени. Много ярких красок в осеннем лесу! Березы, ясени и липы желтеют, розовеют листья бересклета, пунцово-красными становятся узорные листья рябины, оранжевыми и багряными листья осин. Чем же обусловлено это цветовое многообразие?
В листьях растений наряду с зеленым хлорофиллом содержатся другие пигменты. Для того чтобы убедиться в этом, проделаем простой опыт. Прежде всего приготовим вытяжку хлорофилла, как это было описано нами выше. Вместе с хлорофиллом в спирте находятся также желтые пигменты. Чтобы разделить их, небольшое количество спиртовой вытяжки (около двух миллилитров) нальем в пробирку, добавим две капли воды и около 4 миллилитров бензина. Вода вводится для того, чтобы легче происходило расслоение двух жидкостей. Закрыв пробирку пробкой или пальцем, следует энергично встряхнуть ее. Вскоре можно заметить, что нижний (спиртовой) слой окрасился в золотисто-желтый цвет, а верхний (бензиновый) – в изумрудно-зеленый. Зеленая окраска бензина объясняется тем, что хлорофилл лучше растворяется в бензине, нежели в спирте, поэтому при встряхивании он обычно полностью переходит в бензиновый слой.
Золотисто-желтая окраска спиртового слоя связана с присутствием ксантофилла, вещества, нерастворимого в бензине. Его формула С40Н56О2. По химической природе ксантофилл близок к каротину, присутствующему в корнях моркови, – С40Н56, поэтому их объединяют в одну группу – каротиноидов. Но каротин также имеется в листьях зеленых растений, только он, как и хлорофилл, лучше растворяется в бензине, поэтому мы не видим его: интенсивно-зеленая окраска хлорофилла «забивает» желтый цвет каротина, и мы не различаем его, как ранее ксантофилл в спиртовой вытяжке. Чтобы увидеть каротин, нужно преобразовать зеленый пигмент в соединение, нерастворимое в бензине. Этого можно достигнуть с помощью щелочи. В пробирку, где произошло отделение ксантофилла, добавим кусочек щелочи (КОН или NаОН). Пробирку закроем пробкой и тщательно взболтаем ее содержимое. После расслоения жидкостей можно увидеть, что картина распределения пигментов изменилась: нижний спиртовой слои окрасился в зеленый цвет, а верхний – бензиновый – в желто-оранжевый, характерный для каротина.
Эти опыты наглядно свидетельствуют о том, что в зеленом листе одновременно с хлорофиллом присутствуют желтые пигменты – каротиноиды. При наступлении холодов образования новых молекул хлорофилла не происходит, а старые быстро разрушаются. Каротиноиды же устойчивы к низким температурам, поэтому осенью эти пигменты становятся хорошо заметными. Они и придают листьям многих растений золотисто-желтый и оранжевый оттенок. Каково же значение каротиноидов в жизни растений? Установлено, что эти пигменты защищают хлорофилл от разрушения светом. Кроме того, поглощая энергию синих лучей солнечного спектра, они передают ее на хлорофилл. Это позволяет зеленым растениям более эффективно использовать солнечную энергию для синтеза органического вещества.
Осенний лес окрашен, однако, не только в желтые тона. С чем связана лиловая и багряная окраска листьев? Наряду с хлорофиллом и каротиноидами в листьях растений имеются пигменты, которые носят название антоцианов. Они хорошо растворимы в воде и содержатся не в цитоплазме, а в клеточном соке вакуолей. Эти пигменты очень разнообразны по окраске, которая зависит в основном от кислотности клеточного сока. В этом легко убедиться на опыте.
Прежде всего приготовьте вытяжку антоцианов. С этой целью листья бересклета или какого-то другого растения, окрашенные осенью в красные или фиолетовые тона, измельчите ножницами, поместите в колбочку, прилейте воды и нагрейте на спиртовке Вскоре раствор станет красновато-синим от присутствия антоцианов. Полученную вытяжку пигментов налейте в две пробирки. В одну добавьте слабой соляной или уксусной кислоты, а в другую – раствор аммиака. Под действием кислоты раствор станет розовым, тогда как в присутствии щелочи – в зависимости от количества и концентрации этой щелочи – зеленым, синим и желтым. Антоцианы, как и каротиноиды, более устойчивы к низким температурам, чем хлорофилл. Поэтому они и обнаруживаются в листьях осенью. Исследователи установили, что образованию антоцианов способствуют высокое содержание Сахаров в растительных тканях, сравнительно низкая температура и интенсивное освещение.
Увеличение содержания сахаров в осенних листьях происходит за счет гидролиза крахмала. Это имеет важное значение для транспортировки ценных питательных веществ из отмирающих листьев во внутренние части растений. Ведь сам крахмал нетранспортабелен в растении. Однако скорость оттока образующихся в результате его гидролиза Сахаров из листьев при низких температурах невелика. Кроме того, при падении температуры ослабляется дыхание растений и, следовательно, лишь незначительное количество Сахаров подвергается окислению. Все эти факторы благоприятствуют накоплению в растительных тканях Сахаров, которые начинают использоваться в синтезе других веществ, в частности антоцианов.
О превращении избытка сахаров в антоцианы свидетельствуют и другие факты. Если у виноградной лозы путем кольцевания (удаление части коры в виде кольца) затруднить отток продуктов фотосинтеза, то листья, расположенные выше кольца, через две-три недели приобретают красный цвет из-за накопления антоцианов. При этом их образуется так много, что зеленая окраска хлорофилла становится незаметной.
То же самое наблюдается не только при понижении температуры или кольцевании, но и при недостатке фосфора. Если, например, томаты выращивать на питательном растворе, лишенном этого элемента, то нижняя часть листьев, а также стебли приобретают синий цвет. Дело в том, что при отсутствии фосфора в растениях не может осуществляться процесс окисления Сахаров без соединения с остатком фосфорной кислоты молекула сахара остается неактивной. Поэтому в растительных тканях происходит накопление избыточных количеств Сахаров, которые используются на синтез антоцианов. Увеличение содержания этих веществ ведет к посинению стеблей и листьев растений, испытывающих нехватку фосфора.
Образование антоцианов зависит также от интенсивности света. Если осенью внимательно приглядеться к яркой окраске деревьев и кустарников, то можно заметить, что багряный цвет имеют в основном те листья, которые лучше всего освещены. Раздвиньте пылающий огненными красками куст бересклета, и вы увидите внутри желтые, бледно-желтые и даже зеленые листья. Во время дождливой и облачной осени листва дольше сохраняется на деревьях, однако она не так ярка из-за недостатка солнца. Преобладают желтые тона, обусловленные присутствием каротиноидов, а не антоцианов. Низкая температура также способствует образованию антоцианов. Если стоит теплая погода, то лес изменяет свою окраску медленно, но едва ударит морозец, как сразу запылают осины и клены. М.М. Пришвин в миниатюре «Светильники осени» писал: «В темных лесах загорелись светильники осени, иной лист на темном фоне так ярко горит, что даже больно смотреть. Липа стоит уже вся черная, но один яркий лист ее остался, висит, как фонарь, на невидимой нити и светит».
Радуга флоры
Уж коли мы заговорили о пигментах растений, следует рассказать и о причинах разнообразия окраски цветков. Зачем цветкам их яркая, сочная окраска? В конечном счете для того, чтобы привлечь к себе насекомых-опылителей. Многие растения опыляются лишь определенными видами насекомых, поэтому окраска цветков часто зависит от того, для каких именно насекомых предназначены цветовые сигналы. Дело в том, что в отношении цвета насекомые бывают довольно капризны. Скажем, пчелы, шмели, осы предпочитают розовые, фиолетовые и синие цветки, а около желтых обычно толкутся мухи. Красный же цвет многие насекомые, наделенные не слишком совершенным зрением, путают с темно-серым. Поэтому в наших широтах чисто-красные цветки довольно редки. Исключение – мак, но и его лепестки имеют примесь желтого цвета; обычно именно этот оттенок и замечают пчелы. Лучше других насекомых красный цвет различают бабочки – они-то, как правило, и опыляют красные цветки наших широт, например гвоздики. А вот среди тропических растений красный цвет более распространен, и отчасти это связано с тем, что опыляют их цветки не насекомые, а птицы: колибри или нектарницы, у которых зрение более развито.
Бывает, что у одного и того же растения окраска цветков с возрастом изменяется. Это хорошо заметно у ранневесеннего растения медуницы: розовый цвет ее молодых цветков сменяется по мере старения синим. Старые цветки медуницы пчелы уже не посещают: они, как правило, опылены и нектара не содержат. И в этом случае смена окраски служит сигналом для насекомых – не теряйте времени даром! А вот у гилии (США) – красивого растения из семейства синюховых, родственницы флоксов, произрастающей в горах штата Аризона (США), цветки первоначально имеют алый цвет, который, как уже отметили, привлекает птиц. Но когда колибри покидают горы, гилия меняет окраску вновь появляющихся цветков: они становятся бледно-красными или даже белыми.
Окраска большинства цветков определяется присутствием различных пигментов. Самые распространенные – каротиноиды, растворимые в жирах соединения: каротин, его изомеры и производные. В растворе все они имеют бледно-желтую, оранжевую или светло-красную окраску. Названия каротиноидов, содержащихся только в цветках, столь же красивы, как и придаваемая ими окраска: эшшольксантин, петалоксантин, газанияксантин, ауроксантин, хризантемаксантин, рубихром.
Наряду с каротиноидами окраску цветков определяют и антоцианы. Оттенки этих пигментов очень разнообразны – от розового до черно-фиолетового. Несмотря на такое цветовое многообразие, все антоцианы устроены по одному типу – они представляют собой гликозиды, то есть соединения сахара с неуглеводной частью, так называемым агликоном. Примером может служить красящее вещество, содержащееся в цветках василька, – антоцианин. Его агликон – цианидин – один из самых распространенных, образуется в результате отщепления двух молекул глюкозы от антоциана.
Как уже говорилось, антоциановые пигменты могут изменять свою окраску в зависимости от кислотности среды. Вспомните два вида герани, распространенной в средней полосе: герань лесную и герань луговую. У лесной лепестки розовые или лиловые, а у луговой – синие. Различие в цвете обусловлено тем, что сок герани лесной более кислый. Если приготовить водную вытяжку из лепестков герани либо лесной, либо луговой – и изменить ее кислотность, то в кислой среде раствор станет розовым, а в щелочной – синим. Такую же операцию можно проделать и над целым растением. Если цветущую фиалку поместить под стеклянный колпак рядом с блюдцем, куда налит нашатырный спирт (он при испарении выделяет аммиак), то ее лепестки станут зелеными; а если вместо нашатырного спирта в блюдце будет дымящаяся соляная кислота, они окрасятся в красный цвет.
Мы уже говорили, что одно и то же растение медуницы может иметь цветки разной окраски: розовые – молодые и синие – старые. Посинение лепестков по мере их старения можно объяснить индикаторными свойствами антоцианов. Клеточный сок растения, в котором растворен пигмент, имеет кислую реакцию, а цитоплазма – щелочную. Вакуоли с клеточным соком отделены от цитоплазмы мембраной, которая обычно непроницаема для антоцианов. Однако с возрастом в мембране возникают дефекты, и в результате пигмент начинает проникать из вакуолей в цитоплазму. А поскольку реакция здесь иная, меняется и окраска цветков.
Чтобы убедиться в справедливости этой точки зрения, возьмите ярко-красный лепесток какого-то растения, например герани, розы, и раздавите его между пальцами. При этом также произойдет смешение содержимого цитоплазмы и вакуоли, в результате лепесток в месте повреждения посинеет. Впрочем, было бы неправильно связывать окраску антоцианов лишь с их индикаторными свойствами. Исследования последних лет показали, что она определяется и некоторыми другими факторами. Цвет антоциановых пигментов может меняться, например, в зависимости от того, с какими ионами они находятся в комплексе. При взаимодействии с ионами калия комплекс приобретает пурпурную окраску, а с ионами кальция или магния – синюю. Если срезать цветущий колокольчик и поместить его в раствор, содержащий ионы алюминия, то лепестки посинеют. То же самое наблюдается, если соединить растворы антоцианина и соли алюминия.
Многим читателям, возможно, знаком роман Александра Дюма «Черный тюльпан», в котором в остросюжетной форме рассказывается о выведении сорта тюльпана необычного черного цвета. Вот как описывает его автор романа: «Тюльпан был прекрасен, чудесен, великолепен; стебель его восемнадцати дюймов вышины. Он стройно вытягивался кверху между четырьмя зелеными гладкими, ровными, как стрела, листьями. Цветок его был сплошь черным и блестел, как янтарь». Почти пять веков преследовали неудачи садоводов, пытавшихся вывести черный тюльпан. И вот, Фризский институт цветоводства в Гааге сделал официальное заявление о том, что в Голландии черный тюльпан получен в результате последовательного скрещивания двух сортов – «Царица ночи» и «Венский вальс». В работе принимали участие шесть голландских исследовательских центров. Полученный цветок идеален по своим классическим размерам.
Садоводы стремятся создать также черные розы. Выведены такие сорта, которые при неярком освещении действительно кажутся черными (на самом деле они темно-красного цвета). На Гавайских островах растут дикие черные розы. В честь бессмертного произведения Гете «Фауст» садоводы создали сорт анютиных глазок черного цвета под названием «Доктор Фауст». Анютины глазки, как известно, были любимыми цветами – великого немецкого поэта и ботаника.
Черная или почти черная окраска цветков обусловлена присутствием в околоцветнике антоцианов. Кроме каротиноидов и антоцианов, лепесткам могут придавать окраску и другие вещества, в том числе флавоны и флавонолы. А какой пигмент окрашивает в молочный цвет вишневые сады, превращает в снежно-белые сугробы кусты черемухи? Оказывается, никаких белых пигментов в их лепестках нет. Белый цвет придает им. воздух. Если рассмотреть под микроскопом лепесток черемухи или любого другого белого цветка, то можно увидеть множество прозрачных и бесцветных клеток, разделенных обширными пустыми промежутками. Именно благодаря этим заполненным воздухом межклетникам лепестки сильно отражают свет и потому кажутся белыми. А если раздавить такой лепесток между пальцами, то на месте сдавливания появится прозрачное пятно: здесь воздух будет вытеснен из межклетников.
И все же в природе есть белая краска, например, ею окрашена в нарядный белый цвет кора нашей любимой березы. Это красящее вещество так и называется – бетулин, от латинского названия березы – Betula. Заблуждаются те, кто считает, что береза – единственное растение с белой корой. Это не так. В Австралии произрастает эвкалипт затопляемый. Он назван так потому, что растет в руслах пересыхающих рек и в сезон дождей оказывается стоящим в воде. Стволы этих эвкалиптов имеют чисто-белый цвет, эффектно выделяющийся на фоне окружающих зеленых зарослей.
У треххвойной сосны Бунге также белая кора. Это редкий вид, встречающийся в природе в основном в горах Центрального Китая. Растение разводится по всей стране возле дворцов и храмов. Белоствольные сосны производят неизгладимое впечатление. Еще много интересного можно было бы рассказать об окраске растений и о растительных пигментах, которые давно привлекают внимание исследователей всего мира. Более 30 лет назад известный индийский ученый Т.Р. Сешадри, много занимавшийся изучением природных красящих веществ, писал: «Музыка красок более сложна и изменчива по своей природе, нежели музыка звуков. Возможно даже, что в действительности она еще более утонченна, чем мы предполагаем».
Зеленые животные – реальность или фантазия!
В произведениях фантастического жанра нередко можно прочитать о человекоподобных существах зеленого цвета. Зеленая окраска этих организмов, обусловленная хлорофиллом, позволяет им самостоятельно синтезировать органические вещества из неорганических за счет энергии света. Возможно ли такое в природе? Прежде всего следует заметить, что на Земле имеются животные, питающиеся подобным образом. Например, хорошо известная всем биологам эвглена зеленая, часто встречающаяся в застоявшихся лужах. Ботаники считают эвглену водорослью, а зоологи до сих пор по традиции относят ее к животным. В чем дело?
Эвглена свободно передвигается в воде при помощи жгутика. Такой способ передвижения характерен как для ряда простейших животных, так и для некоторых ботанических объектов, например зооспор отдельных видов водорослей. Эвглена содержит хлорофилл, поэтому при интенсивном ее размножении вода в лужах приобретает изумрудно-зеленую окраску. Наличие хлорофилла позволяет ей питаться углекислым газом подобно всем зеленым растениям. Однако, если водоросль перенести в воду, содержащую некоторые органические вещества, то она теряет зеленую окраску и начинает, подобно животным, питаться готовыми органическими веществами. Эвглену все-таки нельзя назвать типичным животным, поэтому поищем других представителей. питающихся, подобно растениям, при помощи хлорофилла.
Еще в середине XIX века немецкий зоолог Т. Зибольд обнаружил в телах пресноводной гидры и некоторых червей хлорофилл. Позднее он был найден в организмах и других животных: гидроидных полипов, медуз, кораллов, губок. коловраток, моллюсков. Выяснено, что некоторые морские брюхоногие моллюски, питающиеся сифоновыми водорослями, не переваривают хлоропласты этих растений, а длительное время содержат их в организме в функционально-активном состоянии. Хлоропласты сифоновых водорослей кодиума хрупкого и кодиума паутинистого, попадая в организм моллюсков, не перевариваются, а остаются в нем.
Попытки освободить моллюсков от хлоропластов, поместив их в темноту на полтора месяца, оказались безуспешными, равно как и выведение их из яиц. Бесхлоропластные личинки моллюсков погибали на ранней стадии развития. Внутри животной клетки хлоропласты плотно упакованы и занимают значительный объем. Благодаря им моллюски, не имеющие раковины, оказываются окрашенными в интенсивно зеленый цвет.
Почему же сифоновые водоросли «полюбились» моллюскам? Дело в том. что в отличие от других зеленых водорослей они не имеют клеточного строения. Их крупное, часто причудливое по форме тела представляет собой одну гигантскую «клетку». Слово «клетка» я взял в кавычки не случайно. Хотя клеточные стенки в теле сифоновых водорослей отсутствуют, вряд ли можно назвать их одноклеточными организмами, скорее это конгломерат не вполне разделившихся клеток. Подтверждением тому служит наличие не одного, а множества клеточных ядер. Такое строение назвали сифонным, а сами водоросли – сифоновыми. Отсутствие клеточных стенок, безусловно, облегчает процесс поглощения водоросли животными клетками.
Ну а каковы хлоропласты этого растения? В теле водоросли содержатся один или несколько хлоропластов. Если их много, они имеют дисковидную или веретеновидную форму. Одиночные обладают сетчатым строением. Ученые считают, что сетчатая структура создается в результате соединения мелких хлоропластов друг с другом.
Многие ученые наблюдали усвоение углекислого газа хлоропластами, находящимися в животных клетках. У свежесобранных моллюсков, элизии зеленой интенсивность фотосинтетического усвоения углекислого газа составляла 55–67% величины, определенной для неповрежденной водоросли кодиума хрупкого, из которого моллюсками были «приобретены» хлоропласты. Любопытно, что и содержание хлорофилла на 1 грамм сырой массы ткани у водоросли и животного было сходным. Благодаря фотосинтезу моллюски фиксировали углекислый газ на протяжении всех 93 дней опыта. Правда, скорость фотосинтеза постепенно ослабевала и к концу эксперимента составляла 20–40% от первоначальной.
В 1971 году ученые наблюдали выделение кислорода в ходе фотосинтеза хлоропластов, налюдящихся в клетках тридакны. Тридакны – типичные обитатели тропических морей. Особенно широко они распространены на коралловых рифах Индийского и Тихого океанов. Великаном среди моллюсков выглядит тридакна гигантская, достигающая иногда длины 1,4 метра и общей массы 200 килограммов. Тридакны интересны для нас своим симбиозом с одноклеточными водорослями. Обычно они так располагаются на дне, чтобы их полупрозрачная мантия, выступающая между створками раковины, была обращена вверх и сильно освещалась солнцем. В ее межклеточном пространстве в большом количестве поселяются зеленые водоросли. Несмотря на значительные размеры, моллюск питается только теми веществами, которые вырабатывают водоросли-симбионты.
В Средиземном море и у берегов Франции в Атлантике встречается червь конволюта, у которого под кожным покровом также обитают зеленые водоросли, осуществляющие синтез органических веществ из неорганических. Благодаря активности своих «квартирантов» червь не нуждается в дополнительных источниках пиши, поэтому желудочно-кишечный тракт у него атрофировался. Во время отлива множество конволют покидает свои норы для того, чтобы принять солнечные ванны. В это время водоросли под их кожей интенсивно фотосинтезируют. Некоторые виды этих червей находятся в полной зависимости от своих поселенцев. Так, если молодой червь не «заразится» водорослями, то погибнет от голода. В свою очередь водоросли, поселившиеся в теле конволюты, теряют способность к существованию вне его организма. «Заражение» происходит с помощью «свежих», не живших еще в симбиозе с червями водорослей в момент, когда личинки червя выходят из яиц. Эти водоросли, по всей вероятности, привлекаются какими-то веществами, выделяемыми яйцами червей.
В связи с рассмотрением вопроса функционирования хлоропластов в клетках животных чрезвычайно большой интерес представляют опыты американского биохимика М. Насса, в которых было показано, что хлоропласты сифоновой водоросли каулерпы, харовой водоросли нителлы, шпината и африканской фиалки захватываются клетками соединительной ткани (так называемыми фибробластами) мышей. Обычно в фибробластах, заглотавших инородное тело (этот процесс ученые называют фагоцитозом), вокруг поглощенной частицы образуется вакуоль. Постепенно чужеродное тело переваривается и рассасывается – исчезает. Когда же в клетки ввели хлоропласты, вакуоли не возникали, а фибробласты даже не пытались их переварить.
Пластиды сохраняли свою структуру и способность к фотосинтезу на протяжении трех недель. Клетки, ставшие из-за их присутствия зелеными, нормально делились. При этом хлоропласты стихийно распределялись по дочерним клеткам. Пластиды, находившиеся в фибропластах около двух дней, а затем вновь выделенные, оставались неповрежденными. Они усваивали углекислый газ с такой же скоростью, с какой фотосинтезировали свежие хлоропласты, выделенные из растений.
Предположим, что в ходе эволюции возникнут такие существа или их обнаружат на других планетах. Какими они должны быть? Ученые полагают, что в таком животном хлорофилл будет сосредоточен в коже, куда свободно проникает свет, необходимый как для синтеза зеленого пигмента, так и для образования органических веществ. «Зеленый человек» должен делать кое-что наоборот: днем, подобно сказочному королю, ходить в невидимой для всех одежде, а ночью, напротив, одеваться, чтобы согреться.
Проблема заключается в том, сможет ли такой организм получать с помощью фотосинтеза достаточно пищи. Исходя из максимально возможной интенсивности фотосинтеза растений в самых благоприятных условиях существования, можно подсчитать, сколько органического вещества сможет образовать зеленая кожа этого человека. Если принять, что 1 квадратный дециметр зеленого растения за 1 час синтезирует 20 миллиграммов Сахаров, то 170 квадратных дециметров человеческой кожи, доступной солнечным лучам, смогут образовать за это время 3,4 грамма. За 12-часовой день количество органического вещества составит 40,8 грамма. В этой массе будет концентрироваться около 153 калорий энергии. Такого количества явно недостаточно для удовлетворения энергетических потребностей человеческого организма, которые составляют 2000–4000 калорий в сутки.
Примем во внимание, что «зеленому человеку» не нужно думать о пропитании и быть слишком деятельным, поскольку пища сама поступает в его организм из хлоропластов кожи. Нетрудно прийти к заключению, что отсутствие физической нагрузки и малоподвижный образ жизни сделают его похожим на обычное растение. Иначе говоря, «зеленого человека» весьма трудно будет отличить от опунции.
Расчеты исследователей показывают: для того, чтобы образовать достаточное количество органического вещества, «зеленый человек» в ходе эволюции должен в 20 раз увеличить поверхность своей кожи. Это может произойти за счет возрастания числа складок и отростков. Для этого ему необходимо будет обзавестись подобием листьев. Если это произойдет, то он станет совсем малоподвижным и еще более похожим на растение.
Таким образом, существование крупных фотосинтезирующих животных и человека на Земле и в космосе едва ли возможно. Ученые полагают, что в любой биологической системе, хотя бы отдаленно напоминающей биосферу Земли, обязательно должны существовать растительноподобные организмы, обеспечивающие пищей и энергией как самих себя, так и животных. Во второй половине XIX столетия было установлено, что энергия солнечного света усваивается и трансформируется при помощи зеленого пигмента хлорофилла.
На основе проведенных опытов можно сказать что, зеленая окраска хлорофилла определяется наличием в нем атома металла вне зависимости от того, будет ли это магний, медь или цинк.Современная наука подтвердила правильность взглядов К.А. Тимирязева относительно исключительной важности для фотосинтеза именно красных лучей солнечного спектра. Оказалось, что коэффициент использования красного света в ходе фотосинтеза выше, чем синих лучей, которые также поглощаются хлорофиллом. Красные лучи, по представлениям К.А. Тимирязева, играют основополагающую роль в процессе мироздания и созидания жизни.
Как известно растения поглощают углекислый газ, который присоединяется к пятиуглеродному веществу под названием рибулезодифосфат, где потом он в дальнейшем участвует во многих других реакциях. Изучение особенностей фотосинтеза у разных растений, безусловно, будет способствовать расширению возможностей человека в управлении их фотосинтетической деятельностью, продуктивностью и урожаем. В целом фотосинтез это один из основополагающих процессов жизни, на котором основана большая часть современной растительной фауны на поверхности земли.
biofile.ru
Получение акварельных красок из растений
Получение акварельных красок из растений
Пономарев Даниил Александрович 11ГБОУ СОШ "ОЦ" с.Лопатино
Глубокова Анастасия Николаевна 11ГБОУ СОШ "ОЦ" с.Лопатино
Текст работы размещён без изображений и формул.Полная версия работы доступна во вкладке "Файлы работы" в формате PDF
Введение
Актуальность: Явления и объекты природы привлекают своей красотой, яркостью красок, разнообразием. Наблюдая за ними, происходит обогащение своего чувственного опыта, на котором и основывается дальнейшее творчество. Немногим известно, что для большинства видов красок, к примеру, акварельных, масляных, гуашевых, темперных – применяется одна и та же материальная основа, не меняющаяся долгие века.
Нам захотелось узнать откуда берутся краски в природе. Можно ли их получить для дальнейшего использования в быту.
Цель: Получение красок из растений
Предмет: получение окрасок
Объект: краски из растений.
Гипотеза: из растений можно получить краски.
Задачи:
Изучить литературу по теме краски.
Получение красок из растений.
Методы исследования:
Теоретические: изучение литературы.
Практические: лабораторные опыты, наблюдение.
Глава 1. Общие сведения
1.1 История открытия красок
Много тысяч лет назад люди научились окрашивать ткани натуральными красителями которые содержатся в некоторых видах животных или в растениях. Растительные пигменты (красители) дают глубокие и мягкие цвета. Ткани, окрашенные такими красителями, при стирке не линяют, не выгорают на солнце, безопасны для здоровья.
О том, какого мастерства достигло красильное ремесло в средние века, можно судить на основании того факта, что, имея в своем распоряжении 5-6 естественных красящих веществ, мастер красильни обеспечивал Императорскую шпалерную мануфактуру шерстяной и шелковой пряжей, окрашенной в 800 обязательных цветов и оттенков.
Узор на ткани, сделанный с помощью красителя индиго (1873 г.) Основным желтым красителем древнего Востока, Греции и Рима был шафран, который и в наше время иногда добавляют в тесто, чтобы придать ему сдобный вид. В Риме шафраном красили улицы, по которым император возвращался с победоносной армией. И позже, в Европе, шафран ценился весьма высоко. Известен даже итало-швейцарский военный конфликт, в котором главным военным приобретением были не земли, золото или прекрасные королевны, а всего лишь... 800 фунтов шафрана. Для получения синего цвета в средние века в европейские странах использовали растение вайду, но затем из южных земель завезли индиго. Французским законом 1563 года этот краситель был отнесен к жизненно необходимым предметам импорта, хотя стоил очень дорого.
Знаменитый пурпур древние добывали из особой улитки багрянки, водившейся в Средиземном море. Ремесленники измельчали ее тело с водой и полученным соком пропитывали ткань. При окислении кислородом воздуха эта жидкость окрашивалась в пурпурный цвет. Из десяти тысяч улиток можно было получить немногим более одного грамма красителя; поэтому он ценился дороже золота. Для получения алого красителя специально разводили насекомое кошениль, паразитирующее на кактусах. Для приготовления грамма красителя требовалось 150 тысяч высушенных насекомых. Самым распространенным красным красителем древности был крапп, который добывали из корня марены. Красящее вещество марены - ализарин, сам по себе он имеет желтый цвет и дает красную окраску только после протравы ткани солями алюминия. Марена широко культивировалась в Европе с давних времен. Специальным декретом Людовика XV под эту культуру были отведены громадные поля на юге Франции. А цыганка Кармен в известной новелле Проспера Мериме насмешливо называет англичан раками потому, что они носили красные, окрашенные мареной, мундиры. Сейчас в промышленности используется огромное количество разных синтетических красителей, но каждый человек может попробовать окрасить ткань самостоятельно природными красками из растений. В тексте ты можешь прочитать информация о том, из каких растений получают красители разных цветов.
1.2. КРАСЯЩИЕ ПИГМЕНТЫ У РАСТЕНИЙ
МОРКОВЬ – каротин (от красного до оранжевого), флавонол (от желтой до оранжевой), флавон (от желтой до оранжевой),
ЛУКОВАЯ ШЕЛУХА - бета–каротин (желто-оранжевый)
СВЕКЛА – антоциан (от розового до темно-синего)
ЕЖЕВИКА – антоциан (от розового до темно-синего), катехин (бесцветный)
МАЛИНА – антоциан (от розового до темно-синего), катехин (бесцветный)
ЧЕРНОПЛОДНАЯ РЯБИНА – антоциан (от розового до темно-синего), флавонол (от желтой до оранжевой), флавон (от желтой до оранжевой), лейкоантоцианы (бесцветный)
КРАСНАЯ СМОРОДИНА – бета-каротин (желто-оранжевый), ретинол (красно-оранжевый)
ЖЕЛТАЯ СМОРОДИНА – хролофилл (зеленый)
Желтые краски
Восковник, невысокий кустарник с большими листьями, распространен на севере.
Крушина - волчьи ягоды, красящее вещество находится в коре; произрастает на всей территории России, Кора некоторых видов крушины в свежем виде дает желтую окраску, а в сухом - коричневую.
Береза - красящее вещество содержится в листьях и молодой коре; листья и кора собираются в начале лета; из листьев получается ярко-желтая краска, из коры - желтоватая.
Золототысячник - трава красит шерсть.
Полынь - трава красит в соломенный и палевый цвет, с квасцами - в лимонный цвет.
Подмаренник - цветы с прибавлением квасцов красят в темно-желтый цвет.
Барбарис - кустарник. Красящее вещество получается из коры, корней и древесины.
Синие краски
Вайда (синило, синиль, фарбовник) - растет в умеренной полосе России, красящее вещество содержится в листьях.
Герань лесная - красящее вещество в цветах.
Ежевика - ягоды красят в темно-синий цвет.
Черника - ягоды красят шерсть, смоченную, квасцами (1:10), в фиолетовый цвет.
Шалфей луговой - трава красит в темно-синий цвет.
Зеленые краски
Бузина - используют не спелые ягоды, как для красной краски, а листья бузины, которые дают хороший зеленый цвет.
Хвощ болотный - растет повсюду; красящее вещество в стебле, дает зеленый цвет.
Щавель - растет почти повсюду; красящее вещество в листьях.
Можжевельник - растет почти повсюду; красящее вещество в ягодах.
Коричневые краски
Ольха черная - распространена в умеренной полосе России, красящее вещество в листьях, молодых ветвях и коре.
Сухая кора крушины - дает коричневую окраску,
Кора сливяного дерева - дает коричневую окраску.
Щавель конский - корень его, выкопанный осенью, дает коричневый цвет.
Красные краски
Крушина та же, что для получения желтого цвета; для красного цвета собирается не кора, а молодые ветки и листья до цветения.
Марена красильная или крап - растет на юге, в Крыму, Закавказье; красящее вещество в корне растения, который выкапывается до цветения.
Бузина - кустарник, растет почти повсюду; красящее вещество в спелых ягодах.
Душица - трава красит шерсть.
Серые краски
Барвинок - трава красит шерсть в темно-серый цвет.
Ель - кора красит шерсть.
Толокнянка - листья красят шерсть в светло-серый цвет.
Копытень - красит шерсть в темно-серый цвет.
Глава 2. Изготовление красок
Главные составные части акварельной краски – краситель и вода. Чтобы краска не растекалась по бумаге нужно добавить вязкое вещество: мед, патоку или глицерин. И последняя добавка – антисептик и дезинфицирующее вещество. Так как краски растительного происхождения, а их необходимо защитить от действия микроорганизмов (плесневелых грибков, которые обязательно захотят питаться нашими красками).
В домашних условиях акварельные краски можно приготовить двумя способами:
1. Густая вытяжка из растений + связующее вещество
2. Пигмент( сухой краситель) + вода + связующее вещество.
Мы использовали первый способ, т.к. извлекать из растений сухой краситель не было необходимости.
Оборудование и реактивы для получения красок:
- чугунная кастрюля;
- стакан 200 мл;
- ложка;
- ситечко;
- фарфоровые чаши для выпаривания растворов;
- медный купорос;
- уксусная кислота;
- глицерин;
Краски готовятся следующим образом.
1. Основа для изготовления краски.
1. Получение растительных красителей из натурального сырья.
Мы использовали растения луковая шелуха, желтая смородина, черноплодная рябина, красная смородина, свекла свежая и варенная, малина, ежевика, морковь свежая и варенная,
Из листьев или корней растения сделали концентрированный отвар, из овощей и ягод отжали сок. Затем выпаривали на водяной бане до образования концентрированного раствора. Получилась примерно 1 ч.ложка красителя.
Затем начинается самое интересное. Мы готовили акварельные краски, не уступающие по своим качествам магазинным. Для получения различных оттенков акварельных красок мы решили использовать уксус и медный купорос. Медный купорос даёт различные оттенки зелёного цвета, но добавлять его нужно буквально крупинку. И, конечно, лучше не использовать, если краски делать для детей.
При добавлении уксуса, краски становятся более прозрачными. Самые лучшие краски получились из растений и ягод.
Мы составили таблицу растений-красителей.
Таб.1 Растения красители.
|
Название растения |
Без добавок |
Уксусная кислота |
Медный купорос |
|
Луковая шелуха |
Желтый |
Светло коричневый |
Коричневый |
|
Малина |
Розовый |
Синий |
Фиолетовый |
|
Морковь свежая |
Оранжевый |
Оранжевый |
Зелёный |
|
Морковь варёная |
Оранжевый |
Оранжевый |
Оранжевый |
|
Варёная свёкла |
Красный |
Жёлтый |
Оранжевый |
|
Свежая свёкла |
Розовый |
Оранжевый |
Желтый |
|
Красная смородина |
Розовый |
Бирюзовый |
Фиолетовый |
|
Ежевика |
Фиолетовый |
Фиолетовый |
Тёмно фиолетовый |
|
Жёлтая смородина |
Жёлтый |
Жёлтый |
Зелёный |
|
Чёрноплодная рябина |
Розовый |
Синий |
Фиолетовый |
Выводы
Целью данной работы является получение красок из растений. Для этого были поставлены следующие задачи:
Изучить литературу по теме
Получение красок из растений.
Все поставленные перед собой цели успешно достигнуты. В результате исследования выяснилось, что гипотеза подтвердилась. Из приведённых опытов видно, что получить краски из растений вполне возможно. Самые лучшие краски получились из ягод. Из малины самые равномерные и разнообразные цвета. Из свежей моркови самые не стойкие краски.
Список литературы:
Кирилл и Мефодий. Электронная энциклопедия. Статья «Акварель» из «Энциклопедического словаря Брокгауза и Ефрона» (1890 –1907).
Кукушкин Ю.Н. - Химия вокруг нас - Дрофа, 2003г.
Ольгин О. - Опыты без взрывов.- Изд. второе, переработанное. – М.: Химия, 1986. – 192 с.
Интернет-ресурсы:
http://art.ioso.ru/wiki/index.php/Акварельная_живопись
http://www.art-tuts.com/painting-basis/lessons-painting/51-art-paint.html
http://www.bibliotekar.ru/slovarZhivopis/62.htm
http://kamensky.perm.ru/proj/him/givop_2.htm
Просмотров работы: 35
school-science.ru
Природные органические пигменты | Наука


Антоцианы придают некоторым цветам красный, пурпурный или фиолетовый цвет.
Природные органические пигме́нты (лат. pigmentum — краска) — традиционное название большой группы разнородных химических соединений, которые выполняют многие важные функции в организмах живых существ (например антоцианы, каротиноиды, меланин, хлорофилл, гемоглобин, билирубин и др.)


Ликопин придает помидорам оранжево-красный цвет, а хлорофилл определяет зелёный цвет листьев


Темнокожая женщина племени ати. Смуглая кожа, загар и чёрные волосы: их обуславливает защитный пигмент, меланин. Негроиды имеют наследственный мехинизм защиты от сильного солнечного облучения.
История изучения природных пигменты началась с химического, оптического, биологического и биохимического исследования хлорофилла, в конце 18 века. Сегодня биологические пигменты (биопигменты, биохромы [1]) — название несколько устаревшее, условное; так объединяют окрашенные биологически активные вещества. Их цвет, природа которого обусловлена характером хромофорных групп, спектром поглощения (или отражения) веществ, т.е. эффектом избирательного поглощения/отражения отдельных спектральных участков падающего света. Цвет, обусловленный пигментами в ряде случаев играет важную функциональную роль, например цвет хлорофилла - пигмента фотосинтеза (он определяет зелёную окраску растений) обусловлен поглощением красных лучей. В других случаях цвет вторичен и нефункционален, лишь напоминая о структуре вещества и его былых биохимических предшественниках (билирубин, стеркобилин). Биологические пигменты включают пигменты среды, синтезированные различные вещества, например порфирины, каротиноиды, антоцианы и бетаины и цветные пигменты. Многие биологические структуры, например кожа, радужка глаз, мех и волосы содержат пигменты группы меланина в специализированных клетках, названных хроматофорами.
Пигментация или интерференция?  Править
Править


Бабочка Морфо из Центральной Америки обладает отличительной переливчатой синей окраской благодаря интерференции, а не из-за пигментации.
Цвет в природе определяется не только пигментами. Переливы павлиньего пера, как и окраска большинства бабочек — всё это проявления интерференции света в естественных наноструктурах. Это явление аналогично эффекту иризации минералов.
Цвет пигмента отличается от «структурного», интерференционного цвета прежде всего тем, что он не зависит от угла падения света на объект. В то же время структурный цвет — результат избирательного отражения, обычно из-за многослойных прозрачных и полупрозрачных структур, что вызывает эффект иризации, переливчатости. Например, цвет крыльев бабочек нередко зависит от интерференции («структурный цвет»), хотя многие бабочки имеют клетки, которые содержат и пигменты.[2]
Физика и химия изменений видимой окраски Править
Править


Изменение структуры и цвета гемоглобина в процессе поглощения кислорода (при оксигенации крови) и при выделении кислорода (дезоксигенация). (Компьютерное моделирование структурных превращений при химической реакции).
Наиболее распространённые группы природных пигментов  Править
Править
Пигменты фотосинтеза  Править
Править


Модель молекулы хлорофилла.
Пигменты сред живой и неживой природы включают разнообразие различных видов молекул, включая порфирины, каротиноиды, anthocyanins и betalains. Все биологические пигменты выборочно поглощают определенные длины волны света, отражая другие. Поглощённый свет, может использоваться биологической системой для протекания различных биохимических реакций. Отраженные длины волн определяют цвет, который воспринимается глазом. Пигменты в растениях также служат, для привлечения опылителей (пчёл, бабочек и др.).
Хлорофилл — первичный пигмент в средах; это — порфирин, который интенсивно поглощает желтые и синие длины волны спектра, отражая зеленый. Присутствие относительного изобилия хлорофилла, придает растениям их зеленый цвет. Все растительные и животные среды земли и зеленые морские водоросли обладают двумя формами этого пигмента: хлорофилл a и хлорофилл b. Водоросли, диатомовые водоросли, и другой фотосинтетический heterokonts содержат хлорофилл c вместо b, в то время как красные морские водоросли обладают только хлорофиллом a. Все хлорофиллы служат первичным использованием биологических средств, для поглощения света и использования его в процессах питания фотосинтез.
Каротиноиды — красный, оранжевый, или желтый tetraterpenoids. Они функционируют как дополнительные пигменты в биологических средах, помогая поддерживать процесс фотосинтеза, собирая длины волны света, не поглощенного хлорофиллом. Самые знакомые каротиноиды — каротин (оранжевый пигмент, найденный в моркови), lutein (желтый пигмент, найденный во фруктах и овощах), и lycopene (красный пигмент, ответственный за цвет помидоров). Каротиноиды выступают, как антиокислители и оказывают положительную роль для функционирования нормального зрения.
Антоцианины (буквально «синий цветок»), растворимые в воде флавоноидные пигменты, которые кажутся красными или синими, в зависимости от кислотности среды (pH). Они встречаются во всех тканях более высоких природных образований, обеспечивая цвет листьям, стебельным образованиям, корням, цветам, и плодам, хотя не всегда в достаточном количестве, чтобы быть примечательным. Anthocyanins пигменты являются самыми различимыми в лепестках цветов, где они могут составить целых 30 % сухого веса ткани. Они также ответственны за фиолетовый цвет, замеченный на обратной, не освещаемой стороне тропических растений, типа Tradescantia zebrina; на этих тканях растений, антоцианин ловит свет, который прошел сквозь лист и отражает его назад к областям, имеющим хлорофилл, чтобы максимизировать использование доступного света.
Betalains — красные или желтые пигменты. Как anthocyanins они растворимы в воде, но в отличие от anthocyanins они получены индолом составов, синтезируемые из тирозина. Этот класс пигментов найден только в Caryophyllales (включая кактус и амарант), и никогда не происходит на тканях с anthocyanins. Betalains ответственны за глубокий красный цвет например свеклы, и используются в коммерческих целях как пищевой краситель.
Пигменты у животных  Править
Править


Отличительная (защитная)пигментация бабочки монарха напоминает потенциальным хищникам, что это является ядовитым созданием
Пигменты типа меланина в коже животных, могут служить для защититы ткани от ультрафиолетовой радиации. Пигменты могут также помочь в сексуальном привлечении партнёра при воспроизводстве, идентифицируя разновидность и род животных потенциальным партнёром, или сигнализируя о готовности размножаться. Некоторые биологические структуры в животных, типа heme групп, окрашены в результате их специфического строения, и их цвет не служит этим функциям.
Считается, что некоторые cephalopods используют пигментированные хроматофоры для общения с сородичами.
Пигментация используется многими животными для защиты, посредством камуфляжа, мимикрии или предупреждающей окраски. Хамелеоны используют пигменты для маскировки, чтобы смешаться с окружающей их средой, управляя поглотительными уровнями пигментов своей кожи в видимой области спектра.
Болезни и состояния  Править
Править
Разнообразие болезней и нарушений, которые вызывают пигментацию, возникает как у людей, так и у животных, в виде отсутствия или потери пигментации (или клеток пигмента), или в виде их избытка — вырабатывания лишнего пигмента.
- Альбинизм — наследственное нарушение, характеризующийся полной или частичной потерей меланина. Людей и животных, которые страдают от альбинизма, называют «альбиносами».
- Чешуйчатый ихтиоз, также названный «болезнь масштаба рыбы», является унаследованным условием, при котором один признак проявляется лишним производством меланина. Также бывает кожа более темная, чем нормальная, и характеризуется затемненными, чешуйчатыми, сухими участками.
- Melasma — состояние, в котором темно-коричневые участки пигмента появляются на лице, под влиянием гормональных изменений. Когда это происходит в течение беременности, это явление называют маской беременности.
- Глазная пигментация — накопление пигмента в глазу, и может быть вызвана latanoprost лечением.[3]
- Витилиго — условие, в котором наблюдается потеря на отдельных участках кожи меланоцитов - производящих пигмент меланин клеток.
Коммерческое применение пигментов  Править
Править
Некоторые природные растительные пигменты широко используются в качестве красок, хотя многие из них, несмотря на отличный цвет, недостаточно устойчивы или слишком дороги.
Пигменты у морских животных  Править
Править
Каротиноиды  Править
Править
Каротиноиды / Carotenoprotein[4]
Каротиноиды — самая широкая группа пигментов, найденных в природе. Более чем 600 различных видов каротиноидов найдены у животных и в растительных клетках. В клетках растений каротиноиды выполняют отчасти светозащитные функции, играют роль антиоксидантов, убирающих лишние свободные радикалы, образованные в процессе фотосинтеза. Этот пигмент обычно находится в хлоропласте клеток и другого фотосинтетического организма, типа морских водорослей, гриба, и некоторых бактерий. С другой стороны, животные неспособны к созданию их собственных каротиноидов. Таким образом, они полагаются на клетки для этих пигментов.
Каротиноиды формируют комплексы с белками, которые известны как carotenoproteins. Эти комплексы естесвенны среди морских животных. Сarotenoprotein-комплексы ответственны за различные цвета (красный, фиолетовый, синий, зеленый, и т. д.) у морских беспозвоночных для того, чтобы соединять ритуалы и камуфляж. Есть два главных типа carotenoproteins: Тип A и Тип B.
- A-тип имеет каротиноиды (хромоген), которые являются stoichiometrically, связанным с простым белком (гликопротеин).
- B-тип имеет каротиноиды, которые связаны с lipo белком, и обычно менее устойчиво.
В то время как A-тип обычно находится на поверхности (снарядов и кожи) морских беспозвоночных, то B-тип находится обычно в яйцах, яичниках, и крови. Цвета и характерное поглощение этих carotenoprotein комплексов основаны на химическом закреплении chromogen и подединиц белка.
Например, синий carotenoprotein, linckiacyanin имеет приблизительно 100—200 молекул каротиноида в каждый комплекс.[5] Кроме того, функции этих комплексов белка пигмента также изменяют их химическую структуру также. Carotenoproteins, которые являются в пределах фотосинтетической структуры, более обычны, но усложнены. Комплексы белка пигмента, которые являются вне фотосинтетической системы, менее обычны, но имеют более простую структуру. Например, есть только два из этих синих astaxanthin-белков[6] в медузе, Velella velella, содержит только приблизительно 100 каротиноидов в комплекс.
Самый общий carotenoprotein — astaxanthin, который испускает фиолетовый-синое-зелений пигмент. Цвет Астаксантина сформирован, создавая комплексы с белками в определенном заказе. Например, crustochrin имеет приблизительно 20 astaxanthin молекул, связанных с белком. Когда комплексы взаимодействуют экситонным-экситонным взаимодействием, это понижает максимум спектральной поглощательной способности, изменяя различные цветные пигменты!
У омаров есть различные типы комплексов астраксантин-белок. Первый из них — crustacyanin (Макс. длина волны 632 нм), синий сланцем пигмент, найденный в щитке омара. Второй — crustochrin (Макс 409), желтый пигмент, который найден на внешнем слое щитка. Наконец, lipoglycoprotein и ovoverdin формируют яркий зеленый пигмент, который обычно присутствует во внешних слоях щитка и яиц омара.[7],[8]
Тетрапирролы  Править
Править
Tetrapyrroles [9] — следующая самая общая группа фотопигментов. Они имеют четыре кольца pyrrole, каждое кольцо, состоящее из C4h5NH. Главная роль tetrapyrroles — их связь в биологическом процессе окисления. Tetrapyrroles имеет главную роль в электронном транспорте и действует как замена для многих ферментов. Кроме того, они также играют роль в пигментации тканей морского организма.
Меланин  Править
Править
Меланин (Melanin [10]) — класс составов, который служит пигментом с различными структурами, ответственными за темные, коричневые, желтоватые фотопегменты пигменты у морских животных. Это произведено, поскольку тирозин аминокислоты преобразован в меланин, который найден в коже, волосах, и глазах. Полученный из аэробного окисления фенолов, они — полимеры.
Есть несколько различных типов меланинов, полагающих, что они являются совокупностью меньших составляющих молекул, типа азота, содержащего меланины. Есть два класса пигментов: черные и коричневые нерастворимые эвмеланины, которые получены из аэробного окисления тирозина в присутствии tyrosinase, и разрешимых щелочью phaeomelanins, которые располагаются от желтого цвета до красного коричневого цвета, являясь результатом отклонения eumelanin тропы через вмешательство цистеина и/или глутатнона. Eumelanins обычно находятся в коже и глазах. Несколько различных меланинов включают melanoprotein (темно-коричневый меланин, это сохранено в высоких концентрациях в мешочке чернил Сепии каракатицы Officianalis), echinoidea (найденный в долларах песка, и сердцах морских пострелов), holothuroidea (найденный в морских огурцах), и ophiuroidea (найденный в ломком и звездах змеи). Эти меланины — возможно полимеры, которые являются результатом повторного сцепления простого bi-polyfunctional monomdric промежуточные звенья, или высоких молекулярных масс. Составы benzothiazole и tetrahydroisoquinoline показывают акт систем как УЛЬТРАФИОЛЕТОВЫЕ-АБСОРБИРУЮЩИЕ составы. Есть несколько различных типов меланинов, как полагают, что они являются совокупностью меньших составляющих молекул, типа азота, содержащего меланины.
Биолюминесценция  Править
Править


Биолюминесценция может также использоваться, чтобы привлечь добычу. На удилище болтается светящийся придаток, в передней части его большие и зубастые челюсти в качестве приманки для рыб поменьше.
Биолюминесценция [11] — единственный источник света в глубоком море, морские животные испускают видимую световую энергию, названную биолюминесценцией, подмножество хемилюминесценции. Это — химическая реакция, в которой химическая энергия преобразована, чтобы осветить энергию. Оценено, что 90 % глубоководных животных производят своего рода биолюминесценцию. Полагая, что большая пропорция видимого легкого спектра поглощена перед достижением глубокого моря, большинство испускаемого света от морских животных является синим и зеленым. Однако, некоторые разновидности могут испустить красно-инфракрасный свет, и даже был род, который, как находят, испускает желтую биолюминесценцию. Орган, который является ответственным за эмиссию биолюминесценции, известен как photophores. Этот тип только присутствует в кальмаре и рыбе, и используется, чтобы осветить их брюшные поверхности, которые маскируют их силуэты от хищников. Использования photophores в морских животных отличаются, типа линз для того, чтобы управлять интенсивностью цвета, и интенсивности произведенного света. Кальмары имеют и photophores и хроматофоры, который управляет обоими из этих intensities. Другая вещь, которая является ответственной за эмиссию биолюминесценции, которая является очевидной во взрывах света, который медуза испускает, начинается с luciferin (photogen) и концы с легким эмитентом (photagogikon.) Luciferin, luciferase, соль, и кислород реагируют и объединение, чтобы создать единственную единицу, названную фотобелками, которые могут произвести свет когда реагируется с другой молекулой, типа Приблизительно +. Использование медузы это как защитный механизм; когда меньший хищник пытается пожрать медузу, это высветит ее огни, которые поэтому соблазнили бы большего хищника и выгнали бы меньшего хищника. Это также используется как сцепляющееся поведение.
В строящем риф коралле и актиниях, они fluoresce; свет поглощен в одной длине волны, и повторно испускается в другом. Эти пигменты могут действовать как естественные солнцезащитные крема, помощь в фотосинтезе, служить предупреждением окраски, привлекать помощников, предупреждать конкурентов, или смущать хищников.
Следует заметить, что Биолюминесценция проявляется не только у морских животных. Способность клеток светиться при воздействии фотонов лучей света в настоящее время используется учёными при флюоресцентной микроскопии, например, при исследовании живых клеток сетчатки глаза. При флюоресцентной микроскопии сетчатки птиц (цыплёнка) колбочки и палочки светились разными цветами своими жировыми капельками (фиолетовым, синим, зелёным, красным).
Хроматофоры Править
Править
Хроматофоры — цветной пигмент, активно и быстро изменяющий окраску биологических клеток, которые непосредственно стимулируются центральными моторными нейронами. Они прежде всего используются для быстрой экологической адаптации к маскировке. Процесс изменения цветного пигмента их кожи полагается на единственную высоко развитую клетку хроматофора и много мускулов, нервы, глии и клетки кожи. Хроматофоры заключают и содержат пузырьки, который хранит три различных жидких пигмента. Каждый цвет обозначен тремя типами ячеек хроматофора: erythrophores, melanophores и xanthophores.
- Первый тип — erythrophores, который содержит красноватые пигменты, типа каротиноидов и pteridines.
- Второй тип — melanophores, который содержит черные и коричневые пигменты, типа меланинов.
- Третий тип — xanthophores, который содержит желтые пигменты в формах каротиноидов.
Различные цвета сделаны комбинацией различных слоев хроматофоров. Эти клетки обычно располагаются ниже кожи или измеряют животных, есть две категории цветов, произведенных ячейкой — biochrome и schematochromes.
Biochromes — цвета, химически формирующих микроскопические, естественные пигменты. Их химический состав создан, чтобы взять в небольшом количестве цвета света и отразить остальные. И напротив, schematochromes (структурные цвета) — цвета, созданные легкими изменениями от бесцветной поверхности и преломлений тканями. Schematochromes действуют как призмы, преломляя и рассеивая видимый свет к среде, которая в конечном счете отражает определенную комбинацию цветов. Эти категории определены движением пигментов в пределах хроматофоров. Физиологические цветные изменения краткосрочны и быстры. Они найдены в рыбах, и — следствие ответа животного на изменение в окружающей среде. Напротив, морфологические цветные изменения — долгосрочные изменения, которые происходят в различных стадиях животного, и приводит к изменению чисел хроматофоров. Чтобы изменять цветные пигменты, прозрачность, или непрозрачность, ячейки изменяются в форме и размере, и распространяют или заключают их внешнее покрытие.
Фотозащитные пигменты Править
Править
Фотозащитные пигменты — пигменты создаваемые от УЛЬТРАФИОЛЕТОВЫХ-A и УЛЬТРАФИОЛЕТОВЫХ-B лучей морских животных и развились, чтобы иметь составы, которые поглощают УЛЬТРАФИОЛЕТОВЫЙ свет и средство как солнцезащитный крем. Mycosporine-подобные аминокислоты (МААС) могут поглотить УЛЬТРАФИОЛЕТОВЫЕ лучи в 310—360 нм. Меланин — другой известный УЛЬТРАФИОЛЕТОВЫЙ ЗАЩИТНИК. Каротиноиды и фотопигменты оба косвенно действуют как фотозащитные пигменты, поскольку они подавляют свободныt радикалы кислорода. Они также добавляют фотосинтетические пигменты, которые поглощают легкую энергию в синей области.
Защитная роль пигментов Править
Править
Защитная роль пигментов — известно, что животные используют их цветные образцы, чтобы отпугивать хищников, однако, наблюдалось, что пигмент губки подражал химикату, который вовлекал регулирование линьки amphipod, который, как известно, охотился на губки. Так, всякий раз, когда, что amphipod ест губку, химические пигменты предотвращают линьку, и в конечном счете умирает amphipod.
Экологическое влияние на цвет Править
Править
Экологическое Влияние на Цвет — когда окраска у беспозвоночных изменяется в зависимости от глубины, водной температуры, источника пищи, водных потоков, географического местоположения, светового освещения и отложений осадков. Например, количество каротиноида, который уменьшается у актиния при более глубоком погружении в океан. Таким образом, морская жизнь, которая проживает на более глубоких водах, является менее блестящей, чем у организмов, которые живут в хорошо освещенных областях из-за сокращения пигментов. В колониях колониального ascidian-cyanophyte симбиоза цоколь Trididemnum, их цвета отличаются и зависят от светового режима, в котором они живут. Колонии, которые выставлены полному солнечному свету, тяжело твердеют, более толсты, и белы. По контрасту колонии, которые живут в заштрихованных областях, имеют больше phycoerythrin (пигмент, который поглощает зеленый цвет) по сравнению с phycocyanin (пигмент, который поглощает красный), более тонкий, и являются фиолетовыми. Фиолетовый цвет в заштрихованных колониях происходит главным образом из-за phycobilin пигмента морских водорослей, означая, что изменение подвергания в свете изменяет цвета этих колоний.
Адаптивная окраска Править
Править
Aposematism — окраска предупреждения, чтобы сигнализировать потенциальным хищникам, чтобы их избежать. Во многих chromodrorid nudibranchs они рбразуются из неприятных и ядовитых химикалий, испускаемых от губок и хранят их в их repugnatorial гландах (расположенный вокруг края мантии). Хищники nudibranchs учились избегать их определенный nudibranchs основанный на их ярких цветных образцах. Добыча также защищает себя их ядовитыми составами в пределах от разнообразия органических и неорганических составов.
Физиологическая роль пигментов Править
Править
Фотопигменты морских животных преследуют несколько различных целей, кроме защитных ролей. Некоторые пигменты, как известно, защищают от УФ - излучения (см. фотозащитные пигменты.) В nudibranch Nembrotha Kubaryana, tetrapyrrole пигмент 13, как находили, был мощным антибактериальным агентом. Также в этом существе, tamjamines A, B, C, E, и F (изображают 79a-e) показан антибактериальный препарат, предназначен для антиопухолей и для иммунодепрессивных действий.
Sesquiterpenoids признаны за их синие и фиолетовые цвета, но они также показывают различные биологические активности, типа антибактериального, immunoregulating, антибактериальный препарат, и цитостатический, так же выступает в качестве запрещающей деятельности против разделения клетки в оплодотворенном морском постреле и ascidian яйцах. Несколько других пигментов показали, чтобы быть цитостатическим. Фактически, два новых каротиноида, которые были изолированы из губки Phakellia stelliderma, показали умеренную цитотоксичность против клеток лейкемии мыши. Другие пигменты с медицинской причастностью включают scytonemin, topsentins, и debromohymenialdisine имеют несколько ведущих составов в области воспаления, ревматического артрита и osteoarthritis соответственно. Есть свидетельство, что topsentins являются мощными посредниками immunogenic инфляции, и topsentin и scytonemin — мощные ингибиторы нейрогенного воспаления.
- ↑ http://www.britannica.com/EBchecked/topic/65803/biochrome accessed 27 July 2010
- ↑ http://en.wikipedia.org/wiki/Biological_pigment
- ↑ Rang, H. P. (2003). Pharmacology. Edinburgh: Churchill Livingstone. ISBN 0-443-07145-4. Page 146
- ↑ Nadakal , A. M.. «Carotenoids and Chlorophyllic Pigments in the Marine Snail, Cerithidea Californica Haldeman, Intermediate Host for Several Avian Trematodes.» Marine Biological Laboratory. JSTOR, n.d. Web. 26 May 2010. <http://www.jstor.org/pss/1538938>.
- ↑ Milicua, JCG. «Structural characteristics of the carotenoids binding to the blue carotenoprotein from Procambarus clarkii.» Structural characteristics of the carotenoids binding to the blue carotenoprotein from Procambarus clarkii. N.p., 25 Oct. 1984. Web. 24 May 2010. <resources.metapress.com/pdf-preview.axd?code=l163k1j75x721w72&size=largest>.
- ↑ Zagalsky, P.. «Colouration in Marine Invertebrates» A central role for astaxanthin complexes." Crustacean. N.p., n.d. Web. 25 May 2010. <srs.dl.ac.uk/Annual_Reports/AnRep01_02/pdf/08_09%20Crustacyanin.pdf>.
- ↑ ZAGALSKY, Peter F. . «The lobster carapace carotenoprotein, a-crustacyanin.» A possible role for tryptophan in the bathochromic spectral shift of protein-bound astaxanthin. N.p., n.d. Web. 25 May 2010. <www.biochemj.org/bj/274/0079/2740079.pdf>.
- ↑ CHANG, KENNETH. «The New York Times > Science > Yes, It’s a Lobster, and Yes, It’s Blue.» The New York Times — Breaking News, World News & Multimedia. NY Times, 15 Mar. 2005. Web. 24 May 2010. <http://www.nytimes.com/2005/03/15/science/15blue.html>.
- ↑ Schmidt-Danner, Claudia. " BIOSYNTHESIS OF PORPHYRIN COMPOUNDS." Tetrapyrroles. N.p., n.d. Web. 25 May 2010. <www3.cbs.umn.edu/BMBB/faculty/csd/HTML/research_tetrapyrroles.htm>.
- ↑ Bandaranayake, Wickramasinghe. "The nature and role of pigments of marine invertebrates ." Natural Products Report. Cambridge, n.d. Web. 25 May 2010. <www.rsc.org/delivery/_ArticleLinking/DisplayArticleForFree.cfm?doi=b307612c&JournalCode=NP>.
- ↑ Webexhibits. "Bioluminescence | Causes of Color." WebExhibits. Web. 02 June 2010. <http://www.webexhibits.org/causesofcolor/4ADA.html>.
- Бриттон Г. Биохимия природных пигментов. — Москва: Мир, 1986. — 422 с. — 3050 экз.
- Всеволодов Н. Н. Биопигменты — фоторегистраторы: фотоматериал на бактериородопсине. — Москва: Наука, 1999. — 224 с. — (Теоретическая и прикладная биофизика). — ISBN 5-02-003930-6.
- Конев С. В., Волотовский И. Д. Ввведение в молекулярную фотобиологию. — Минск: Наука и техника, 1971. — 230 с.
ru.science.wikia.com
Учебно- исследовательская работа "Исследование влияния пигментов на окрас растений"
ГБОУ СПО «Новокузнецкий техникум строительных технологий и сферы обслуживания»
Исследование влияния пигментов на окрас растений
Работа на конкурс «Творческий поиск»
Номинация: учение с увлечением
Автор: Синяева Арина,
группа ЛД 1-14
Руководитель: Слюсарь Кристина Сергеевна,
преподаватель химии и биологии
Новокузнецк, 2015
Оглавление
Стр.
Введение…………………………………………………………………….. 3
Глава 1. Пигменты и их биологическое значение……………………….. 4
Глава 2. Значение окраски растений в природе………………………… . 6
Глава 3. Экспериментальная часть…………………………………………9
3.1. Изучение индикаторных свойств антоцианов……………………….. 10
3.2. Качественная реакция на ионы кальция и магния в антоцианах…….12
3.3. Обнаружение магния в антоцианах мокрым путем………………..…13
3.4. Изучение индикаторных свойств каротиноидов…………………… .14
3.5. Обнаружение воздуха в межклетниках лепестков фиалки………….. 15
Заключение…………………………………………………………………...17
Список литературы…………………………………………………………..18
Введение
В эпоху технического прогресса и индустриализации, роста городов в жизни человека все более значительную роль играет природа. Парки, зеленые зоны и другие места отдыха бывают слишком удалены от нашего жилья. Растения и цветы в доме, на приусадебном участке и на улицах города сокращают разрыв между человеком и природой.
Моя будущая профессия ландшафтного дизайнера предполагает проектирование и строительство садово-парковых объектов, а также скверов, улиц, частных усадеб, подбор ассортимента растений и малых архитектурных форм и уход за зелеными насаждениями, а так же цветочное оформление объектов. В связи с чем, мне представляется интересным изучение строения и жизнедеятельности растений.
Изучая ботанику, я обратила внимание на разнообразие окраски их цветков. Известно, что окраска определяется пигментами, но пигменты не так разнообразны, как окраска цветков растений. Таким образом, представляется интересным изучение вопроса возникновения окраски у цветков растений.
В качестве рабочей нами была принята следующая гипотеза: окраска цветков у растений определяется не только наличием пигментов.
Цель работы: выяснить, как возникает разнообразие окраски цветков у растений.
Для достижения этой цели поставлены следующие задачи:
- изучить виды пигментов и их значение;
- выяснить значение окраски растений в природе;
- провести эксперимент по обнаружению пигментов и изучению их свойств.
В качестве методов исследования были выбраны: наблюдение, сравнение, эксперимент, анализ литературных источников.
Объект исследования –органы покрытосеменных растений.
Предмет исследования - разнообразие окраски растений.
Глава 1. Пигменты и их биологическое значение
Биологические пигменты (биохромы) — окрашенные вещества, входящие в состав тканей организмов. Цвет пигментов определяется наличием в их молекулах хромофорных групп, избирательно поглощающих свет в определённой части видимого спектра солнечного света. Пигментная система живых существ — звено, связывающее световые условия окружающей среды и обмен веществ организма. Биологические пигменты играют важную роль в жизнедеятельности живых существ.
Биологические пигменты подразделяются на несколько классов в зависимости от своего строения: каротиноиды, хиноны, флавоноиды, пигменты на основе порфирина.
Каротиноиды
Каротиноиды — наиболее распространённый класс биологических пигментов. Они обнаружены у большинства живых существ, в том числе у всех без исключений растений, многих микроорганизмов. Каротиноиды так же обуславливают окраску многих животных, особенно насекомых, птиц и рыб. Каротиноиды и их производные, помимо прочего, являются основой зрительных пигментов, отвечающих за восприятие света и цвета у животных.
К каротиноидам относятся такие пигменты, как каротин, гематохром, ксантофилл, ликопин, лютеин, родопсин (зрительный пурпур) и другие.
Хиноны
Хиноны — химические соединения, производные моноциклических или полициклических ароматических углеводородов, в составе которых присутствует ненасыщеный циклический дикетон. Их окраска варьирует от бледно-жёлтой до оранжевой, красной, пурпурной, коричневой и почти чёрной. Обнаружены у многих грибов, лишайников и в некоторых группах беспозвоночных. Широко используемый краситель ализарин относится к группе хинонов.
Флавоноиды
Флавоноиды — O-гетероциклические фенольные соединения. В природе синтезируются почти исключительно высшими растениями. В их число входят антоцианы, обуславливающие наиболее яркие цвета растений — красные, пурпурные, синие части цветов и плодов. Ярко-красные розы, голубые васильки, фиолетовые анютины глазки содержат в клеточном соке антоцианы. Если орган растения имеет розовый, голубой, синий, фиолетовый и даже черный цвет, то нет никакого сомнения в том, что его окраска обусловлена антоцианами.
Флавоны, флавонолы, ауроны, халконы определяют жёлтую и оранжевую окраску плодов и листьев.
Пигменты на основе порфирина
В эту группу входят биологические пигменты, в составе которых присутствует порфириновый комплекс. Гем, один из видов порфиринов, входит в качестве простетической группы в состав таких соединений, как гемоглобин, билирубин, цитохром c, цитохром P450 и другие. К этой группе относятся также растительные пигменты — хлорофилл, феофитин и т. п. Как правило, пигменты этого класса участвуют в фотохимических процессах, а также являются ферментами, задействованными в обмене веществ. Их роль как собственно красителей второстепенна.
Глава 2. Значение окраски растений в природе
Окраска цветков привлекает насекомых-опылителей. Яркая окраска – это «опознавательный знак», показывающий, где насекомые могут найти нектар и пыльцу.
Наблюдая за растениями, мы заметили, что разные виды насекомых предпочитают разные цвета: пчелы, шмели, осы посещают синие, фиолетовые и розовые цветы, желтые - мухи, а на красные садятся преимущественно бабочки.
Известно, что насекомых привлекает нектар и пыльца, которая служит для них пищей. А находят цветки они по яркой окраске лепестков и по аромату. Перелетая с одного цветка на другой, насекомые производят опыление.
У примитивных цветковых растений приманкой для насекомых служит только пыльца. В этом случае опыление осуществляется преимущественно жуками.
При появлении у растений нектарников круг насекомых – опылителей расширился. Кроме жуков в него вошли: перепончатокрылые (пчелы, шмели), двукрылые (мухи), чешуекрылые (бабочки). Разные насекомые различают разные цвета, а красный цвет многие насекомые не видят. Они путают его с темно-серым, поэтому в наших широтах красные цветки довольно редки. Исключение составляет мак, но и он имеет примесь желтого цвета, обычно именно этот оттенок улавливают насекомые. Лучше других красный цвет различают бабочки. Эта группа опылителей встречается во всех частях земного шара. Но поскольку нектар служит им пищей лишь на кратковременной взрослой стадии, их эффективность ниже, чем пчел. Значительная часть бабочек ведет ночной образ жизни, поэтому цветки растений, которые они опыляют, окрашены в светлые тона, различаемые при тусклом освещении. Цветки некоторых растений, например, душистого табака испускают аромат только ночью, когда активны, опыляющие их бабочки. В отличие от этого, цветки, опыляемые дневными бабочками, окрашены преимущественно в яркие тона и хорошо заметны днем.
Очень часто насекомые в процессе длительной эволюции приспосабливаются к опылению какого-то одного вида растений, что имеет больший биологический смысл. Растению это выгодно потому, что вероятнее всего насекомое перенесет его пыльцу на экземпляр того же вида, а опылителям – потому, что они «настраиваются» на определенные сигналы, идущие от цветков и гораздо легче находят их, игнорируя сигналы, идущие от других цветков.
Среди цветущих тропических растений красный цвет преобладает, что связано с опылением птицами, а именно колибри, обладающими развитым зрением. Насчитывается до 300 видов колибри, питающихся нектаром. Они зависают над цветком в трепещущем полете и достают нектар из глубины цветка с помощью длинного клюва и трубкообразного языка, при этом пыльца, прилипшая к голове птицы, падает на длинные, выступающие рыльца пестиков. В качестве примера можно привести комнатное растение филлокактус (декабрист). Описанный способ питания требует очень точного соответствия между длиной клюва колибри и глубиной трубки цветка, и поэтому один вид колибри способен добывать нектар обычно только из одного вида тропических растений.
Бывает, что у одного и того же растения окраска цветков с возрастом изменяется. Это хорошо заметно у медуницы, распускающейся ранней весной: розовый цвет ее молодых лепестков сменяется с возрастом на синий. Вакуолярный сок, в котором растворен пигмент антоциан имеет кислую реакцию среды (рН меньше 7), а цитоплазма – щелочную. По мере старения растения в вакуолярной мембране развиваются дефекты. Антоцианы вытекают в цитоплазму и в ее щелочной среде синеют, словно индикатор. Старые цветы пчелы, как правило, не посещают, они уже опылены и не содержат нектара.
С пигментами связана светочувствительность растений, сезонная регуляция метаболизма, роста и цветения, подготовка и переход к фазе покоя, регуляция процессов прорастания семян.
Поглощая ультрафиолетовые лучи, флавоны и флавонолы предохраняют хлорофилл и цитоплазму клеток от разрушения. Очень важная функция, выполняемая каротиноидами, флавонами и флавонолами, состоит в нейтрализации свободных радикалов, нарушающих протекание биохимических процессов в растениях, т.е. эти пигменты обладают антиоксидантными свойствами.
Флавоновые пигменты иногда применяются растениями для самозащиты – в качестве противогрибковых агентов, выполняют функции резерва питательных веществ.
Глава 3. Экспериментальная часть
Растительные пигменты – это крупные органические молекулы, поглощающие свет определенной длины волны. В большинстве случаев, за появление окраски отвечают определенные участки этих молекул – хромофоры. Обычно хромофорный фрагмент состоит из группы атомов, объединенных в цепи или кольца с чередующимися одинарными и двойными связями (-С=С-С=С-). Чем больше таких чередующихся связей, тем глубже окраска.
Рисунок 1. Структурная формула альфа-каротина.

Кроме того, поглощение света усиливается при наличии в молекуле
кольцевых структур.
Рисунок 2. Структурная формула хлорофилла

Рисунок 3. Структурная формула антоциана

Антоцианы – это гликозиды, возникающие при соединении различных сахаров с циклическими соединениями, называемыми антоцианидами.
Из курса химии нам известно, что циклические соединения меняют свою структуру при изменении кислотности среды. Зависимость разнообразия окраски от водородного показателя среды возможно проверить экспериментально.
3.1. Изучение индикаторных свойств антоцианов
Антоцианы – водорастворимые пигменты. Из свеклы, плодов черной смородины и цветков узумбарской фиалки мы приготовили их водную вытяжку. Для этого 1 грамм растительного вещества поместили в огнеупорный стаканчик, залили 5 мл воды и довели до кипения на плитке. От нагревания происходит разрушение вакуолей и самих клеток, и пигменты выходят из клеточного сока в воду, окрашивая ее. Полученный раствор отфильтровали. В чистую пробирку налили 2-3 мл вытяжки пигментов фиалки узумбарской светло-синего цвета, добавили 1-2 капли разбавленной соляной кислоты. Окраска изменилась на бледно-розовую.
Определили рН раствора с помощью индикаторной бумаги, она была меньше 7 и добавляли по каплям разбавленную щелочь (гидроксид натрия). Окраска поменялась с бледно-розовой на ярко-желтую.
Тоже самое проделали с соком черной смородины и красной свеклы. В кислой среде красный сок свеклы стал ярко-красным, а в щелочной – ярко-желтым. Свекольный сок в кислой среде приобрел ярко-красную окраску, а в щелочной – сине-зеленую.
Таблица №1. Изменение окраски водной вытяжки антоцианов различных растений в кислой и щелочной среде
| наименование вытяжки | характер среды | окраска |
| вытяжки пигментов фиалки узумбарской | кислая | бледно-розовая |
| щелочная | ярко-желтая | |
| вытяжки пигментов черной смородины | кислая | ярко-красная |
| щелочная | ярко-желтая | |
| вытяжки пигментов свекольного сока | кислая | ярко-красная |
| щелочная | сине-зеленая |
Рисунок 4. Изучение индикаторных свойств антоцианов
1 2 3 4 5 6

Вывод: антоцианы изменяют окраску в зависимости от рН среды. Их водные растворы можно использовать в качестве кислотно-щелочных индикаторов.
Изменения окраски связаны с перестройками в молекуле антоциана.
В присутствии щелочей и кислот в молекулах антоцианов происходит перегруппировка двойных и одинарных связей между атомами углерода, что приводит к образованию нового хромофора. В щелочной среде антоцианы приобретают синий или сине-зеленый цвет. При действии минеральных и органических кислот антоцианы образуют соли красного цвета.
Значит, окраска антоцианов зависит от рН клеточного сока и поэтому может меняться при созревании плодов и отцветании цветков.
Цвет антоцианов влияет также способность этих пигментов образовывать комплексные соединения с металлами: например, с кальцием или магнием окраска становится синяя. Доказать это присутствие ионов кальция и магния в вытяжке антоцианов возможно с помощью качественных реакций.
3.2. Качественная реакция на ионы кальция и магния в антоцианах
Капельный метод (реакция проводится на стеклянной пластине) +Микрокристаллоскопический методы (с использованием микроскопа).
Чтобы обнаружить ионы кальция в вытяжке антоцианов, мы провели качественную реакцию на его определение чувствительным методом – капельным. Для сравнения был взят эталон – соль кальция (хлорид кальция CaCl2). На предметное стекло поместили каплю хлорида кальция и каплю серной кислоты, упарили слегка на крышке водяной бани. При этом образовались красивые характерные пучки игл - кристаллы гипса: CaSO4·2h3O, легко различимые под микроскопом. Аналогичную реакцию проводили с вытяжкой антоциана. Каплю, вытяжки антоциана поместили на предметное стекло, добавили каплю серной кислоты и слегка упарили на водяной бане. Под микроскопом мы увидели пучки игл, сравнив с эталоном, и сделали для себя вывод, что они похожи на пучки игл, как и в эталоне.
Рисунок 5. Качественная реакция на ионы кальция и магния в антоцианах


Вывод:
1) В водной вытяжке антоцианов содержится ионы кальция.
2) Для проявления синего цвета необходимо наличие в клетках цветков комплексного соединения антоциана с кальцием.
Комплексные соединения антоцианов с молибденом имеют фиолетовый цвет, с железом и магнием – синий, с никелем и медью – белый, с калием -пурпурный.
3.3. Обнаружение магния в антоцианах мокрым путем
Чтобы обнаружить ионы магния в вытяжке антоциана, мы использовали качественную реакцию на его определение. Для этого использовали эталон – соль хлорида магния (MgCl2), с которым была проведена качественная реакция. В пробирку поместили по 0,5 мл раствора хлорида магния и хлорида аммония, к полученной смеси прибавили 5 капель гидрофосфата натрия, тщательно перемешали и затем добавили водный раствор аммиака до щелочной среды (проверка индикаторной бумажкой). Выпал характерный белый осадок фосфата магний-аммония: MgNh5PO4
MgCl2+Na2HPO4MgHPO4 + 2NaCl
MgHPO4 + Nh4MgNh5PO4
Аналогичную реакцию проводили с водной вытяжкой антоциана. В пробирку поместили 0,5 мл водного раствора антоциана и 0,5 мл хлорида аммония, к полученной смеси прибавили водный раствор аммиака до появления в смеси раствора щелочной среды (проверка индикатором). Выпал небольшой осадок белого цвета, сравнив его с эталоном, обнаружили сходство.
Рисунок 6. Обнаружение магния в антоцианах мокрым путем

Вывод:
1) В водной вытяжке антоцианов содержится ионы магния.
2) Для проявления синего цвета необходимо наличие в клетках цветков комплексного соединения антоциана с магнием.
Зависимость цвета каротиноидов от кислотности среды так же возможно проверить опытным путем.
3.4. Индикаторные свойства каротиноидов
Каротиноиды нерастворимы в воде, но хорошо извлекаются из пластид органическими растворителями. Мы поместили кусочки моркови в спирт и оставили на 30 минут, затем профильтровали. Спирт окрасился в ярко-оранжевый цвет. Провели опыт на определение индикаторных свойств каротиноидов, но окраска спирта не изменилась при воздействии кислот и щелочей.
Рисунок 7. Индикаторные свойства каротиноидов

 Вывод: цвет каротиноидов не зависит от кислотности среды.
Вывод: цвет каротиноидов не зависит от кислотности среды.
У каротиноидов невозможно выделить какой-нибудь один хромофорный фрагмент, потому что их молекулы включают цепочки атомов с чередующимися одинарными и двойными связями разной длины. Цепочке каждого типа соответствует свой индивидуальный хромофор. По мере удлинения цепи окраска пигментов изменяется от желтой к красной и даже красно-фиолетовой. В молекулах желтых и желто-красных пигментов имеется 11 двойных связей, чередующихся с одинарными, а в молекулах красного виолоксантина – 13.
3.5. Обнаружение воздуха в межклетниках лепестков фиалки
В растительном мире широко распространена белая окраска цветков. А вот какой пигмент обеспечивает белый цвет в природе? Известно, что белый цвет коры берез обусловлен пигментом бетулином. А чем обусловлена белоснежная окраска цветков вишни, черемухи или фиалки?
1. Мы рассмотрели под микроскопом лепесток белого цветка фиалки и увидели большое количество межклетников, заполненных воздухом.
2.Осторожно сжали лепесток пальцами. Воздух из межклетников выходит и лепесток становится бесцветным и прозрачным, как лед.
3.Погрузили лепестки в воду. Через несколько часов лепестки стали бесцветными, так как вода через устьица проникла в межклетники и вытеснила воздух.
Рисунок 8. Обнаружение воздуха в межклетниках лепестков фиалки

Вывод: белый цвет лепестков цветов обусловлен развитой системой межклетников. Значит, белый цвет им придает воздух.
Заключение
Таким образом, используя, такие методы как наблюдение, сравнение, эксперимент, анализ литературных источников, мы изучили виды пигментов и их значение, выяснили значение окраски растений в природе и провели эксперимент по обнаружению пигментов и изучению их свойств.
В результате работы над темой исследования, гипотеза подтвердилась. Мы выяснили, что окраска цветков у растений зависит от присутствия пигментов, кислотности клеточного сока, способности пигментов образовывать комплексные соединения с металлами, а также от строения ткани, в которой содержатся пигменты: ее толщины, количества межклетников, плотности находящегося на поверхности воскового налета.
Список литературы
Никишин, Ю.А. Ботаника [Текст]/ Ю.А. Никишин. – Москва: Просвещение, 2006. – 565 с.
Павлов О. С.Уход за растениями [Текст]/О.С. Павлов. –Санкт-Петербург: ОНИКС XXI век, 2009.- 200 с.
Самуйлова Л. И. Аналитическая химия [Текст]/ Самуйлова Л. И., Пучкова Т.Е.- Москва: Гелеос, 2005.- 400 с.
Хомченко Л.А. Биология растений [Текст]/ Хомченко Л.А.- Москва: Книга плюс, 2013.- 450 с.
Интернет-ресурсы:
Исследовано в России [Электронный ресурс] : многопредмет. науч. журн. / Моск. физ.-техн. ин-т. – Электрон. журн. – Долгопрудный : МФТИ, 2011. – Режим доступа к журн. :http://zhurnal.mipt.rssi.ru. (дата обращения: 25.12.2014).
multiurok.ru
Растительные пигменты как альтернатива синтетическим красителям и индикаторам
В статье представлены результаты химического эксперимента по выделению пигментов из растений и получению природных красителей и индикаторов. Рассмотрена возможность использования полученных красителей для окрашивания тканей и индикаторов для определения кислотности моющих средств.
Ключевые слова: растительные пигменты, растительные красители и индикаторы, хроматография
Окраска растений обусловлена содержанием в них различных пигментов. Растительные пигменты – это крупные органические молекулы, поглощающие свет определенной длины волны [1]. Одним из направлений применения растений, богатых пигментами, служит получение природных красителей и индикаторов.
Красители – органические соединения, обладающие способностью поглощать и преобразовывать световую энергию в ультрафиолетовой и инфракрасной областях спектра [4]. Растительные красители являются распространенным экологически безопасным и доступным сырьем.
Индикаторы – это химические вещества, окраска которых меняется в зависимости от рН среды [3]. Проблема получения индикаторов достаточно актуальна, так как природные индикаторы играют большую роль и широко используются при химических исследованиях. Преимуществом растительных индикаторов является дешевизна, быстрота и наглядность исследования.
Цель работы:изучить свойства растительных пигментов и выявить возможность их применения в качестве красителей и индикаторов.
Методы исследования:теоретические (анализ учебной и научно-популярной литературы), экспериментальные (химический эксперимент).
Организация исследования.На первом этапе был проведен анализ научно-популярной литературы по выбранной теме, который показал, что в растительных клетках обычно встречаются зеленые пигменты – хлорофиллы (рис. 1), желто-оранжевые – каротиноиды и разнообразные флавоноиды.

Рис.1. Структурная формула хлорофилла
Каждая из групп растительных пигментов представлена несколькими отличающимися по химическому строению, окраске и поглощению света пигментами. Например, к группе флавоноидов относят антоцианы, определяющие красную, синюю, фиолетовую окраску цветов; флавоны, флавонолы, ауроны и халконы — жёлтую и оранжевую. Пигмент группы флавоноидов кверцетин содержится в коре дуба (рис. 2), катехин – в листьях чая. Пигмент группы каротиноидов рубиксантин содержится в плодах шиповника (рис. 3.).
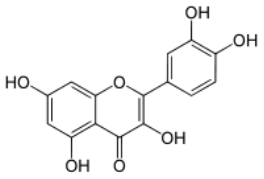
Рис. 2. Структурная формула кверцитина

Рис.3. Структурная формула рубиксантина
Второй этап был связан с химическим экспериментом по получению природных индикаторов и красителей.
Технология получения красителей включает два основных процесса: извлечение красящих веществ и приготовление концентрированного красителя, который стабилен при хранении и пригоден для непосредственного использования. После того, как красители перешли в раствор, мы испытывали их способность к окрашиванию хлопчатобумажной ткани.
В результате окрашивания ткани растворами перечисленных растений получили следующие цвета: из шелухи лука – светло-коричневый, из корнеплодов свеклы – светло-бордовый, из ягод калины – светло-розовый, из коры дуба – желто-коричневый. Все полученные результаты представлены в таблице 1.
Таблица 1
Результаты окрашивания ткани полученными растительными красителями
|
Растение |
Используемая часть |
Цвет красителя на ткани |
|
Лук репчатый |
Сухие чешуи |
Темно-коричневый |
|
Свекла столовая |
Корнеплод |
Светло-бордовый |
|
Калина красная |
Ягоды |
Светло-розовый |
|
Дуб обыкновенный |
Кора |
Желто-коричневый |
|
Боярышник |
Кора |
Красно-коричневый |
|
Чистотел |
Листья и стебли |
Желто-зеленый |
|
Крапива |
Листья и стебли |
Серо-желтый |
|
Краснокочанная капуста |
Листья |
Сиреневый |
|
Черника |
Ягоды |
Фиолетовый |
|
Рябина черноплодная |
Ягоды |
Серо-синий |
|
Флокс белый |
Цветы |
Желто-зеленый |
В результате проведенного опыта убедились в том, что растительные красители способны длительное время удерживаться на ткани и не уступают по своим свойствам синтетическим красителем. Недостатком подобного окрашивания является получение не ярких, а светлых оттенков; получение зеленых красителей из растительного сырья является затруднительным; при стирке ткани в обычной воде она сильно линяет.
Природные индикаторы получали из свеклы, моркови, краснокочанной капусты, будры, тюльпана, чистотела, черного чая, луковой шелухи, боярышника и шиповника. Сначала навеску сырья массой 5-10 г погружали в экстрагент объемом 50 мл. Полученные экстракты фильтровали с помощью фильтровальной бумаги, и полученный фильтрат наливали в заранее подготовленную колбу. Для определения эффективности индикатора был использован универсальный буферный раствор, обладающий большой буферной емкостью (pH от 2 до 12) из h4PO4, Ch4COOH, h4BO3, молярность 0,04 моль/л, концентрация кислот 100% [2].
К сожалению, из-за неустойчивости антоцианов их отвары быстро плесневеют и скисают, поэтому готовить такие индикаторы надо непосредственно перед работой с ними. Лучшими оказались индикаторы из краснокочанной капусты, будры и красного тюльпана. В растворе этих индикаторов наблюдался более выраженный переход из нейтральной среды в кислотную и щелочную. Более подробные результаты представлены в таблице 2.
Таблица 2
Результаты по приготовлению индикаторов
|
Растительный индикатор |
Изменение окраски индикатора в зависимости от среды |
||
|
Кислая |
Нейтральная |
Щелочная |
|
|
Цветы будры плющевидной |
Розовый |
Светло-розовый |
Ярко-зеленый |
|
Цветы красного тюльпана |
Теплый розовый |
Светло-розовый |
Темно-зеленый |
|
Плоды боярышника |
Розово-красный |
Светло-розовый |
Сине-зеленый |
|
Плоды шиповника |
Светло-желто-розовый |
Светло-желтый |
Желтый |
|
Листья краснокочанной капусты |
Розово-красный |
Бледно-фиолетовый |
Зеленый |
|
Листья черного чая |
Желто-коричневый |
Оранжево-коричневый |
Коричневый |
|
Листья чистотела |
Светло-желтый |
Желтый |
Темно-желтый |
|
Корнеплод моркови |
Светло-желтый |
Светло-желтый |
Светло-желтый |
|
Корнеплод свеклы |
Малиновый |
Красный |
Желто-коричневый |
|
Луковая шелуха |
Светло-оранжевый |
Оранжевый |
Коричневый |
С помощью приготовленных индикаторов из краснокочанной капусты и боярышника определили среду распространенных моющих средств и выяснили, что стиральные порошки «Зифа» и «Лоск» имеют щелочную среду, а моющее средство «Ферри» слабощелочную (табл.3). При использовании средств для мытья посуды, имеющих щелочную среду, нарушается нормальная кислотная среда кожи рук, которая в норме имеет слабокислую среду рН=5,5.
Таблица 3
Изменение окраски индикаторов и красителей
|
Природный индикатор |
Изменение окраски индикатора |
||
|
Стиральный порошок «Зифа» |
Стиральный порошок «Лоск» |
Средство для мытья посуды «Фэри» |
|
|
Краснокочанная капуста |
зеленый (щелочная среда) |
зеленый (щелочная среда) |
сине-зеленый (слабощелочная среда) |
|
Боярышник |
сине-зеленый (щелочная среда) |
сине-зеленый (щелочная среда) |
светло-зеленый (слабощелочная среда) |
Таким образом, при применении средств для мытья посуды необходимо использовать резиновые перчатки, защищающие кожу от действия на нее щелочной среды, которая разрушает кислотную мантию эпидермиса и вызывает кожные заболевания. Хотя на этикетках этих моющих средств производитель указывает, что они не оказывают вредного воздействия на кожу.
Также в ходе работы было проведено исследование содержания растительных пигментов в крапиве, краснокочанной капусте, свекле и моркови. Разделение растительных пигментов производили методом распределительно-сорбционной бумажной восходящей хроматографии, который основан на различии в коэффициентах распределения индивидуальных веществ между двумя фазами – органической и водной. В результате проведенного поэтапного эксперимента получили распределение отдельных пигментов на хроматографической бумаге (рис.4).
Ближе всех к старту находится желто-зеленое пятно хлорофилла в. Выше располагается пятно хлорофилла а, окрашенное в сине-зеленый цвет. Ещё дальше от старта расположился желто-коричневый след ксантофилла. Ближе всех к фронту растворителя подошел каротин, цвет пятна которого – желтый. Таким образом, каротиноиды, по сравнению с хлорофиллом, адсорбируются на фильтровальной бумаге хуже, поэтому передвигаются по ней дальше хлорофилла.

Рис.4. Распределение пигментов на хроматографической бумаге
В ходе проведенного исследования можно сделать следующие выводы:
Растительные пигменты - органические соединения, присутствующие в клетках и тканях растений и окрашивающие их. Они принадлежат к трем классам: хлорофиллы, каротиноиды и флавоноиды.
Используя растительные пигменты в качестве природных красителей, установили, что они являются пригодными для окраски тканей. При использовании растительных пигментов в качестве индикаторов было установлено, что они проявляют свойства кислотно-основного индикаторов и являются вполне «точными» определителями кислотности жидкостей.
Проведенный анализ растительных пигментов методом распределительной хроматографии показал, что спиртовая вытяжка листьев крапивы, краснокочанной капусты, корнеплодов свеклы и моркови содержит такие пигменты, как хлорофилл, каротин и ксантофилл.
Литература:
- Грищенко А. Игра цветов, или пигменты в нашей жизни / А. Грищенко, С.В. Кодацкая // Биология – Первое сентября. – 2010. – №6 [Электронный ресурс]. – URL: http://bio.1september.ru/view_article.php?ID=201000604 (дата обращения: 21.02.2015).
- Лурье Ю.Ю. Справочник по аналитической химии. – М.: Химия, 1989. – 448 с.
- Павлова С. Растительные индикаторы в школьной лаборатории / С. Павлова, В. Макарова, А.П. Петрова // «Проба пера». Естественные и математические науки: материалы VII школьной международной заочной научно-исследовательской конференции. – Новосибирск: СибАК, 2013. – С.161-168.
- Селиванов Е.В. Красители в биологии и медицине. – Барнаул: Азбука, 2003. – 40 с.
moluch.ru










