Круговорот углерода в природе. Углерод в растениях
ЦИКЛ УГЛЕРОДА | Энциклопедия Кругосвет
Содержание статьиЦИКЛ УГЛЕРОДА, круговорот углерода, – циклическое перемещение углерода между миром живых существ и неорганическим миром атмосферы, морей, пресных вод, почвы и скал. Это один из важнейших биогеохимических циклов, включающий множество сложных реакций, в ходе которых углерод переходит из воздуха и водной среды в ткани растений и животных, а затем возвращается в атмосферу, воду и почву, становясь снова доступным для использования организмами. Поскольку углерод необходим для поддержания любой формы жизни, всякое вмешательство в круговорот этого элемента влияет на количество и разнообразие живых организмов, способных существовать на Земле.
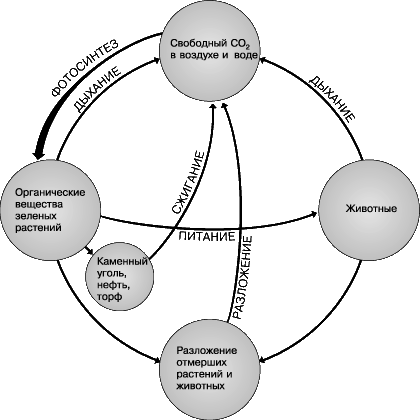
Источники и резервы углерода.
Основной источник углерода для живых организмов – это атмосфера Земли, где данный элемент присутствует в виде диоксида углерода (углекислого газа, СО2). В течение многих миллионов лет концентрация СО2 в атмосфере, по-видимому, существенно не менялась, составляя ок. 0,03% веса сухого воздуха на уровне моря. Хотя доля СО2 невелика, его абсолютное количество поистине огромно – ок. 750 млрд. т. В атмосфере СО2 переносится ветрами как в вертикальном, так и в горизонтальном направлениях.
Диоксид углерода присутствует в воде, где он легко растворяется, образуя слабую угольную кислоту Н2СО3. Эта кислота вступает в реакции с кальцием и другими элементами, образуя минералы, называемые карбонатами. Карбонатные породы, например известняк, находятся в равновесии с диоксидом углерода, который содержится в контактирующей с ними воде. Аналогичным образом количество СО2, растворенного в океанах и пресных водах, определяется его концентрацией в атмосфере. Общее количество растворенных и осадочных углеродсодержащих веществ оценивается примерно в 1,8 трлн. т.
Углерод в соединении с водородом и другими элементами является одним из основных компонентов клеток растений и животных. Например, в организме человека он составляет ок. 18% массы тела. Многочисленность и очень широкое распространение живых организмов не позволяют удовлетворительно оценить общее содержание в них углерода. Можно, однако, приблизительно оценить суммарное количество углерода, связываемого растениями, а также выделяемого в процессе дыхания растений, животных и микроорганизмов. Установлено, что зеленые растения поглощают в год ок. 220 млрд. т CO2. Почти такое же количество этого вещества выделяется в неорганическую среду в процессе дыхания всех живых организмов, а также в результате разложения и сгорания органических веществ.
При определенных условиях разложения и сгорания созданных живыми организмами веществ не происходит, что ведет к накоплению углеродсодержащих соединений. Так, например, древесина живых деревьев может быть на 3–4 тысячелетия надежно защищена от микробного разложения и от пожара корой, способной противостоять действию микробов и огня. Древесина же, попавшая в торфяное болото, сохраняется еще дольше. В обоих случаях связанный в ней углерод оказывается как бы в ловушке и надолго выводится из круговорота. В условиях, когда органическое вещество оказывается захороненным и изолированным от воздействия воздуха, оно разлагается только частично и содержащийся в нем углерод сохраняется. Если впоследствии в течение миллионов лет эти органические остатки подвергаются давлению вышележащих отложений и нагреванию за счет земного тепла, значительная часть его превращается в ископаемое топливо, например в каменный уголь или нефть. Ископаемое топливо образует природный резерв углерода. Несмотря на интенсивное его сжигание, начавшееся с 1700-х годов, неизрасходованными еще остаются примерно 4,5 трлн. т.
Фотосинтез.
Основной путь, посредством которого углерод из мира неорганического перемещается в мир живого, – это осуществляемый зелеными растениями фотосинтез. Данный процесс представляет собой цепь реакций, в ходе которых растения поглощают из атмосферы или воды диоксид углерода, связывая его молекулы с молекулами специального вещества – акцептора СО2. В ходе других реакций, идущих с потреблением солнечной (световой) энергии, происходит расщепление молекул воды и использование высвобождающихся ионов водорода и связанного СО2 в синтезе богатых углеродом органических веществ, в том числе акцептора СО2.
На каждую молекулу СО2, которую поглощает растение, чтобы синтезировать органические вещества, выделяется молекула кислорода, образованная при расщеплении воды. Предполагается, что именно таким путем образовался весь свободный кислород атмосферы. Если бы процесс фотосинтеза на Земле внезапно прекратился и нарушился углеродный цикл, то, согласно имеющимся расчетам, весь свободный кислород исчез бы из атмосферы примерно за 2000 лет. См. также ФОТОСИНТЕЗ.
Другие реакции.
Зеленое растение использует углерод образуемых им органических веществ разными способами. Например, он может накапливаться в составе крахмала, запасаемого в клетках, или целлюлозы – основного структурного материала растений и питательного вещества для многих других организмов. И крахмал и целлюлоза усваиваются в качестве пищи только после расщепления на составляющие их 6-углеродные сахара (т.е. сахара, содержащие по шесть атомов углерода в молекуле). В отличие от крахмала – нерастворимого высокомолекулярного соединения – 6-углеродные сахара легко растворимы и, перемещаясь по растению, служат источником энергии и материалом для роста и обновления клеток, а также для их восстановления в случае повреждений. Проростки, например, расщепляют запасенные в семени крахмал и жиры, получая из них более простые органические вещества, используемые в процессе клеточного дыхания (для высвобождения их энергии) и для роста.
У животных поглощенная пища подвергается аналогичному процессу переваривания. Прежде чем ее основные компоненты могут быть усвоены, они должны быть преобразованы: углеводы – в 6-углеродные сахара, жиры – в глицерин и жирные кислоты, белки – в аминокислоты. Эти продукты переваривания служат животному источниками энергии, высвобождаемой при дыхании, а также строительными блоками, необходимыми для роста организма и обновления его компонентов. Подобно растениям, животные способны переводить питательные вещества в форму, удобную для запасания. Аналог крахмала у животных – это гликоген, образуемый из излишков 6-углеродных сахаров и накапливаемый в качестве энергетического резерва в печени и мышечных клетках. Избыток сахара может превращаться также в жирные кислоты и глицерин, которые вместе с такими же веществами, поступающими с пищей, используются для синтеза жиров, накапливаемых в ткани. Таким образом, процессы синтеза обеспечивают запасание богатых углеродом и связанной энергией веществ, что позволяет организму выживать в периоды нехватки пищи.
Одна из характерных особенностей всего живого – постоянная потребность в энергии. Организм получает энергию посредством дыхания – целой серии процессов, в ходе которых сложные углеродсодержащие молекулы превращаются в простые. Большинство растений и животных способно только к аэробному дыханию, т.е. они поглощают кислород из воздуха, образуя диоксид углерода и воду в качестве конечных продуктов. Однако существуют некоторые бактерии, простейшие и даже многоклеточные животные (кишечные паразиты), являющиеся анаэробами: они способны жить в отсутствие кислорода в среде; при этом конечными продуктами их анаэробного дыхания (брожения разных типов) тоже служит диоксид углерода и вода. Очень немногие организмы (например, дрожжи) могут быть как аэробами, так и анаэробами. В аэробных условиях дрожжи образуют в качестве конечных продуктов диоксид углерода и воду, а в анаэробных – диоксид углерода и этиловый спирт. Таким образом, независимо от типа дыхания оно всегда ведет к высвобождению углерода в форме диоксида, который затем снова вовлекается в глобальный цикл.
После своей смерти растения и животные становятся пищей для т.н. редуцентов – организмов, осуществляющих разложение органического вещества. Большая часть редуцентов представлена бактериями и грибами, клетки которых выделяют наружу, в свое непосредственное окружение, небольшие количества пищеварительной жидкости, расщепляющей субстрат, а затем потребляют продукты такого «переваривания». Как правило, редуценты имеют ограниченный набор ферментов и соответственно используют в качестве пищи и источника энергии только немногие типы органических веществ. Обычные дрожжи, например, перерабатывают только 6- и 12-углеродные сахара, содержащиеся в разрушенных клетках перезрелых фруктов или в густом (с мякотью) соке, полученном при их раздавливании. Однако при достаточной длительности воздействия разнообразных редуцентов все углеродсодержащие вещества растений или животных в конце концов разрушаются до диоксида углерода и воды, а высвобожденная энергия используется организмами, осуществляющими разложение. Многие искусственно синтезированные органические соединения тоже подвержены биологическому разрушению (биодеградации) – процессу, в ходе которого редуценты получают энергию и необходимый строительный материал, а в атмосферу выделяется углерод в форме диоксида углерода.
www.krugosvet.ru
Углерод, ассимиляция растениями - Справочник химика 21
Мир растений — исполинское производство высокомолекулярных соединений, в котором осуществляется биохимический синтез высших полисахаридов и лигнина. Катализаторами сложных процессов, приводящих к синтезу высокомолекулярных соединений в растениях, служат белки-ферменты исходным сырьем в синтезе углеводов является двуокись углерода, которая, будучи конечным продуктом окисления любых углеродсодержащих соединений, непрерывно выделяется в атмосферу. Единственным природным процессом, в котором двуокись углерода претерпевает обратное превращение в сложные органические соединения, является ее ассимиляция растениями. Таким образом поддерживается круговорот углерода и сохраняется его баланс на земном шаре. [c.12] Зеленые растения поглощают из воздуха диоксид углерода и вьщеляют кислород (ассимиляция диоксида углерода растениями). Прямо или косвенно все вещества, содержащиеся в растениях, образуются из ассимилированного диоксида углерода. Органические вещества, синтезированные в растениях в результате эндотермических реакций, содержат большую часть поглощенной солнечной энергии. Эти вещества используются частично растениями и животными, благодаря чему углерод, ассимилированный растениями, возвращается в виде СО2. В этих биологических процессах освобождается вся энергия, поглощенная при первоначальной ассимиляции диоксида углерода. Следовательно, в природе происходят, с одной стороны, биологический круговорот углерода, начиная с неорганической [c.14]Органические вещества, синтезированные в растениях в результате эндотермических реакций, содержат большую часть поглощенной солнечной энергии. Эти вещества используются частично растениями и животными, благодаря чему углерод, ассимилированный растениями, возвращается в виде СО2. В этих биологических процессах освобождается вся энергия, поглощенная при первоначальной ассимиляции диоксида углерода. Следовательно, в природе происходят, с одной стороны, биологический круговорот углерода, начиная с неорганической [c.14]
Ржавление железа, полимеризация высыхающих масел, выветривание угля, старение каучука и резины, прогоркание жиров и масел, обмен веществ у бактерий, дыхание животных, ассимиляция двуокиси углерода зелеными растениями, окислительные процессы при усвоении пищи, холоднопламенное горение, [c.267]
Кетопентозы. Ъ-Рибулоза — эпимер D-рибозы играет важную роль в ассимиляции двуокиси углерода зелеными растениями и, по всей вероятности, в аэробном распаде углеводов. [c.241]
Фотосинтезы углеводов в растениях. Ассимиляция двуокиси углерода зелеными растениями под влиянием света является единственной реакцией в природе, за счет которой органические вещества образуются из неорганического материала, и, следовательно, опа является источником всего органического на земном шаре. [c.259]
Согласно одной из старых теорий (А. Байер, 1870 г.), первичным продуктом ассимиляции двуокиси углерода в растениях является формальдегид, в результате полимеризации которого образуется глюкоза, а из последней — крахмал. В результате новых исследований установлено, что формальдегид не возникает в качестве промежуточного продукта в этом синтезе. Таким образом, не существует какой-либо аналогии между описанными выше синтезами и фотосинтезом в растениях. Последний можно изобразить следующим стехиометрическим уравнением [c.260]
Можно утверждать, что без катализа вообще была бы невозможна жизнь. Достаточно сказать, что лежащий в основе жизнедеятельности процесс ассимиляции двуокиси углерода хлорофиллом растений является фотохимическим и каталитическим процессом. Простейшие органические вещества, полученные в результате ассимиляции, претерпевают затем ряд сложных превращений. В химические функции живых клеток входит разложение и синтез белка, жиров, углеводов, синтез различных, часто весьма сложных молекул. Таким образом, клетка является своеобразной и весьма совершенной химической лабораторией, а если учесть, что все эти процессы каталитические — лабораторией каталитической. Катализаторами биологических процессов являются особые вещества — ферменты. Если сравнивать известные нам неорганические катализаторы с ферментами, то прежде всего поражает колоссальная каталитическая активность ферментов. Так. 1 моль фермента алкогольдегидрогеназа в 1 сек при комнатной температуре превращает 720 моль спирта в уксусный альдегид в то время как промышленные катализаторы того же процесса (в частности, медь) при 200 °С в 1 сек превращают не больше 0,1—1 моль на один грамм-атом катализатора. Или, например, 1 моль фермента каталазы при О °С разлагает в одну секунду 200 ООО моль перекиси водорода. Наиболее же активные неорганические катализаторы (платиновая чернь) при 20 °С разлагают 10—80 моль перекиси в 1 сек на одном грамм-атоме катализатора. Приведенные примеры показывают, что природные биологические катализаторы во много раз превосходят по активности синтетические неорганические катализаторы. Высокая специфичность и направленность действия, а также способность перерабатывать огромное количество молекул субстрата за короткое время при температуре существования живого организма и позволяет ферментам в достаточном количестве давать необходимые для жизнедеятельности соединения или уничтожать накапливающиеся в процессе жизнедеятельности бесполезные, а иногда и вредные продукты. [c.258]
При усвоении (ассимиляции) растениями двуокиси углерода образуются высшие полисахариды, от процесс суммарно выражается уравнением [c.7]
Многие вещества при обыкновенной температуре и атмосферном давлении термодинамически неустойчивы по сравнению с входящими в их состав простыми веществами. Во многих химических реакциях образуются не наиболее термодинамически устойчивые молекулы, а другие, менее устойчивые (метастабильные, лабильные) молекулы, однако они достаточно устойчивы, чтобы существовать длительное время и принимать участие в других реакциях. Вследствие инертности их молекул такие вещества на первый взгляд не отвечают условиям устойчивости, устанавливаемым законами термодинамики, и определяются законами химической кинетики. Наконец, существуют реакции, протекающие в направлении, противоположном направлению установления равновесия, под влиянием некоторых внешних воздействий. Примером является ассимиляция двуокиси углерода зелеными растениями при действии света (см. стр. 196). Изучение подобных реакций также относится к области химической кинетики. [c.267]
Ряд работ Буссенго по физиологии растений был связан с вопросами ассимиляции углерода листьями растений. Буссенго установил, что источником углерода служит рассеянная в природе углекислота, и провел многочисленные исследования по выявлению отношения между объемами разложенной углекислоты и образовавшегося кислорода, росту растений в темноте, влиянию внешних условий на ассимиляцию углерода листьями и т. д. [c.47]
Уже давно высказывались предположения, что в процессе ассимиляции углерода зелеными растениями происходит восстановление углекислоты, причем образуется простейший альдегид [c.138]
Крахмал является одним из продуктов ассимиляции углерода зелеными растениями и служит для них пищевым резервом. Крахмал скопляется главным образом в клубнях и семенах, но находится И в других частях растения. [c.403]
Фотохимические реакции весьма распространены. Достаточно указать на так называемую реакцию фотосинтеза, протекающую в растениях при участии зеленого пигмента — хлорофилла — при поглощении солнечной радиации. Фотосинтез сводится к ассимиляции оксида углерода (IV) с образованием углеводов и выделением кислорода. Это многостадийный процесс, суммарное уравнение которого можно записать в виде [c.269]
Крахмал (СвН Оэ) . Крахмал — широко распространенный в природе полисахарид, образующийся в растениях как конечный продукт ассимиляции ими двуокиси углерода из воздуха под влиянием [c.259]
Биологическое значение кислорода трудно переоценить. Только немногие низшие живые организмы (дрожжи, некоторые бактерии), называемые анаэробными, могут существовать при отсутствии кнсло-рода. Теплокровные животные погибают без кислорода в течение нескольких минут. Как животные, так и растения при дыхании поглощают атмосферный кислород, а выделяют оксид углерода (IV). Но у зеленых растений на свету происходит и обратный процесс — ассимиляция, при котором поглощается оксид углерода (IV), а выделяется кислород. В результате круговорота кислорода поддерживается постоянное содержание его в воздухе. Разумеется, круговорот кислорода в природе тесно связан с круговоротом углерода (см. схему) [c.375]
В 1870 г. Байер, основываясь на опытах Бутлерова, получившего первое сахаристое вещество уплотнением формальдегида, высказал предположение, что муравьиный альдегид является первым продуктом ассимиляции углерода растениями [c.206]
В 1870 г. Байер высказал предположение о том, что ассимиляция углерода зелеными частями растений протекает через промежуточное образование форм альдегида, который далее полимеризуется в сахаристые вещества. [c.555]
Зеленые растения поглощают из воздуха диоксид углерода и выделяют кислород (ассимиляция диоксида углерода растениями). Прямо или косвенно все вещества, содержащиеся в растениях, образуются из ассимилированного диоксида углерода. [c.14]
Углеводы образуются в растениях в ходе фотосинтеза, благодаря ассимиляции хлорофиллом, под действием солнечных лучей, углекислого газа, содержащегося в воздухе, а образующийся при этом кислород выделяется в атмосферу. Углеводы являются первыми органическими веществами в кругообороте углерода в природе. [c.41]
Байер впервые предположил (1870), что в процессе фотосинтеза в растениях на первой фазе образуется муравьиный альдегид, и первую стадию ассимиляции двуокиси углерода и воды выразил уравнением [c.295]
Химическое действие света не только благоприятствует реакциям присоединения, окисления и восстановления, замещения, изомеризации, полимеризации и расщепления, но ведет даже к особого рода синтезу. Важность этой темы оправдывает, пусть даже беглый, обзор полученных результатов . Одними из первых наблюдений химического действия света, не считая, естественно, процесса ассимиляции угольной кислоты растениями, были наблюдения Дж. Дэви (1812) над образованием фосгена, или хлорокиси углерода, из окиси углерода и хлора [c.384]
Основные научные работы посвящены изучению химизма ассимиляции углерода зелеными растениями, проблеме окислительных процессов в живой клетке, учению о ферментах. Дал (1893) объяснение химизма процесса ассимиляции углекислого газа хлорофильиыми растениями с образованием сахара, согласно которому в основе этого процесса лежит сопряженная окис-лительно-восстановительная реакция, происходящая за счет элементов воды. Показал, что источником выделяющегося при ассимиляции молекулярного кислорода являет- [c.41]
Основные научные работы посвящены изучению механизма фотосинтеза. Показал (1941), что первичный процесс фотосинтеза заключается в фотолизе молекулы воды, в результате чего образуются кислород, выделяющийся в атмосферу, и водород, идущий на восстановление двуокиси углерода. Используя радиоактивный изотоп углерод-14 в качестве метки и метод хроматографии на бумаге, установил последовательность фо-тосинтетического цикла (цикла Кэлвина) ассимиляция двуокиси углерода зеленььми растениями — превращение его в органические вещества — последующее восстановление. Создал (1956) схему полного пути углерода при фотосинтезе, ставшую классической. Предложил модель превращения световой энергии в химическую. Показал, что превращения фосфата пентозы играют большую роль в жизнедеятельности не только растений, но и животных. Изучал вопрос о происхождении и развитии жизни на Земле. [c.279]
Крупнейший ученый-биохимик и революционный деятель. Академик. Герой Социалистического Труда. Лауреат премии им. В. И. Ленина и Государственной премии СССР. В 1918 г. организовал Центральную химическую лабораторию при ВСНХ, преобразованную затем в Физико-химический институт им. л. я. Карпова, директором которого был до конца жизни. В 1935 г. организовал совместно с известным биохимиком (впоследствии академиком) Л. И. Опариным Институт биохимии АН СССР. Президент Всесоюзного хи.мического общества им. Д. И. Менделеева (1935— 1946 гг.). Основные труды посвящены важнейшим проблемам биохимии химизму ассимиляции углерода зелеными растениями проблеме окислительных процессов, происходящих в живой клетке учению о фер.ментах [c.138]
Эта первая книга нового типа но питанию растений содержала тщательные анализы газов, гумуса и золы. Измерения Соссюра окончательно доказали правильность учения Ингенхуза о воздушном питании и показали, какие элементы добываются растением из почвы. Они подтвердили догадку Сенебье, что растения довольствуются питанием за счет малого количества двуокиси углерода, постоянно присутствующей в воздухе, и что это единственный источник их углеродного фонда . Соссюр первый сопоставил количества поглощенного углекислого газа и выделяемого кислорода. Наконец, и это самое главное, он показал, что возрастание сухого веса, вызванное ассимиляцией определенного количества двуокиси углерода, значительно больше веса содержащегося в ней углерода так как в воздух выделяется такое количество кислорода, которое эквивалентно кислороду, содержащемуся в усвоенной углекислоте, то большая прибавка в весе не может быть отнесена к совместной с углеродом ассимиляции кислорода за счет этого источника. [c.31]
АССИМИЛЯЦИЯ. Усвоение живыми организмами различных питательных веществ, обеспечивающее их жизнь, рост и размножение. Особенно важна для жизни всех организмов Л. углерода зелеными растениями из углекислого газа в щроцессе фотосинтеза. Диссимиляцией называется процесс, обратный А. [c.32]
Как уже было указано, содержание СО2 в воздухе составляет 0,03 об.% ил 0,047 вес.%. С другой стороны, зная вес воздуха (стр. 398), можно легко вычислить общий вес двуокиси углерода в нем (2,5-101Б кг). Это количество является небольшим по сравнению с количеством двуокиси углерода, ассимилированным наземными и морскими растениями. Хотя количество ассимилируемой двуокиси углерода не может быть определено точно, согласно некоторым приближенным оценкам, оно составляет не меньше 5-1013 ежегодно. Таким образом, запаса двуокиси углерода в атмосфере хватило бы только на 50 лет, если бы он не возобновлялся. Каким бы приближенным ни был этот расчет, очевидно, что запас двуокиси углерода невелик. Следовательно, необходимо допустить, что баланс расхода и образования двуокиси углерода устанавливается за короткий срок, так как примерно 100 лет, на протяжении которых проводились более точные анализы воздуха, не наблюдалось заметных колебаний средней концентрации СО2 в воздухе. Основным источником увеличения концентрации СОг в атмосфере является гниение растений, затем идет дыхательный процесс животных. В результате этих процессов почти весь углерод пищи превращается в СО2. Для того чтобы иметь представление об этих количествах, произведем расчет количества СО2, выделяемой человеком. Человек в состоянии покоя выдыхает примерно 4 см СО2 на 1 кг веса в 1 мин следовательно, человек, вес которого равен 70 кг, выдыхает примерно 800 г СО2 в сутки, а З-Ю человек на Земле производят всего примерно 8,7-10ЧА г СО2 в год. Это количество представляет около 1,7% указанного выше ежегодного рас-хода на ассимиляцию растениями. Менее важны количества СО2, выделяющейся при гниении мертвых животных. [c.488]
Первый из этих процессов в небольшой степени компенсируется за счет добычи и сжигания угля и нефти. Годовая добыча угля и нефти составляет примерно 4,5- кг. В них содержится 85% (3,8-1012 кг) углерода, при горении которого образуется 1,4-101 кг СОг. Примерно 30% этого количества СОг ежегодно потребляется при ассимиляции растениями. Второй процесс необратимого исчезновения двуокиси углерода из атмосферы (минерализация) также компенсируется в небольшой степени за счет двуокиси углерода вулканического происхождения. Таким образом, баланс двуокиси углерода в природе аефицитен на долгий срок. [c.489]
Основные иссд[едования К, А. Тимирязева по физиологии растений гюсвящены процессу фотосинтеза. Для проведения опытов он сконструировал, ряд ор[[гииад[ЬНых приборов. К. А. Тимирязев установил зависимость фотосинтеза от интенсивности света и его спектрального состава, показал, что ассимиляция растениями углерода из углекислого газа воздуха происходит за счет энергии Солнечного света, главным образом красных и синих д[учей, поглощаемых хлорофиллом. [c.9]
Гайических веществ клетки, диссимиляция (катаболиче-ские процессы, которые являются экзергоническими). Различают две основные формы диссимиляции — дыхание и брожение. Процессы образования-биологических соединений и веществ, поступающих из внешней среды,— биосинтетические процессы (анаболические) идут с затратой энергии (эндергонические), т. е. представляют собой ассимиляцию. Важнейший биосинтетический процесс — ассимиляция углерода зелеными растениями и бактериями путем использования энергии света (фотосинтез) или энергии других химических реакций (хемосинтез). [c.174]
Среди многочисленных фотохимических реакций особое значение имеет реакция ассимиляции углерода растениями, без которой не мо1 ла бы существовать жизнь на земле. Эта реакция может быть 3Jписана в виде [c.362]
Квантовый выход этой реакции блнзо1Механизм реакции ассимиляции углерода растениями до сих пор полностью не выяснен. Сильно. эндотермический процесс усвоения двуокиси углерода растениями с образованием углеводов осуществляется за счет энергии солнечных лучей. [c.362]
Полимеризацией формальдегида А. М. Бутлеров осуществил первый в науке синтез сахаристого вещества. Основываясь на этом синтезе, Вайер в 1870 г. высказал предположение, что формальдегид является первым продуктом ассимиляции (усвоения) углерода растениями [c.228]
Исследовались продукты фотосиптетической ассимиляции меченной С двуокиси углерода у короткодневных и длиннодневиых растений при разных фотопериодах [135]. При этом показано, что длина дня не оказывает влияния на состав продуктов фотосинтеза у растений с различным фотопериодом. Установлены сходство и различия в продуктах фотосинтеза у растений различных видов [136]. Наиболее обстоятельно исследовано фотосинтетическое включение С в кетокислоты растений [c.84]
Две важнейшие специфические для растений функции осуществляются фо-тосмитезнруюшимн клетками, которые содержат хлоропласты и служат для всего организма источником органических веществ-продуктов ассимиляции углерода, и всасывающими клетками, которые поглощают из окружающей среды воду и растворенные минеральные вещества. У большинства высших растений эти две функции не могут выполняться одними и теми же клетками, так как для первой из них нужен свет, а вторая осуществляется в толше почвы в темноте. Для каждого из этих процессов требуется и ряд других условий. Фотосинтез, например, должен протекать в особой микросреде, где строго регулируется относительная влажность и содержание СОг. Достигается это с помощью устьиц-особых отверстий в покрытом кутикулой эпидермисе, которые способны открываться и закрываться в зависимости от тургора замыкающих клеток (рис. 19-10). С другой стороны, для эффективного поглощения веществ из почвы нужна очень большая всасывающая поверхность, которую обеспечивают корни необходимы также мембранные транспортные [c.175]
Рихард Вильштеттер (1872—1942 гг.) — выдающийся немецкий химик-оргаппк. Основные работы его связаны с исследованием строения хлорофилла, изучением химии ферментов и процессов ассимиляции двуокиси углерода растениями. За научные заслуги Вильштеттер был избран иностранным членом Академии наук СССР. [c.609]
chem21.info
Углеродное сельское хозяйство – новая надежда для огородников
В большинстве случаев письма приходят в течение одной минуты, но иногда для этого требуется до 10 минут. Возможно письмо еще не успело прийти. Проверьте пожалуйста внимательно папку Входящие (Inbox). В некоторых случаях письмо может попасть в папку Спам (Spam).
Логин или e-mail: Или войдите с помощью этих сервисов:


www.ogorod.ru
Углерод, его химическое и биологическое значение
Углерод.
Биологическое значение.
Все без исключения живые организмы построены из соединений углерода. Особенностью атома углерода является их способность соединяться между собой, образуя сколь угодно длинные цепи, которые могут быть и разветвленными, содержащими миллионы и миллиарды атомов углерода, соединенных с атомами других элементов (самые из известных молекул – это молекулы белков, содержащих до миллиарда углеродных звеньев). Их длина может даже достигать одного метра!
Углерод в организме. Углерод - важнейший биогенный элемент, составляющий основу жизни на Земле, структурная единица огромного числа органических соединений, участвующих в построении организмов и обеспечении их жизнедеятельности (биополимеры, а также многочисленные низкомолекулярные биологически активные вещества - витамины, гормоны, медиаторы и другие). Значительная часть необходимой организмам энергии образуется в клетках за счет окисления Углерода. Возникновение жизни на Земле рассматривается в современное науке как сложный процесс эволюции углеродистых соединений.
Уникальная роль Углерода в живой природе обусловлена его свойствами, которыми в совокупности не обладает ни один других элемент периодической системы. Между атомами Углерода, а также между Углеродом и другими элементами образуются прочные химические связи, которые, однако, могут быть разорваны в сравнительно мягких физиологических условиях (эти связи могут быть одинарными, двойными и тройными). Способность Углерода образовывать 4 равнозначные валентные связи с других атомами Углерода создает возможность для построения углеродных скелетов различных типов - линейных, разветвленных, циклических. Показательно, что всего три элемента - С, О и Н - составляют 98% общей массы живых организмов. Этим достигается определенная экономичность в живой природе: при практически безграничном структурном разнообразии углеродистых соединений небольшое число типов химических связей позволяет намного сократить количество ферментов, необходимых для расщепления и синтеза органических веществ. Особенности строения атома Углерода лежат в основе различных видов изомерии органических соединений (способность к оптической изомерии оказалась решающей в биохимической эволюции аминокислот, углеводов и некоторых алкалоидов).
Согласно общепринятой гипотезе А. И. Опарина, первые органических соединения на Земле имели абиогенное происхождение. Источниками Углерода служили метан (СН4) и цианистый водород (HCN), содержавшиеся в первичной атмосфере Земли. С возникновением жизни единственным источником неорганического Углерода, за счет которого образуется все органическое вещество биосферы, является оксид углерода (IV) (СО2), находящийся в атмосфере, а также растворенный в природных водах в виде НСО3. Наиболее мощный механизм усвоения (ассимиляции) Углерода (в форме СО2) - фотосинтез - осуществляется повсеместно зелеными растениями (ежегодно ассимилируется около 100 млрд. т СО2). На Земле существует и эволюционно более древний способ усвоения СО2 путем хемосинтеза; в этом случае микроорганизмы-хемосинтетики используют не лучистую энергию Солнца, а энергию окисления неорганических соединений. Большинство животных потребляют Углерод с пищей в виде уже готовых органических соединений. В зависимости от способа усвоения органических соединений принято различать автотрофные организмы и гетеротрофные организмы. Применение для биосинтеза белка и других питательных веществ микроорганизмов, использующих в качестве единственного источника Углерода углеводороды нефти, - одна из важных современное научно-технических проблем.
Содержание Углерода в живых организмах в расчете на сухое вещество составляет: 34,5-40% у водных растений и животных, 45,4-46,5% у наземных растений и животных и 54% у бактерий. В процессе жизнедеятельности организмов, в основные за счет тканевого дыхания, происходит окислительный распад органических соединений с выделением во внешнюю среду СО2. Углерод выделяется также в составе более сложных конечных продуктов обмена веществ. После гибели животных и растений часть Углерода вновь превращается в СО2 в результате осуществляемых микроорганизмами процессов гниения. Таким образом происходит круговорот Углерода в природе. Значительная часть Углерода минерализуется и образует залежи ископаемого Углерода: каменные угли, нефть, известняки и другие. Помимо основной функции - источника Углерода - СО2, растворенная в природных водах и в биологических жидкостях, участвует в поддержании оптимальной для жизненных процессов кислотности среды. В составе СаСО3 Углерод образует наружный скелет многих беспозвоночных (например, раковины моллюсков), а также содержится в кораллах, яичной скорлупе птиц и других Такие соединения Углерода, как HCN, СО, ССl4, преобладавшие в первичной атмосфере Земли в добиологический период, в дальнейшем, в процессе биологической эволюции, превратились в сильные антиметаболиты обмена веществ.
Помимо стабильных изотопов Углерода, в природе распространен радиоактивный 14С (в организме человека его содержится около 0,1 мккюри). С использованием изотопов Углерода в биологических и медицинских исследованиях связаны многие крупные достижения в изучении обмена веществ и круговорота Углерод в природе. Так, с помощью радиоуглеродной метки была доказана возможность фиксации Н14СО3- растениями и тканями животных, установлена последовательность реакций фотосинтеза, изучен обмен аминокислот, прослежены пути биосинтеза многих биологически активных соединений и т. д. Применение 14С способствовало успехам молекулярной биологии в изучении механизмов биосинтеза белка и передачи наследственной информации. Определение удельной активности 14С в углеродсодержащих органических остатках позволяет судить об их возрасте, что используется в палеонтологии и археологии
Применение
Графит используется в карандашной промышленности. Также его используют в качестве смазки при особо высоких или низких температурах.
Алмаз, благодаря исключительной твердости, незаменимый абразивный материал. Алмазным напылением обладают шлифовальные насадки бормашин. Кроме этого, ограненные алмазы — бриллианты используются в качестве драгоценных камней в ювелирных украшениях. Благодаря редкости, высоким декоративным качествам и стечению исторических обстоятельств, бриллиант неизменно является самым дорогим драгоценным камнем. Исключительно высокая теплопроводность алмаза (до 2000 Вт/м·К) делает его перспективным материалом для полупроводниковой техники в качестве подложек для процессоров. Но относительно высокая цена (около 50 долларов/грамм) и сложность обработки алмаза ограничивают его применение в этой области.
В фармакологии и медицине широко используются различные соединения углерода — производные угольной кислоты и карбоновых кислот, различные гетероциклы, полимеры и другие соединения. Так, карболен (активированный уголь), применяется для абсорбции и выведения из организма различных токсинов; графит (в виде мазей) — для лечения кожных заболеваний; радиоактивные изотопы углерода — для научных исследований (радиоуглеродный анализ).
Углерод играет огромную роль в жизни человека. Его применения столь же разнообразны, как сам этот многоликий элемент.
Углерод является основой всех органических веществ. Любой живой организм состоит в значительной степени из углерода. Углерод — основа жизни. Источником углерода для живых организмов обычно является СО2 из атмосферы или воды. В результате фотосинтеза он попадает в биологические пищевые цепи, в которых живые существа пожирают друг друга или останки друг друга и тем самым добывают углерод для строительства собственного тела. Биологический цикл углерода заканчивается либо окислением и возврашением в атмосферу, либо захоронением в виде угля или нефти.
Углерод в виде ископаемого топлива: угля и углеводородов (нефть, природный газ) — один из важнейших источников энергии для человечества. В смеси с техническими маслами в качестве смазочного материала. Из смеси графита с глиной изготавливают плавильные тигли. Графит используют в ядерной промышленности, как поглотитель нейтронов.
Кокс применяют в металлургии, как восстановитель. Древесный уголь – в кузнечных горнах, для получения пороха (75%KNO3 + 13%C + 12%S), для поглощения газов (адсорбция), а также в быту. Сажу применяют, как наполнитель резины, для изготовления черных красок – типографская краска и тушь, а также в сухих гальванических элементах. Стеклоуглерод применяют для изготовления аппаратуры для сильно агрессивных сред, а также в авиации и космонавтике.
Активированный уголь поглощает вредные вещества из газов и жидкостей: им заполняют противогазы, очистительные системы, его применяют в медицине при отравлениях.
mirznanii.com
Круговорот углерода в природе - Экологический дайджест FacePla.net
Создано 07.01.2010 16:16 Автор: Александр Компанеец
Мы не беремся однозначно утверждать, что деятельность человека является основной причиной глобального изменения климата, но также глупо было бы утверждение того, что человек не влияет на окружающую среду. Мы стараемся рассматривать имеющиеся у нас факты и знания, и делиться ими с нашими читателями. Разные существуют мнения по поводу влияния парниковых газов на повышение средней годовой температуры на Земле. Кто-то считает это всемирным заговором, целью которого является передел сфер влияния на рынке энергоресурсов и в целом промышленности, кто-то видит в этом испытания метеорологического оружия. Наша задача донести до Вас различные мнения и фактическую информацию, чтобы Вы самостоятельно могли формировать свое мнение.
Одно остается неоспоримым: мы влияем на нашу планету и жизнь на Земле сильно и непосредственно, и в наших руках менять силу и направление этого воздействия - сделать эту планету цветущим оазисом или малопригодной для жизни пустыней. На мой взгляд, современный уровень технологий вполне позволяет каждому из нас включиться в процесс создания экологически дружественного общества и начать, как это обычно бывает, необходимо с себя.
В этой статье мы расскажем про углерод – основной строительный кирпичик жизни. И почему нас так пугают, тем из чего состоят все живые формы на Земле.
Глобальный круговорот углерода в природе можно разделить на две основные категории: геологический, временной цикл которого исчисляется миллионами лет, и значительно более быстрый – биологический с временным циклом от нескольких дней до нескольких тысячелетий. Мы, люди, имеем влияние на обе эти категории.
Глобальный углеродный круговорот являет собой перемещение углерода между различными «резервуарами», и происходит благодаря множеству различных химических, физических, геологических и биологических процессов. Поверхность современного океана является наиболее активным буфером обмена углерода на Земле, однако на больших глубинах такого быстрого обмена с атмосферой происходить не может.

На диаграмме Вы можете проследить основные направления движения и места залегания углерода в экосистеме Земли. Обычно принято выделять четыре основных места концентрации углерода, это:
- · Атмосфера
- · Наземная биосфера, включающая неживой органический материал, такой как почва и осадочные породы
- · Океаны, которые содержат углерод в растворенном виде и живую и неживую морскую органику
- · Ископаемые ресурсы органического происхождения.
В атмосфере Земли углерод преимущественно существует в виде диоксида (CO2). И хотя его содержание кажется ничтожно малым (около 0.04% и по утверждениям ученых продолжает расти), он играет важнейшую роль в поддержании жизни на Земле. Существует еще несколько газов, таки как, например метан, содержащих углерод, которые также играют свою роль в углеродном обмене. В концепции теории глобального потепления эти газы называют парниковыми, и считается, что именно повышение концентрации этих газов приводит к парниковому эффекту и как следствие к глобальному повышению температуры.
Углерод. Куда он девается?
1. Солнечный свет позволяет растениям поглощать углекислый газ из атмосферы благодаря явлению фотосинтеза, выделяя в атмосферу кислород. Наиболее активными, эффективными и долговечными «хранителями» углерода являются деревья. В процессе развития и роста деревья очень быстро поглощают и накапливают углерод, а в зрелом возрасте способны хранить его сотни лет. Поэтому сохранение и умножение лесов – одна из важнейших задач сохранения и поддержания глобального углеродного баланса.
2. Ближе к полюсам поверхность океанов становится прохладнее, а CO2 более растворимым. В холодных водах океана углекислый газ поглощается, а при повышении температуры воды у поверхности приводит к выделению излишков газа в атмосферу. Вот почему повышение средней глобальной температуры может ускорить процесс нарушения природного баланса углерода в атмосфере.
3. В верхних слоях океана находятся наиболее продуктивные живые организмы, чьи ткани, органы и раковины строятся на основе углерода, и тем самым абсорбируют атмосферный углерод, растворенный в верхних слоях воды. Наряду с лесами на суше, морские живые организмы - это важнейшие «утилизаторы» атмосферного углерода. Мировой океан содержит около 36000 гигатонн углерода. Потепление же морской воды препятствует привычному формированию живых организмов, тем самым снижая темпы поглощения углерода.
4. По мере того как морские обитатели погибают, твердые части их тел, такие как раковины, клешни и кости оседают на морское дно, формируя залежи осадочных пород – своего рода долгосрочный углеродный депозит.
Углерод. Откуда он берется?
Углерод возвращается в оборот несколькими различными способами.
1. Дыхание животных и растений.
2. Разложение животных и растений. Этим занимаются бактерии, превращая части мертвых организмов животных и растений в углекислый газ в присутствии кислорода или метан в противном случае.
3. Ну и кончено, сжигание ископаемого органического топлива: нефть, уголь, торф и природный газ. За эту часть выбросов несет ответственность человечество и наша с Вами цивилизация. И именно этой части экологи приписывают все возможные грехи. С доводами экологов трудно не согласится, особенно, учитывая масштабы этого действа. Добавьте к этому лесные пожары, причиной которых тоже зачастую становятся люди.
4. Производство цемента приводит к выбросу углерода в атмосферу при нагревании карбоната кальция (известняка, CaCO3).
5. Нагревание поверхности океанов приводит дополнительному выделению углекислого газа из морской воды.
6. Ну и конечно, вулканическая деятельность – неотъемлемая часть углеродного цикла. Вулканы выбрасывают пар, углекислый газ и диоксид серы.
Ну углерод, и что?
Как мы видим углекислый газ это не яд, не загрязняющий фактор, а естественная и необходимая часть жизненного цикла нашей планеты. Почему же нас беспрерывно пугают этим страшным CO2, используя практически все источники информации? Мы не собираемся здесь разоблачать мировой заговор правящей верхушки, но я думаю, сможем объяснить, почему именно углекислый газ выбран в качестве фактора «устрашения». Уровень влияния человека, предприятия, страны, цивилизации на природу необходимо как-то измерять, так как это влияние не может более оставаться незамеченным и не учтенным. А уровень выбросов углекислого газа и является той удобной и универсальной мерой. Мы можем измерить, сколько энергии затрачивается на производство товара или услуги, но на сколько чистой была эта энергия нам помогает определить именно количество углерода выброшенного в атмосферу при получении конечного продукта.
Для этой цели и был введен термин углеродного следа (carbon footprint), показывающий, сколько стоит экологии тот или иной продукт, услуга или иная человеческая деятельность.Например, доставка почты с помощью электромобиля, почтальона на велосипеде или грузовика с двигателем внутреннего сгорания для конечного получателя закончится одинаково – конвертом в почтовом ящике, но результат для экологии в целом будет отличаться в десятки, а, то и в сотни раз. Когда Вы выйдете забирать почту доставленную классическим грузовиком, Вы будете вдыхать уже совершенно другой воздух, и с каждой следующей доставкой он не будет становиться лучше. Так что, по возможности используйте электронную почту. Ибо доставка электронного письма оставляет наименьший экологический след.
www.facepla.net
Поступление диоксида углерода в растение
Газообмен у растений происходит путем диффузии, и на пути от атмосферного воздуха до хлоропластов С02 преодолевает ряд препятствий, составляющих диффузное сопротивление. Кроме константы диффузии сюда относятся сопротивление на поверхности раздела фаз, длина пути диффузии и его поперечное сечение. В целом сопротивление транспорту С02 создают: сопротивление пограничного слоя (воздушной пленки около листа), физиологически регулируемое устьичное сопротивление, диффузное сопротивление в системе межклетников, сопротивление при растворении и транспорте СО; в жидкой фазе клеточной стенки и в цитоплазме, а также сопротивление в процессе карбоксил ирования.
Сначала тормозить диффузию может пограничный слой между листом и окружающим воздухом. Толщина его зависит от величины и расположения листьев, их опушенности и силы ветра. В безветренную погоду он имеет толщину в несколько миллиметров, л сильный ветер полностью его сдувает. Густое и высокое опушс ние увеличивает пограничный слой, поэтому С02 быстрее пере ходит в лист, чем притекает извне, и воздушная оболочка вокру| листа становится беднее С02 Но в целом сопротивление norp;i ничного слоя ниже, чем последующие устьичное и мезофиллы юс сопротивление.
У наземных растений С02 проникает в лист через устьица. Ус тьичное сопротивление — главное препятствие для свободного поступления диоксида углерода в растение. Закрытые устьица
практически полностью перекрывают поток С02 При недостатке спета, когда устьичные щели суживаются, устьичное сопротивление становится фактором, ограничивающим диффузию С02. Но при широко раскрытых устьицах это сопротивление ниже сопротивления мезофилла. Изменяя ширину устьичных щелей, растение контролирует поступление С02 и одновременно потерю воды. Количество, распределение, размеры, форма, подвижность устьиц видоспецифичны, но в некоторой степени зависят от условий местообитаний и индивидуальных особенностей растений. Для поступления С02 в растение решающее значение имеет площадь отверстий устьиц. С ее уменьшением устьичное сопротивление диффузии экспоненциально возрастает. Суммарная площадь устьичных щелей, или относительная площадь пор, определяется умножением густоты расположения устьиц (числа устьиц на 1 мм2 листовой поверхности) на максимальную площадь устьичной щели. У большинства растений отверстия устьиц занимают 0,5—1,5% поверхности листа. Из-за слабой открытости минимальная площадь устьичных щелей отмечена у листьев вечнозеленых жестко- шегных растений в засушливом маквисе и кустарничковых пустошах.
Максимальная диффузия газов в лист достигается при максимальном открытии устьиц, которое зависит от формы замыкающих клеток и особенностей строения их стенок. Степень открытости устьиц зависит также от состояния растения и внешней среды. Из экологических факторов наиболее значимы свет, температура, влажность воздуха и водообеспе- чсипость. Из внутренних факторов сильнее всего на поступление диоксида углерода влияют парциальное давление в межклетниках, гидратации растения, баланс ионов и фитогормонов. На состояние устьиц влито г также возраст листьев, стадия развития растения и эндогенные су- гочпые ритмы. При хорошем водоснабжении устьица открываются тем шире, чем интенсивнее освещение (фотоактивное открывание). Так, при снижении его содержания ниже критического уровня они Открываются и в темноте. Решающее влияние концентрации С02 на от ьрытость устьиц прослеживается у суккулентов с САМ-фотосинтезом. Vi ром, когда при расщеплении малата в межклетниках накапливается их устьица хемоактивно закрываются, а ночью, когда С02 активно расходуется на образование органических кислот и ее содержание в межклетниках остается низким, они открыты (см. разд. 6А.2.2). Реакцию м II.ни индуцирует и ряд других веществ (S02, озон, сульфат алюминия и ip.). На состояние устьиц воздействуют также токсины паразитов (например, выделения гриба Helminthosporium maydis) и вещества, применяемые для борьбы с ними (например, фунгицид фенилмеркурацетат).
Гемисратура влияет на скорость открывания устьиц через выработку терши для их движения. При более высокой (но неэкстремальной) юмпературе энергии у клетки больше и устьица открываются быстрее модельных растений при невысоких положительных температурах (ниже 5 °С) устьица открываются очень медленно и не полностью, а при отрицательных температурах они остаются закрытыми (B.Jlapxep, 1978). При сверхоптимальных температурах устьица также открываются не полностью, однако у ряда видов в жару (40 — 45 °С) ширина устьиц вновь достигает максимума.
eco-rasteniya.ru
Углерод
Углерод Выполнил: Серенков Андрей Ученик 11 «Б» класса Проверил: Комарчева Е.А. Канск 2005План 1. Роль углеродов в живой природе 2.Распространение в природе. 3. Физические и химические свойства. 4. Роль углеводов в живой природе. Углерод (лат. Carboneum), С - химический элемент IV группы периодической системы Менделеева. Известны два стабильных изотопа 12С (98,892 %) и 13С (1,108 %). Углерод известен с глубокой древности. Древесный уголь служил для восстановления металлов из руд, алмаз - как драгоценный камень. Значительно позднее стали применяться графит для изготовления тиглей и карандашей. В 1778 К. Шееле, нагревая графит с селитрой, обнаружил, что при этом, как и при нагревании угля с селитрой, выделяется углекислый газ. Химический состав алмаза был установлен в результате опытов А.Лавуазье (1772) по изучения горения алмаза на воздухе и исследований С.Теннанта (1797), доказавшего, что одинаковые количества алмаза и угля дают при окислении равные количества углекислого газа. Углерод как химический элемент был признан только в 1789 А.Лавуазье. Латинское название сarboneum углерод получил от сarbo — уголь. Среднее содержание углерода в земной коре 2,3*10-2 % по массе (1*10 –2в ультраосновных, 1*10 –2 в основных, 2*10 –2 в средних, 3*10 –2 в кислых горных породах). Углерода накапливается в верхней части земной коры (биосфере): в живом веществе 18 % углерода, в древесине 50 %, в каменном угле 80 %, в нефти 85 %, антраците 96 %. Значит часть углерода литосферы сосредоточена в известняках и доломитах. Число собственных минералов углерода - 112; исключительно велико число органических соединений углерода - углеводородов и их производных. С накоплением углерода в земной коре связано накопление и многих других элементов, сорбируемых органическим веществом и осаждающихся в виде нерастворимых карбонатов и т.д. По сравнению со средним содержанием в земной коре человечество в исключительно больших количествах извлекает углерод из недр (уголь, нефть, природный газ), т.к. эти ископаемые — основные источники энергии. Углерод широко распространён также в космосе; на Солнце он занимает 4-е место после водорода, гелия и кислорода. Известны четыре кристаллические модификации углерода: графит, алмаз, карбин и лонсдейлит. Графит - серо-черная, непрозрачная, жирная на ощупь, чешуйчатая, очень мягкая масса с металлическим блеском. При комнатной температуре и нормальном давлении (0,1 Мн/м2, или 1кгс/см2) графит термодинамически стабилен. Алмаз - очень твердое, кристаллическое вещество. Кристаллы имеют кубическую гранецентрированную решетку: а=3,560Б. При комнатной температуре и нормальном давлении алмаз метастабилен. Заметное превращение алмаза в графит наблюдается при температурах выше 1400°С в вакууме или в инертной атмосфере. При атмосферном давлении и температуре около 3700°С графит возгоняется. Жидкий углерод может быть получен при давлении выше 10,5 Мн/м2 (1051 кгс/см2) и температурах выше 3700°С. Для твердого углерода (кокс, сажа, древесный уголь) характерно также состояние с неупорядоченной структурой “аморфный” углерод, который не представляет собой самостоятельной модификации; в основе его строения лежит структура мелкокристаллического графита. Нагревание некоторых разновидностей “аморфного” углерода выше 1500-1600°С без доступа воздуха вызывает их превращение в графит. Физические свойства “аморфный” углерода очень сильно зависят от дисперсности частиц и наличия примесей. Плотность, теплоемкость, теплопроводность и электропроводность “аморфный” углерода всегда выше, чем графита. Карбин получен искусственно. Он представляет собой мелкокристаллический порошок черного цвета (плотность 1,9 - 2 г/см3). Построен из длинных цепочек атомов С, уложенных параллельно друг другу. Лонсдейлит найден в метеоритах и получен искусственно; его структура и свойства окончательно не установлены. Конфигурация внешней оболочки атома углерода 2s22p2. Для углерода характерно образование четырех ковалентных связей, обусловленное возбуждение внешней электронной оболочки до состояния 2sp3. Поэтому углерод способен в равной степени как притягивать, так и отдавать электроны. Химическая связь может осуществляться за счет sp3-, sp2- и sp- гибридных орбиталей, которым соответствуют координационные числа 4,3 и 2. Число валентных электронов углерода и число валентных орбиталей одинаково; это одна из причин устойчивости связи между атомами углерода. Уникальная способность атомов углерода соединяться между собой с образованием прочных и длинных цепей и циклов привела к возникновению громадного числа разнообразных соединений углерода, изучаемых органической химией. В соединениях углерод проявляет степени окисления -4; +2; +4. Атомный радиус 0,77Б,ковалентные радиусы 0,77Б, 0,67Б, 0,60Б соответственно в одинарной, двойной и тройной связях; ионной радиус С4- 2,60Б, С4+ 0,20Б. При обычных условиях углерод химически инертен, при высоких температурах он соединяется со многими элементами, проявляя сильные восстановительные свойства. Все формы углерода устойчивы к щелочам и кислотам и медленно окисляются только очень сильными окислителями (хромовая смесь, смесь концентриров. HNO3 и KCIO3 и др.). “Аморфный” углерод реагирует с фтором при комнатной температуре, графит и алмаз - при нагревании. Непосредственно соединение углерода с хлором происходит в электрической дуге; с бромом и йодом углерод не реагирует, поэтому многочисленные углерода галогениды синтезируют косвенным путем. Из оксигалогенидов общей формулы COX2 (где Х - галоген) наиболее известная хлорокись COCI2 (фосген). При температурах выше 1000°С углерод взаимодействует со многими металлами, давая карбиды. Все формы углерода при нагревании восстанавливают окислы металлов с образованием свободных металлов (Zn, Cd, Cu, Pb и др.) или карбидов (CaC2, Mo2C, WC, TaC и др.). Углерод реагирует при температурах выше 600 - 800°С с водяным паром и углекислым газом. Все формы углерода нерастворимы в обычных неорганических и органических растворителях, но растворяются в некоторых расплавленных металлах (например, Fe, Ni, Co). Углерод - важнейший биогенный элемент, составляющий основу жизни на Земле, структурная единица огромного числа органических соединений, участвующих в построении организмов и обеспечении их жизнедеятельности (биополимеры, а также многочисленные низкомолекулярные биологически активные вещества - витамины, гормоны, медиаторы и др.). Значительную часть необходимой организмам энергии образуется в клетках за счет окисления углерода. Возникновение жизни на Земле рассматривается в современной науке как сложный процесс эволюции углеродистых соединений. Уникальная роль углерода в живой природе обусловлена его свойствами, которыми в совокупности не обладает ни один другой элемент периодической системы. Между атомами углерода, а также между углеродом и другими элементами образуются прочные химические связи, которые, однако, могут быть разорваны в сравнительно мягких физиологических условиях (эти связи могут быть одинарными, двойными и тройными). Способность углерода образовывать 4 равнозначные валентные связи с другими атомами. Углерод создает возможность для построения углеродных скелетов различных типов - линейных, разветвленных, циклических. Показательно, что всего три элемента - С, О, Н - составляют 98 % общей массы живых организмов. Этим достигается определенная экономичность в живой природе: при практически безграничном структурном разнообразии углеродистых соединений небольшое число типов химических связей позволяет на много сократить количество ферментов, необходимых для расщепления и синтеза органических веществ. Особенности строения атома углерода лежит в основе различных видов изомерии органических соединений (способность к оптической изомерии оказалась решающей в биохимической эволюции аминокислот, углеводов и некоторых алкалоидов). Согласно гипотезе А. И. Опарина, первые органические соединения на Земле имели абиогенное происхождение. Источниками углерода служили (СН4)и цианистый водород (HCN),содержавшиеся в первичной атмосфере Земли. С возникновением жизни единственным источником неорганического углерода, за счет которого образуется всё органическое вещество биосферы, является углерода двуокись (СО2),находящийся в атмосфере, а также растворенная в природных водах в виде НСО3. Наиболее мощный механизм усвоения (ассимиляция) углерода (в форме СО2) - фотосинтез - осуществляется повсеместно зелеными растениями. На Земле существует и эволюционно более древний способ усвоения СО2 путем хемосинтеза; в этом случае микроорганизмы - хемосинтетики используют не лучистую энергию Солнца, а энергию окисления неорганических соединений. Большинство животных потребляют углерод с пищей в виде уже готовых органических соединений. В зависимости от способа усвоения органических соединений принято различать автотрофные организмы и гетеротрофные организмы. Применение для биосинтеза белка и других питательных веществ микроорганизмов, использующих в качестве единственного источника углерода, углеводороды нефти, - одна из важных современных научно - технических проблем. Помимо стабильных изотопов углерода, в природе распространен радиоактивный 14С (в организме человека его содержится около 0,1мккюри). С использованием изотопов углерода в биологических и медицинских исследованиях связаны многие крупные достижения в изучении обмена веществ и круговорота углерода в природе. Так, с помощью радиоуглеродной метки была доказана возможность фиксации Н14СО3 растениями и тканями животных, установлена последовательность реакции фотосинтеза, изучен обмен аминокислот, прослежены пути биосинтеза многих биологически активных соединений и т. д. Применение 14С способствовало успехам молекулярной биологии в изучении механизмов биосинтеза белка и передачи наследственной информации. Определение удельной активности 14С в углеродсодержащих органических остатках позволяет судить об их возрасте, что используется в палеонтологии и археологии.www.coolreferat.com










