Химические свойства хлорофилла. Хлорофилл его свойства значение хлорофилла в жизни растений
30 Хлорофилл. Свойства. Состояние в раст. Условия оразования.
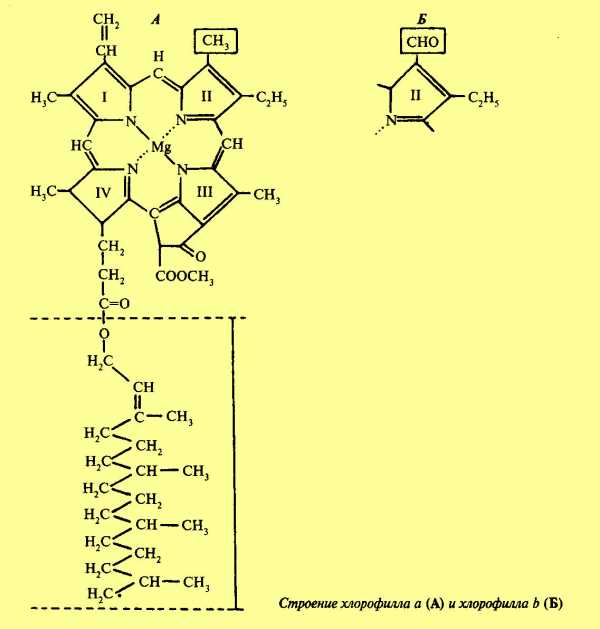
Хлорофилл не представляет собой индивидуальное вещество, а имеет несколько форм (около десяти). Главными являются две формы — хлорофилл А (C55H7205N4Mg), сине-зеленого цвета, и хлорофилл Б (C55H7o06N4Mg), желто-зеленого цвета. Обе эти формы всегда присутствуют в растении, причем содержание хлорофилла А в листе в 3 раза больше по сравнению с хлорофиллом Б. По химической природе хлорофилл - сложный эфир дикарбоновой орг. кислоты хлорофиллина и двух спиртов — метанола СН3ОН и фитола. Фитол —это высокомолекулярный спирт С20Н39ОН с длинной углеводородной цепью, придающий хлорофиллу гидрофобные свойства, что сказывается на его химических свойствах.
Особый интерес представляет строение центра молекулы хлорофилла, ее парфириновое ядро, так как именно эта часть обусловливает важные свойства, присущие данному пигменту.
В центре молекулы хлорофилла находится атом магния, который соединен с 4 атомами азота, входящими в свою очередь в 5-членные пиррольные кольца, связанные между собой метановыми мостиками СН. К одному из пиррольных колец через пропноновую кислоту присоединен фитол, а к другому через циклопентановое кольцо — метанол. Самой интересной представляется связь двухвалентного магния, с четырьмя атомами азота. Эти особенности строения и наличие переменных связей обусловливают активацию молекулы при поглощении квантов света и переход электронов на высшие энергетические уровни. Вследствие этого происходит возбуждение хлорофилла, обусловливающее возникновение у него способности к о/в реакциям. Химические свойства. Как всякий сложный эфир, хлорофилл имеет высокую реакционную способность. Его составные часто придают молекуле различные свойства: хлорофиллин — гидрофильные, фитол — гидрофобные, что влечет за собой избирательную растворимость: хлорофилл не-растворим в воде, но растворяется в органических растворителях — спиртах, эфирах, бензоле, ацетоне, хлороформе. Хлорофилл реагирует со щелочами, которые разрывают эфирные связи. При этом образуются соли хлорофиллина. Зеленая окраска вытяжки при этом сохраняется. Хлорофилл реагирует также с кислотами, при низкой концентрации вытесняющими магний и замещающими его на водород. При этом зеленая окраска исчезает, образуется бурое вещество феофитин. Зеленая окраска снова может быть возвращена замещением водорода на металл — цинк или медь, но при этом вещество уже не будет иметь свойств, присущих хлорофиллу. Значит, зеленая окраска пигмента обусловлена металлом, а оптические его свойства — магнием. Оптические свойства. Флуоресценция — испускание поглощенных световых лучей с измененной длиной волны. Зеленая в проходящем свете вытяжка хлорофилла в отраженном свете отсвечивает темным вишнево-красным светом. Это явление хорошо наблюдается в растворах, хлорофилла, но не видно в листе. Флуоресценция происходит вследствие рассеивания света, поглощённого хлорофиллом и не использованного на фотосинтез. Спектр поглощения хлорофилла имеет два максимума: в красной части спектра (650 — 680 нм) и в сине-фиолетовой части (430 — 460 нм). Спектр поглощения хлорофилловой вытяжки изменяется в зависимости от концентрации пигмента. При низкой это два узких пика, положение которых указано выше. При очень высокой концентрации хлорофилл поглощает все лучи спектра, кроме зеленых и крайних красных, граничащих с ИК. В листе хлорофилл поглощает также почти все лучи, кроме указанных выше, что и обусловливает его зеленую окраску. Условия образования хлорофилла. Проростки споровых и голосеменных растений появляются уже зелеными — с хлорофиллом. Покрытосеменные растения в семенах его не имеют, он должен каждый раз образовываться заново. Для этого растениям необходимо действие ряда внутренних и внешних факторов. К первым относится прежде всего генетическая природа образования хлорофилла. При отсутствии такой способности вырастают бесцветные растения — альбиносы. Из внешних экологических факторов для синтеза хлорофилла необходим прежде всего свет. Только после освещения в проростке начинается синтез пигмента. Существенным фактором образования хлорофилла является железо, которое катализирует этот процесс. При недостатке этого элемента (что чаще всего происходит при щелочной реакции среды) вырастают растения с бледно-зелеными верхними листьями. Эта болезнь называется хлорозом. Необходим для синтеза пигмента также азот, сост. основу каждой молекулы хлорофилла.
studfiles.net
2. Какова роль хлорофилла в жизни растений?
Самая важная - синтез кислорода
ту же самую, что и кровь у человека.
Не вздумай попрбовать.... хоть ты и не цветок....
Это зеленый пигмент растений. Также, он помогает растениям улавливать энергию солнечного света, тем самым осуществляя фотосинтез.
Он участвует в образовании кислорода. Сам процесс фотосинтеза состоит из двух фаз: темновой и светловой.
Никто не ответил правильно! Хлорофилл нужен растениям прежде всего для образования ОРГАНИЧЕСКИХ ВЕЩЕСТВ, то бишь глюкозы, а кислород выступает как побочный продукт, который выводится. Уравнение фотосинтеза: 6угл. газ+6вода=глюкоза+6кислород.
Наличие в клетках растений красящих веществ помогает им наиболее эффективно поглощать и использовать солнечные лучи. Все пигменты растений представляют собой избирательно работающие физико-химические фильтры - ловушки солнечного света. Если хлорофилл листьев поглощает только красные и сине-фиолетовые лучи, используемые в процессе фотосинтеза для образования сложных органических соединений из простых минеральных веществ почвы и воздуха, то ярко-окрашенные цветки, благодаря содержанию в них разнообразных пигментов, улавливают лучи иной длины волны и превращают их в другие формы энергии. Эти формы энергии используются растениями для созревания пыльцы и яйцеклеток, синтеза ароматических веществ, повышения температуры в органах размножения, что ускоряет течение обменных процессов
touch.otvet.mail.ru
Биология для студентов - 19. Хлорофилл, его химическая структура, свойства, биосинтез
Важнейшую роль в процессе фотосинтеза играют зеленые пигменты — хлорофиллы. Французские ученые П.Ж. Пелетье и Ж. Кавенту (1818) выделили из листьев зеленое вещество и назвали его хлорофиллом (от греч. «хлорос» — зеленый и «филлон» — лист). В настоящее время известно около десяти хлорофиллов. Они отличаются по химическому строению, окраске, распространению среди живых организмов. У всех высших растений содержатся хлорофиллы а и b. Хлорофилл с обнаружен в диатомовых водорослях, хлорофилл d — в красных водорослях. Кроме того, известны четыре бактериохлорофилла (a, b, c и d), содержащиеся в клетках фотосинтезирующих бактерий. В клетках зеленых бактерий имеются бактериохлорофиллы с и d, в клетках пурпурных бактерий — бактериохлорофиллы а и b.
Основными пигментами, без которых фотосинтез не идет, являются хлорофилл а для зеленых растений и бактериохлорофиллы для бактерий. Впервые точное представление о пигментах зеленого листа высших растений было получено благодаря работам крупнейшего русского ботаника М.С. Цвета (1872—1919). Он разработал новый хроматографический метод разделения веществ и выделил пигменты листа в чистом виде. Хроматографический метод разделения веществ основан на их различной способности к адсорбции. Метод этот получил широкое применение. М.С. Цвет пропускал вытяжку из листа через стеклянную трубку, заполненную порошком — мелом или сахарозой (хроматографическую колонку). Отдельные компоненты смеси пигментов различались по степени адсорбируемости и передвигались с разной скоростью, в результате чего они концентрировались в разных зонах колонки. Разделяя колонку на отдельные части (зоны) и используя соответствующую систему растворителей, можно было выделить каждый пигмент. Оказалось, что листья высших растений содержат хлорофилл а и хлорофилл b, а также каротиноиды (каротин, ксантофилл и др.). Хлорофиллы, так же как и каротиноиды, нерастворимы в воде, но хорошо растворимы в органических растворителях. Хлорофиллы а и b различаются по цвету: хлорофилл а имеет сине-зеленый оттенок, а хлорофилл — желто-зеленый. Содержание хлорофилла а в листе примерно в три раза больше по сравнению с хлорофиллом b.
По химическому строению хлорофиллы — сложные эфиры дикарбоновой органической кислоты — хлорофиллина и двух остатков спиртов — фитола и метилового. Эмпирическая формула — C55H7205N4Mg. Хлорофиллин представляет собой азотсодержащее металлорганическое соединение, относящееся к магнийпорфиринам.
В хлорофилле водород карбоксильных групп замещен остатками двух спирит — метилового СН3ОН и фитола С20Н39ОН, поэтому хлорофилл является сложным эфиром.
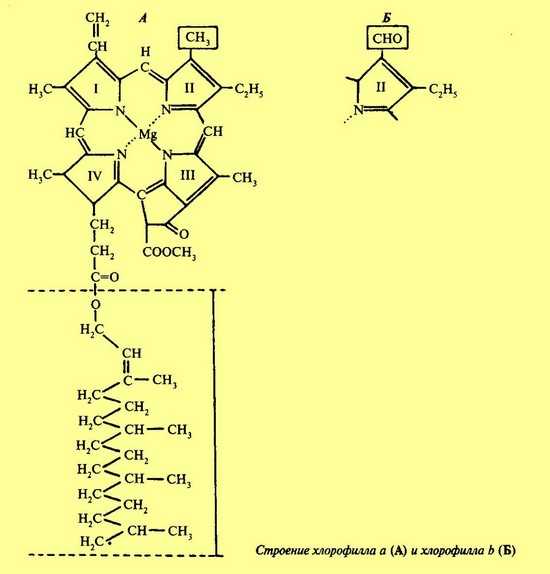
Хлорофилл b отличается от хлорофилла а тем, что содержит на два атома водорода меньше и на один атом кислорода больше (вместо группы СН3 группа СНО). В связи с этим молекулярная масса хлорофилла а — 893 и хлорофилла b — 907. В центре молекулы хлорофилла расположен атом магния, который соединен четырьмя атомами азота пиррольных группировок. В пиррольных группировках хлорофилла имеется система чередующихся двойных и простых связей. Это N есть хромофорная группа хлорофилла, обусловливающая поглощение определённых лучей солнечного спектра и его окраску. Диаметр порфиринового ядра составляет 10 нм, а длина фитольного остатка — 2 нм. Расстояние между атомами азота пиррольных группировок в ядре хлорофилл составляет 0,25 нм. Интересно, что диаметр атома магния равен 0,24 нм. Таким образом, магний почти полностью заполняет пространство между атомами азота пиррольных группировок. Это придает ядру молекулы хлорофилла дополнительную прочность.
Одной из специфических черт строения хлорофилла является наличие в его молекуле помимо четырех гетероциклов еще одной циклической группировки из пяти углеродных атомов — циклопентанона. В циклопентановом кольце содержится кетогруппа, обладающая большой реакционной способностью. Есть данные, что в результате процесса энолизации по месту этой кетогруппы к молекуле хлорофилла присоединяется вода. Молекула хлорофилла полярна, ее порфириновое ядро обладает гидрофильными свойствами, а фитольный конец — гидрофобными. Это свойство молекулы хлорофилла обусловливает определенное расположение ее в мембранах хлоропластов. Порфириновая часть молекулы связана с белком, а фитольная цепь погружена в липидный слой.
Извлеченный из листа хлорофилл легко реагирует как с кислотами, так и со щелочами. При взаимодействии со щелочью происходит омыление хлорофилла, в результате чего образуются два спирта и щелочная соль кислоты хлорофиллина.
В интактном живом листе от хлорофилла может отщепляться фитол под воздействием фермента хлорофиллазы. При взаимодействии со слабой кислотой извлеченный хлорофилл теряет зеленый цвет, образуется соединение феофитин, у которого атом магния в центре молекулы замещен на два атома водорода.
Хлорофилл в живой интактной клетке обладает способностью к обратимому фотоокислению и фотовосстановлению. Азот пиррольных ядер может окисляться (отдавать электрон) или восстанавливаться (присоединять электрон).
Исследования показали, что свойства хлорофилла, находящегося в листе и извлеченного из листа, различны, так как в листе он находится в комплексном соединении с белком. Это доказывается следующими данными:
- Спектр поглощения хлорофилла, находящегося в листе, иной по сравнению с извлеченным хлорофиллом.
- Хлорофилл невозможно извлечь абсолютным спиртом из сухих листьев. Экстракция протекает успешно, только если листья увлажнить или к спирту добавить воды, которая разрушает связь между хлорофиллом и белком.
- Выделенный из листа хлорофилл легко подвергается разрушению под влиянием самых разнообразных воздействий (повышенная кислотность, кислород и даже свет).
Между тем в листе хлорофилл достаточно устойчив ко всем перечисленным факторам. Для гемоглобина характерно постоянное соотношение — на 1 молекулу белка приходится 4 молекулы гемина. Между тем соотношение между хлорофиллом и белком различно и претерпевает изменения в зависимости от типа растений, фазы их развития, условий среды (от 3 до 10 молекул хлорофилла на 1 молекулу белка). Связь между молекулами белка и хлорофиллом осуществляется путем нестойких комплексов, образующихся при взаимодействии кислотных групп белковых молекул и азота пиррольных колец. Чем выше содержание дикарбоновых аминокислот в белке, тем лучше идет их комплексирование с хлорофиллом (Т.Н. Годнев).
Важным свойством молекул хлорофилла является их способность к взаимодействию друг с другом. Переход из мономерной в агрегированную форму возник в результате взаимодействия двух и более молекул при их близком расположении друг к другу. В процессе образования хлорофилла его состояние в живой клетке закономерно меняется. В настоящее время показано, что хлорофилл в мембранах пластид находится в виде пигментлипопротеидных комплексов с различной степенью агрегации.
vseobiology.ru
| По химическому строению хлорофиллы — сложные эфиры дикарбоновой органической кислоты — хлорофиллина и двух остатков спиртов — фитола и метилового. Эмпирическая формула — C55H7205N4Mg. Хлорофиллин представляет собой азотсодержащее металлорганическое соединение, относящееся к магнийпорфиринам. В хлорофилле водород карбоксильных групп замещен остатками двух спирит — метилового СН3ОН и фитола С20Н39ОН, поэтому хлорофилл является сложным эфиром. На рисунке дана структурная формула хлорофилла а. Хлорофилл b отличается тем, что содержит на два атома водорода меньше и на один атом кислорода больше (вместо группы СН3 группа СНО). В связи с этим молекулярная масса хлорофилла а — 893 и хлорофилла b — 907. В 1960 г. Г.Б. Вудворд осуществил полный синтез хлорофилла. В центре молекулы хлорофилла расположен атом магния, который соединен четырьмя атомами азота пиррольных группировок. В пиррольных группировках хлорофилла имеется система чередующихся двойных и простых связей. Это N есть хромофорная группа хлорофилла, обусловливающая поглощение определённых лучей солнечного спектра и его окраску. Диаметр порфиринового ядра составляет 10 нм, а длина фитольного остатка — 2 нм. Расстояние между атомами азота пиррольных группировок в ядре хлорофилл составляет 0,25 нм. Интересно, что диаметр атома магния равен 0,24 нм. Таким образом, магний почти полностью заполняет пространство между атомами азота пиррольных группировок. Это придает ядру молекулы хлорофилла дополнительную прочность. Еще К.А. Тимирязев обратил внимание на близость химического строения двух важнейших пигментов: зеленого — хлорофилла листьев и красного — гемина крови. Действительно, если хлорофилл относится к магнийпорфиринам, то гемин — к железопорфиринам. Сходство это не случайно и служит еще одним доказательством единства всего органического мира. Одной из специфических черт строения хлорофилла является наличие в его молекуле помимо четырех гетероциклов еще одной циклической группировки из пяти углеродных атомов — циклопентанона. В циклопентановом кольце содержится кетогруппа, обладающая большой реакционной способностью. Есть данные, что в результате процесса энолизации по месту этой кетогруппы к молекуле хлорофилла присоединяется вода. Молекула хлорофилла полярна, ее порфириновое ядро обладает гидрофильными свойствами, а фитольный конец — гидрофобными. Это свойство молекулы хлорофилла обусловливает определенное расположение ее в мембранах хлоропластов. Порфириновая часть молекулы связана с белком, а фитольная цепь in пружена в липидный слой.
Извлеченный из листа хлорофилл легко реагирует как с кислотами, так и со щелочами. При взаимодействии со щелочью происходит омыление хлорофилла, в результате чего образуются два спирта и щелочная соль кислоты хлорофиллина. В интактном живом листе от хлорофилла может отщепляться фитол под воздействием фермента хлорофиллазы. При взаимодействии со слабой кислотой извлеченный хлорофилл теряет зеленый цвет, образуется соединение феофитин, у которого атом магния в центре молекулы замещен на два атома водорода. Хлорофилл в живой интактной клетке обладает способностью к обратимому фотоокислению и фотовосстановлению. Способность к окислительно-восстановительным реакциям связана с наличием в молекуле хлорофилла сопряженных двойных связей с подвижными л-электронами и атомов азота с неподеленными электронами. Азот пиррольных ядер может окисляться (отдавать электрон) или восстанавливаться (присоединять электрон). Исследования показали, что свойства хлорофилла, находящегося в листе и извлеченного из листа, различны, так как в листе он находится в комплексном соединении с белком. Это доказывается следующими данными: 1. Спектр поглощения хлорофилла, находящегося в листе, иной по сравнению с извлеченным хлорофиллом. 2. Хлорофилл невозможно извлечь абсолютным спиртом из сухих листьев. Экстракция протекает успешно, только если листья увлажнить или к спирту добавить воды, которая разрушает связь между хлорофиллом и белком. 3. Выделенный из листа хлорофилл легко подвергается разрушению под влиянием самых разнообразных воздействий (повышенная кислотность, кислород и даже свет). Между тем в листе хлорофилл достаточно устойчив ко всем перечисленным факторам. Следует отметить, что хотя крупный русский ученый В. Н. Любименко и предлагал этот комплекс назвать хлороглобином, по аналогии с гемоглобином, связь между хлорофиллом и белком иного характера, чем между гемином и белком. Для гемоглобина характерно постоянное соотношение — на 1 молекулу белка приходится 4 молекулы гемина. Между тем соотношение между хлорофиллом и белком различно и претерпевает изменения в зависимости от типа растений, фазы их развития, условий среды (от 3 до 10 молекул хлорофилла на 1 молекулу белка). Связь между молекулами белка и хлорофиллом осуществляется путем нестойких комплексов, образующихся при взаимодействии кислотных групп белковых молекул и азота пиррольных колец. Чем выше содержание дикарбоновых аминокислот в белке, тем лучше идет их комплексирование с хлорофиллом (Т.Н. Годнев). Белки, связанные с хлорофиллом, характеризуются низкой изоэлектрической точкой (3,7—4,9). Молекулярная масса этих белков порядка 68 кДа. Вместе с тем хлорофилл может взаимодействовать и с липидами мембран. Важным свойством молекул хлорофилла является их способность к взаимодействию друг с другом. Переход из мономерной в агрегированную форму возник в результате взаимодействия двух и более молекул при их близком расположении друг к другу. В процессе образования хлорофилла его состояние в живой клетке закономерно меняется. При этом и происходит его агрегация (АА. Красновский). В настоящее время показано, что хлорофилл в мембранах пластид находится в виде пигментлипопротеидных комплексов с различной степенью агрегации. |
fizrast.ru
Фотосинтез и хлорофилл | Биология
Понятие о фотосинтезе
Фотосинтез – это процесс образования органических веществ из неорганических с помощью солнечной энергии. Солнечная энергия, поглощенная хлорофиллоносной клеткой, трансформируется в химическую энергию органических соединений и запасается в их молекулах.
В основе фотосинтеза лежит окислительно-восстановительный процесс с образованием углевода и выделением молекулярного кислорода (O2) в случае, если окисляется вода. Фотосинтезирующие бактерии часто используют не воду, а иные вещества, и кислород при таком фотосинтезе не образуется.
Одним из главных компонентов процесса фотосинтеза являются пигменты хлорофиллы. Возбужденная светом молекула хлорофилла приобретает способность участвовать в окислительно-восстановительных процессах, то есть отдавать или принимать электроны. При этом молекула хлорофилла способна также на некоторое время запасать энергию света в виде энергии возбужденных электронов и преобразовывать ее в энергию химических связей.
Над проблемой фотосинтеза и расшифровкой его физико-химических процессов работали многие ученые. Так, в 1727 году английский ботаник и химик С. Гейлс в книге «Статика растений» высказал предположение о том, что растения значительную часть «пищи» получают из воздуха. Сходные мысли высказывал и М.В. Ломоносов. В своем труде «Слово о воздушных явлениях» (1753) он писал: «Преизобильное ращение тучных дерев, которые на бесплодном песку корень свой утверждали, ясно изъявляет, что листами жирный тук из воздуха впитывают». Так, наряду с представлением о корневом питании возникла идея о воздушном питании растений.
В 1774 году опыты английского химика Дж. Пристли показали, что растения выделяют кислород. В 1782 году швейцарский естествоиспытатель Ж. Сенебье установил, что растения на свету не только выделяют кислород, но и поглощают углекислый газ, и назвал этот процесс углеродным питанием.
В середине XIX века немецкие ученые Ю. Майер и Г. Гельмгольц предположили, что зеленые растения поглощают лучистую энергию и превращают ее в химическую. Экспериментальное доказательство этой точки зрения было получено только в 1875 году русским ученым – физиологом растений Климентом Аркадьевичем Тимирязевым, который показал, что при ассимиляции CO2 хлорофилл служит оптическим сенсибилизатором (то есть веществом, увеличивающим чувствительность к свету), что именно хлорофилл непосредственно участвует в процессе фотосинтеза и что в хлоропласте лучистая энергия Солнца превращается в химическую энергию углеводов.
В итоге к концу XIX века результаты изучения фотосинтеза у растений позволили выразить его общее уравнение, в котором свет и хлорофилл выполняют важнейшую роль:
Хлорофилл
Светопоглощающие пигменты представлены тремя классами веществ: хлорофиллы, фикобилины и каротиноиды. Хлорофиллы – зеленые пигменты, фикобилины – красные, синие и сине-голубые – присутствуют у красных водорослей и цианобактерий; каротиноиды (каротины и ксантофиллы) – желтого, оранжевого и красного цвета – входят в состав хлоропластов всех растений и хромопластов незеленых частей растения: корнеплодов моркови, редиса, плодов томата и др.
Хлорофилл – зеленый пигмент растений и фотосинтезирующих бактерий, с помощью которого они улавливают энергию солнечного света и осуществляют фотосинтез.
Впервые хлорофилл в кристаллическом виде был получен русским физиологом и ботаником, академиком И.П. Бородиным в 1883 году, а его элементарный состав был установлен немецким химиком Р. Вильштеттером в 1914 году. Но еще в 1906 году русский физиолог Михаил Семенович Цвет, впервые используя разработанный им метод хроматографического анализа, доказал существование двух весьма близких друг другу по химическому составу соединений – хлорофиллов a и b.
Однако структурная формула хлорофиллов a и b была установлена только к 1940 году немецким биохимиком Г. Фишером, который в 1930 году получил Нобелевскую премию за расшифровку структуры гемоглобина, показав, что гемоглобин состоит из белка глобина и железосодержащего производного протопорфирина – гема. Фишер определил, что основу молекулы хлорофилла составляет аналог гема – Mg-порфириновый комплекс, где центральное место занимает атом магния, и что хлорофилл, как и гемоглобин, проявляет свою активность только в комплексе с белками.Хлорофилл поглощает свет в красной и синей частях спектра, но пропускает лучи, которые при смешении дают зеленый цвет. По физико-химическим свойствам хлорофилл представляет собой твердое аморфное вещество сине-черного цвета. Он нерастворим в воде, но хорошо растворяется в органических растворителях: этиловом эфире, бензоле, ацетоне, этиловом спирте. Раствор хлорофилла a в этиловом эфире имеет сине-зеленый цвет, хлорофилла b – желто-зеленый.
В настоящее время известны около 10 типов хлорофиллов (a, b, c, d, e и др.), отличающиеся друг от друга по химическому строению, окраске, спектрам поглощения солнечного света и распространению среди живых организмов.
Разные хлорофиллы избирательно поглощают солнечную энергию. Для хлорофиллов группы а максимумы поглощения локализованы в красной части спектра в пределах 650–700 нм и в синей части спектра в диапазоне 430–460 нм. Максимум поглощения хлорофилла 6 находится в пределах 642–644 и 452–455 нм. Все хлорофиллы слабо поглощают оранжевый и желтый свет и практически не поглощают зеленые и инфракрасные лучи.
Среди пигментов растений наиболее распространенными являются две формы хлорофилла a, работающие в диапазоне спектра с длиной волны 680 и 700 нм. Хлорофилл a, улавливающий свет с длиной волны 680 нм, называют коротковолновым хлорофиллом680 или пигментом680 (П680), а поглощающий свет в диапазоне 700 нм – длинноволновым хлорофиллом700 или пигментом700 (П700). Все другие формы хлорофилла групп b, c, d и каротиноиды, присутствующие в хлоропласте, улавливают свет в том диапазоне спектра, где хлорофиллы a его не воспринимают. Это позволяет фотосинтезирующим пигментам использовать большее количество диапазонов и энергии света и, следовательно, максимально обеспечивать процесс фотосинтеза. Различают два типа фотосинтезирующих пигментов: главные (основные) и вспомогательные.
Главными (основными) являются пигменты, испускающие электроны, непосредственно участвующие в доставке энергии для фотосинтеза. Вспомогательными являются те, которые передают испускаемые ими электроны главным пигментам, усиливая их. Хлорофилл a считается основным пигментом, все остальные формы хлорофилла и желтые пигменты (каротиноиды) – вспомогательными.
Все светопоглощающие молекулы пигментов собраны в большие группы (состоящие из нескольких сотен молекул) – так называемые антенные комплексы, которые с помощью специальных белков прочно связаны между собой и с тилакоидной мембраной хлоропласта таким образом,что световая энергия, поглощенная любым из них, передается одной-единственной молекуле хлорофилла, которую называют реакционным центром (РЦ). Светособирательный антенный комплекс можно сравнить с воронкой, собирающей лучистую энергию и направляющей ее к единому реакционному центру.
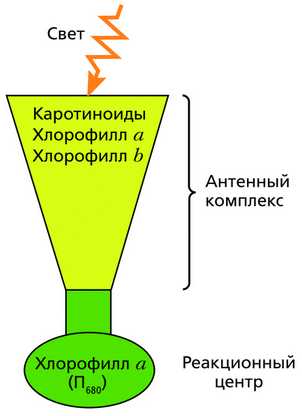 Антенный комплекс передачи энергии в фотосинтезе Особенность хлорофилла. Хлорофилл обладает особым свойством; при поглощении энергии кванта света его молекула возбуждается, и от нее отрываются электроны, которые переходят (перескакивают) на более высокие вакантные орбитали (то есть на энергетически более высокие уровни). Энергия электронов может сохраняться благодаря их присоединению к слабому акцептору, при этом образуется сильный донор электронов, от которого эти электроны вновь, как по цепочке, передаются от одного вещества к другому. Такое перемещение электронов называют электронным транспортом или цепью переносчиков, а сам путь передачи электронов – электрон-транспортной цепью. Соединения, отдающие электроны, называют донорами, а принимающие их – акцепторами.
Антенный комплекс передачи энергии в фотосинтезе Особенность хлорофилла. Хлорофилл обладает особым свойством; при поглощении энергии кванта света его молекула возбуждается, и от нее отрываются электроны, которые переходят (перескакивают) на более высокие вакантные орбитали (то есть на энергетически более высокие уровни). Энергия электронов может сохраняться благодаря их присоединению к слабому акцептору, при этом образуется сильный донор электронов, от которого эти электроны вновь, как по цепочке, передаются от одного вещества к другому. Такое перемещение электронов называют электронным транспортом или цепью переносчиков, а сам путь передачи электронов – электрон-транспортной цепью. Соединения, отдающие электроны, называют донорами, а принимающие их – акцепторами.
«Выскочившие» из реакционного центра электроны быстро захватываются акцепторами. При этом в молекуле хлорофилла образуется положительно заряженная «дырка» с очень высоким сродством к электронам. Эту «дырку» быстро заполняет электрон, отдаваемый находящимся поблизости донором электронов. Часто в таких случаях донором электронов является вода. Электрон-транспортная цепь находится в тилакоидной мембране. Потеря электрона означает окисление переносчика, а присоединение электрона – восстановление молекулы. Любой этап переноса электрона сопровождается высвобождением или поглощением энергии. На некоторых участках электрон-транспортной цепи перенос электрона сопровождается переносом протона.
Локализация процесса фотосинтеза
Процесс фотосинтеза у растений происходит в хлоропластах, где важную роль выполняют мембраны тилакоидов.
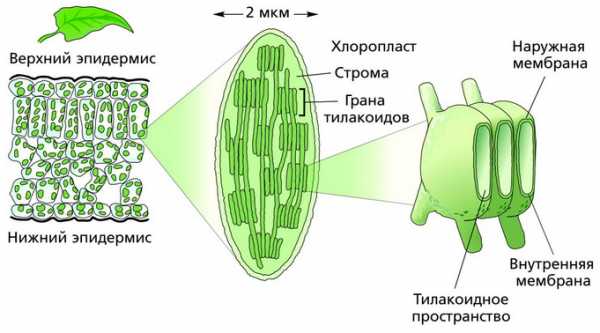 Хлоропласт из клетки мякоти листа
Хлоропласт из клетки мякоти листа
Напомним, хлоропласты, находясь в цитоплазме, отделены от нее двумя мембранами: высокопроницаемой наружной и менее проницаемой внутренней. Во внутреннюю встроены специальные транспортные белки. Между двумя мембранами находится узкое межмембранное пространство. Кроме того, в тилакоидах, гранах и ламеллах, отделенных от стромы тилакоидной мембраной, также имеется межмембранное пространство – тилакоидное. Поэтому в хлоропластах создаются три различных пространства: тилакоидное, межмембранное и строма, различающиеся между собой составом ферментов и химических веществ, что обусловливает возможность протекания в них разных метаболических процессов. Особенно многофункциональной оказывается тилакоидная мембрана. В ней локализованы все основные фотосинтетические пигменты: зеленые – хлорофиллы и вспомогательные – желтые и красные – каротиноиды, участвующие в поглощении и использовании энергии света; все энергетические системы хлоропласта; системы запасания энергии; разнообразные белки – переносчики электронов, образующие электрон-транспортную цепь и ферментативный комплекс АТФ-синтазы.
blgy.ru