Растения воюют друг с другом молекулярно-генетическим оружием. Молекула растения
ФИЗИОЛОГИЯ РАСТИТЕЛЬНОЙ КЛЕТКИ
Все клетки обладают такими свойствами живого как способность к самовоспроизведению, метаболизм (обмен веществ), раздражимость, рост, изменчивость и адаптация к внешней среде. Однако надо учитывать, что каждая клетка многоклеточного организма находится в тесном взаимодействии с другими клетками и что организм - это единое целое, а не сумма клеток.
Клетка обладает сложной структурной организацией и представляет собой систему, дифференцированную на отдельные органеллы. Растительная клетка имеет клеточную стенку и протопласт. Протопласт состоит из ядра с ядрышком, цитоплазмы и включенных в нее мембранных (вакуоль, пластиды, митохондрии, аппарат Гольджи, лизосомы, эндоплазматический ретикулум) и немембранных (микротрубочки, рибосомы) органелл. Все органеллы погружены в матрикс цитоплазмы - гиалоплазму или основную плазму (рис. 2.1).
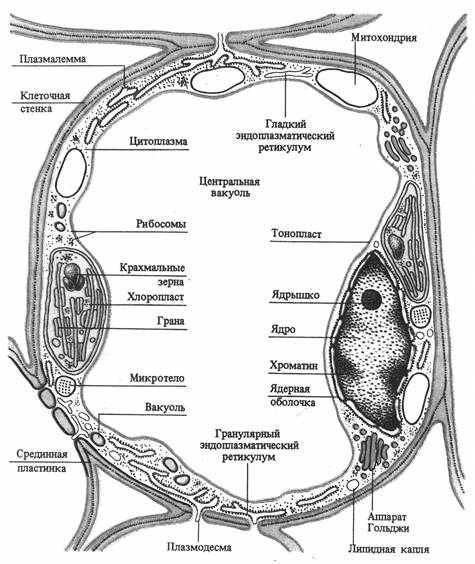
Рис. 2.1. Схема строения клетки мезофилла листа (по В. В. Полевому).
Все окруженные полупроницаемой мембраной компоненты клетки представляют собой замкнутые образования, в которых происходят разнообразные биохимические реакции. Цитоплазматический матрикс также разделен на отсеки эндоплазматической сетью. Тем самым достигается дополнительное пространственное разделение (компартментализация).
Основные физиологические функции структурных компонентов клетки: клеточная стенка - обеспечение прочности, защита, опорная функция; плазмалемма - транспорт веществ из и внутрь клетки, защита, рецепция; ядро - хранение и передача генетической информации; ядрышко - синтез РНК; вакуоль - осморегуляция, запасание веществ, переваривание; основная плазма - гликолиз; митохондрии - дыхание; хлоропласты – фотосинтез; аппарат Гольджи - секреция, образование компонентов клеточной стенки; эндоплазматическая ретикулум - транспорт веществ в клетке; лизосомы - внутриклеточное пищеварение; сферосомы - накопление и хранение жира; микротела (пероксисомы, глиоксисомы) - фотодыхание, глиоксалатный цикл; микротрубочки - ориентация микрофибрилл целлюлозы; рибосомы - синтез белка.
2.1. Раздражимость
Это способность клетки реагировать на действие внешних и внутренних факторов – раздражителей и передавать возбуждение в другие клетки. Восприятие раздражения обозначают термином перцепция или рецепция. У растений нет органов чувств, но есть рецепторные белки и клетки, воспринимающие разные воздействия. Различают фото-, хемо- и механорецепторы.
Возбуждение представляет собой измененное состояние клетки. В отсутствие раздражения растительная клетка имеет отрицательный потенциал покоя от -50 до -200 мВ, то есть протоплазма заряжена отрицательно по отношению к наружной поверхности. Это связано с тем. что внутри клетки находится больше ионов хлора и калия, но меньше ионов кальция, чем снаружи.
В ответ на раздражение возникает потенциал противоположного знака - потенциал действия, который может распространяться и на время сравняться или превысить потенциал покоя. Потенциал действия образуется в результате выхода ионов хлора из клетки и поступления ионов кальция в клетку.
Раздражение воспринимается клеткой, если его сила превышает пороговую величину. Следующие друг за другом подпороговые раздражения могут суммироваться, если интервалы между ними незначительны. Минимальное время, необходимое для рецепции, называют временем презентации.
Установлены следующие законы раздражимости:
1. Закон силы раздражения: чем больше раздражение, тем сильнее ответная реакция.
2. Закон длительности раздражения: чем длительнее раздражение, тем сильнее ответная реакция.
3. Закон количества раздражения: чем больше сила раздражения, тем меньше время презентации.
4. Закон градиента раздражения: чем выше скорость нарастания силы раздражителя, тем больше ответная реакция.
При действии чрезмерно сильных и (или) длительных воздействий чувствительность клеток к раздражителю снижается и клетки могут погибнуть.
Реституция - это восстановление исходного состояния после раздражения. Она идет с затратой энергии и тормозится под действием наркотиков, ингибиторов дыхания, при недостатке кислорода и снижении температуры. Во время реституции клетки находятся в рефрактерном периоде, когда новое раздражение не вызывает возбуждения.
2.2. Репликация, транскрипция и трансляция
Хранение наследственной информации осуществляется дезоксирибонуклеиновой кислотой (ДНК). ДНК - это полимер, мономерами которого являются дезоксирибонуклеотиды. В их состав входят углевод 2-дезокси-b-D-рибоза, остаток фосфорной кислоты и азотистые основания четырех типов: два пуриновых - аденин и гуанин, и два пиримидиновых - тимин и цитозин. Молекула ДНК состоит из двух полинуклеотидных цепочек, скрепленных между собой водородными связями между азотистыми основаниями. Полинуклеотидная цепочка образована чередующимися остатками 2-дезокси-b-D-рибозы и фосфорной кислоты, которая присоединена к 5 атому углерода кольца углевода с одной стороны и к 3 атому с другой стороны. Азотистые основания ответвляются от цепочки, присоединяясь к 1 атому углерода кольца углевода. Азотистые основания, противостоящие друг другу в полинуклеотидных цепочках, комплементарны друг другу: пуриновому основанию соответствует пиримидиновое (аденину – тимин, гуанину – цитозин). У каждой цепочки молекулы ДНК один конец заканчивается пятым (фосфатным), а другой - третьим (гидроксильным) углеродным атомом углевода. Они обозначаются как 5’ и 3’- концы. Цепочки в молекуле ДНК антипараллельны. В одной цепочке нуклеотиды связаны в направлении 5’ ® 3’, а в другой - 3’ ® 5’. Полинуклеотидные цепочки образуют двойную спираль. Каждый виток спирали содержит 10 пар азотистых оснований (рис. 2.2).

Рис. 2.2. Схема строения молекулы ДНК в виде двойной спирали (а) и прямой лесенки (б) (по В. Олфри и А. Мирскому).
1 – остаток 2-дезокси-β-D-рибозы, 2, 3, 4, 5 – азотистые основания (тимин, аденин, гуанин, цитозин, соответственно), 6 – остатки фосфорной кислоты.
Во время репликации (синтеза) ДНК каждая из цепей родительской ДНК служит матрицей для образования комплементарной дочерней цепи из предшественников – дезоксирибонуклеозидтрифосфатов: дезоксиаденозин-, дезоксицитидин-, дезоксигуанозин- и дезокситимидинтрифосфата. При их полимеризации происходит освобождение молекул пирофосфата, которые расщепляются пирофосфатазой. Репликация ДНК осуществляется по полуконсервативному механизму: одна из цепей дочерней молекулы ДНК является частью родительской молекулы, а другая – вновь синтезированной.
ДНК-полимераза способна синтезировать ДНК только в направлении от 5¢-конца к 3¢-концу. Поэтому на одной цепи ДНК образование дочерней цепи, называемой ведущей, происходит непрерывно, синтез другой цепи происходит прерывисто в виде коротких фрагментов Оказаки, получивших свое название в честь ученого, впервые их обнаружившего. Эта вторая дочерняя цепь получила название отстающей. Фрагменты Оказаки также синтезируются в направлении 5¢ ® 3¢, но перемещение ДНК-полимеразы вдоль матричной цепи ДНК при образовании каждого фрагмента противоположно направлению движения при синтезе ведущей цепи. Ведущая и отстающая цепи ДНК синтезируются координировано, что обеспечивается димеризацией ДНК-полимеразных комплексов у бактерий и наличием разных ДНК-полимераз у эукариотов. Для соединения двух фрагментов Оказаки ДНК-лигазой сначала удаляется РНК-затравка с помощью экзонуклеазы и РНКазы Н – нуклеазы, специфически расщепляющей РНК в ДНК-РНК-гибридах.
Процесс репликации ДНК разделяют на три этапа: инициацию, элонгацию и терминацию. Для начала репликации необходим праймер (затравка) – короткий олигодезокси- или олигорибонуклеотид, комплементарный соответствующему участку ДНК-матрицы.
В ходе репликации ДНК ее цепи расходятся из точки репликации, образуя Y-подобную структуру, которая называется репликативной вилкой. Именно в этом месте локализован репликативный комплекс, состоящий из нескольких белков. ДНК-хеликаза перемещается в репликативной вилке впереди ДНК-синтезирующего комплекса, расплетает цепи родительской ДНК и стимулирует образование затравок праймазой. ДНК-синтезирующий комплекс содержит ДНК-полимеразу, подвижный связывающий белок RPA и ДНК-зависимую АТФазу, которая узнает и связывается с единственным праймером ведущей цепи ДНК и с каждым праймером фрагментов Оказаки отстающей цепи, что делает возможным присоединение к праймерам ДНК-полимеразы и белка RPA. RPA связывается с образующимися одноцепочечными участками, облегчая процесс расплетения. RPA охватывает молекулу ДНК позади ДНК-зависимой АТФазы, стимулирует АТФазную активность и оставляет 3¢-конец праймера доступным для ДНК-полимеразы. ДНК-полимераза начинает элонгацию цепей ДНК, присоединяя первый дезоксирибонуклеозидмонофосфат к 3¢-концевому нуклеотиду РНК-затравки.
Передача информации от ДНК осуществляется посредством информационной или матричной рибонуклеиновой кислоты (мРНК). Синтез мРНК называется транскрипцией. Молекула мРНК, комплементарная одной из цепей матричной ДНК, образуется в ходе сополимеризации четырех рибонуклеозидтрифосфатов (аденин-, гуанозин-, цитозин- и урацилтрифосфата) с образованием 3¢-5¢-фосфодиэфирных связей и освобождением неорганического пирофосфата. Транскрипцию осуществляет фермент ДНК-зависимая РНК-полимераза. Синтез мРНК молекулами РНК-полимеразы начинается в определенных местах ДНК, называемых промоторами, и завершается на особых нуклеотидных последовательностях – терминаторах. Совокупность нуклеотидов ДНК, заключенных между промотором и терминатором, называют транскрипционной единицей или транскриптоном.
Процесс транскрипции подразделяют на 4 стадии: связывание РНК-полимеразы с ДНК и распознавание промотора, инициация, элонгация и терминация. Предполагается, что после первоначального непрочного связывания с ДНК в случайном месте молекула РНК-полимеразы перемещается вдоль двойной спирали ДНК до тех пор, пока не обнаружит последовательность нуклеотидов промотора. В этом месте связывание молекулы фермента с ДНК становится более прочным. Инициация транскрипции начинается с образования на промоторе предъиниционного комплекса, состоящего из РНК-полимеразы и матричной ДНК. После сборки предъинициационный комплекс претерпевает температурно-зависимые конформационные изменения, которые сопровождаются локальным плавлением, то есть расплетением двойной спирали ДНК, и комплекс становится способным к транскрипции. При наличии рибонуклеозидтрифосфатов происходит образование первых фосфодиэфирных связей в молекуле синтезируемой мРНК, после чего начинается стадия элонгации, то есть последовательное удлинение синтезируемой молекулы мРНК.
В 1992 г. М. Чэмберлен с сотрудниками разработали общую модель элонгации мРНК, согласно которой перемещение РНК-полимеразы вдоль ДНК и присоединение нуклеотидов к растущей цепи мРНК в активном центре фермента разделены во времени. Это разделение возможно потому, что у РНК-полимеразы имеется два сайта (участка), удерживающих растущую цепь мРНК, и два участка связывания ДНК-матрицы. Молекула РНК-полимеразы перемещается вдоль ДНК подобно гусенице: когда один сайт связывания ДНК фиксирован, другой перемещается вперед. ДНК-зависимые РНК-полимеразы фагов, состоящие из одной субъединицы, синтезируют РНК в условиях in vitro со скоростью 200-400 нуклеотидов в секунду. При перемещении фермента вдоль матрицы цепи ДНК подвергаются плавлению и повторному отжигу, в результате которого восстанавливается исходная структура ДНК. Стадия элонгации заканчивается после достижения РНК-полимеразой терминатора транскрипции. Затем синтезированная РНК и РНК-полимераза освобождаются из транскрипционного комплекса. Только минус-цепь ДНК служит матрицей для синтеза мРНК.
Участки ДНК, несущие информацию о строении белка - экзоны, разделены неинформативными интронами. В процессе транскрипции считывается информация как с экзонов, так и с интронов. Образуется предшественник мРНК - про-мРНК. Молекулы про-мРНК претерпевают созревание - процессинг. В ядре из про-мРНК происходит вырезание интронов и объединение экзонов - сплайсинг. К образовавшейся мРНК прикрепляется особая группировка поли-А и к одному из концов мРНК присоединяется защитная химическая группировка КЭП. После этого мРНК соединяется с белком, образуя инфорсому. Она выходит через поры в ядерной оболочке в цитоплазму. мРНК высвобождается из инфорсомы и одноцепочечная неспирализованная молекула мРНК присоединяется к участку малой субъединицы рибосомы, который примыкает к большой субъединице. К рибосоме прикрепляется небольшой участок цепи мРНК, содержащий один кодон, состоящий из трех азотистых оснований. Один кодон соответствует одной аминокислоте. Однако некоторые аминокислоты кодируются несколькими разными кодонами. Таким образом, первый этап синтеза белка - трансляции заключается в образовании комплекса между мРНК и рибосомой.
Перенос аминокислот в цитоплазме к рибосомам осуществляется транспортными РНК ( тРНК или 4S-РНК) из 70-80 нуклеотидов с молекулярной массой 25-30 кД. Они составляют почти 10 % от всей клеточной РНК и растворены в гиалоплазме. Поэтому тРНК еще называют растворимой РНК. В состав белков входят 20 аминокислот и каждой аминокислоте соответствует своя тРНК. Благодаря определенному расположению комплементарных нуклеотидов полинуклеотидная цепочка тРНК образует вторичную структуру, получившей название “клеверного листа”. Рентгеноструктурный анализ позволил установить третичную структуру тРНК. Она оказалась составленной из двух стеблей наподобие латинской буквы L.
Каждая тРНК имеет триплет оснований - антикодон, ответственный за прикрепление к комплементарному кодону мРНК. Для того, чтобы аминокислота присоединилась к тРНК необходима ее активация или обогащение энергией. Активация аминокислоты происходит за счет ее реакции с аденозинтрифосфорной кислотой (АТФ) - вещества с макроэргическими связями (~). Реакция идет при участии фермента аминоацилсинтетазы (кодазы). Образовавшийся аминоациладенилат остается связанным с ферментом и вступает в реакцию с тРНК с образованием аминоацил-тРНК.
Аминоацил-тРНК антикодоном присоединяется к кодону мРНК на малой субъединице рибосомы. После того как первая аминокислота со своей тРНК вошла в малую субъединицу рибосомы, происходит смыкание малой и большой субъединиц рибосомы. После смыкания субъединиц тРНК вместе с аминокислотой переносится на большую субъединицу. Одновременно мРНК перемещается на один кодон. В результате в малую субъединицу входит следующий кодон, кодирующий другую аминокислоту. К этому кодону с помощью антикодона присоединяется вторая тРНК со своей аминокислотой. В рибосоме оказываются две аминокислоты, ориентированные друг около друга таким образом, что карбоксильная группа первой аминокислоты оказывается рядом с аминогруппой второй аминокислоты. В результате сближения этих групп и с участием фермента большой субъединицы рибосомы пептидилтрансферазы аминокислоты соединяются пептидной связью. Образовавшийся дипептид присоединен ко второй тРНК, а первая тРНК освобождается и уходит в цитоплазму. В результате дипептид со второй тРНК оказывается связанным с большой субъединицей рибосомы, а мРНК перемещается еще на один кодон (рис. 2.3). Присоединение аминокислотных остатков - элонгация повторяется многократно, пока не образуется полипептидная цепочка белка. Окончание образования полипептидной цепочки - терминация связано с тем, что в малую субъединицу вступает терминальный кодон мРНК. Образовавшаяся полипептидная цепочка покидает рибосому. Большое значение имеет объединение рибосом в цепочки - полисомы. В этом случае одна молекула мРНК может последовательно присоединяться к ним и служить матрицей для синтеза нескольких одинаковых молекул белка. Когда синтез белка закончен, мРНК распадается. Синтез белковой молекулы идет с большой скоростью и поэтому время жизни мРНК невелико (от нескольких секунд до 1-2 минут). Однако, на определенных фазах развития растений (например, в набухающих и прорастающих семенах) синтезируются так называемые долгоживущие молекулы мРНК.

Рис. 2.3. Схема синтеза полипептидной цепи в рибосоме (по В. В. Полевому).
В заключение можно сказать, что из поколения в поколение передаются молекулы ДНК, которые несут в себе информацию о составе белковых молекул. План построения белка записан в ДНК с помощью триплетного кода, представленного чередованием азотистых оснований. Под влиянием внешних условий или спонтанно ДНК может изменяться. Эти изменения могут быть полезными, бесполезными и вредными. Полезные изменения, дающие организмам преимущество в борьбе за существование, могут закрепляться по наследству в ходе естественного или искусственного отбора.
Возникающие в процессе трансляции белки являются полимерами, мономерами которых служат аминокислоты. Белки представляют собой цепочки остатков аминокислот, соединенных между собой пептидными связями. Молекулярная масса белков зависит от количества мономеров и колеблется от нескольких тысяч до миллионов. Разнообразие белков определяется различной последовательностью аминокислотных остатков. Белки, также как и аминокислоты - амфотерные соединения, то есть имеют положительный и отрицательные заряды. У каждого белка своя изоэлектрическая точка - значение рН, при которой молекула белка не имеет заряда.
Молекула белка имеет первичную, вторичную, третичную и четвертичную структуру. Первичная структура определяется последовательностью аминокислотных остатков в белковой молекуле. Между аминокислотами, входящими в полипептидную цепочку, возможны водородные и другие связи. В результате этого полипептидная цепочка приобретает особенное расположение в пространстве, чаще всего в виде спирали. Это вторичная структура. По конформации полипептидной цепи различают фибриллярные и глобулярные белки. Фибриллярные белки сохраняют вытянутую форму спирали. У глобулярных белков спираль сворачивается в шарообразную глобулу, которая представляет собой третичную структуру белка. Она поддерживается кроме водородных связей гидрофобными взаимодействиями и дисульфидными связями, возникающими между двумя сульфгидрильными (SH) группами. Белки могут состоять из нескольких полипептидных цепочек и их взаимное расположение в пространстве и вокруг друг друга представляет собой четвертичную структуру.
2.3. Регуляции ферментативной активности в клетке
Химические процессы в клетке протекают с большой скоростью благодаря действию биологических катализаторов - ферментов или энзимов. Белковую часть фермента называют апоферментом. Небелковый компонент, прочно связанный, называют простетической группой, слабо связанный, обслуживающий несколько ферментов - коферментом. В состав простетических групп и коферментов входят металлы (железо, медь, цинк), витамины и их производные. Эндоферменты функционируют в клетке, а экзоферменты выделяются из клетки или локализуются в плазмалемме и действуют снаружи от нее.
Ферменты обладают специфичностью как к субстратам (субстратная специфичность), так и к определенным химическим реакциям (специфичность действия). Названия ферментов обычно заканчиваются суффиксом “аза”, за исключением некоторых общепринятых названий, например, пепсин, трипсин и другие. Название, как правило, отражает природу субстрата (хитиназа расщепляет хитин), или функцию фермента (аминотрансфераза переносит аминогруппы), или же то и другое вместе (алкогольдегидрогеназа). Ферменты разделяют на 6 классов: 1) оксиредуктазы - катализируют окислительно-восстановительные реакции, 2) трансферазы - перенос целых атомных группировок от одного соединения к другому, 3) гидролазы - распад органических соединений с участием воды, 4) лиазы - присоединение какой-либо атомной группировки к органическим соединениям или отщепление от субстратов определенной группы без участия воды, 5) изомеразы - превращение одних изомеров в другие, 6) лигазы или синтетазы - синтез органических соединений, происходящий при участии АТФ с использованием энергии этой кислоты.
Ферменты, катализирующие одну и ту же реакцию и встречающиеся у одного организма, но различающиеся по своим физико-химическим свойствам (например, по электрофоретической подвижности, следовательно, по молекулярной массе и заряду) называют изоферментами или изозимами. Наличие изоферментов позволяет организмам лучше приспосабливаться к меняющимся условиям внешней среды.
Катализ осуществляется в результате образования фермент-субстратного комплекса, что приводит к сближению реагирующих молекул или созданию напряженных химических связей путем их растягивания. Субстрат должен соответствовать активному центру не только пространственно, но и по распределению зарядов, расположению групп атомов и так далее. Окончательная подгонка происходит лишь в процессе взаимодействия субстрата с ферментом, претерпевающим при этой реакции конформационные изменения. Продукты реакции отделяются от фермента и молекулы фермента регенерируются. Благодаря своей способности регенерироваться, то есть возвращаться к первоначальному состоянию, одна и та же молекула фермента может катализировать большой объем превращений.
Скорость и направленность ферментативных реакций в клетке зависит от количества фермента, температуры и рН. Как всякая химическая реакция, ферментативные реакции зависят от температуры, что принято оценивать величиной температурного коэффициента (Q10), который показывает во сколько раз данный процесс ускоряется при повышении температуры на 10 Со. Поскольку ферменты являются белками, то повышение температуры свыше 35-40 Со вызывает их частичную инактивацию, а дальнейшее повышение температуры приводит уже к необратимой денатурации. У каждого фермента имеется свой оптимум рН, при котором лучше всего проявляется его активность. Это связано с тем, что рН влияет на заряд функциональных групп фермента, составляющих его активный центр, а от заряда зависит возможность образования фермент-субстратного комплекса.
Известны следующие механизмы внутриклеточной регуляции функционирования ферментов:
1. Метаболитная регуляция. Она происходит в результате изменения концентрации метаболитов и не затрагивает активность или число ферментных молекул. Различают регуляцию в местах разветвления путей обмена веществ и регуляцию по принципу обратной связи. В первом случае ферменты конкурируют за один и тот же субстрат и выбор пути определяется концентрацией общего для конкурирующих ферментов субстрата и степенью сродства фермента к субстрату. Под обратной связью понимается влияние более позднего члена цепи взаимосвязанных реакций на более ранний.
2. Ферментная регуляция. При этом типе регуляции изменяется активность ферментов. Изменение ферментативной активности может осуществляться несколькими путями: а) Обратимое или необратимое превращение неактивных предшественников ферментов - зимогенов в активные ферменты. Например, b-амилаза инактивирована в запасающих клетках эндосперма семян злаков из-за соединения с запасными белками посредством дисульфидных связей ( -S-S-). К началу прорастания семян из живых клеток алейронового слоя в эндосперм поступают вещества, разрушающие дисульфидные связи. Активированная b-амилаза принимает участие в гидролизе запасного крахмала; б) Изменение активности фермента под влиянием эффекторов. Связываясь с ферментом, эффекторы могут повышать его активность - это положительные эффекторы - активаторы или уменьшать ее - это отрицательные эффекторы - ингибиторы. Эффектор может влиять на активность фермента, взаимодействуя с активным центром (изостерический эффект) или изменяя конформацию ферментной молекулы в результате связывания с ее аллостерическим центром (аллостерический эффект). Изостерический эффект происходит в том случае, когда эффектор и субстрат похожи по своему строению и конкурируют друг с другом за активный центр фермента. Такой тип ингибирования называют конкурентным ингибированием.
3. Генная регуляция. В этом случае изменяется количество ферментных молекул в клетке из-за включения или выключения синтеза ферментов. Регулирующие факторы действуют на ДНК, РНК или рибосомы.
4. Мембранная регуляция. Различают контактную и дистанционную мембранную регуляцию активности ферментов. Контактная регуляция – связывание ферментов с мембранами или их освобождение меняет их активность. Дистанционная мембранная регуляция активности ферментов осуществляется косвенным путем в результате транспорта через мембраны субстратов и коферментов, удаления продуктов реакции, ионных и рН сдвигов в компартментах клетки.
2.4. Поступление воды в клетку
При температуре выше абсолютного нуля все молекулы находятся в постоянном движении. Диффузия - это процесс, ведущий к равномерному распределению молекул газов или растворенного вещества и растворителя благодаря их постоянному движению. Диффузия всегда направлена от большей концентрации вещества к меньшей. Количество вещества J, диффундирующего в единицу времени через воображаемое поперечное сечение, зависит от величины градиента dc/dx(градиент – мера изменения какого-либо параметра с расстоянием или временем) и от природы диффундирующего вещества, влияющего на коэффициент диффузии D. Это 1-й закон диффузии Фика, который описывается следующим уравнением:
J = - D · dc/dx,
так как суммарный поток направлен в сторону области меньшей концентрации, в уравнении стоит знак минус.
Скорость диффузии уменьшается с увеличением ее продолжительности. Проходимое путем диффузии расстояние пропорционально не времени, как при равномерном движении, а ее квадратному корню. Это 2-й закон диффузии Фика:
dc/dt = D · dc2/dx2,
где dc/dt – изменение концентрации вещества во времени.
Диффузия воды через полупроницаемую мембрану называется осмосом. Полупроницаемая мембрана - это мембрана хорошо проницаемая для воды и непроницаемая или плохо проницаемая для растворенных в воде веществ. Осмотическая ячейка - это пространство, окруженное полупроницаемой мембраной и заполненное каким-либо водным раствором. Все клеточные мембраны, в том числе плазмалемма и тонопласт, являются полупроницаемыми мембранами. Вода проходит в клетку через водные поры в плазмалемме, образованные специальными белками аквапоринами.
Внутри осмотической ячейки раствор развивает осмотическое давление p:
p = i · c · R · T,
где с – концентрация раствора в молях, Т - абсолютная температура, R - газовая постоянная 0,082 л · атм/град · моль, i – изотонический коэффициент, равный 1 + a(n-1), где a - степень электролитической диссоциации, n – число ионов, на которые распадается молекула электролита.
Благодаря осмотическому притоку воды в клетку там возникает гидростатическое давление, называемое тургорным. Это давление прижимает цитоплазму к клеточной стенке и растягивает ее. Клеточная стенка имеет ограниченную эластичность и оказывает равное противодавление. Эластическое растяжение ткани благодаря тургорному давлению ее клеток придает твердость не одревесневшим частям растений. Завядающие побеги становятся дряблыми, так как при потере воды тургорное давление падает. Тургорное давление противодействует притоку воды в клетку. Давление, с которым вода осмотически притекает в клетку, равно таким образом, разности между осмотическим давлением p и тургорным давлением P. Эту величину называют сосущей силой S: S = p - P. Вода поступает в клетку из внешнего раствора, если его потенциальное осмотическое давление меньше сосущей силы клетки и, наоборот, вода выходит из клетки в раствор с более высоким потенциальным осмотическим давлением.
При термодинамической трактовке сосущая сила заменяется водным потенциалом yw. Водный потенциал можно определить как работу, необходимую для того, чтобы поднять потенциал связанной воды до потенциала чистой, то есть свободной воды. Термин водный потенциал не совсем точен. Правильнее, но менее употребителен термин разность потенциалов воды, поскольку он определяется разностью между химическими потенциалами воды в системе mw (например, вакуоле) и чистой воды mow при атмосферном давлении. Абсолютные значения mw и mow неизвестны, но их разность можно определить. Она всегда отрицательна. Потенциал воды в растворе, растении, почве и атмосфере меньше 0. Потенциал чистой воды равен 0.
Можно также заменить p и P на потенциалы, а именно на осмотический потенциал yp (отрицательный) и потенциал давления yр (как правило, положительный). В таком случае осмотическое уравнение превращается в уравнение потенциала воды:
- yw = - yp - yр ( размерность бар = эрг · см-3 ·106)
Величину осмотического потенциала можно определить плазмолитическим методом. Плазмолиз - это процесс, обусловленный потерей воды клеткой. Он проявляется в отходе протопласта от клеточной стенки. В отдельных местах цитоплазма может в течение более или менее продолжительного времени сохранять связь с клеточной стенкой, образуя так называемые нити Гехта. Наблюдаются различные формы плазмолиза: выпуклый плазмолиз при небольшой вязкости цитоплазмы и вогнутый плазмолиз при высокой вязкости цитоплазмы (рис. 2.4). При переносе плазмолизированных тканей в гипотонический раствор или чистую воду вода поступает в клетку и происходит деплазмолиз. Количество воды в клетке увеличивается, объем вакуоли возрастает и она прижимает цитоплазму к клеточной стенке. Плазмолитический метод основан на подборе изоосмотического (изотонического) раствора, то есть имеющего осмотический потенциал равный осмотическому потенциалу клетки. Раствор, при котором начался плазмолиз, имеет осмотический потенциал примерно равный осмотическому потенциалу клетки. Зная концентрацию наружного раствора в молях, можно вычислить осмотический потенциал клетки.

Рис. 2.4. Формы плазмолиза.
1 – последовательные этапы плазмолиза в клетках листа мха, 2 – выпуклая форма плазмолиза (колпачковый плазмолиз) в клетке эпидермиса чешуи лука с окрашенной антоцианом вакуолью: а – ядро, б – цитоплазма, в – вакуоль (по Д. А. Сабинину – цит. по С. И. Лебедеву).
Иногда при сильном завядании протопласт не отстает от клеточной стенки как при плазмолизе, а сжимается и тянет ее за собой. При этом клеточная стенка прогибается. Это явление называют циторризом. Развивается натяжение или отрицательное давление стенки и потенциал тургорного давления приобретает отрицательное значение. В этом случае величина водного потенциала определяется уже не разностью, а суммой осмотического потенциала и потенциала давления: -yw = -yp + yp.
Величина осмотического потенциала позволяет судить о способности растения поглощать воду из почвы и удерживать ее, несмотря на иссушающее действие атмосферы. Осмотический потенциал колеблется у разных растений в пределах от -5 до -200 бар. У водных растений осмотический потенциал около -1 бара. У большинства растений средней полосы осмотический потенциал колеблется от -5 до -30 бар, растения степей и пустынь имеют более отрицательный осмотический потенциал. Осмотический потенциал различен и у разных жизненных форм. У деревьев он более отрицателен, чем у кустарников и травянистых растений, соответственно. У светолюбивых растений осмотический потенциал более отрицателен, чем у теневыносливых растений.
Поступление воды в клетку обусловлено не только осмотическим давлением, но и силой набухания. Набуханием называют поглощение жидкости или пара высокомолекулярным веществом (набухающим телом), сопровождаемое увеличением объема. Явление набухания обусловлено коллоидальными и капиллярными эффектами. В протоплазме преобладает набухание на коллоидальной основе (гидратация коллоидов), а в клеточной стенке наблюдаются оба эффекта: капиллярный - накопление воды между микрофибриллами и в межмицеллярных пространствах и коллоидальный - гидратация полисахаридов, особенно гемицеллюлоз.
У некоторых частей растений поглощение воды происходит исключительно путем набухания, например, у семян. Вода диффундирует в набухающее тело. Благодаря большому сродству набухающего тела к воде при набухании может возникать давление набухания в несколько сотен атмосфер. Силу набухания обозначают термином матричный потенциал yt.
Таким образом, для клетки характерны следующие уравнения водного потенциала:
вакуоль: -yw = -yp - yp
протоплазма: -yw = -yp - yp - yt
клеточная стенка: -yw = - yt
Вода в клетку может поступать также в процессе пиноцитоза, когда часть плазмалеммы под влиянием различных причин, чаще всего в результате адсорбции на плазмалемме крупных молекул и вирусных частиц, прогибается внутрь клетки, внешние края такой инвагинации смыкаются и виде пузырька - везикулы с адсорбированной частицей и внешним раствором проходит внутрь цитоплазмы.
2.5. Поступление ионов в клетку
Все неорганические питательные вещества поглощаются в форме ионов, содержащихся в водных растворах. Поглощение ионов клеткой начинается с их взаимодействия с клеточной стенкой. Ионы могут частично локализоваться в межмицеллярных и межфибриллярных промежутках клеточной стенки, частично связываться и фиксироваться в клеточной стенке электрическими зарядами.
Поступившие ионы легко вымываются. Объем клетки, доступный для свободной диффузии ионов, получил название свободного пространства. Свободное пространство включает межклетники, клеточные стенки и промежутки, которые могут возникать между клеточной стенкой и плазмалеммой. Иногда его называют кажущееся свободное пространство (КСП). Термин “кажущееся” означает, что его объем зависит от объекта и природы растворенного вещества. КСП занимает в растительных тканях 5-10 % объема. Свободное пространство всего растения получило название апопласт, в отличие от симпласта - совокупности протопластов всех клеток.
Поглощение и выделение веществ в КСП - физико-химический пассивный процесс, не зависимый от температуры и ингибиторов энергетического и белкового обменов. Клеточная стенка обладает свойствами ионообменника, так как в ней адсорбированы ионы Н+ и НCO-3, обменивающиеся в эквивалентных количествах на ионы внешнего раствора. В клеточную стенку входят амфотерные белковые соединения, заряд которых меняется при изменение рН. Поэтому адсорбция ионов зависит от величины рН. Из-за преобладания отрицательных фиксированных зарядов в клеточной стенке происходит первичное концентрирование катионов (особенно двух- и трехвалентных).
Для того, чтобы проникнуть в цитоплазму и включиться в обмен веществ, ионы должны пройти через плазмалемму. Транспорт ионов через мембрану может быть пассивным и активным. Пассивное поглощение не требует затрат энергии и осуществляется путем диффузии по градиенту концентрации вещества, для которого плазмалемма проницаема. Пассивное передвижение ионов определяется не только химическим потенциалом m, как это имеет место при диффузии незаряженных частиц, но и электрическим потенциалом e. Оба потенциала объединяют в виде электрохимического потенциала `m: `m = m + nFe, где m - химический, e - электрический, `m - электрохимический потенциалы, n - валентность иона, F - константа Фарадея. Любая разность электрических потенциалов, которая возникает на мембранах, вызывает соответствующее перемещение ионов.
Электрический потенциал на мембране - трансмембранный потенциал может возникнуть по следующим причинам: 1) если поступление ионов идет по градиенту концентрации, но благодаря разной проницаемости мембр
Похожие статьи:
poznayka.org
ксилема, флоэма и сок в физиологии растений — Сириус агро плант
Флоэма и ксилема являются сосудистыми тканями трахеофитных растений, то есть в них расположены сосуды растений, которые осуществляют транспортировку сока в растительных организмах: папоротникообразных, голосеменных и покрытосеменных, сообщая корневую систему с лиственными структурами посредством стебля. Обе являются переносчиками сока.
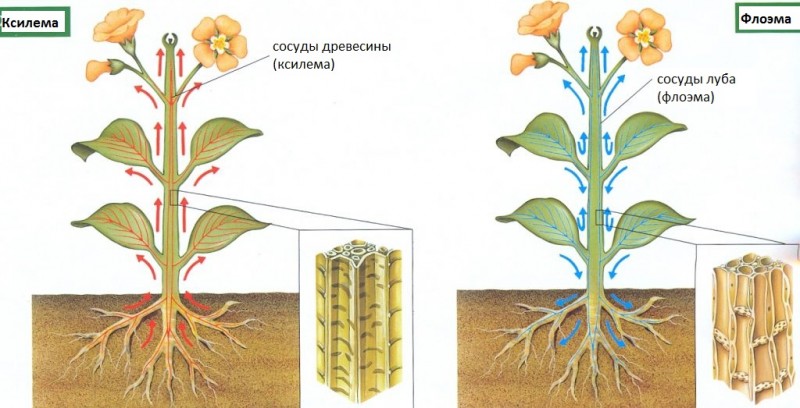
Ксилема транспортирует необработанный «сырой» сок (сырье или неорганический сок, поскольку он состоит из питательных веществ, поглощенных из почвы растением, воды и минеральных солей) и расположена в самом внутреннем слое стебля. Она транспортирует сок от корней к листьям, где будет проходить фотосинтез. Ксилема образована мертвыми клетками, которые имеют функцию предотвращения деформации, вызванной давлением сока.
Флоэма транспортирует переработанный сок (или органический сок, продукт фотосинтеза, где питательные вещества превращаются в глюкозу) и находится в самом внешнем слое стебля. Она транспортирует переработанный сок из хлорофильных частей (мест, где происходит фотосинтез) к живыми частями растения — областям, где глюкоза будет превращаться в энергию. Флоэма образована живыми клетками, вытянутыми и без ядра.

Транспортировка необработанного сока, образованного водой и минеральными солями, осуществляемая ксилемой, происходит из способности поглощения корней и распределения в основной пункт назначения к листьям. Ее основной состав включает сосуды, трахеи, трахеиды, волокна и паренхимные клетки.
Транспортировка переработанного сока, образованного органическими веществами, полученными при фотосинтезе, осуществляется через флоэму, начиная от листьев в направлении остальных органов, главным образом, энергетического резерва (корней и стеблей). Она состоит из ситовидных элементов, сопровождающих клеток, волокон и паренхимных клеток.
Растения как автотрофные организмы
У растений автотрофное питание, другими словами, они могут производить органические молекулы (главным образом глюкозу) из простых неорганических веществ с помощью внешнего источника энергии, энергии света.
Итак, питательные вещества, которые требуются растению, очень просты: вода, минеральные соли и углекислый газ (мы не называем солнечную энергию, потому что это не вещество, а тип энергии). Растения в процессе фотосинтеза, происходящего в хлоропластах клеток, продуцируют глюкозу, которая является органической молекулой, служащей источником химической энергии (а также для создания других малых и больших структурных молекул, например, целлюлозы).
В связи с этим растение испытывает следующие трудности:
- Фотосинтез происходит главным образом в клетках листьев на определенной высоте над землей (иногда несколько метров), но воду и минеральные соли следует добывать из почвы, корнями. Поэтому растение должно транспортировать эти простые вещества вверх, преодолевая силу тяжести.
- Не все клетки растения выполняют фотосинтез (например, клетки корней нет). Поэтому, как только глюкоза вырабатывается в клетках листьев, часть ее должна транспортироваться в другие места для снабжения всех клеток.
Растение должно поглощать воду и минеральные соли через корни. Для этого клетки самого поверхностного слоя корня имеют очень тонкие расширения в виде нитей, которые выступают наружу, называемые абсорбирующими или корневыми волосками. Таким образом, контактная поверхность корня с внешней средой значительно увеличивается.
Клетки, которые составляют абсорбирующие волоски, имеют важную способность: они способны переносить минеральные соли из внешней среды во внутреннюю часть клетки, даже если концентрация солей внутри клетки больше, чем снаружи (затратив некоторую энергию, конечно). Таким образом, концентрация солей становится больше внутри клеток по отношению к внешней стороне.
Существуют две альтернативы для проникновения воды в корень: вода может проходить через клетки, переходя из одной в другую через небольшие отверстия, называемые плазмодесмами (внутриклеточный или упрощенный транспорт) или проходить через пространства клеточных стенок, которые отделяют одну клетку от другой (внеклеточный или апопластический транспорт).
Как только вода была поглощена, достигнута первая цель: вода и минеральные соли находятся внутри корневых клеток… но все еще далеки от их цели, которая является листьями.
Транспортировка необработанного сока через ксилему
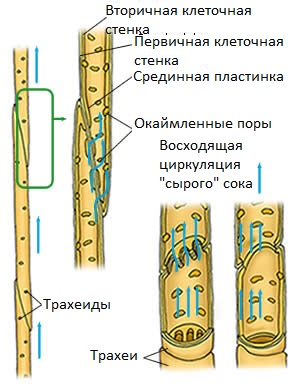
Для доставки воды, минеральных солей и других веществ, производимых корневыми клетками, к листьям у растений есть гениальная система проводимости, образованная очень специализированными клетками, которые в совокупности называются ксилемой.
Ксилема — очень своеобразная ткань, потому что многие из ее клеток «жертвуют» собой, чтобы выполнить свою функцию! Хотя это звучит немного противоречиво, клетки ксилемы более эффективны мертвыми, чем живыми. По мере их роста они утолщают клеточные стенки, образуя спиральные или кольцевые структуры. Кроме того, они соединяются друг с другом для образования различных типов трубок. Наконец, они умирают, клетка исчезает, но ее клеточная стенка остается, что будет способствовать образованию удлиненных каналов, наподобие трубок, которые проходят по всему стеблю от корней до листьев.
Существует два основных типа проводящих трубок. Первый тип — трахеиды, представляющие собой очень узкие и удлиненные клетки, в которых прохождение веществ из одной клетки в другую осуществляется через окаймленные поры в клеточных стенках, расположенные на большой части этих стенок. Другим типом являются сосуды или трахеи с несколько большим диаметром и с законченными отверстиями (перфорациями) в зонах стенок, отделяющих от других клеток.
Вы, вероятно, задаетесь вопросом: «Если клетки трубок ксилемы мертвы, как им удается транспортировать сок?»
Хитрость заключается в использовании физических механизмов, которые не требуют вмешательства биологических процессов. Вода поднимается через трубки ксилемы благодаря нескольким физическим процессам, которые вместе образуют механизм, часто называемый натяжение-адгезия(прилипание)-когезия(сцепление). Основные идеи этого механизма были предложены более века тому назад Генри Диксоном. Механизм натяжение-адгезия-когезия основан на следующих явлениях или процессах.
Капиллярность
Капилярность — это любопытное явление, которое заставляет некоторые жидкости подниматься против гравитации спонтанно, внутри очень тонких протоков. Чем меньше диаметр канала, тем выше высота восходящего столба жидкости. Это движение, вызванное силой, возникшей в результате конфликта между двумя другими: поверхностное натяжение воды и адгезия воды к твердым поверхностям некоторых веществ:
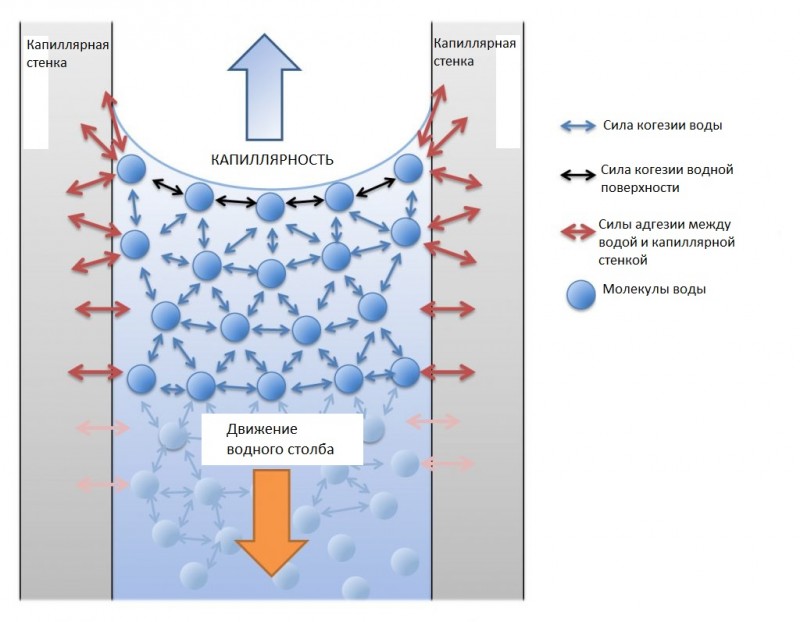
- Когезия и поверхностное натяжение:
Молекулы воды, благодаря своей полярности, устанавливают между собой союзы, которые отвечают за сильное сцепление (объединение), существующее между ними.
Внутри массы воды каждая молекула одинаково привлекается в равной мере своими соседями, но только на поверхности жидкости, контактирующей с воздухом, все меняется: сплоченность молекул воды «вытягивает» молекулы воды внутрь жидкости, а также в направлении, параллельном поверхности жидкости.
Таким образом, сцепление заставляет слой молекул, контактирующих с воздухом, иметь натяжение, которое заставляет их вести себя как эластичная пленка.
Поверхность воды оказывает сопротивление деформации, поскольку ситуация максимального баланса будет такова, в которой поверхность контакта вода-воздух минимальна. Сила поверхностного натяжения отвечает за форму, которую принимают капли воды, а также за то, что легкие насекомые способны ходить по поверхности воды без погружения.
- Поверхностное натяжение и адгезия:
Между молекулами воды и твердыми поверхностями многих веществ также может быть установлена притягивающая сила, которая заставляет воду прилипать к этим поверхностям. Если адгезия к твердой поверхности сильнее когезии между молекулами воды, на краю жидкости, контактирующей с твердым материалом будет образовываться вогнутая кривизна поверхности.
Однако, поверхностное натяжение воды создает силу, которая тянет молекулы, образующие нижнюю часть кривой, чтобы попытаться уменьшить контактную поверхность воздух-вода, создавая плоскую пленку.
В результате создается возрастающая результирующая сила, которая приводит к небольшому подъему водного столба. Конечным результатом является то, что вода может буквально подняться по каналу, преодолевая силу тяжести.
Эвапотранспирация и натяжение
Капиллярность очень хорошо дает понять, как сырой сок может спонтанно подниматься через очень тонкие трубки ксилемы, но как только столб воды или сырой сок достигает конца трубки, капиллярности недостаточно, чтобы объяснить, как этот сок может продолжать подниматься из корня.
Механизм, который нам не ясен, связан с испарением воды, которая вырабатывается в листьях, и расходами этой воды при фотосинтезе.
Когда молекулы воды удаляются с конца трубки ксилемы из-за транспирации листьев, отверстие, как правило, немедленно заполняется другими молекулами, которые ниже. Это создает натяжение или отрицательное давление, которое буквально тянет столб воды вверх.
Сильное сцепление между молекулами воды предотвращает разрыв столбика сока внутри трубки, так что весь сок внутри трубки поднимается как единое целое. Естественно, из корней должна быть постоянная подача воды. В противном случае, как и в ситуациях засухи, столбик сока может быть прерван, что вызовет проблемы для растения.
Следующий рисунок объясняет явление натяжения, вызванного эвапотранспирацией:
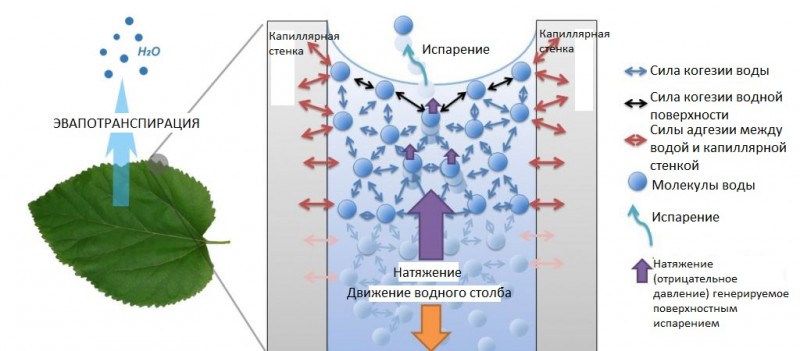
Транспортировка переработанного сока через флоэму
К настоящему моменту мы не решили и более половины проблемы, потому что, как только фотосинтетические клетки образуют углеводы, необходимо распределить эти молекулы и их производные во многие другие отдаленные клетки, которые не способны их произвести.
Для этого распределения растения имеют другую ткань, называемую флоэмой, которая также образует каналы, проходящие через растение, но с некоторыми важными отличиями по сравнению с ксилемой.
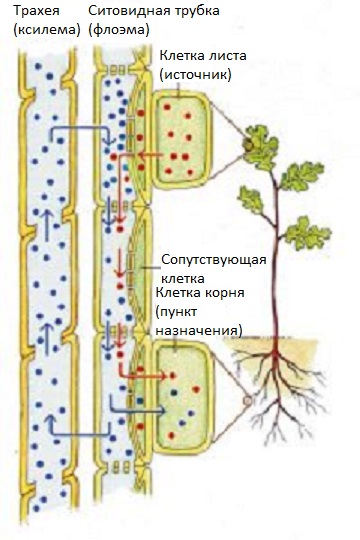
Во-первых, проводящие клетки флоэмы живые, хотя они теряют свое ядро и довольно много органелл. В целом, они имеют меньший диаметр, чем проводники ксилемы.
Как и в ксилеме, клетки флоэмы выстраиваются рядами и соединяют свои стенки. В зонах соединения образуются структуры, называемые ситовидными пластинками. В этих областях имеются небольшие отверстия диаметром до 15 мкм (не такие большие, как перфорации ксилемы), которые позволяют передавать переработанный сок из одной ячейки в другую. Каналы, образованные объединением множества этих клеток, называются ситовидными трубками.
В течение некоторого времени считалось, что переработанные вещества могут транспортироваться путем диффузии через трубки флоэмы, но когда были сделаны расчеты, чтобы узнать скорость транспортировки через флоэму, стало ясно, что необходим другой механизм.
В настоящее время считается, что механизмом движения переработанного сока через флоэму является механизм, который предложил немецкий ученый Эрнст Мюнх в 1926 году. Этот механизм называется потоком под давлением и состоит в следующем.
Как только фотосинтетические клетки образуют органические молекулы, благодаря фотосинтезу, особенно глюкозу и фруктозу, большая часть этих молекул связывается с образованием сахарозы, которая является предпочтительной органической молекулой для переноса углеводов через растение.
Сахароза транспортируется во флоэму, из-за этого переработанный сок содержит высокую концентрацию этого вещества (сахароза составляет 90% веществ, присутствующих в переработанном соке, конечно, без учета воды). Поскольку концентрация сахарозы внутри флоэмы намного выше, чем снаружи, создается осмотическое давление, которое заставляет воду поступать во флоэму, тем самым увеличивая ее давление. Это давление подталкивает переработанный сок вдоль протоков флоэмы.
Как только они достигают места назначения, которое является конечным пунктом протоков флоэмы, большое количество сахарозы извлекается из флоэмы, «вытаскивая» с ней определенное количество воды. Это способствует циркуляции переработанного сока, вызывая падение давления в конечном пункте. Сахароза, поступив к месту назначения, может использоваться для разных целей.
Резюме
Подводя итоги, можно отметить, что корни поглощают минеральные соли посредством активного транспорта, что генерирует осмотическое давление, вызывающее поглощение воды.
Эти вещества достигают проводников ксилемы, которые отвечают за транспортировку сырого сока от корней к фотосинтетическим структурам за счет механизма когезия-адгезия-натяжение.
После того как вырабатываются органические вещества, проводники флоэмы отвечают за транспортировку переработанного сока, богатого органическими молекулами, из листьев в другие области растения посредством механизма потока под давлением, основанного на механизмах осмотического давления.
Инга Костенко, Mivena Украина
Анна Устименко, Клуб Sirius Agro Plant
siriusap.com
Биологические молекулы • Джеймс Трефил, энциклопедия «Двести законов мироздания»
Жизнь — таинственная, сложная, загадочная — не что иное как совокупность достаточно крупных молекул и довольно простых химических реакций. Если бы вам понадобилось конструировать крупные молекулы, вы пошли бы по одному из двух путей. Либо, как в кустарном ювелирном деле, вы стали строить каждую молекулу «с нуля», проделывая каждый раз уникальную работу. Либо — этот путь используется в современных строительных технологиях — вы бы изготовили набор простых молекул, из которых можно собирать самые разнообразные молекулы большего размера, сочетая модули тем или иным образом. Оказывается, именно такое модульное строение имеют биологические молекулы. Согласно теории эволюции, таким и должен был быть самой простой путь к крупным молекулам, поскольку в начале эволюционного процесса необходимость в конструировании очень сложных молекул отсутствовала. Со временем же могли добавляться новые модули, расширяя коллекцию крупных разнородных элементов, что вполне соответствует духу эволюции.
Белки
Основной структурной единицей белков являются молекулы аминокислот. Чтобы понять, что такое аминокислота, представьте себе совокупность атомов, у которых с одной стороны наружу выступает водород, с другой — соединенные между собой кислород и водород, а посередине расположены разнообразные другие компоненты. Подобно тому как бусины нанизываются на нить, из этих аминокислот собираются белки — ион водорода (Н+) одной аминокислоты объединяется с ионом гидроксила (ОН–) другой аминокислоты с образованием молекулы воды. (Представьте, как каждый раз при соединении двух аминокислотных молекул между ними пробегает капелька воды.) Среди белков самую важную роль играют белки-ферменты (см. Катализаторы и ферменты), регулирующие химические реакции в клетках; но белки также являются важными структурными компонентами живых организмов. Например, ваши волосы и ногти состоят из белков.
Углеводы
Углеводы содержат кислород, водород и углерод в соотношении 1:2:1. Во многих живых системах молекулы углеводов выполняют роль источников энергии. Одним из важнейших углеводов можно считать сахар глюкозу, содержащую шесть атомов углерода (С6Н12О6). Глюкоза — конечный продукт фотосинтеза и, следовательно, основа всей пищевой цепи в биосфере. Соединяя молекулы глюкозы, как основные строительные модули, можно получить сложные углеводы. Как и белки, углеводы играют вспомогательную роль в клетках, поскольку входят в клеточные структуры. Например, растительные волокна состоят из целлюлозы, которая представляет собой вереницу сцепленных особым образом молекул глюкозы.
Липиды
Липиды — это нерастворимые в воде органические молекулы. Вы получите правильное представление о липидах, если вообразите капельки жира, плавающие на поверхности бульона. В живых организмах липиды выполняют две важные функции. Один класс молекул — фосфолипиды — состоят из маленькой головки, содержащей фосфатную группу (атом фосфора, соединенный с четырьмя атомами кислорода), и длинного углеводородного хвоста. Углеводородный хвост этой молекулы гидрофобен, то есть энергетическое состояние молекулы минимально, когда этот хвост находится не в воде. Напротив, фосфатная головка гидрофильна, то есть энергетическое состояние молекулы минимально при контакте головки с водой . Если поместить молекулы фосфолипидов в воду, они будут стремиться достичь минимального энергетического состояния и выстроятся таким образом, что их хвосты окажутся вместе, а головки — врозь. Такая двухслойная структура очень стабильна, поскольку головки будут в контакте с водой, но вода будет вытеснена из области, окружающей хвосты молекул. Для перемещения липидным молекулам необходима энергия — либо чтобы удалить гидрофильные участки из воды, либо чтобы поместить в воду гидрофобные участки. Из таких липидных двухслойных структур состоят клеточные мембраны и мембраны, разделяющие компоненты клетки. Эти пластичные и прочные молекулы отделяют живое от неживого.
Кроме того, в липидах запасается энергия. Липиды могут накапливать примерно вдвое больше энергии на единицу массы, чем углеводы. Вот почему, когда вы переедаете и ваш организм хочет запасти энергию на случай непредвиденных обстоятельств в будущем, когда пищи не будет, он станет запасать ее в форме жира. На этом простом факте строится многомиллиардная индустрия диетических продуктов.
Нуклеиновые кислоты
Молекулы ДНК и РНК (см. Центральная догма молекулярной биологии) переносят информацию о химических процессах, идущих в клетке, и участвуют в передаче содержащейся в ДНК информации в цитоплазму клетки. В ДНК живого организма закодированы белки-ферменты, которые катализируют все химические реакции, происходящие в этом организме.
Молекулы-переносчики энергии
Жизнедеятельность требует затрат энергии. В частности, нужно, чтобы энергия, произведенная в одном месте, могла быть использована в другом. Эту функцию в клетке осуществляет целая армия специализированных молекул. Пожалуй, самые важные из них — аденозин трифосфат (АТФ) и аденозин дифосфат (АДФ). Обе молекулы устроены так: группа из атомов углерода, водорода и азота (она называется аденин) присоединена к молекуле рибозы (это сахар), и все это вместе крепится к хвосту из фосфатов. Из названий молекул понятно, что в хвосте АДФ содержится два фосфата, а в хвосте АТФ — три. Когда в клетке происходит химический процесс, например фотосинтез, образующаяся энергия идет на присоединение третьего фосфата к хвосту АДФ. Полученная молекула АТФ затем переносится в другие части клетки. Там запасенная энергия может быть использована в других химических процессах: она выделяется при отщеплении последнего фосфата от АТФ, в результате чего АТФ вновь превращается в АДФ.
Как мы уже упоминали, существуют и другие молекулы, которые переносят энергию в клетке. Набор таких молекул чем-то напоминает разные варианты оплаты счетов. Вы можете выбрать наличные, банковский перевод, кредитную карту и т. д. — в зависимости от того, какой способ вам удобнее. Так же и клетка для поддержания своей жизнедеятельности может использовать АТФ (эквивалент наличных денег) или любую другую из большого набора более сложных молекул.
См. также:
elementy.ru
Как растения защищаются от загара
Несмотря на то, что для растений солнце – это жизнь, им, как и нам с вами, тоже вредны некоторые части солнечного спектра. Ультрафиолет действует одинаково на все клетки, вызывая повреждения ДНК, так что растениям приходится от него защищаться.
Биологам уже было известно, что защиту им обеспечивает белок UVR8. Как именно этот белок работает, впервые выяснили ученые из Исследовательского института Скриппса (Scripps Research Institute) и опубликовали свои результаты в последнем выпуске Science.
«Это древняя молекула, играющая фундаментальную роль в жизни растений, - говорит профессор Элизабет Гетзофф (Elizabeth Getzoff), cлова которой приводит EurekAlert. – Знания о ее работе позволят нам понять, как растения приспосабливаются к росту с разным режимом солнечного освещения».
Экран от солнца
Еще в 2002 году биологи открыли роль белка UVR8 в защите от ультрафиолета. Они убедились, что растение резуховидка Таля (Arabidopsis), лишенное гена этого белка, плохо переносит облучение UV-B лучами. А если ген в растении работает, то белок UVR8 улавливает UV-B лучи (вызывающие загар) и запускает защитный ответ всего организма. Начинают работать гены репарации ДНК и другие защитные белки.
Так как ученые нашли молекулы, аналогичные UVR8, в древних по просхождению растениях, такие как водоросли и мхи, они полагают, что этот защитный механизм сформировался давно, еще когда на планете не было озонового слоя, и все живые организмы подвергались жесткому ультрафиолету.
Как работает молекула
В последней работе исследователи изучили строение UVR8 в кристаллической форме методом рентгеновской кристаллографии. Они увидели архитектуру молекулы и расположение атомов с высоким разрешением. Молекула представляет собой димер, то есть состоит из двух частей – субъединиц, каждая в форме «бублика». Поглощение UV-B фотона активизирует сенсорный центр, в который входит аминокислота триптофан. Вслед за этим связи молекулы ослабляются, и димер распадается на две единицы.
Половинки молекулы попадают в клеточное ядро, где запускают работу защитных генов. Сделав свое дело, через несколько часов субъединицы снова объединяются и готовы к работе. Ученые подчеркивают, что UVR8 - уникальная молекула, которая даже не требует химической модификации, чтобы «поймать» вредный фотон и активизировать защиту.
Сенсор молекулы работает на основе аминокислоты триптофана, которая входит в состав пирамидальной структуры. Заменив триптофан на другую аминокислоту – фенилаланин, ученые сместили спектр чувствительности молекулы с UV-B-диапазона на UV-С-диапазон.
www.infox.ru
органические вещества, макро- и микроэлементы
В конце 19 столетия сформировалась отрасль биологии, названная биохимией. Она изучает химический состав живой клетки. Главная задача науки – познание особенностей обмена веществ и энергии, регулирующих жизнедеятельность растительных и животных клеток.

Понятие о химическом составе клетки
В результате тщательных исследований учёными была изучена химическая организация клеток и установлено, что живые существа имеют в своем составе более 85 химических элементов. Причём некоторые из них обязательны практически для всех организмов, а другие специфичны и встречаются у конкретных биологических видов. А третья группа химических элементов присутствует в клетках микроорганизмов, растений и животных в достаточно малых количествах. Химические элементы в состав клеток входят чаще всего в виде катионов и анионов, из которых образуются минеральные соли и вода, а также синтезируются углеродсодержащие органические соединения: углеводы, белки, липиды.
Органогенные элементы
В биохимии к ним относятся карбон, гидроген, оксиген и нитроген. Их совокупность составляет в клетке от 88 до 97% от других химических элементов, находящихся в ней. Особенно важен карбон. Все органические вещества в составе клетки состоят из молекул, содержащих в своём составе атомы углерода. Они способны соединяться между собой, образуя цепи (разветвлённые и неразветвленные), а также циклы. Эта способность углеродных атомов лежит в основе поразительного разнообразия органических веществ, входящих в состав цитоплазмы и клеточных органоидов.
Например, внутреннее содержимое клетки состоит из растворимых олигосахаридов, гидрофильных белков, липидов, различных видов рибонуклеиновой кислоты: транспортной РНК, рибосомальной РНК и информационной РНК, а также свободных мономеров – нуклеотидов. Подобный химический состав имеет и клеточное ядро. Оно также содержит молекулы дезоксирибонуклеиновой кислоты, входящие в состав хромосом. Все вышеперечисленные соединения имеют в своём составе атомы нитрогена, карбона, оксигена, гидрогена. Это является доказательством их особенно важного значения, так как химическая организация клеток зависит от содержания органогенных элементов, входящих в состав клеточных структур: гиалоплазмы и органелл.
Макроэлементы и их значения
Химические элементы, которые также очень часто встречаются в клетках различных видов организмов, в биохимии называются макроэлементами. Их содержание в клетке составляет 1,2% – 1,9%. К макроэлементам клетки относятся: фосфор, калий, хлор, сера, магний, кальций, железо и натрий. Все они выполняют важные функции и входят в состав различных клеточных органелл. Так, ион двухвалентного железа присутствует в белке крови – гемоглобине, который транспортирует кислород (в этом случае он называется оксигемоглобин), углекислый газ (карбогемоглобин) или угарный газ (карбоксигемоглобин).
Ионы натрия обеспечивают важнейший вид межклеточного транспорта: так называемый натрий-калиевый насос. Они также входят в состав межтканевой жидкости и плазмы крови. Ионы магния присутствуют в молекулах хлорофилла (фотопигмент высших растений) и участвуют в процессе фотосинтеза, так как образуют реакционные центры, улавливающие фотоны световой энергии.
Ионы кальция обеспечивают проведение нервных импульсов по волокнам, а также являются главным компонентом остеоцитов – костных клеток. Соединения кальция широко распространены в мире беспозвоночных животных, у которых раковины состоят из карбоната кальция.
Ионы хлора принимают участие в перезарядке клеточных мембран и обеспечивают возникновение электрических импульсов, лежащих в основе нервного возбуждения.
Атомы серы входят в состав нативных белков и обуславливают их третичную структуру, «сшивая» полипептидную цепь, вследствие чего формируется глобулярная белковая молекула.
Ионы калия участвуют в транспорте веществ через клеточные мембраны. Атомы фосфора входят в состав такого важного энергоёмкого вещества, как аденозинтрифосфорная кислота, а также являются важным компонентом молекул дезоксирибонуклеиновой и рибонуклеиновых кислот, являющихся главными веществами клеточной наследственности.
Функции микроэлементов в клеточном метаболизме
Около 50 химических элементов, составляющих менее 0,1% в клетках, называются микроэлементами. К ним относят цинк, молибден, йод, медь, кобальт, фтор. При незначительном содержании они выполняют очень важные функции, так как входят в состав многих биологически активных веществ.

Например, атомы цинка находятся в молекулах инсулина (гормона поджелудочной железы, регулирующего уровень глюкозы в крови), йод является составной частью гормонов щитовидной железы – тироксина и трийодтиронина, контролирующих уровень обмена веществ в организме. Медь, наряду с ионами железа, участвует в кроветворении (образовании эритроцитов, тромбоцитов и лейкоцитов в красном костном мозге позвоночных животных). Ионы меди входят в состав пигмента гемоцианина, присутствующего в крови беспозвоночных животных, например моллюсков. Поэтому цвет гемолимфы у них голубой.
Ещё меньше содержание в клетке таких химических элементов, как свинец, золото, бром, серебро. Они называются ультромикроэлементами и входят в состав растительных и животных клеток. Например, в зерновках кукурузы химическим анализом были выявлены ионы золота. Атомы брома в большом количестве входят в состав клеток слоевища бурых и красных водорослей, например саргассума, ламинарии, фукуса.
Все ранее приведённые примеры и факты объясняют, как взаимосвязаны химический состав, функции и строение клетки. Таблица, приведённая ниже, показывает содержание различных химических элементов в клетках живых организмов.

Общая характеристика органических веществ
Химические свойства клеток различных групп организмов определённым образом зависят от атомов карбона, доля которых составляет более 50% клеточной массы. Практически все сухое вещество клетки представлено углеводами, белками, нуклеиновыми кислотами и липидами, которые имеют сложное строение и большую молекулярную массу. Такие молекулы называются макромолекулами (полимерами) и состоят из более простых элементов – мономеров. Белковые вещества играют чрезвычайно важную роль и выполняют множество функций, которые и будут рассмотрены ниже.
Роль белков в клетке
Биохимический анализ соединений, входящих в живую клетку, подтверждает высокое содержание в ней таких органических веществ, как белки. Этому факту есть логическое объяснение: белки выполняют разнообразные функции и участвуют во всех проявлениях клеточной жизнедеятельности.
Например, защитная функция белков заключается в образовании антител – иммуноглобулинов, вырабатываемых лимфоцитами. Такие защитные белки, как тромбин, фибрин и тромбобластин, обеспечивают свёртываемость крови и предотвращают её потерю при травмах и ранениях. В состав клетки входят сложные белки клеточных мембран, имеющие способность распознавать чужеродные соединения – антигены. Они изменяют свою конфигурацию и сообщают клетке о потенциальной опасности (сигнальная функция).
Некоторые белки выполняют регуляторную функцию и являются гормонами, например окситоцин, вырабатываемый гипоталамусом, резервируется гипофизом. Поступая из него в кровь, окситоцин воздействует на мышечные стенки матки, вызывая её сокращение. Белок вазопрессин также выполняет регуляторную функцию, контролируя кровяное давление.

В мышечных клетках находятся актин и миозин, способные сокращаться, что обуславливает двигательную функцию мышечной ткани. Для белков характерна и трофическая функция, например, альбумин используется зародышем в качестве питательного вещества для своего развития. Белки крови различных организмов, например гемоглобин и гемоцианин, переносят молекулы кислорода – выполняют транспортную функцию. Если более энергоёмкие вещества, такие как углеводы и липиды, полностью использованы, клетка приступает к расщеплению белков. Один грамм этого вещества даёт 17, 2 кДж энергии. Одной из важнейших функций белков является каталитическая (белки-ферменты ускоряют химические реакции, протекающие в компартментах цитоплазмы). На основании вышесказанного мы убедились в том, что белки выполняют множество очень важных функций и обязательно входят в состав животной клетки.
Биосинтез белка
Рассмотрим процесс синтеза белка в клетке, который происходит в цитоплазме с помощью таких органелл, как рибосомы. Благодаря деятельности специальных ферментов, при участии ионов кальция рибосомы объединяются в полисомы. Основные функции рибосом в клетке – синтез белковых молекул, начинающийся процессом транскрипции. В результате него синтезируются молекулы иРНК, к которым и присоединяются полисомы. Затем начинается второй процесс – трансляция. Транспортные РНК соединяются с двадцатью различными видами аминокислот и приносят их к полисомам, а так как функции рибосом в клетке — это синтез полипептидов, то эти органеллы образуют комплексы с тРНК, а молекулы аминокислот связываются между собой пептидными связями, образуя макромолекулу белка.
Роль воды в процессах метаболизма
Цитологические исследования подтвердили тот факт, что клетка, строение и состав которой мы изучаем, в среднем на 70% состоит из воды, а у многих животных, ведущих водный способ жизни (например, кишечнополостных) её содержание достигает 97—98%. С учётом этого химическая организация клеток включает в себя гидрофильные (способные к растворению) и гидрофобные (водоотталкивающие) вещества. Являясь универсальным полярным растворителем, вода играет исключительную роль и напрямую влияет не только на функции, но и на само строение клетки. Таблица, представленная ниже, показывает содержание воды в клетках различных типов живых организмов.

Функция углеводов в клетке
Как мы выяснили ранее, к важным органическим веществам – полимерам - относятся также углеводы. К ним относятся полисахариды, олигосахариды и моносахариды. Углеводы входят в состав более сложных комплексов – гликолипидов и гликопротеидов, из которых построены клеточные мембраны и надмембранные структуры, например гликокаликс.
Кроме углерода, в состав углеводов входят атомы оксигена и гидрогена, а некоторые полисахариды содержат ещё азот, серу и фосфор. В клетках растений углеводов много: клубни картофеля содержат до 90% крахмала, в семенах и плодах содержание углеводов до 70%, а в животных клетках они встречаются в виде таких соединений, как гликоген, хитин и трегалоза.
Простые сахара (моносахариды) имеют общую формулу Cnh3nOn и делятся на тетрозы, триозы, пентозы и гексозы. Две последние наиболее распространены в клетках живых организмов, например, рибоза и дезоксирибоза входят в состав нуклеиновых кислот, а глюкоза и фруктоза принимают участие в реакциях ассимиляции и диссимиляции. Олигосахариды часто встречаются в растительных клетках: сахароза запасается в клетках сахарной свёклы и сахарного тростника, мальтоза содержится в проросших зерновках ржи и ячменя.

Дисахариды имеют сладковатый вкус и хорошо растворяются в воде. Полисахариды, являясь биополимерами, представлены в основном крахмалом, целлюлозой, гликогеном и ламинарином. К структурным формам полисахаридов относится хитин. Основная функция углеводов в клетке — энергетическая. В результате гидролиза и реакций энергетического обмена полисахариды расщепляются до глюкозы, а она затем окисляется до углекислого газа и воды. В результате один грамм глюкозы освобождает 17,6 кДж энергии, а запасы крахмала и гликогена, по сути, являются резервуаром клеточной энергии.
Гликоген откладывается в основном в мышечной ткани и клетках печени, растительный крахмал – в клубнях, луковицах, корнеплодах, семенах, а у членистоногих, например пауков, насекомых и ракообразных, главную роль в энергообеспечении играет олигосахарид трегалоза.
Углеводы отличаются от липидов и белков способностью к бескислородному расщеплению. Это чрезвычайно важно для организмов, живущих в условиях дефицита или отсутствия кислорода, например для анаэробных бактерий и гельминтов – паразитов человека и животных.
Есть ещё одна функция углеводов в клетке – строительная (структурная). Она заключается в том, что эти вещества являются опорными структурами клеток. Например, целлюлоза входит в состав клеточных стенок растений, хитин образует внешний скелет многих беспозвоночных и встречается в клетках грибов, олисахариды вместе с молекулами липидов и белков образуют гликокаликс – надмембранный комплекс. Он обеспечивает адгезию – слипание животных клеток между собой, приводящее к образованию тканей.
Липиды: строение и функции
Эти органические вещества, являющиеся гидрофобными (нерастворимыми в воде) можно извлечь, то есть экстрагировать из клеток с помощью неполярных растворителей, таких как ацетон или хлороформ. Функции липидов в клетке зависят от того, к какой из трёх групп они относятся: к жирам, воскам или стероидам. Жиры наиболее широко распространены во всех типах клеток.
Животные накапливают их в подкожной жировой клетчатке, нервная ткань содержит жир в виде миелиновых оболочек нервов. Он также накапливается в почках, печени, у насекомых – в жировом теле. Жидкие жиры – масла - встречаются в семенах многих растений: кедра, арахиса, подсолнечника, маслины. Содержание липидов в клетках колеблется от 5 до 90% (в жировой ткани).

Стероиды и воски отличаются от жиров тем, что они не имеют в составе молекул остатков жирных кислот. Так, стероиды – это гормоны коркового слоя надпочечников, влияющие на половое созревание организма и являющиеся компонентами тестостерона. Они также входят в состав витаминов (например, витамина Д).
Основные функции липидов в клетке – это энергетическая, строительная и защитная. Первая обусловлена тем, что 1 грамм жира при расщеплении даёт 38,9 кДж энергии – намного больше чем другие органические вещества – белки и углеводы. Кроме того, при окислении 1г жира выделяется почти 1,1 гр. воды. Именно поэтому некоторые животные имея запас жира в своем теле, могут долгое время находиться без воды. Например, суслики могут быть в спячке более двух месяцев, не нуждаясь в воде, а верблюд не пьёт воду при переходах через пустыню в течение 10–12 суток.
Строительная функция липидов заключается в том, что они являются неотъемлемой частью клеточных мембран, а также входят в состав нервов. Защитная функция липидов состоит в том, что слой жира под кожей вокруг почек и других внутренних органов защищает их от механических травм. Специфическая теплоизоляционная функция присуща животным, длительное время находящимся в воде: китам, тюленям, морским котикам. Толстый подкожный жировой слой, например, у синего кита составляет 0,5 м, он защищает животное от переохлаждения.
Значение кислорода в клеточном метаболизме
Аэробные организмы, к которым относится подавляющее большинство животных, растения и человек, используют атмосферный кислород для реакций энергетического обмена, приводящих к расщеплению органических веществ и выделению определённого количества энергии, аккумулируемого в виде молекул аденозинтрифосфорной кислоты.
Так, при полном окислении одного моля глюкозы, происходящего на кристах митохондрий, выделяется 2800 кДж энергии, из которых 1596 кДж (55%) запасается в виде молекул АТФ, содержащих макроэргические связи. Таким образом, основная функция кислорода в клетке – осуществление аэробного дыхания, в основе которого лежит группа ферментативных реакций так называемой дыхательной цепи, происходящих в клеточных органеллах – митохондриях. У прокариотических организмов - фототрофных бактерий и цианобактерий - окисление питательных веществ происходит под действием кислорода, диффундирующего в клетки на внутренние выросты плазматических мембран.
Нами была изучена химическая организация клеток, а также рассмотрены процессы биосинтеза белка и функция кислорода в клеточном энергетическом обмене.
fb.ru
| # | Name | ID | URL | Short URL |
| Introduction to methods of resolving the biomolecule structure | ||||
| 1 | Synthetic protein | 1vye | open | |
| 2 | Synthetic protein | 1rik | open | |
| 3 | Myoglobin (X-Ray) | 1a6m | open | |
| 4 | Myoglobin (NMR) | 1myf | open | |
| Electron-transfer reactions in mitochondria | ||||
| 5 | Respiratory complex I | 4hea | open | |
| 6 | Respiratory complex II | 1nek | open | |
| 7 | Respiratory complex III | 1bgy | open | |
| 8 | Respiratory complex IV | 1qle | open | |
| 9 | Cytochrome c | 3cyt | open | |
| 10 | Procaryotic ribosome large subunit | 1ffk | open | |
| Molecular Structure of Plant Photosystems | ||||
| 11 | Photosystem II | 1s5l | open | goo.gl/mIjPy |
| 12 | Light-harvesting complex II | 2bhw | open | goo.gl/s2f5d |
| 13 | Phycobiliprotein | 2bv8 | open | goo.gl/YgmsM |
| 14 | Cytochrome b6/f | 1um3 | open | goo.gl/b3krl |
| 15 | Plastocyanin | 2pcf | open | goo.gl/91PTW |
| 16 | Photosystem I | 1jb0 | open | goo.gl/YWXf2 |
| 17 | Ferredoxin | 1a70 | open | goo.gl/ucHTe |
| 18 | ATP Synthase F0 subunit | 1c17 | open | |
| 19 | ATP Synthase F1 subunit | 1e79 | open | |
| 20 | Bacterial photosystem of the purple bacteria | 1prc | open | goo.gl/KJd2Y |
| 21 | Ferredoxin | 1a70 | open | goo.gl/ucHTe |
| 22 | Photosystem II | 1s5l | open | goo.gl/mIjPy |
| Structure of Plant Receptor Molecules | ||||
| 23 | Phytochrome B | 1jnu | open | goo.gl/LbiVm |
| 24 | Cryptochrome | 1u3d | open | goo.gl/hEQgU |
| 25 | TIR1 – Nuclear auxin receptor | 2p1q | open | goo.gl/V3a3b |
| 26 | ABP1 – Cytoplasmic auxin receptor | 1lrh | open | goo.gl/z3l4A |
| 27 | AHK4 – Cytokinin receptor | 3t4l | open | goo.gl/PK1Mf |
| 28 | GID1 – Gibberellin receptor | 2zsh | open | goo.gl/sUwqA |
| 29 | BRI1 – Brassinosteroid receptor | 3rj0 | open | goo.gl/vERQ6 |
| 30 | Jasmonate receptor | 3ogl | open | goo.gl/E3MoT |
| 31 | PYR1 – Abscisic acid receptor | 3k90 | open | goo.gl/7ApA6 |
| 32 | Calmodulin | 1cll | open | goo.gl/9ObY4 |
| 33 | Calmodulin in complex with CDPK | 1cm1 | open | |
| 34 | Homeodomain in complex with DNA | 1b8i | open | goo.gl/Qlhwu |
| 35 | Leucine zipper protein in complex with DNA | 1nwq | open | goo.gl/jgA28 |
| 36 | bHLH-motif domain in complex with DNA | 1a0a | open | goo.gl/ZlFLV |
| 37 | Zinc-finger TATA-motif in complex with DNA | 1g2d | open | goo.gl/5G0G8 |
| Структура нуклеиновых кислот | ||||
| 38 | A-form of DNA | molbio_dnaaform | open | |
| 39 | B-form of DNA | molbio_dnabform | open | |
| 40 | Z-form of DNA | molbio_dnazform | open | |
| 41 | Hydrogen bonds in B-form of DNA | molbio_dnahbonds | open | |
| 42 | H-form of DNA | molbio_dnahform | open | |
| 43 | Переход B-формы ДНК в ДНК Z-формы | molbio_dnaz2b | open | |
| 44 | Topoisomerase I | molbio_top1 | open | |
| 45 | Topoisomerase IIa | molbio_top2 | open | |
| 46 | Topoisomerase IV | molbio_gyrase | open | |
| 47 | Gyrase B | molbio_gyraseb | open | |
| 48 | EcoRI | molbio_ecori | open | |
| 49 | Cas9 | molbio_cas9 | open | |
| Организация бактериальных и эукариотических геномов | ||||
| Молекулярные механизмы копирования полинуклеотидов | ||||
| Процессинг первичных РНК-транскриптов | ||||
| Трансляция - рибосомальный синтез белка | ||||
| 50 | Aminoacyl-tRNA synthetase type I | 1qrs | open | |
| 51 | Aminoacyl-tRNA synthetase type II | 1asz | open | |
| 52 | Structure of the 30S procaryotic ribosomal subunit | 1j5e | open | |
| 53 | Structure of the 50S procaryotic ribosomal subunit | 1q7y | open | |
| 54 | Structure of the 50S procaryotic ribosomal subunit | 1jgo | open | |
| 55 | Распознавание последовательности SD в 70S рибосоме | 4v4j | open | |
| 56 | Распознавание последовательности SD в 70S рибосоме | 4v5g | open | |
| 57 | Факторы инициации IF-1, IF-2 и тРНК | 1zo1 | open | |
| 58 | Комплекс EF-Tu с тРНК и ГТФ | 1b23 | open | |
| 59 | Фактор терминации RF-1 | 1zbt | open | |
| 60 | Фактор терминации RF-2 | 1gqe | open | |
| 61 | Фактор терминации RRF | 1ek8 | open | |
| 62 | Шаперонин GroEL/GroES | 1aon | open | |
| 01 – Introduction | ||||
| 63 | 2 nucleosomes of Xenopus laevis | lnmo_1zbb | open | |
| 64 | Nucleosome of Xenopus laevis | lnmo_1aoi | open | |
| 65 | Synthetic protein | lnmo_1vye | open | |
| 66 | α-helix / ferritin-like protein | lnmo_1bcf | open | |
| 67 | Гомеодомен-подобный белок | lnmo_1enh | open | |
| 68 | Immunoglobulin-like β-sandwich | lnmo_1cd8 | open | |
| 69 | Four-bladed β-propeller | lnmo_1pex | open | |
| 70 | Single-stranded left-handed β helix | lnmo_1lxa | open | |
| 71 | β-prism II | lnmo_1jpc | open | |
| 72 | α/β structure | lnmo_1pfk | open | |
| 73 | α+β structure | lnmo_2pil | open | |
| 74 | α+β structure, GFP-like | lnmo_1ema | open | |
| 02 – Nucleic acids | ||||
| 75 | Cytidine | lnmo_cytidine | open | |
| 76 | Hydrogen bonds in B-form of DNA | lnmo_dnahbonds | open | |
| 77 | A-form of DNA | lnmo_dnaaform | open | |
| 78 | B-form of DNA | lnmo_dnabform | open | |
| 79 | Z-form of DNA | lnmo_dnazform | open | |
| 80 | H-form of DNA | lnmo_dnahform | open | |
| 81 | DNA quadruplex structure | lnmo_dnaqform | open | |
| 82 | RNA hairpin | lnmo_1ylg | open | |
| 83 | TT dimer | lnmo_1ttd | open | |
| 84 | TT dimer reparation by photolyase | lnmo_1tez | open | |
| 85 | tRNA | lnmo_1tra | open | |
| 86 | TATA-box binding protein | lnmo_1tgh | open | |
| 87 | Enhanceosome component | lnmo_1t2k | open | |
| 88 | Homeodomain in complex with DNA | lnmo_1b8i | open | goo.gl/Qlhwu |
| 89 | Leucine zipper protein in complex with DNA | lnmo_1nwq | open | goo.gl/jgA28 |
| 90 | bHLH-motif domain in complex with DNA | lnmo_1a0a | open | goo.gl/ZlFLV |
| 91 | Zinc-finger TATA-motif in complex with DNA | lnmo_1g2d | open | |
| 92 | EcoRI-DNA post-reactive complex | lnmo_1qps | open | |
| 03 – Storage and transport proteins I | ||||
| 93 | Myoglobin (X-Ray) | lnmo_1a6m | open | |
| 94 | Hemoglobin | lnmo_1hho | open | |
| 95 | Erythrocruorin | lnmo_2gtl | open | |
| 96 | Ferritin | lnmo_3is7 | open | |
| 97 | Transferrin | lnmo_1h76 | open | |
| 98 | Siderophore | lnmo_4k19 | open | |
| 99 | Lipid storage protein lipovitellin | lnmo_1lsh | open | |
| 04 – Biological membranes and transport proteins II | ||||
| 100 | Cholesterol | lnmo_cholesterol | open | |
| 101 | Lipid micelle | lnmo_m65 | open | |
| 102 | Crystalline structure lipid bilayer | lnmo_popc-crystal | open | |
| 103 | Gel structure lipid bilayer | lnmo_popc-gel | open | |
| 104 | Fluid structure lipid bilayer | lnmo_popc-fluid | open | |
| 105 | Bacteriorhodopsin embedded into lipid bilayer | lnmo_popc-br | open | |
| 106 | FepA membrane protein | lnmo_1fep | open | |
| 107 | FauA membrane receptor for siderophore | lnmo_3efm | open | |
| 108 | Maltoporin | lnmo_1mal | open | |
| 109 | α-Hemolysin | lnmo_7ahl | open | |
| 110 | Calcium ATPase | lnmo_1su4 | open | |
| 111 | Aquaporin | lnmo_2abm | open | |
| 112 | Sodium-potassium channel | lnmo_2zxe | open | |
| 05 – Biological signaling | ||||
| 113 | Acetylcholine receptor | lnmo_2bg9 | open | |
| 114 | Acetylcholine binding protein | lnmo_1uv6 | open | |
| 115 | Acetylcholine binding protein in complex with α-cobratoxin | lnmo_1yi5 | open | |
| 116 | Insulin | lnmo_4ins | open | |
| 117 | Insulin receptor | lnmo_2dtg | open | |
| 118 | Insulin receptor domain in complex with insulin | lnmo_3w14 | open | |
| 119 | Insulin receptor transmembrane domain | lnmo_2mfr | open | |
| 120 | Insulin receptor tyrosine kinase domain | lnmo_1irk | open | |
| 121 | Insulin receptor tyrosine kinase domain | lnmo_1ir3 | open | |
| 122 | G-Protein | lnmo_1gg2 | open | |
| 123 | Calmodulin | lnmo_1cll | open | |
| 124 | Calmodulin in complex with CDPK | lnmo_1cm1 | open | |
| 06 – Hormone reception | ||||
| 125 | Adrenergic receptor | lnmo_2rh2 | open | |
| 126 | Rhodopsin | lnmo_1f88 | open | |
| 127 | TIR1 – Nuclear auxin receptor | lnmo_2p1q | open | goo.gl/V3a3b |
| 128 | Estrogene receptor (ligand-binding domain) | lnmo_1a52 | open | |
| 129 | Estrogene receptor (DNA-binding domain) | lnmo_1hcq | open | |
| 130 | BRI1 – Brassinosteroid receptor | lnmo_3rj0 | open | goo.gl/vERQ6 |
| 07 – Drug action | ||||
| 131 | Estrogene receptor binded to tamoxifen | lnmo_3ert | open | |
| 132 | Serotonin receptor binded to ergotamine | lnmo_4iar | open | |
| 133 | MDR-transporter | lnmo_2onj | open | |
| 08 – Structural proteins | ||||
| 134 | Actin | lnmo_1atn | open | |
| 135 | Actin and gelsolin complex | lnmo_1yvn | open | |
| 136 | Actin and profilin complex | lnmo_1hlu | open | |
| 137 | Actin in complex with myosin | lnmo_1alm | open | |
| 138 | Cadherin | lnmo_1l3w | open | |
| 139 | Collagen | lnmo_1bkv | open | |
| 140 | Бактериальный микрокомпартмент | lnmo_2zv5 | open | |
| 141 | GroES/GroEL shaperonine | lnmo_1aon | open | |
| 09 – Photosynthesis | ||||
| 142 | Photosystem II | lnmo_1s5l | open | goo.gl/mIjPy |
| 143 | Light-harvesting complex II | lnmo_2bhw | open | goo.gl/s2f5d |
| 144 | Phycobiliprotein | lnmo_2bv8 | open | goo.gl/YgmsM |
| 145 | Cytochrome b6/f | lnmo_1um3 | open | goo.gl/b3krl |
| 146 | Plastocyanin | lnmo_2pcf | open | goo.gl/91PTW |
| 147 | Photosystem I | lnmo_1jb0 | open | goo.gl/YWXf2 |
| 10 – Molecular machines | ||||
| 148 | ATP Synthase F0 subunit | lnmo_1c17 | open | |
| 149 | ATP Synthase F1 subunit | lnmo_1e79 | open | |
| 150 | 26S Proteasome | lnmo_4cr2 | open | |
pozhvanov.com
Растения воюют друг с другом молекулярно-генетическим оружием
Некоторые травы подавляют рост растений-конкурентов, стимулируя в них генетическую активность.
Территориальное поведение ассоциируется у нас только с животными. Например, с кошками: сразу представляешь себе двух котов, вставших в театральные позы и истошно орущих друг на друга – один, значит, чужак, и зашёл на не свою территорию. То же самое можно увидеть у множества других видов, у птиц и зверей, рыб и амфибий, рептилий и насекомых. Но многие наверняка бы удивились, если бы им сказали, что и растения могут защищать то место, где они растут, от нежелательных соседей. Биологам же это давно известно: деревья, травы и кусты, конечно, не дерутся ветвями и не бегают по участку, однако у них есть химические способы воздействия на конкурентов – разнообразные вещества, которые вредят нежданному гостю.
Глядя на зелёный луг, мы и не подозреваем, какая борьба разворачивается между растениями под землёй. (Фото Jay Dickman / CORBIS.)‹
›
Свойство одних организмов выделять химические соединения, которые тормозят или подавляют развитие других, называют аллелопатией. Хотя она известна не только у растений, но и у микроорганизмов, у грибов, у животных, механизм её во многих случаях остаётся загадочной. Сейчас уже известны много различных молекул, которые растения выделяют в почву через корни; здесь они разрушаются или видоизменяются бактериями, продукты бактериальной химической работы всасываются корневой системой конкурента, после чего у того, к примеру, останавливается рост.
Исследователи из Тюбингенского университета и Института биологии развития Общества Макса Планка решили выяснить, как действуют циклические гидроксамовые кислоты, выделяемые некоторыми видами трав – продукты деградации этих кислот известны своей фитотоксичностью. Оказалось, что они подавляют работу гистоновых деацетилаз, специальных ферментов, которые управляют активностью множества разных генов. Известно, что ДНК в клеточном ядре находится в комплексе с упаковочными белками – гистонами, и активность того или иного участка ДНК, активность записанных в нём генов будет зависеть от того, насколько плотно он связан с гистонами (если упаковка слабая, то с ДНК смогут работать молекулярные машины, занимающиеся синтезом матричной РНК для белкового синтеза). Плотность ДНК-гистоновой упаковки зависит от модификаций самих гистонов, и здесь становится понятно, как другие ферменты, ацетилазы и деацетилазы, влияют на работу генов: присоединяя ацетильную группу к гистонам, ацетилазы делают упаковку ДНК более рыхлой – гены активируются; деацетилазы, напротив, делают упаковку более плотной – и гены отключаются.

Теперь вспомним про циклические гидроксамовые кислоты, точнее, про продукты их превращения в почве. Попав в клетки чужого растения, они подавляют работу деацетилаз – соответственно, активность генов резко возрастает. Именно поэтому, как пишут авторы работы в статье в The Plant Cell, у конкурента начинаются проблемы с ростом. Происходит так, очевидно, потому, что гены активируются без разбора, баланс между ними нарушается, и из-за беспорядка на генетической «кухне» растению становится плохо. Правда, остаётся вопрос, почему растения-хозяева не страдают от собственного химического (или лучше сказать, молекулярно-биологического) оружия.
Пока что это первый случай, когда удалось достаточно полно раскрыть молекулярный механизм растительной аллелопатии, хотя, надо думать, прогресс здесь не заставит себя долго ждать: во-первых, на основе таких веществ можно создать более-менее избирательные гербициды, останавливающие рост сорняков и вредных инвазивных видов, а во-вторых, им можно было бы найти применение в медицине – воздействуя на структуру ДНК-белковых комплексов, подобные молекулы могли бы подавлять рост опухолей. И это не такая уж фантазия – с одной стороны, гистоновые деацетилазы и так уже используются в качестве противораковых препаратов, а с другой стороны, по словам самих исследователей, в их экспериментах производные гидроксамовых кислот действительно подавляли рост человеческих раковых клеток.
www.nkj.ru










