Волонтер фотосинтеза. Пигменты и ферменты фотосинтеза у растений находятся в
РОЛЬ ПИГМЕНТОВ В ПРОЦЕССЕ ФОТОСИНТЕЗА
Хлорофилл (разд. 25.1)-пигмент, содержащийся в листьях растений, который играет главную роль в превращении солнечной энергии в химическую в процессе фотосинтеза. [c.466]Вся жизнь на земле в конечном счете зависит от синтеза углеводов за счет усвоения углекислоты из атмосферы. Солнечный свет обеспечивает энергией этот процесс, в целом известный под названием фотосинтеза. Первой стадией фотосинтеза является поглощение фотона пигментами в многоклеточных растениях наиболее важную роль играет хлорофилл-а. Энергия фотона трансформируется в химическую энергию, обеспечивающую протекание реакции СО2—и образование углерод-углеродных связей эта реакция представляет собой восстановительное карбоксилирование, со- [c.216]
У хиноновых пигментов нет какой-либо одной общей функции. Они не играют важной роли в качестве пигментов в фотосинтезе или фоторецепторов в других процессах. Они [c.118]Органоиды - зто протоплазматические тельца разного размера ядро, пластиды, митохондрии. Ядро содержит нуклеиновые кислоты (ДНК и РНК) оно является центром процессов синтеза, регулирует жизненные функции и служит носителем наследственных свойств клетки благодаря содержащимся в нем хромосомам. Для растений характерно наличие пластид, которые вьшолняют функции, связанные с фотосинтезом, и классифицируются в зависимости от наличия пигментов (см. 8.5.3 и 11.10). Более мелкие тельца митохондрии играют важную роль в дыхательной активности, запасают и передают энергию. В органоидах клетки образуются ферменты - биокатализаторы синтеза органических веществ - и Другие белки возникают в результате клеточного дыхания богатые энергией соединения синтезируются полисахариды и т.д. [c.195]
Для поглощения энергии солнечного света, обеспечивающего процесс фотосинтеза, в живой клетке должен быть специальный аппарат, аккумулирующий световые кванты. Наиболее важную роль играют пигменты. Поэтому далее будут рассмотрены различные пигменты, участвующие в фотосинтезе. [c.184]
Во втором томе с большой полнотой сведен материал по трем основным группам вопросов 1) спектроскопия и флуоресценция фотосинтетических пигментов 2) кинетика процесса фотосинтеза в зависимости от концентрации двуокиси углерода, интенсивности и спектрального состава света и 3) квантовые выходы фотосинтеза и возможная роль в процессе фотосинтеза различных других пигментов, помимо хлорофилла. [c.5]
Процессы фотосинтеза весьма детально изучаются в течение ряда лет, однако они еще ни в коей мере не могут считаться окончательно выясненными. В особенности спорной является первая стадия фотосинтеза— образование восстанавливающего первичного продукта под действием света. Мы знаем, что для этого необходимы зеленые красители листьев — хлорофилл а и Ь в некоторых ассимилирующих бактериях соответствующую роль играет бактериальный. хлорофилл . Возможно, что для процессов ассимиляции необходимы также другие пигменты так, неоднократно высказывалось мнение, что в процессах ассимиляции принимает участие р-каротин. [c.983]
Пиррольные кольца лежат также в основе строения хлорофилла— зеленого пигмента растений, играющего важную роль в процессах фотосинтеза различных веществ в растениях [c.222]
Детали синтеза углеводов и механизмов фотофосфорилирования лежат за пределами настояш,ей книги. Однако мы остановимся здесь на роли в этих процессах пигментов, поскольку они имеют фундаментальное значение в улавливании и утилизации энергии света. Светособирающая роль хлорофилла в фотосинтезе— вероятно, наиболее яркий пример специфических биологических фотофункций природного пигмента. Функционирование каротиноидов и фикобилинов в качестве вспомогательных пигментов также прямо связано с их светопоглощающими свойствами. Другие окрашенные молекулы, в том числе цитохромы и флавопротеины, участвуют в фотосинтезе как часть электронтранспортных систем способность этих соединений поглощать видимый свет не имеет отношения к их функционированию. Ниже будут освещены вопросы о том, как поглощающие свет пигменты расположены в фотосинтетическом аппара- [c.328]
Хлорофилл принадлежит к группе жирорастворимых пигментов, он растворяется в жирах и органических растворителях. Хлорофилл, как показали работы К. А. Тимирязева и его последователей, играет огромную роль в процессе ассимиляции углекислого газа. Процесс фотосинтеза представляет собой окислительно-восстановительное взаимодействие углекислого газа и воды, идущее в присутствии хлорофилла, который поглощает энергию солнечных лучей. Фотосинтез в настоящее время является главным источником образования органических веществ на Земле. [c.61]
Само это сходство между спектром поглощения хлорофилла и спектром действия фотосинтеза является одним из лучших доказательств того, что роль главного рецепторного пигмента в фотосинтезе играет именно хлорофилл. Отдельные особенности спектра действия фотосинтеза указывают, что в поглощении света при этом процессе участвуют также и желтые пигменты — каротиноиды, которые наряду с хлорофиллом в большом количестве содержатся в хлоропластах. В отсутствие хлорофилла каротиноиды неспособны осуществлять фотосинтез, поэтому принято считать, что активированные светом каротиноиды передают поглощенную ими энергию хлорофиллу, который в конечном счете и выполняет собственно фото-синтетическую работу. [c.115]
Огромную роль в процессе фотосинтеза играет маг-нимсодержащий растительный пигмент хлорофилл, образующий комплексные соединения с белками и липидами хлор он ластов. Хлорофилл весьма близок по строению к гему. Показано, что и пути образования этих соединений принципиально одинаковы. [c.44]
Можно сравнительно просто определить, какую природу — химическую (т. е. обусловленную пигментом) или физическую (обусловленную структурой) — имеет данный цветовой эффект. Идентификация и характеристика пигмента обычно является стандартной задачей в органической химии. В последующих главах первой части этой книги приведены основные химические свойства наиболее крупных групп природных пигментов. Гораздо более сложной является проблема взаимодействия молекул пигмента с их ближайшим микроокружением, напри-ме с белками в мембранах. Применение сложных современных физико-химических методов, таких, как резонансная рамановская спектроскопия, линейный и круговой дихроизм и ядерный магнитный резонанс, позволяет решить эту проблему, а также получить информацию о молекулярных изменениях, которые претерпевают некоторые пигменты при их функционировании. Вторая часть этой книги представляет собой обзор функций природных пигментов как в роли окрашивающих агентов, так и в роли участников гораздо более сложных процессов, таких, как фотосинтез, зрение и другие фотореакции, которые могут протекать за время порядка пикосекунд. [c.30]
Роль каротиноидов в процессах фотосинтеза. Каротиноиды — обязательные компоненты пигментных систем всех фотосинтезирующих организмов. Они выполняют ряд функций, главные из которых 1) участие в поглощении света в качестве дополнительных пигментов, 2) защита молекул хлорофиллов от необратимого фотоокисления. Возможно, каротиноиды принимают участие в кислородном обмене при фотосинтезе. [c.77]
Хлорофилл, как известно, принимает непосредственное химическое участие в процессе фотосинтеза, являясь одним из звеньев "в цепи окислительно-восстановительных реакций, приводящих к отнятию водорода от воды и присоединению его к СО2. Роль бактериохлорофилла у фотосинтезирующих бактерий, очевидно, такая же, как хлорофилла а У растений. Эти пигменты в растворе способны также сенсибилизировать реакпию фотохимического переноса водорода, как и хлорофилл (Красновский, Войновская,1951 Красновский, Пакшна, 1959). [c.147]
Многие природные пигменты принимают участие в важных метаболических или физиологических процессах. Особенно детально изучено функционирование хлорофилла и других пигментов в фотосинтезе и роль гемоглобина как переносчика кислорода. Во многих случаях, однако, единственной известной функцией пигмента является то, что он придает окраску организму или той его части, которая содержит данный пигмент. [c.29]
Исследования в группе тропана были начаты Под влиянием Альфреда Айнгорна (1857—1917), который открыл новокаин и которому Вильштеттер посвятил докторскую диссертацию эти исследования привели к синтезу кокаина. Работы по изучению ассимиляции угольного ангидрида (в сотрудничестве со Штолем), выполненные С учетом новых взгйядов, выяснили роль хлорофилла в процессе фотосинтеза. Эти работы были собраны Вильштеттером в однотомнике Исследования по ассимиляции угольной кислоты (1918). Исследования хлорофилла, начатые в 1906 г., кроме выделения зеленого пигмента, привели Вильштеттера к установлению химического строения хлорофиллов а ж Ь> [c.370]
Пигменты зеленых частей растений, содержащиеся в хлоропластах наряду с каротино-идами (в соотношении 3 1),-сине-зеленый хлорофилл а (XVI R = = Hj) и желто-зеленый хлорофилл 6 (XVI R = СНО), играющие важную роль в процессах фотосинтеза (см. Хлорофиллы). Кроме [c.491]
Микрофиты — водоросли, играющие огромную роль при формировании фитопланктона и фитобентоса. В составе этих организмов имеется хлорофилл, поэтому на сьету они осуществляют фотосинтез. Их подразделяют па зеленые, синезеленые, диатомовые, эвгленовые и др. Зеленые водоросли,, имеющие ярко-зеленую окраску, развиваются обычно в начале лета спне-зеленые, содержащие кроме хлорофилла еще и растворимый в воде синий пигмент — фикоциан,— преимущественно во второй половине лета диатомовые, также содержащие наряду с хлорофиллом растворимый в воде буры пигмент — диатомин,— ранней весной и поздней осенью. Синезеленые водоросли являются единственными организмами, потребляющими три растворенных в воде газа — азот (включая аммиак), углекислоту и кислород при фотосинтезе они, как и все другие водоросли, выделяют в окружающук> среду кислород. Фотосинтез протекает при наличии света, углекислоты, благоприятной температуры, органических и неорганических соединений,, необходимых для обмена веществ клеток водорослей. При развитии водной флоры основными биогенными элементами, необходимыми для процессов жизнедеятельности, являются углерод, азот, фосфор, калий, кальций, железо, марганец, медь, кремний и некоторые микроэлементы. [c.189]
Пигменты хлоропластов. В процессе фотосинтеза происходит поглощение света пигментами, сосредоточенными в хлоропластах. Пигменты зеленых растений играют важную роль в превращении лучистой энергии света в химическую. У авто-трофных растений уменьшение количества пигментов приводит [c.157]
Фотосинтезирующие растения содержат кроме хлорофиллов так называемые дополнительные, вспомогательные, или сопрововдающие пигменты. К ним относятся гсаротиноиды и содержащиеся у некоторых групп водорослей фикобилины. Вопрос о том какова роль этих пигментов в процессе фотосинтеза, участвует ли поглощаемая ими световая энергия в построении органического вещества долгое время оставался неясным. В последние годы изучению роли этих пигментов уделено оольшое внимание и появилось много нового в выяснении их роли в процессе фотосинтеза. [c.136]
Согласно современным представлениям о процессе фотосинтеза, большинство молекул пигментов фотосинтетического аппарата выполняют лишь обслуживающую роль акцепторов квантов света, передающих поглощенную энергию на реакционные центры, в которых происходят фотохимические реакции, связанные с восстановлением углекислого газа (рис. 30). [c.183]
ХЛОРОФИЛЛ. Зеленый пигмент растений, придающий им зеленую окраску. X. играет в жизнедеятельности растений исключительно важную роль. Находясь в листьях, он поглощает энергию солнечного света и направляет ее на процесс первичного синтеза из углекислого газа и воды сложных и богатых энергией органических веществ и прежде всего таких, как углеводы, аминокислоты, белки. Этот процесс называется фотосинтезом. Главнейшие реакции фотосинтеза протекают во внутриклеточных образованиях — хлоропластах, в которых и сосредоточен X. наряду с желтыми пигментами — каротиноидами. В хлоропластах молекулы X. и каротиноидов являются участниками сложных структур. Так, хло-ропласты содержат чередующиеся слои белковых и жироподобных веществ, с которыми в определенном порядке сочетаются слои пигментов. Периодически слои оказываются более плот- [c.347]
В конечном итоге все жизненные процессы на земле связаны с процессом включения атмосферного диоксида углерода в углеводы. Этот процесс, называемый фотосинтезом, требует больших энергетических затрат и источником энергии для него служит солнечный свет. На первой стадии этого сложного процесса проиходит поглощение фотона пигментами, причем в многоклеточных растениях ключевую роль на этой стадии играет хлорофилл-л. Энергия фотонов впоследствии превращается в химическую энергию, которая использу- [c.309]
Первоначальные исследования в области химии пиррола были связаны с дефадацией двух важных пигментов гема — пигмента крови, обеспечивающего процесс дыхания, и хлорофилла — зеленого пигмента растений, ответственного за процесс фотосинтеза [2] Разложение этих пигментов привело к получению смеси алкилпирролов. Хлорофилл и гем синтезируются в живой клетке из порфобилиногена, причем только ароматические пирролы играют черезвычайно важную роль в основном метаболизме [3,4]. [c.309]
Молекулы с неспаренными электронами обычно отличаются высокой реакционной способностью. Они играют очень важную роль во многих химических и биологических процессах обычно как короткоживущие промежуточные соединения. Например, сигнал ЭПР наблюдается при облучении фотосинтезирующих систем. Он возникает как следствие первоначального акта фотосинтеза — переноса электрона, инициированного поглощением света фотосинтезирующим пигментом. Изучение этого явления сыграло важную роль в понимании механизма фотосинтеза. Органические радикалы и ион-радикалы дают очень характеристичные спектры ЭПР, что позволяет легко их обнаруживать и идентифицировать. Кроме того, наблюдаемые в спектре расщепления дают сведения о распределении спиновой плотности в молекуле. [c.234]
Процесс фотосинтеза чрезвычайно важен для жизни на нашей планете, поскольку он осуществляет утилизацию имеющейся в изобилии солнечной энергии в химически доступную форму путем фиксации СОг с образованием углеводов. Пигменты, и в первую очередь хлорофилл, играют главную роль в фотосинтезе, и поэтому данный процесс еще долго будет оставать- [c.365]
Помимо хлорофилла, в процессах фотосинтеза участвуют пигменты группы каротиноидов, в состав которых входят только водород п углерод, и ксантофиллы, имеющие в составе молекул еще и кислород. Пигме1 ты встречаются в тилакоидных мембранах всех фотоавтотрофных организмов. Каротиноиды играют роль антенных пигментов, чувствительных к солнечному свету в диапазоне волн, недоступном для хлорофилла. Они передают энергию солнечного света в центры реакций и, кроме того, как светофильтры экранируют хлорофилл в листьях, предохраняя его от фотодеструкции, фотоокисления. Этот защитный эффект связывают с наличием конъюгированных двойных связей (их может быть 9 или более), способных гасить возбужденное состояние молекул хлорофилла. Каротиноиды могут выводить кислород из находящегося в возбужденном состоянии комплекса хлорофилл — кислород, предотвращая тем самым окисление хлорофилла (его обесцвечивание). Каротин — протеиновый комплекс С550, расположенный в акцепторной части ФС И, также может участвовать в окислительно-восстановительных процессах. [c.85]
Так, например, ион Мд " является комплексообразователем в пигменте зеленых растений — хлорофилле — бионеорганиче-ском соединении, играющем важную роль в процессе фотосинтеза [c.244]
Как отмечено выше, центральную роль в осуществлении фотосинтеза играет трансформация энергии света в разность потенциалов мембраны фотосинтетического центра и сопряженный с этим синтез АТФ. Недавно, используя методы спектроскопии, рентгеноструктурного анализа и молекулярной генетики, удалось получить детальную картину событий, происходящих при фотосинтезе и выявить пространственное расположение и роль белков и пигментов, участвующих в этом процессе. За эту работу немецкие ученые Р. Хубер, И. Дайзенхофер и X. Михель удостоены Нобелевской премии 1988 г. [c.361]
Значение магния в развитии жизни на земле весьма велико. Он входит в состав зеленого растительного пигмента - хлоро 1Дла, участвуя таким образом в процессе фотосинтеза. Соединения магнвя играют большую роль в деятельности центральной нерной системы живых организмов. [c.6]
Вследствие своей фундаментальной роли в производстве ор-ханического топлива фотосинтез — безусловно наиболее важный из всех биохимических процессов. Это чрезвычайно сложный процесс, включающий большое число химических реакций, которые различны для разных организмов. Процесс фотосинтеза еще не понят до конца, и здесь мы дадим лишь краткое описание его основных особенностей. Зеленые растения содержат в хлоропластах ряд органических питаентов это хлорофиллы, а также и другие пигменты, например каротиноиды. Эти пигменты позволяют растению поглощать свет почти любой длины волны видимой области спектра. Таким образом, даже в пасмурный день свет эффективно поглощается. [c.288]
Другие органоиды клетки — это пластиды и митохондрии. Первые являются носителями ферментов, биокатализаторов каждой живой клетки в зависимости от вида и местонахождения они играют свою роль бесцветные лейкопласты нередко являются крахмалообразователями зеленые хлоропласты служат местом осуществления процесса фотосинтеза — образования органического вещества из углекислоты воздуха и воды за счет энергии солнечных лучей оранжевые хромопласты обусловливают окраску многих плодов. Митохондрии (хондриозомы) — более мелкие образования, содержат значительное количество белка, участвуют в дыхании клетки благодаря их способности запасать и передавать энергию их называют силовыми установками клетки. Клеточный сок представляет собой раствор разнообразных веществ органических и минеральных кислот и их солей, сахаров, пигментов, ферментов, дубильных веществ, различных алкалоидов, глюкозидов и др. [c.14]
В первой части настоящей книги были описаны основные характеристики главных групп природных пигментов. В предыдущих главах второй части обсуждались наиболее известные и понятные биологические функции этих пигментов, а именно окрашивание, улавливание света и распознавание цвета (зрение), а также улавливание энергии света в фотосинтезе. В этой последней главе объединены некоторые другие аспекты фотобиологии, описаны процессы, в которых природные пигменты играют важную роль. Здесь рассмотрены фоторецепторы, такие, как фитохром и флавины, которыми обладают растения и микроорганизмы, а также бактериородопсин, используемый для образования АТР у Haloba teria. [c.391]
Для правильной оценки роли каротиноидов необходимо определить количество поглощенной ими энергии и часть этой энергии, которая используется в процессе фотосинтеза. Решить данный вопрос для каротиноидов труднее, чем для хлорофилла. Изучение фотохимической активности хлорофилла легче, так как поглощение лучей в красной части спектра обусловлено только хлорофлллом, другие пластвдные пишенты растений этих лучей не поглощают,Поглощение же света в сине-фиолетовой части спектра обусловлено не только каротиноидами, но и хлорофиллом и трудно расчленить как используется свет, поглощенный отдельными пигментами. Поэ-тому изложенные выше опыты с водорослями еще не дают точного ответа на поставленный вопрос, для его решения необходимы были иные подходы, иная методика. Ниже характеризуются некоторые особенности работ последнего времени в этом направлении. [c.139]
Как известно, процесс фотосинтеза связан с поглощением света пигментами. О роли, выполняемой пигментами в процессах воздушного питания растений, свидетельствует то, что лишенные окраски формы водорослей способны вести лишь сапрофитный образ жизни, а некоторые бледно-зеленые (слабо окрашенные) высшие растения существуют как паразиты. Встречающиеся у высших растений альбиносные (лишенные хлорофилла) и желтые экземпляры сохраняют жизнеспособность лишь как части нормального зеленого растения. К длительной жизни как самостоятельные организмы альбиносы не способны. [c.108]
Многие исследователи связывали физиологическую роль антоциаиов с их способностью поглощать лучистую энергию солнца и указывали на возможность участия антоциаиов в процессе фотосинтеза. В проведенных Р. В. Нагорной исследованиях определенных закономерностей в реакциях, сопряженны.к с ассимиляцией углерода, у антоциансодержащих растений обнаружено не было. Сравнительные исследования динамики пигментов, интенсивности и продуктивности фотосинтеза, фотохимической активности листьев показали, что между растениями с красными и зелеными листьями не имеется существенных различий. [c.382]
Помимо пигментов ламеллы хлоропластов содержат многие белки, липиды, хиноны, ионы металлов. Роль некоторых из них в процессе фотосинтеза была выяснена с помощью метода дифференциальной спектрофотоме-трии (см. гл. 4). Обнаруженные в хлоропластах два цитохрома— цитохром йб и цитохром — участвуют в фо-тосинтетическом транспорте электронов. В хлоропластах обнаружены также синий медьсодержащий белок пластоцианин, ферредоксин — белок, содержащий негемовое железо, и флавопротеид ферредоксин — ЫАОР+редукта- [c.47]
Крупнейшим достижением органического синтеза XX в. является получение антибиотиков — таких соединений, как пенициллин, стрептомицин, тетрациклин. Осуществлен синтез веществ, играющих важную роль в биологии организмов — стероидов и, в частности, холестерина, являющегося составной частью животных и растительных организмов. Лишь в недалеком прошлом вершиной органического синтеза считалось получение хлорофилла — зеленого пигмента растений. Биологическое значение хлорофилла огро шо. Он участвует в фотосинтезе, одном из самых важных процессов на земле, обусловли- [c.114]
Торов, которые были рассмотрены в т. 1 (см. гл. VI, VII и IX), например карбоксилаза Еа, стабилизирующий катализатор (мутаза ) Ев или деоксйгеназы Ес и Ео- Подобную же роль может играть хлорофилл, если, например, в первичном фотохимическом процессе происходит химическое изменение этого пигмента и требуется некоторое время для его регенерации. Акцепторы или переносчики, такие, как акцептор двуокиси углерода (см. т. I, гл. VIII), тоже являются катализаторами, и недостаток любого такого вспомогательного соединения, в свою очередь, может быть лимитирующим фактором в фотосинтезе. [c.279]
chem21.info
Ферменты, участвующие в фотосинтезе - Справочник химика 21
Гербицидную активность карбаматов связывают с их способностью образовывать водородные связи с молекулой хлор о-филла или с белками ферментов, участвующих в фотосинтезе. [c.274]Снижение интенсивности фотосинтеза при дефиците ионов железа может быть объяснено, если встать на точку зрения Бойченко, считающей, что Ре входит в состав фермента, участвующего в восстановлении углекислого газа. Одним из компонентов этого фермента является также марганец, что может объяснить сильную депрессию фотосинтеза у высших растений и зеленых водорослей при отсутствии Мг. Тот факт, что фоторедукция СО2 не затормаживается при дефиците Мг, дал основание считать, что он участвует в реакциях, связанных с выделением кислорода. [c.127]
Важнейшее значение для ряда жизненных процессов имеют тс-электронные сопряженные системы порфириновых соединений -производных порфирина [4]. Порфириновые комплексы играют роль первичных факторов фотосинтеза, ко-ферментов и ферментов, участвуют в процессах дыхания и переносе кислорода. Среди огромного числа фундаментальных биохимических и биофизических процессов, ответственных за создание энергетических запасов в живом организме, много таких реакций, которые протекают самопроизвольно при участии ферментных катализаторов - металлопорфириновых комплексов. Эти соединения, находясь в организме, испытывают со стороны окружения влияние, подобное тому, которое возникает при их растворении [c.6]В процессе фотосинтеза на разных его этапах образуются моносахариды— пентозы и гексозы, из которых затем синтезируются дисахариды и полисахариды, гликозиды и другие вещества. Из фосфоглицериновой кислоты образуется фосфо-пировиноградная кислота, которая под влиянием специфических ферментов, участвующих в процессах переаминирования, окислительного декарбоксилирования, цикла трикарбоновых кислот и других, может подвергаться различным превращениям. Из фосфопировиноградной кислоты образуются аминокислоты, органические кислоты, жирные кислоты, глицерин и другие вещества. [c.262]
Исследования А. М. Кузина показали, что в качестве первых продуктов фотосинтеза растения образуют уроновые кислоты. Это было подтверждено Е. А. Бойченко, осуществившей восстановление СОз при участии гидрогеназы изолированных хлоропластов в темноте. Эта работа имеет исключительно важное значение, освещая, во-нервых, вопрос о природе одного из ферментов, участвующих в переносе водорода на СО2, и, во-вторых, доказывая, что реакции восстановительного конца фотосинтеза осуществляются темновым путем. [c.13]
КОЙ света, скажем в течение 0,0001 секунды, выделение кислорода в темноте продолжается примерно 0,02 секунды другими словами, темновой интервал в 0,02 секунды необходим для получения максимального выхода кислорода на одну вспышку. В этом опыте непосредственно измеряется время, необходимое для завершения наиболее медленной темновой реакции фотосинтеза. Оно соответствует времени, которое необходимо нашим пароходам для переезда через океан и возвращения в гавань. Было обнаружено также, что имеется предел — некий максимальный выход фотосинтеза, который может дать одна вспышка максимальный эффект — это примерно одна молекула кислорода на 2000 молекул имеющегося в клетке хлорофилла. Такой результат невольно вызывает удивление. Можно было бы ожидать, что за время Короткой вспышки каждая молекула хлорофилла будет иметь возможность выполнить свое дело один раз и даст одну молекулу промежуточного продукта. Максимальный выход должен бы, таким образом, быть равен одной молекуле кислорода на одну или несколько молекул хлорофилла. Джеймс Франк из Чикагского университета предложил объяснение этого парадокса, допустив, что максимальный выход фотосинтеза на вспышку зависит не от числа молекул хлорофилла, а от числа молекул фермента, участвующего во второй стадии (так сказать, от числа кают на пароходах, а не от числа купе в поездах). Это означает, что при вспышке может образоваться столько молекул промежуточного продукта, сколько имеется молекул хлорофилла, но лишь сравнительно небольшое число их может пройти последующую темновую стадию и образовать кислород. [c.43]
Выявлена связь между холодостойкостью и отдельными звеньями обмена веществ растения, в частности активностью окислительных ферментов, участвующих в дыхании, интенсивностью фотосинтеза, содержанием пигментов и т. д. Эти исследования значительно расширили возможности управления холодо- и морозостойкостью растений путем применения различных удобрений, выбором сроков и способов посева, обрезки многолетних деревьев и т. д. [c.631]Согласно экспериментальным данным, полученным в последние годы, восстановление углекислоты высшими растениями осуществляется при участии биметаллической ферментной системы, активируемой марганцем и железом (Бойченко, 1949, 1963, 1966 Бойченко, Саенко, 1959, 1961). Восстановленное железо фермента участвует в восстановлении углекислоты Мп +, имеющийся в составе фермента, способствует образованию липидной гидроперекиси, образование которой предшествует выделению свободного кислорода при фотосинтезе. [c.101]
Углеводы являются чрезвычайно важным классом природных соединений. Исследование их химических свойств может дать ценную информацию о механизмах реакций и стереохимии. Значительным достижением в настоящее время является применение углеводов в качестве хиральных синтонов и заготовок для стерео-специфического синтеза таких соединений, как простагландины, аминокислоты, гетероциклические производные, липиды и т. д. Для биолога значение углеводов заключается в доминирующей роли, которая отводится им в живых организмах, и в сложности их функций. Углеводы участвуют в большинстве биохимических процессов в виде макромолекулярных частиц, хотя во многих биологических жидкостях содержатся моно- и дисахариды, а большинство растений содержит глюкозу, фруктозу и сахарозу. Только растения способны осуществлять полный синтез углеводов посредством фотосинтеза, в процессе которого атмосферный диоксид углерода превращается в углеводы, причем в качестве источника энергии используется свет (см. гл. 28.2). В результате этого накапливается огромное количество гомополисахаридов — целлюлозы (структурный материал) и крахмала (запасной питательный материал). Некоторые растения, в особенности сахарный тростник и сахарная свекла, накапливают относительно большие количества уникального дисахарида сахарозы (а-О-глюкопиранозил-р-О-фруктофуранозида), который выделяют в значительных количествах (82-10 т в год). Сахароза — наиболее дешевое, доступное, Чистое органическое вещество, запасы которого (в отличие от запасов нефти и продуктов ее переработки) можно восполнять. -Глюкоза известна уже в течение нескольких веков из-за ее способности кристаллизоваться из засахаривающегося меда и винного сусла. В промышленном масштабе ее получают гидролизом крахмала, причем в настоящее время применяют непрерывную Схему с использованием ферментов, иммобилизованных на твердом полимерном носителе. [c.127]
Хлоропласты не имеют цитохромоксидазы и поэтому не способны к дыханию [73, 843, 921, 1182, 1952]. Но они содержат много ферментов, участвующих и в других процессах, кроме фотосинтеза [724, 1736]. [c.182]
СВОЙ тип белка, соответствующий тем физиологическим функциям, которые данная мембрана выполняет в клетке. Известно , например, что активные белки (ферменты), регулирующие транспорт минеральных веществ — поступление их в клетку и выход из клетки, — локализуются в плазмалемме и тонопласте ферменты, участвующие в фотосинтезе, сосредоточены в мембранных системах зеленых хлоропластов и наконец, ферменты, катализирующие окислительные реакции процесса дыхания находятся в митохондриальных мембранах. [c.28]
ЦЙНКОВЫЕ УДОБРЕНИЯ, один из ввдов микроудобрений, содержащий в качестве микроэлемента Zn. Последний -постоянный компонент растений (15-22 мг на 1 кг сухого в-ва), входит в состав ряда ферментов, участвующих в окислит.-восстановит. процессах в растит, организмах, способствует биосинтезу витаминов, ускоряет рост и развитие, повышает продуктивность с.-х. культур. При недостатке Zn в растениях нарушается обмен в-в, уменьшается содержание сахарозы и крахмала, развивается хлороз листьев (приобретают желтую окраску), что замедляет образование хлорофилла и снижает активность фотосинтеза. [c.382]
Этот фермент участвует также в дыхании (в окислительном пентозофосфатном цикле). При- фотосинтезе ои катализирует [c.137]
МАРГАНЦЕВЫЕ УДОБРЕНИЯ, один из видов микроудобрений, содержащий в качестве микроэлемента Мп Последний - постоянная составная часть растит организмов (десятитысячные тысячные доли процента), регулирует активность ряда ферментов, влияет на их минер питание, участвует в процессах дыхания и фотосинтеза, в биосинтезе нуклеиновых к-т и др Недостаток этого микроэлемента у растений вызывает хлороз (яблоня, цитрусовые), пятнистость (злаки), ожоги (картофель, ячмень) и т п [c.651]
Диффузия играет большую роль на многих стадиях процесса фотосинтети-ческого включения углерода СОг в углеводы. При этом углекислый газ диффундирует из атмосферы, достигая поверхности листа, а затем проходит через усть-ичные отверстия. Войдя в лист, СО2 диффундирует по межклеточным воздухоносным пространствам, а затем через клеточные оболочки и плазму клеток ме.зо-филла листа. Далее углекислый газ, по-виднмому, в форме НСОг диффундирует через цитоплазму и достигает хлоропластов. Затем СО2 оказывается в хлоропласте и попадает в зону действия ферментов, участвующих в образовании углеводов. Как видно, одну только эту сторону фотосинтеза можно расчленить на много стадий, в каждой из которых важную роль играет диффузия. Если бы с помощью ферментов фиксировался весь углекислый газ, находящийся в сфере их действия, и не происходила бы диффузия новых количеств углекислого газа из атмосферы, окружающей растение, процесс фотосинтеза прекратился бы. Диффузия важна также для многих других аспектов физиологии растений, особенно для проникновения веществ через мембраны. [c.17]
Гербицидную активность карбаматов связывают с их способностью образовывать водородные связи с молекулой хлорофилла или с белками ферментов, участвующих в процессе фотосинтеза. Однако механизм действия N-арилкарбаматов, по-видимому, не так прост, влияние этих соединений на рост растений является результатом нарушения ими нескольких жизненно важных систем. [c.307]
Экспериментально доказано, что цианамид образует малорастворимые (практически совершенно нерастворимые) в воде соли с тяжелыми металлами — железом, медью, цинком — и, таким образом, разрушает ферменты, регулирующие фотосинтез. Кроме того, цианамид уже в первые дни после обработки разрушает пигменты зеленого листа — хлорофилл и каротин. В малых кон-дентрациях цианамид не подавляет ферментов, участвующих в процессе дыхания, и дыхание в первый период восле обработки даже усиливается. По мере увеличения концентрации цианамида в растении он инактивирует каталазу, и интенсивность дыхания резко падает. Нарушаются и другие физиологические процессы, а главное— [c.22]
Это уравнение показывает, что нри фотосинтезе происходит фотолити-ческое расщепление воды, причем образующийся из воды водород восстанавливает углекислый газ. В свое время К. Тимирязевым и А. Бахом было высказано мнение о том, что в основе фотосинтеза лежит цепь окислительно-восстановительных реакций. Известно, что водород в момент выделения восстанавливает хлорофилл. Восстановленный хлорофилл слабо окрашен. При воздействии на него кислородсЛ он окисляется и превращается в обычный хлорофилл зеленого цвета. В хлоропластах обнаружены окислительновосстановительные ферменты, участвующие в процессе фотосинтеза. Экспериментальные данные показывают, что восстановление углекислого газа при фотосинтезе является весьма сложным процессом, причем восстанавливается не свободный углекислый газ, а предварительно связанный с какими-то веществами, имеющимися в хлоропластах. [c.230]
Цинк входит в состав ряда ферментов, участвующих в процессах фотосинтеза и дыхания растений. При недостатке цинка интенсивность этих процессов сниноется. Цинковое голодание приводит к разрушению ростовых веществ и задержке роста растения. [c.420]
В основном связан с функционированием мембран, в том числе с проведением нервных импульсов, поддержанием электрического потенциала, работой (Na+, К+)-насоса, поддержанием анионнокатионного и осмотического баланса. Кофактор ферментов, участвующих в фотосинтезе и дыхании (гликолизе). Компонент клеточного сока растительных вакуолей. [c.280]
Работы по увеличению фотосинтетической активности проводятся в направлении введения генов С4 фотосинтеза в Сз-растения, Ген фосфо-енолпируваткарбоксилазы (РЕРС) фотосинтетической системы кукурузы С4, кодирующий основной фермент, участвующий в фиксации атмосферного СО2 в клетках мезофилла листа, был клонирован и перенесен методом агробактериальной трансформации в Сз-растения риса. Анализ полученных трансгенных растений показал, что активность фермента в клетках риса в 2—3 раза выше, чем у кукурузы, что привело к увеличению фотосинтетической активности и урожайности. [c.69]
Железо, медь, цинк. Эти элементы в соединении со специфическими белками образуют основу ряда ферментных систем. Исключительно важное место в обмене веществ принадлежит, как известно, ферментам Ре- и Си-протеидам. К ферментам Ре-протеидам принадлежат компоненты цитохромной системы (различные цитохромы и цитохромоксидазы, цнтохромпероксидаза), а также каталаза, пероксидазы, ферредоксины, ферритины. Медь входит в простетические группы полифенолаз, аскорбатоксидазы, лакказы. Эти ферменты участвуют в темновых реакциях фотосинтеза и в реакциях дыхания, что и определяет важное значение этих катализаторов для биосинтетических функций растения в целом. [c.432]
Железо входит в состав многих важных ферментов, в том числе цитохромов — переносчиков электронов, участвующих а процессе дыхания, а также окислительных ферментов перокси базы и каталазы. Во всех этих ферментах железо присутствует в простетической группе в виде гема (аналог хлорофилла), в котором центральный атом железа связан с четырьмя пиррольны-ми кольцами, соединенными в большую циклическую структуру.. В таких ферментах железо функционирует благодаря своей способности обратимо окисляться и (восстанавливаться (Ре ++е ч= ч Ре +) негеминовое железо может действовать таким же образом. Медь также обладает свойством обратимо окисляться и восстанавливаться (Си2++е-ч Си+). Вполне вероятно, что марганец, входящий в состав фермента супероксиддисмутазы, играет такую же роль во многих окислительных реакциях. Железо имеет существенное значение и для ферментов, участвующих в синтезе хлорофилла. Кроме того, оно является составной частьк> ферредоксина—соединения, функционирующего в качестве переносчика электронов в процессе фотосинтеза. Недостаток железа вызывает глубокий хлороз в развивающихся листьях, которые могут стать совершенно белыми. [c.211]
Мембраны формируют также специализированные компартменты внутри клетки. Такие внутриклеточные мембраны образуют многочисленные морфологически различимые структуры (органеллы) — митохондрии, эндоплазматический ретикулум, сар-коплазматический ретикулум. комплекс Гольджи, секреторные гранулы, лизосомы и ядерные мембраны. В мембранах локализованы ферменты, функционирующие как интегральные элементы процесса возбуждения и ответа на него, а также ферменты, участвующие в преобразовании энергии в таких процессах, как фотосинтез и окислительное фосфорилирование. [c.127]
Образующаяся перекись расщепляется при гидролитическом действии фермента до фосфогликолата и 3-фосфоглицерата. Несмотря на то что это предположение является общепринятым, оно все же кажется неубедительным. Молекулярный кислород обычно не способен быстро реагировать с органическими субстратами (известны лишь немногие исключения, например дигидрофлавины гл. 8, разд. И, 7), если не считать тех случаев, когда в реакции участвуют ионы переходных металлов (гл. 10, разд. Б,3). Дальнейшее исследование необычной реакции, катализируемой рибулозодифосфат-карбоксилазой, несомненно, представит большой теоретический я практический интерес последний связан с тем, что эта реакция имеет большое значение в снижении выхода фотосинтеза (гл. 13, разд. Д, 9). [c.176]
Важнейшая функция хлоропластов — участие в процессе фотосинтеза. Для них характерна подвижность. Форма зеленых пластид сильно варьирует, а число их определенно для каждого вида растений. У кукурузы хлоропласты имеют форму линзы, диаметр их составляет 5—7 мкм, толщина — 3—5 мкм (рис. 38) В составе хлоропластов, кроме белков и липидов, выявлены пигменты (хлорофилл а я Ь, каротиноиды), иуклеииовые кислоты (ДНК и РНК), ферменты, участвующие в фотосинтезе, рибосомы, крахмал. [c.125]
Согласно современным представлениям, в тилакоид-ных мембранах локализованы все фотосиитетические пигменты хлоропласта и ферменты, необходимые для осуществления световых реакций фотосинтеза. В строме содержатся ферменты, участвующие в темновых превращениях диоксида углерода. Таким образом, сложная и тонкая структура хлоропласта обеспечивает пространственное разделение отдельных реакций а тем самым и эффективный ход фотосинтеза в целом. Образующиеся в пластидах продукты ассимиляции траиспор- [c.74]
Обсуждение метаболизма кислот по типу толстянковых в гл. 15 сосредоточено иа истории его открытия, а также на биохимических и экологических аспектах САМ, Гл. 16 касается фотосинтеза в органах размножения н различных путей метаболизма малата у растений. В приложении А опнсаиы методики выделения хлоропластов, а в приложении Б дана номенклатура ферментов, участвующих в С.,-, С4-метаболизме и САМ-путях ассимиляции углерода при с[зотосиитезе. [c.7]
Итак, мы убедились в том, что индукция связана с автока-талитическим накоплением промежуточных продуктов ВПФ-Д нкла (разд. 7.7). Это не означает, что активация ферментов, участвующих в фотосинтезе, под действием света не играет никакой роли. Более подробно мы рассмотрим этот вопрос в гл. 9. Хотелось бы обратить внимание на то, что не следует смешивать активацию ферментов светом с появлением под действием освещения условий, благоприятных для катализа. Например, на свету pH стромы будет более щелочным, чем в темноте, что способствует действию ферментов с более щелочными оптиму-мами pH. Кроме того, при высоких значениях pH ферменты могут переходить из менее активной формы в более активную. Хотя эти эффекты по своей природе совершенно различны, они могут приводить к одному и тому же конечному результату. Если же оба проявляются одновременио, их действие может стать аддитивным. Однако на этом основании довольно трудно объяснить практически полное отсутствие фотосиитетической ассимиляции углерода сразу (в течение 1—2 мин) после начала освещения. При прочих равных условиях нулевая скорость должна говорить о том, что ферменты И0л1юстью лишены активности. Тем не менее, хотя активность может сильно меняться при освещении, некоторые ферменты (иапример, РуБФ-карб- [c.186]
У Сз-растений концентрация Pi в цитозоле, по-видимому, играет регуляторную роль в процессе передачи углерода на синтез сахарозы (гл. 9). У С -растений такие ферменты, участвующие в последних стадиях синтеза сахарозы, как глюкозо-1-фосфат — уридилилтрансфераза и сахарозофосфатсинтетаза, локализованы в цитоплазме. Поэтому синтез сахарозы, вероятно, как и у Сз-растений, идет В цитоплазме. Уровень Pi в цитозоле клеток обкладки проводящих пучков может влиять на скорость выхода ФГК или триозофосфата из хлоропластов. В ходе дальнейших превращений ФГК или триозофосфатов в сахарозу, которые осуществляются в цитозоле клеток обоих типов. Pi снова высвобождается и возвращается обратно в хлоропласты клеток обкладки проводящих пучков (разд. 11.6). Б хлоропластах мезофилла, Сграстений Pi поглощается в обмеи на ФЕП (разд. 12.5). У Сз-растений в первичном обмене на переносчике фосфата участвуют Pi и ДГАФ, а выход ФГК в процессе фотосинтеза незначителен. Следовательно, и содержание ФГК в цитозоле может быть тоже относительно невелико. Предполагают, что у С4-растений ФГК выходит шз клеток обкладки проводящих пучков и затем восстанавливается в хлоропластах мезофилла Поэтому уровень ФГК в цитозоле в процессе фотосинтеза может быть сравнительно высок. Содержание ФГК в цитозоле клеток мезофилла может частично контролировать скорость синтеза сахарозы за счет обмена ФГК—ДГАФ в хлоропластах. В отличие от условий, существующих в клетках Сз-растений, для цитозоля клеток мезофилла С4-Растений характерен высокий уровень Pj, что способствует обмену ФЕП и ингибированию [c.394]
В течение первых фаз прорастания проросток питается за счет готовых органических веществ, находящихся в эндосперме или семядолях. Как только появляются первые зеленые листья, начинается фотосинтез. На этом фаза гтроростка заканчивается и растепие переходит в ювенильную фазу. На свету в клетках листьев из пропластид развиваются пластиды. Еще до завершения роста пластид с развитой гранулярно-ламеллярной структурой начинается образо- 8ние ферментов, участвующих в процессе фотосинтеза. Так, один [c.234]
В зеленом листе растения под воздействием солнечной радиации протекает целый комплекс фотохимических процессов, в результате которых из воды, углекислого газа и минеральных солей образуются крахмал, клетчатка, белки, жиры и другие сложные органические вещества. Процесс фотосинтеза о гень сложен. Он осуществляется при непосредственном участии важнейшего природного фотокатализатора — хлорофилла и сопровождается целым циклом химических превращений, не зависящих от солнечной радиации. В этих превращениях участвует большое число разнообразных биокатализаторов— ферментов. Суммарное уравнение фотосинтеза обычно выражают в виде реакции превращения двуокиси углерода и воды в гексозу [c.176]
Фотосинтез в растениях. В зеленом листе растения под во действием энергии солнечной радиации протекает целый комплекс фотосинтетических процессов, исходным материалом для которых служат СОа, НаО и минеральные соли. Конечными продуктам.I являются крахмал, клетчатка, белки, жиры и другие сложные оргя-нические вещества. Процесс фотосинтеза осуществляется при непо средственном участии важнейшего природного фотокатализатора — хлорофилла . В этом процессе участвуют также и многие друпк-окислительно-восстановительные ферменты (бнокатализаторы). [c.144]
В клетках зеленых растений хлорофилл содержится в особых частицах — хлоропластах, которые и являются химическим заводом , осуществляющим фотосинтез. Кроме хлорофилла, в процессе фотосинтеза участвует целая система ферментов. Из углекислого газа в процессе фотосинтеза образуются триозы (глицериновый альдегид СН. ОН—СНОН—СНО, диоксиацетон НОСН2СОСН2ОН), которые далее превращаются в гексозу и затем в крахмал. Все эти превращения идут через стадию эфиров фосфорной кислоты. [c.304]
К настоящему времени выяснена основная коферментная роль KoQj . Он оказался обязательным компонентом дыхательной цепи (см. главу 9) осуществляет в митохондриях перенос электронов от мембранных дегидрогеназ (в частности, НАДН-дегидрогеназы дыхательной цепи, СДГ и т.д.) на цитохромы. Таким образом, если никотинамидные коферменты участвуют в транспорте электронов и водорода между водорастворимыми ферментами, то KoQj благодаря своей растворимости в жирах осуществляет такой перенос в гидрофобной митохондриальной мембране. Пластохиноны выполняют аналогичную функцию переносчиков при транспорте электронов в процессе фотосинтеза. [c.243]
chem21.info
Волонтер фотосинтеза
Статья на конкурс «био/мол/текст»: Реакции углекислого газа в форме СО2 или бикарбоната (HCO3−) в клетке контролируются карбоангидразой самым активным ферментом среди всех известных, ускоряющим обратимую реакцию гидратации атмосферного СО2. В данной статье мы рассмотрим процесс фотосинтеза и роль карбоангидразы в нем.Обратите внимание!
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучший обзор».
Спонсор конкурса — дальновидная компания Life Technologies. Спонсор приза зрительских симпатий — фирма Helicon.Разве заронилсяВтуне хоть единыйСолнца луч на землю?Или не возник он,В ней преображенный,В изумрудных листьях.
Н.Ф. Щербина [1].
История познания процесса, который испорченный воздух вновь превращает в хороший
Представления о фотосинтезе складывались постепенно, начиная с 16 века. В 18 веке Джозеф Пристли — известный английский ученый-химик — открыл кислород. Как химика Пристли заинтересовал вопрос: почему воздух полей и лесов чище городского? Ученый предположил, что растения очищают его от веществ, выделяемых людьми при дыхании, а также дымящимися трубами заводов и фабрик. С целью проверки своего предположения ученый провел эксперимент над мышью, которую посадил под стеклянный колпак (рис. 1). Вскоре животное погибло. Тогда экспериментатор поместил под такой же колпак другую мышь, но уже вместе с веткой мяты. «Это было сделано в начале августа 1771 года. Через 8 дней я нашел, что мышь прекрасно могла жить в той части воздуха, в которой росла ветка мяты. Побег мяты вырос почти на 3 дюйма...». Опыт заинтересовал ученых. Многие пытались повторить его в своих лабораториях, но результаты получались противоречивыми. Голландский врач Ян Ингенхауз (1730–1799) усомнился в правильности такого использования растений и провел ряд экспериментов с целью проверки действительности этого приема. В результате своих опытов он сделал открытие, что только зеленые части растений могут улучшать воздух, да и то лишь на свету [2].
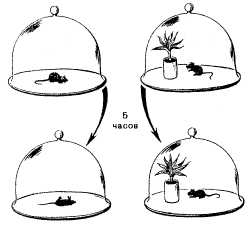
Рисунок 1. Эксперимент Д. Пристли.
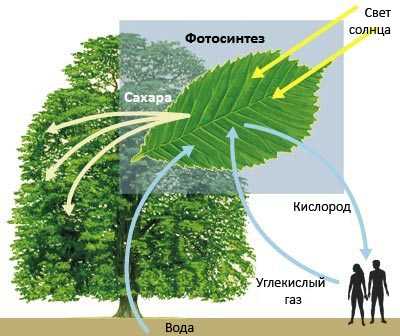
Рисунок 2. Цикл выделения и поглощения углекислого газа и кислорода между животными и растениями. Рисунок из Process of photosynthesis for kids.
Сам термин «фотосинтез» был предложен в 1877 году известным немецким физиологом растений Вильгельмом Пфеффером (1845–1920). Он считал, что из углекислого газа и воды зеленые растения на свету образуют органические вещества и выделяют кислород. А энергия солнечного света усваивается и трансформируется при помощи зеленого пигмента хлорофилла. Термин «хлорофилл» был предложен в 1818 году французскими химиками П. Пельтье и Ж. Каванту. Он образован из греческих слов «хлорос» — зеленый — и «филлон» — лист. Позже исследователи подтвердили, что для питания растений требуется диоксид углерода и вода, из которых создается бóльшая часть массы растений [2].
Российский ученый Климент Аркадьевич Тимирязев (1843–1920) показал, что фотосинтез проходит с наибольшей интенсивностью в тех областях солнечного спектра, где находятся максимумы поглощения хлорофилла. К середине 19 века было установлено, что фотосинтез является процессом, как бы обратным дыхательному. Французский ученый Жан Батист Буссенго (1802–1887) в своих работах, опубликованных в это время, утверждал, что в процессе фотосинтеза происходит выделение кислорода из углекислого газа. Это мнение в научной литературе господствовало длительное время. В конце 19 века биохимик Алексей Николаевич Бах (1857–1946) на основе экспериментальных исследований пришел к выводу, что при ассимиляции диоксида углерода источником выделяющегося молекулярного кислорода являются пероксиды, образующиеся из воды. Он же высказал предположение о биокаталитической роли белков-ферментов в фотосинтезе. В 20 веке было установлено, что процесс фотосинтеза начинается на свету в фоторецепторах хлоропластов, однако многие из последующих стадий могут протекать в темноте. В 1941 американский биохимик Мелвин Кальвин (1911–1997) показал, что первичный процесс фотосинтеза заключается в разложении молекул воды под действием света, в результате чего образуются кислород, выделяющийся в атмосферу, и водород, идущий на восстановление диоксида углерода до органических веществ. Используя радиоактивный изотоп углерода 14С, бумажную хроматографию и классические методы органической химии, Кальвин и его группа смогли проследить биосинтетические пути фотохимических процессов. К 1956 году стал ясным полный путь превращения углерода при фотосинтезе, который был назван циклом Кальвина [2].
Фотосинтез — сложный многоступенчатый процесс (рис. 3). На каком именно этапе необходима энергия света? Оказалось, что реакция синтеза органических веществ, включения углекислого газа в состав их молекул непосредственно энергии света не требует. Эти реакции назвали темновыми, хотя идут они не только в темноте, но и на свету, — просто свет для них не обязателен [2].
Роль фотосинтеза в жизни человеческого общества
В последние годы человечество столкнулось с дефицитом энергоресурсов. Грядущее истощение запасов нефти и газа побуждает ученых искать новые, возобновляемые источники энергии. Чрезвычайно заманчивые перспективы открывает использование в качестве энергоносителя водорода. Водород — источник экологически чистой энергии. При его сжигании образуется только вода: 2Н2+О2 = 2Н2О [2]. Водород выделяют высшие растения и многие бактерии.
Что касается бактерий, то большинство из них живет в строго анаэробных условиях и не может использоваться для масштабного производства этого газа. Однако недавно в океане открыли штамм аэробных цианобактерий, очень эффективно вырабатывающих водород. Cyanobacterium cyanothece 51142 совмещает в себе сразу два фундаментальных биохимических пути — это запасание энергии в светлое время суток во время фотосинтеза и азотфиксация с выделением водорода и затратой энергии — ночью. Выход водорода, и так достаточно высокий, удалось в лабораторных условиях дополнительно повысить, «отрегулировав» длительность светового дня. Зарегистрированный выход — 150 микромоль водорода на миллиграмм хлорофилла в час — самый высокий, который удавалось наблюдать для цианобактерий. Если экстраполировать эти результаты на чуть большего размера реактор, выход составит 900 мл водорода с литра бактериальной культуры за 48 часов. С одной стороны, это вроде бы и не много, но если представить себе раскинувшиеся на тысячи квадратных километров экваториальных океанов реакторы с бактериями, работающими в полную силу, то итоговое количество газа может быть впечатляющим [5].
Новый процесс получения водорода основан на преобразовании энергии ксилозы, наиболее распространенного простого сахара. Ученые из Virginia Tech взяли набор ферментов у ряда микроорганизмов и создали уникальный синтетический фермент, аналогов которому не существует в природе, что позволит извлекать большие количества водорода из любого растения. Данный фермент при температуре всего 50 °C освобождает с помощью ксилозы беспрецедентно большой объем водорода — примерно в три раза больше, чем лучшие современные «микробные» методики. Суть процесса сводится к тому, что энергия, запасенная в ксилозе и полифосфатах, расщепляет молекулы воды и позволяет получить высокочистый водород, который можно сразу отправлять в топливные ячейки, вырабатывающие электричество. Получается эффективнейший экологически чистый процесс, который требует немного энергии только на запуск реакции [6]. По энергоемкости водород не уступает высококачественному бензину. Растительный мир представляет собой огромный биохимический комбинат, который поражает масштабами и разнообразием биохимических синтезов [2].
Существует ещё один путь использования человеком солнечной энергии, усвоенной растениями, — непосредственная трансформация световой энергии в электрическую. Способность хлорофилла под действием света отдавать и присоединять электроны лежит в основе работы генераторов, содержащих хлорофилл. М. Кальвин в 1972 году выдвинул идею создания фотоэлемента, в котором в качестве источника электрического тока служил бы хлорофилл, способный при освещении отнимать электроны от одних веществ и передавать их другим. В настоящее время по этому направлению ведется множество разработок [2]. Например, ученый Андреас Мершин (Andreas Mershin) и его коллеги из Массачусетского технологического института создали батареи на основе светособирающего комплекса биологических молекул — фотосистемы I из цианобактерии Thermosynecho coccuselongates (рис. 4). Под обычным солнечным светом ячейки показали напряжение холостого хода в 0,5 В, удельную мощность 81 мкВт/см2 и плотность фототока в 362 мкА/см2. А это, по уверению изобретателей, в 10000 раз больше, чем у любой показанной ранее биофотовольтаики, основанной на природных фотосистемах [7].
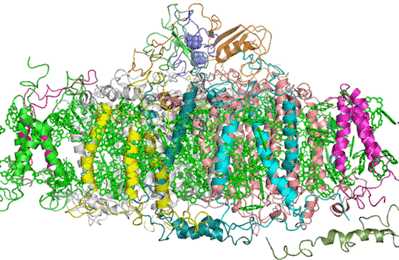
Рисунок 4. Пространственная структура фотосистемы 1 (ФС1). ФС являются важными компонентами комплексов, отвечающих за фотосинтез в растениях и водорослях. Они состоят из нескольких вариаций хлорофилла и сопутствующих молекул — белков, липидов и кофакторов. Общее число молекул в таком наборе — до двух с лишним сотен. Рисунок из [7].
КПД полученных батарей составил всего-то около 0,1%. Тем не менее, создатели диковинки считают её важным шагом на пути массового внедрения солнечной энергетики в быт. Ведь потенциально такие устройства могут производиться с крайне низкими затратами [7]! Создание фотоэлементов — это только начало в промышленном получении альтернативных видов энергии для всего человечества [2].
Ещё одной важной задачей фотосинтеза растений является обеспечение людей органическими веществами. Причем не только для употребления в пищу, но и для фармацевтики, промышленного производства бумаги, крахмала и т.д. Фотосинтез является главной точкой входа неорганического углерода в биологический цикл. Весь свободный кислород атмосферы — биогенного происхождения и является побочным продуктом фотосинтеза. Формирование окислительной атмосферы (так называемая кислородная катастрофа) полностью изменило состояние земной поверхности, сделало возможным появление дыхания, а в дальнейшем, после образованияозонового слоя, позволило жизни существовать на суше. Учитывая значение процесса фотосинтеза, раскрытие его механизма является одной из наиболее важных и интересных задач, стоящих перед физиологией растений [2].
Перейдем же к одному из самых интересных ферментов, работающих «под капотом» фотосинтеза.
Самый активный фермент: волонтер фотосинтеза
В естественных условиях концентрация СО2 довольно низка (0,04% или 400 мкл/л), поэтому диффузия СО2 из атмосферы во внутренние воздушные полости листа затруднена. В условиях низких концентраций углекислоты существенная роль в процессе ее ассимиляции при фотосинтезе принадлежит ферменту карбоангидразе (КА). Вероятно, КА способствует обеспечению рибулозобисфосфаткарбоксилазы/оксигеназы (РБФК/О, или RuBisCO) субстратом (СО2), запасенным в строме хлоропласта в виде иона бикарбоната. РБФК/О — один из важнейших ферментов в природе, поскольку он играет центральную роль в основном механизме поступления неорганического углерода в биологический круговорот и считается наиболее распространённым ферментом на Земле [8].
Карбоангидраза — чрезвычайно важный биокатализатор, относящийся к числу самых активных ферментов. КА катализирует обратимую реакцию гидратации СО2 в клетке:
СО2 + Н2О = Н2СО3 = Н+ + НСО3−.
Карбоангидразная реакция проходит в две стадии. В первой стадии образуется ион бикарбоната НСО3−. Во второй стадии освобождается протон, и именно эта стадия лимитирует процесс [8].
| Карбоангидраза | 36 000 000 |
| β-Амилаза | 1 100 000 |
| Фосфоглюкомутаза | 1 240 |
Гипотетически КА клеток растений может выполнять различные физиологические функции в соответствии с местом расположения. При фотосинтезе кроме быстрого перевода НСО3− в СО2, который необходим для РБФК/О, она может ускорять транспорт неорганического углерода через мембраны, поддерживать рН-статус в разных частях клеток, смягчать изменения кислотности в стрессовых ситуациях, регулировать транспорт электронов и протонов хлоропласте [10].
Карбоангидраза присутствует практически во всех исследованных видах растений. Несмотря на многочисленные экспериментальные факты в пользу участия карбоангидразы в фотосинтезе, окончательный механизм участия фермента в этом процессе ещё предстоит выяснить [10].
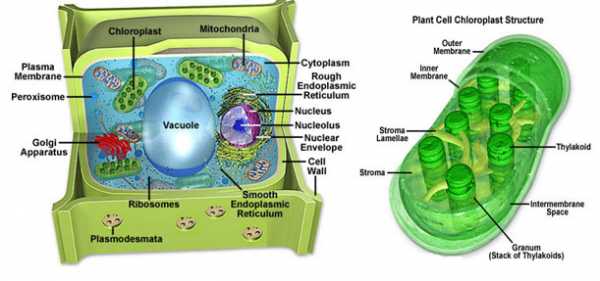
Рисунок 5. Строение растительной клетки и хлоропласта. Рисунок из Molecular Expressions.
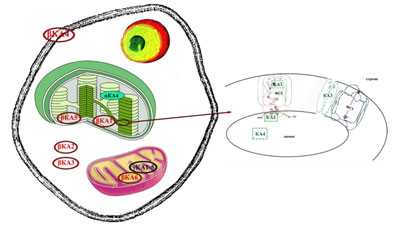
Рисунок 6. Расположение карбоангидраз в клетке высших растений. Рисунок из [12].
Многочисленная «семья» карбоангидраз
В высшем растении Arabidopsis thaliana обнаружено 19 генов трех (из пяти установленных к настоящему времени) семейств, кодирующих карбоангидразы. В высших растениях обнаружены КА, принадлежащие к α-, β- и γ-семействам. В митохондриях найдено пять КА γ-семейства; КА β-семейства обнаружены в хлоропластах, митохондриях, цитоплазме, плазмалемме (рис. 6). О восьми α-КА известно только то, что α-КА1 и α-КА4 находятся в хлоропластах. К настоящему времени в хлоропластах высших растений обнаружены карбоангидразы α-КА1, α-КА4, β-КА1 и β-КА5. Из этих четырех КА известно местонахождение только одной, и она находится в строме хлоропласта (рис. 6) [10].
КА относятся к металлоферментам, которые содержат атом металла в активном центре. Обычно таким металлом, который связан с лигандами реакционного центра КА, является цинк. КА полностью отличаются друг от друга на уровне их третичных и четвертичных структур (рис. 7), но особенно удивительно, что активные центры всех КА сходны [11].
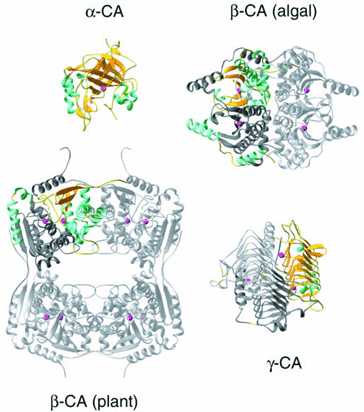
Рисунок 7. Четвертичная структура представителей трех семейств КА. Зеленым цветом обозначены α-спирали, желтым — участки β-складчатости, розовый — атомы цинка в активных центрах ферментов. В структурах α и γ-КА превалирует β-складчатая организация белковой молекулы, в структуре β-КА преобладают α-витки. Картинка из [11].
Расположение КА в клетках растений
Разнообразие форм КА намекает на множественность функций, которые они выполняют в различных частях клетки. Для определения внутриклеточного местонахождения шести β-карбоангидраз использовали эксперимент, основанный на мечении КА зеленым флуоресцентным белком (ЗФБ) [14]. Карбоангидразу методами генетической инженерии помещали в одну «рамку считывания» с ЗФБ, и экспрессию такого «сшитого» гена анализировали с помощью лазерной конфокальной сканирующей микроскопии (рис. 8). В мезофильных клетках трансгенных растений, в которых β-КА1 и β-КА5 «сшиты» с ЗФБ, ЗФБ-сигнал совпадал в пространстве с флуоресценцией хлорофилла, что указывало на его связь (колокализацию) с хлоропластами [13].
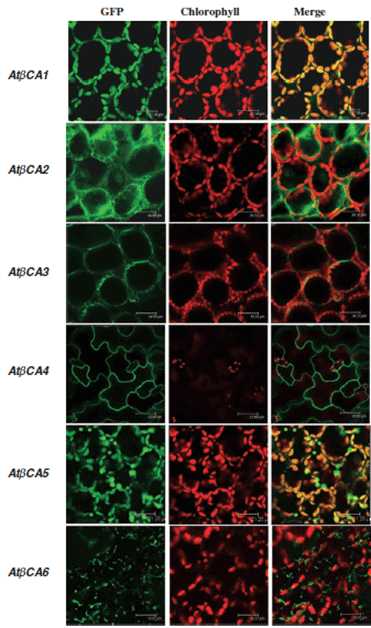
Рисунок 8. Микрофотография клеток с GFP, который «сшит» с кодирующей областью генов β-КА1—6. Зеленый и красный сигналы показывают флуоресценцию GFP и автофлуоресценцию хлорофилла, соответственно. Желтым (справа) показана совмещенная картина. Флуоресценция зафиксирована с помощью конфокального микроскопа. Рисунок из [13].
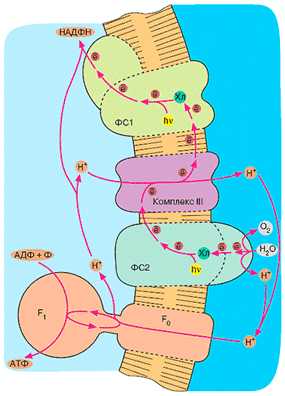
Рисунок 9. Пигментбелковые комплексы ФС1 и ФC2 в тилакоид-ной мембране. Стрелками показан транспорт электронов от одной системе к другой и продукты реакций.

Рисунок 10. Круговорот углерода в природе.
Использование трансгенных растений открывает широкие возможности для исследования участия карбоангидраз в фотосинтезе.
Какими могут быть функции КА в фотосинтезе?
Известно, что ионы бикарбоната необходимы для нормального транспорта электронов на участке электронтранспортной цепи хлоропластов QA →Fe2+ → QB, где QA — это первичный, а QB — вторичный хиноновые акцепторы, причем QB расположен на акцепторной стороне фотосистемы 2 (ФС2) (рис. 9) [15]. Ряд фактов указывает на участие этих ионов в реакции окисления воды и на донорной стороне ФС2 [16]. Наличие в пигментбелковом комплексе ФС2 карбоангидраз, регулирующих поступление бикарбоната к нужному участку, могло бы обеспечивать эффективное протекание этих реакций. Уже высказывалось предположение об участии КА в защите ФС2 от фотоингибирования в условиях интенсивного освещения [16] путем связывания избыточных протонов с образованием незаряженной молекулы СО2, хорошо растворимой в липидной фазе мембраны. Показано присутствие КА в мультиферментном комплексе, осуществляющем фиксацию СО2 и связь рибулезобисфосфаткарбоксилазы/оксигеназы с мембраной тилакоидов [17]. Высказана гипотеза, согласно которой ассоциированная с мембраной КА дегидратирует бикарбонат, продуцируя СО2 [18]. Недавно показано, что внутритилакоидные протоны, аккумулируемые на свету, используются при дегидратации бикарбоната, добавленного в суспензию изолированных тилакоидов, и сделано предположение, что эта реакция может осуществляться на стромальной поверхности мембраны, если КА обеспечивает канал утечки протонов из люмена [19].
Удивительно то, что от одного кирпичика системы зависит настолько многое. И, раскрыв его местоположение и функцию, можно управлять всей системой.
Заключение
Углекислый газ для животных является неиспользуемым продуктом метаболических реакций, так сказать — «выхлопом», выделяющимся при «сжигании» органических соединений. Удивительно — растения и другие фотосинтезирующие организмы используют этот самый углекислый газ для биосинтеза практически всего органического вещества на Земле. Жизнь на нашей планете строится на основании углеродного скелета, и именно углекислый газ является тем «кирпичиком», из которого строится этот скелет. И именно судьба углекислого газа — включается ли он в состав органики или выделяется при ее разложении — лежит в основе круговорота веществ на планете (рис. 10).
- Тимирязев К.А. Жизнь растения. М.: Сельхозиз, 1936;
- Артамонов В.И. Занимательная физиология растений. М.: Агропромиздат, 1991;
- Алиев Д.А., Гулиев Н.М. Карбоангидраза растений. М.: Наука, 1990;
- Чернов Н.П. Фотосинтез. Глава: Строение и уровни организации белка. М.: Дрофа, 2007;
- Бактерии для водородной энергетики;
- Virginia Tech News: «Breakthrough in hydrogen fuel production could revolutionize alternative energy market»;
- Mershin A. (2012). Self-assembled photosystem-I biophotovoltaics on nanostructured TiO2 and ZnO. Sci. Rep. 2, 234;
- Silverman D.N. (1991). The catalytic mechanism of carbonic anhydrase. Can. J. Botany. 69, 1070–1078;;
- Ленинджер А. Основы биохимии. М,: Мир, 1985;
- Иванов Б.Н., Игнатова Л.К., Романова А.К. (2007). Разнообразие форм и функций карбоангидразы высших наземных растений. Физиология растений 54 (№ 1), 1–21;;
- Liljas A., Laurberg M. (2000). A wheel invented three times. The molecular structures of the three carbonic anhydrases. EMBO Rep. 1(1), 16–17;;
- Rudenko N., Ignatova L., Ivanov B. (2007). Multiple sources of carbonic anhydrase activity in pea thylakoids: soluble and membrane-bound forms. Photosynth. Res. 91, 81–89;;
- Fabre N. (2007). Characterization and expression analysis of genes encoding a and b carbonic anhydrases in Arabidopsis. Plant Cell Environ. 30, 617–629;;
- Флуоресцирующая Нобелевская премия по химии;
- Van Rensen J.J.S., Xu C., Govindjee (1999). Role of bicarbonate in photosystem II, the water-plastoquinone oxido-reductase of plant photosynthesis. Physiol. Plant. 105, 585–592;;
- Villrejo A., Shutova T.V., Moskvin O.V. Forssén M., Klimov V.V., Samuelsson G. (2002). A photosystem II-associated carbonic anhydrase regulates the efficiency of photosynthetic oxygen evolution. EMBO J. 21, 1930–1938;;
- Jebanathirajah J.A., Coleman J.R. (1998). Association of carbonic anhydrase with a Calvin cycle enzyme complex in Nicotiana tabacum. Planta 203, 177–182;;
- Pronina N.A., Semanenko V.E. (1984). Fiziol. Rast. 31, 241–251;
- Ignatova L.K., Rudenko N.N., Khristin M.S., Ivanov B.N. (2006). Heterogeneous origin of carbonic anhydrase activity of thylakoid membranes. Biochemistry (Moscow) 71(5), 525–532..
biomolecula.ru
Фотосинтез роль пигментов
Кроме пигментов, участвующих в фотосинтезе, у некоторых эвглен (в частности, у Euglena sanguínea) имеется в большом количестве пигмент красного цвета — астаксантин. Раствор его в масле (гематохром) выполняет роль световой ширмы: регулирует количество света, попадающего на хлоропласты. В условиях интенсивного освещения пигмент скапливается в периферической части клетки и затеняет собой хлоропласты. Клетка при этом окрашивается в различные оттенки красного цвета. При ослаблении освещенности пигмент перемещается к центру клетки, и водоросли становятся ярко-зелеными.[ ...]
Ведущая роль в функционировании пресноводных экосистем принадлежит фитопланктону, за счет фотосинтеза которого в крупных озерах и водохранилищах создается фонд органического вещества, составляющий энергетическую основу для всех последующих этапов продукционного процесса в водоеме (Винберг, 1960). К наиболее распространенным показателям, используемым при изучении планктонных альгоценозов, относятся фото-синтетические пигменты.[ ...]
Важнейшую роль в процессе фотосинтеза играет зеленый пигмент— хлорофилл. В настоящее время известно около 10 хлорофиллов. Они отличаются по химическому строению, окраске, распространению средл жвгыт организмов. У всех высших Беленых растений содержатся хлорофиллы о и Ъ. Хлорофилл с содержится в диатомовых водорослях, хлорофилл — в краспыу водорослях. В клетках пурпурных бактерий — бактерпохлорофиллы а и Ъ. Основными пигментами, без которых фотосинтез не идет, являются хлорофилл а для нелепых растений и бактериохлорофалл для бактерий.[ ...]
Желтые и оранжевые пигменты микроорганизмов — кароти-ноиды — принадлежат к наиболее распространенным и весьма часто встречающимся в микробном мире. Они представляют собой соединения с открытой цепью углеродных атомов и относятся к ненасыщенным углеводородам терпенового типа [264]. М. С. Цвет предложил их назвать каротиноидами по названию пигмента моркови каротина с эмпирической формулой С40Н56. Позже было установлено, что каротин существует в виде трех изомеров: а, ß и у-каротинов, и что они характерны для растений, животных и микробов. Из них у цианофицей обнаруживается -у-каротин (рис. 21, IV). Его функция — защита клетки от окисления; в фотосинтезе он, по-видимому, не участвует [82]. Роль у-каротина у зеленых серобактерий окончательно не выяснена. Кроме того, они содержат и другие каротиноиды, но в меньшем количестве. У других пигментных бактерий каротиноиды очень распространены. У многих бактерий, имеющих желтые, оранжевые и красные оттенки колоний, цвет колоний обусловлен наличием каротиноидов.[ ...]
Помимо хлорофилла, в процессах фотосинтеза участвуют пигменты группы каротиноидов, в состав которых входят только водород и углерод, и ксантофиллы, имеющие в составе молекул еще и кислород. Пигменты встречаются в тилакоидных мембранах всех фотоавтотрофных организмов. Каротиноиды играют роль антенных пигментов, чувствительных к солнечному свету в диапазоне волн, недоступном для хлорофилла. Они передают энергию солнечного света в центры реакций и, кроме того, как светофильтры экранируют хлорофилл в листьях, предохраняя его от фотодеструкции, фотоокисления. Этот защитный эффект связывают с наличием конъюгированных двойных связей (их может быть 9 или более), способных гасить возбужденное состояние молекул хлорофилла. Каротиноиды могут выводить кислород из находящегося в возбужденном состоянии комплекса хлорофилл — кислород, предотвращая тем самым окисление хлорофилла (его обесцвечивание). Каротин — протеиновый комплекс С550, расположенный в акцепторной части ФС II, также может участвовать в окислительно-восстановительных процессах.[ ...]
Пигментные микроорганизмы играют важную роль в освобождении пресноводных водоемов от органических веществ, а также в деструкции синтетических органических соединений в сооружениях по биологической очистке промышленных сточных вод. Пигменты, близкие по строению или идентичные пигментам зеленых растений, содержат бактерии, способные к фотосинтезу,— синезеленые бактерии, а также фототрофные, пурпурные и зеленые серобактерии.[ ...]
Микрофиты — водоросли, играющие огромную роль при формировании фитопланктона и фитобентоса. В составе этих организмов имеется хлорофилл, поэтому на сьету они осуществляют фотосинтез. Зеленые водоросли, имеющие ярко-зеленую окраску, развиваются обычно в начале лета; сине-зеленые, содержащие кроме хлорофилла еще и растворимый в воде синий пигмент — фикоциан,— преимущественно во второй половине лета; диатомовые, также содержащие наряду с хлорофиллом растворимый в воде буры» пигмент — диатомин,— ранней весной и поздней осенью. Синезеленые водоросли являются единственными организмами, потребляющими три растворенных в воде газа — азот (включая аммиак), углекислоту и кислород; при фотосинтезе они, как и все другие водоросли, выделяют в окружающую-среду кислород. Фотосинтез протекает при наличии света, углекислоты, благоприятной температуры, органических и неорганических соединений, необходимых для обмена веществ клеток водорослей. При развитии водной флоры основными биогенными элементами, необходимыми для процессов жизнедеятельности, являются углерод, азот, фосфор, калий, кальций, железо, марганец, медь, кремний и некоторые микроэлементы.[ ...]
Способность зеленых растений осуществлять фотосинтез обусловлена наличием у них пигментов. Максимальное поглощение света осуществляется хлорофиллом. Другие пигменты поглощают оставшуюся часть, преобразуя ее в различные виды энергии. В цветке покрытосеменных благодаря пигментации избирательно улавливается солнечный спектр с определенной длиной волны. Идея двух плазм в органическом мире предопределила симбиотрофное начало растений. Выделенные из всех частей растений симбиотические эндофиты класса Fungi imperfect синтезируют пигменты всех цветов, гормоны, ферменты, витамины, аминокислоты, липиды и поставляют их растению взамен полученных углеводов. Наследственная передача эндофитов гарантирует целостность системы. Некоторые виды растений имеют два вида экто-эндофитных микоризных грибов или грибов и бактерий, сочетание которых обеспечивает окраску цветков, рост и развитие растений (Гельцер, 1990).[ ...]
Использование спектрофотометрического метода дает возможность количественного определения не только основного пигмента фотосинтеза Хл а, но и других компонентов пигментного аппарата водорослей: дополнительных хлорофиллов - Ь и с, желтых пигментов каротиноидов, продуктов распада хлорофилла феопигментов. Этим показателям уделяется гораздо меньше внимания, однако каждый из них выполняет определенную роль в процессе фотосинтеза и несет важную информацию о состоянии водорослевого сообщества как элемента экосистемы. Рассмотрение всего набора пигментных характеристик в различных экологических условиях представляет интерес для более глубокого понимания особенностей функционирования альгоценозов.[ ...]
Это автотрофные фотосинтезирующие эукариотические организмы, в клетках которых в специализированных для фотосинтеза органеллах — хлоропластах — содержится зеленый пигмент — хлорофилл. Среди растений выделяют группы обитателей воды и суши. Ведущее место в водных экосистемах занимают водоросли, играющие роль продуцентов органического вещества и источников кислорода. Мельчайшие водоросли, парящие в поверхностных слоях теплых океанов, благодаря быстрому размножению и большой суммарной биомассе, являются важными поставщиками кислорода для всей атмосферы Земли. Некоторые водоросли используются в пищу животных и человека.[ ...]
Продуценты по характеру источника энергии подразделяют на фотосинтезирующие и хемосинтезирующие. Подавляющее большинство продуцентов Земли представляет собой фотосинтезирующую растительность. Фотосинтез осуществляется главным образом в зеленых растениях, содержащих в своих тканях пигмент зеленого цвета (хлорофилл), являющийся катализатором реакции синтез . Растения используют при фотосинтезе, естественно, не все поступающее солнечное излучение, а только часть спектра с длиной волны 380—710 нм. Ничуть не умаляя величайшего значения растений в существовании современной жизни на Земле, следует упомянуть о цианобактериях (синезеленых «водорослях»), которые сыграли колоссальную роль в начальной стадии эволюции жизни на Земле. Они были теми организмами, которые за счет фотосинтеза положили не только начало развитию этой ветви жизни, но и определили глобальные атмосферные и гидросферные процессы. Фотосинтез осуществляют некоторые бактерии с иным биологическим катализатором, но особенностью протекающих реакций в них является отсутствие выделяемого кислорода.[ ...]
Под водорослями, как видно из предыдущего, объединяют несколько отделов слоевцовых автотрофных растений, обычно живущих в воде. Среди водорослей можно различать три объединения отделов, характеризуемых составом пигментов, играющих роль в поглощении гии в связи с фотосинтезом.[ ...]
ru-ecology.info
Эволюция пигментной системы фотосинтеза
Эволюция фотосинтеза тесно связана со становлением его аппарата (пигментной системы, хлоропластов, листьев и т. д.).
Данные «молекулярной палеонтологии» показывают, что порфириносодержащие структуры были синтезированы из пиррольных соединений уже в процессе химической эволюции, но только с появлением живых организмов они нашли соответствующее применение в качестве хлорофиллов, цитохромов и гемоглобинов. С проникновением порфиринов в коацерваты создалась возможность для обратимых фотохимических окислительно-восстановительных реакций (А. И. Опарин, 1969). Дальнейшее усиление каталитических функций порфиринов было достигнуто путем образования комплексов с Fe, Cu, Mg, Co. К тому же порфирины, обладая антирадиационными свойствами, обеспечивали живым существам успех в борьбе за существование.
Сложен путь эволюции молекулы фоторецептора фотосинтеза. Первично хорошо растворимые в воде порфирины не могли быть включены в мембраны. Поэтому отбор пошел в направлении усиления растворимости их в липидах, что привело к уменьшению в молекуле карбоксильных групп и увеличению гидрофобных радикалов — возникают молекулы с остатком фитола. Присоединение последнего к молекуле хлорофилла и обеспечило возможность взаимодействия пигмента с липидами мембран. В то же время в ходе эволюции фототрофов происходит смена форм пигмента. У зеленых бактерий (наиболее примитивных фототрофов) преобладают бактериохлорофиллы c и d, у пурпурных бактерий — бактериохлорофиллы a и b и фитол, у цианей — хлорофилл a, у бурых и диатомовых водорослей — хлорофилл a и c, у красных — хлорофилл d. В последующем фикобилины заменяются хлорофиллом b (эвгленовые и зеленые водоросли).
Порфирины как фоторецепторы, по-видимому, предшествовали хлорофиллам. Они широко распространены у бактерий, растений и животных, пути их биосинтеза очень древние. Одна из древних форм порфиринов — уропорфирины (возникающие и абиогенно) — обладает способностью воспринимать на свету электрон от доноров. Такие порфирины, поглощая свет умеренной энергии, могли удовлетворить энергетические потребности жизни на начальных этапах ее эволюции. Но по мере увеличения суммы жизни, когда возникли дополнительные потребности в органическом веществе, этого было уже недостаточно. Для создания последнего требовалось усилить фотопоглощающую способность порфиринов, что было достигнуто отбором фототрофов на возможность включения ионов Металлов в порфириновое кольцо. Следует заметить, что порфирины имеют более выраженное химическое сродство к ионам Fe2+, Со2+ и Zn2+, чем к Mg2+. Тем не менее Mg-порфирины появляются у фототрофов предположительно несколько раньше, чем комплексы с другими металлами. Последние стали выполнять иные функции — участие в темновом транспорте электронов.
Порфирины могли синтезироваться на первичной Земле абиогенно, путем конденсации четырех молекул пиррола. В восстановленной атмосфере продуктами подобной конденсации могли быть восстановленные продукты-хлорины. Переход к окисленным формам порфиринов происходил в последующем по мере насыщения атмосферы O2.
Возникновение хлорофилла связывают с превращением уропорфирина или выработкой других путей для его биосинтеза в организме. Если принять во внимание вывод о более эволюционной древности гема, чем хлорофилла (М. Кальвин), то судьба фототрофности первично зависела от отбора организмов по способности образовывать в них комплексы порфиринов с Mg2+. Именно для них могли быть характерны наибольшие Возможности к окислительно-восстановительным превращениям порфириновых соединений.
В ходе эволюции возникает сочетание функций Mg-порфиринов и Fe-порфиронов в молекулах хлорофилла и цитохромов. Порфириновое кольцо стало основой для молекул гема и хлорофилла. Эти молекулы у животных и растений синтезируются из 5-аминолевулиновой кислоты, последняя у растений образуется из глутаминовой кислоты. У животных также около 25% аминолевулиновой кислоты образуется из глутаминовой кислоты. Итак, пути синтеза гема и хлорофилла оказываются очень сходными, что, вероятно, связано с общностью их происхождения. Есть указания и на то, что синтез гема мог служить промежуточным, этапом в реакции биосинтеза хлорофилла (Г. Гаффрон). Отбор по Mg-порфиринам среди фототрофов, кроме того, был обусловлен их способностью оставаться в возбужденном состоянии и образовывать связи с другими компонентами фотосинтетического аппарата. С возникновением фермента метилтрансферазы (S-аденозилметионин-Мg-протопорфирин-метилтрансфераза) окончательно складываются пути биосинтеза хлорофилла у фототрофов.
Порфирины принадлежат к числу наиболее стабильных органических молекул, что обусловлено их циклической структурой и энергией резонанса (38 Дж/моль). Один из представителей порфиринов — хлорофилл — способен долго сохранять энергию поглощенного кванта и передавать ее идентичной молекуле. Как указывает А. А. Красновский, благодаря этим и другим особенностям порфиринов молекула хлорофилла стала основным пигментом, участвующим в процессах фиксации энергии света.
Интересны причины, приведшие к отбору центрального металла в порфириновом кольце. В земной коре элементы встречаются в следующей убывающей концентрации: кремний (27,6%), алюминий, железо, калий, натрий, кальций, магний и титан (0,6%). Соединения кремния, алюминия и титана нерастворимы в воде, поэтому у них трудно образуются порфириновые комплексы. В воде порфириновые комплексы с натрием, калием и кальцием быстро гидролизуются. Наиболее устойчивы и активны комплексы с магнием и железом, способные к возбуждению и обратимому восстановлению или окислению.
Известно, что функцию «ловушек» фотонов выполняет не только хлорофилл, но и другие пигменты. Однако в реакционный центр фотосинтеза у растений входит главным образом хлорофилл, в частности его длинноволновые формы. Роль других пигментов (каротиноиды, фикобилины) в фотосинтезе высших растений менее значительна, они служат для удаления из системы избыточной энергии квантов коротковолнового света, что предохраняет хлорофилл от разрушения. Так, хотя каротиноиды не участвуют в первичных реакциях и фотосинтетическом транспорте электронов, они защищают фотосинтетический аппарат от деструктивного действия света. Роль каротиноидов в фотосинтезе усиливается с увеличением его спектрального диапазона (Дж. Эдвардс, Д. Уокер, 1986).
В случае ингибирования процесса биосинтеза каротиноидов специфическими ингибиторами или при возникновении соответствующих мутаций происходят необратимые нарушения фотосинтетического аппарата (А. Т. Мокроносов, В. Ф. Гавриленко, 1992). Кроме того, каротиноиды участвуют в устранении токсичности O2, процессах оплодотворения (П. М. Жуковский), защите от инфекций и т. д. Поэтому каротиноиды имеются у всех организмов. Разнообразен их состав у фототрофов: только у пурпурных бактерий их обнаружено свыше 20 (М. В. Гусев, Л. А. Минеева, 1985).
В то же время эволюция фототрофности идет в направлении усиления роли хлорофилла. Центральное положение магния в молекуле порфиринов предопределило их преимущественное использование в поглощении, запасании и преобразовании световой энергии. Как подчеркивают А. Т. Мокроносов и В. Ф. Гавриленко (1992), циклическая структура молекулы, физико-химические свойства и природа электронно-колебательных спектров, способность к обратимым окислительно-восстановительным превращениям Mg-порфиринов определили эффективность их участия в фотосинтезе; они способны с 100%-ной эффективностью преобразовывать энергию за счет только жесткой структуры самой молекулы. Начиная с эвгленовых дальнейшая эволюция фототрофности была связана с усложнением структуры молекул Mg-порфиринов и отбором в популяциях в направлении повышения роли хлорофилла в клетке, образование его комплексов с белками. Наконец, повышение эффективности фотосинтеза достигается поддержанием гетерогенности пигментной системы (включая хлорофилл) и потоком энергии от коротковолновых к длинноволновым формам пигментов.
Разнообразие состава пигментов у фототрофных организмов достаточно хорошо показано, что достигается за счет небольших модификаций боковых группировок Mg-порфиринов (хлорофилл и бактериохлорофиллы) или взаимодействием одной и той же молекулы с белковыми и липидными компонентами (А. Т. Мокроносов, В. Ф. Гавриленко, 1992). Известно более 10 нативных форм хлорофилла. Среди них различают хлорофилл a, обнаруженный у водорослей и высших растений; хлорофилл b — у зеленых, харовых, эвгленовых и высших растений; хлорофилл c — у бурых водорослей, золотистых и диатомей; хлорофилл d — у красных водорослей. Бактериохлорофиллы обнаружены у бактерий: a и b — у серных и несерных пурпурных, с и d — у зеленых серобактерий. Кроме того, у цианей и красных водорослей имеются фикоцианин и фикоэритрин. У прокариот есть также каротиноиды, ксантофиллы (лютеин, зеоксантин, виолоксантин и фукоксантин) и фикобилины (фикоцианин и фикоэритрин), причем у разных групп в разном сочетании. Бактериохлорофиллы поглощают лучи с большей длиной волны (705—1100 нм), чем. хлорофиллы. У цианей фотосинтез идет с участием хлорофилла, представленного в виде нескольких спектральных форм. У них обнаружено до 30 различных пигментов, благодаря чему цианеи способны к хроматической адаптации в условиях пещер, куда свет проникает ограниченно. В целом разнообразие состава пигментов фотосинтеза у бактерий и водорослей представляет собой приспособление к условиям с ограниченным доступом света (разнообразные водоемы с разной глубиной).
Окончательный выбор хлорофилла как фотосенсибилизатора объясняют его способностью включаться в липопротеиновые комплексы мембран (и к тому же с увеличением фотосенсибилизационной активности) и концентрироваться на мембранах (что имело значение для упорядочения функции хлорофилла). Фотосенсибилизационная активность хлорофилла в 100 раз превышает таковую у протохлорофилла. Бактериохлорофиллы не могли стать универсальными фотосенсибилизаторами для всех фототрофов ввиду низкой (7,7 Дж/моль) энергии активации по сравнению с хлорофиллом (10,5 Дж/моль). Потенциал энергии их активации оказывается недостаточен для фотолиза воды.
Указанные обстоятельства и определили первоначальное закрепление хлорофилла в роли фотосенсибилизатора. Эволюционную линию, приведшую к образованию бактериохлорофиллов, рассматривают как тупиковую в развитии фототрофности и способности выделять кислород (Р. Клейтон, 1984).
Как показал еще К. А. Тимирязев, фотосинтез осуществляется только в лучах света, поглощаемых хлорофиллом. Указав, что хлорофилл способствовал завоеванию растениями суши, он пишет: «Хлорофилловая функция должна была первоначально выработаться у первобытных морских водорослей, и именно в этой подводной флоре встречаемся с наибольшим разнообразием пигментов. Из всех этих веществ, вероятно, самое важное — хлорофилл». К важным особенностям хлорофилла, определившим его как основной пигмент фотосинтеза, принято относить его способность к окислительно-восстановительным превращениям, поглощать квант света и отдавать электрон акцептору. В клетках фотосинтезирующих тканей этот процесс завершается за доли секунд. За 1 с молекула хлорофилла в окислительно-восстановительном процессе оборачивается в 100 раз (Р. Клейтон, 1984). Поэтому, несомненно, за единицу времени и пространства органическое вещество создавали наиболее продуктивно те из фототрофов, которые использовали хлорофилл как сенсибилизатор. К другим преимуществам хлорофилла следует отнести его «настрой» на красный свет, способность удерживать поглощенную энергию и донорно-акцепторную изменчивость. Все это определило «победу» хлорофилла в энергетической конкуренции:
Для эволюционной стабилизации биомолекул (хлорофилл, родопсин, цитохромы и др.) важное значение имеет их соответствующая организация — «окружение» (Н. Т. Witt, 1983). Предполагают такие ее эволюционные этапы: трехмерное пространство → двухмерная «кювета» из жирных липидов → анизотропия в организации мембран → образование замкнутых мембранных структур (везикул). В итоге специфичность участия хлорофилла и реакций фотосинтеза характеризуется:
- наличием процессов регуляции для утилизации энергии света — кванта;
- кооцерацией функций двух фоторецепторных центров, хлорофилла a и b при переносе электронов от h3O к НАДФ+;
- направленностью потока энергии из возбужденных реакционных центров;
- возникновением циркуляции Н+ и накачки Н+;
- использованием протонного потенциала для образования АТФ;
- использованием h3O как источника электронов.
Говоря о необходимости организации биомолекул, следует обратить внимание на возникновение хлоропласта для укладки молекул хлорофилла и на усложнение структуры самой органеллы фотосинтеза.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
www.activestudy.info
Пигменты фотосинтеза
Для того чтобы свет мог оказывать влияние на растительный организм и, в частности, быть использованным в процессе фотосинтеза, необходимо его поглощение фоторецепторами-пигментами. Пигменты — это окрашенные вещества. Пигменты поглощают свет определенной длины волны. Непоглощенные участки солнечного спектра отражаются, что и обусловливает окраску пигментов. Так, зеленый пигмент хлорофилл поглощает красные и синие лучи, тогда как зеленые лучи в основном отражаются. Видимая часть солнечного спектра включает длины волн от 400 до 700 нм. Вещества, поглощающие весь видимый участок спектра, кажутся черными. Состав пигментов зависит от систематического положения группы организмов. У фотосинтезирующих бактерий и водорослей пигментный состав очень разнообразен (хлорофиллы, бактериохлорофиллы, бактериородопсин, каротиноиды, фикобилины). Их набор и соотношение специфичны для различных групп и во многом зависят от среды обитания организмов. Пигменты фотосинтеза у высших растений значительно менее разнообразны. Пигменты, сконцентрированные в пластидах, можно разделить на три группы: хлорофиллы, каротиноиды, фикобилины.
Хлорофиллы.Важнейшую роль в процессе фотосинтеза играют зеленые пигменты — хлорофиллы. Французские ученые П.Ж. Пелетье и Ж. Кавенту (1818) выделили из листьев зеленое вещество и назвали его хлорофиллом (от греч. «хлорос» — зеленый и «филлон» — лист). В настоящее время известно около десяти хлорофиллов. Они отличаются по химическому строению, окраске, распространению среди живых организмов. У всех высших растений содержатся хлорофиллы а и b. Хлорофилл с обнаружен в диатомовых водорослях, хлорофилл d — в красных водорослях. Кроме того, известны четыре бактериохлорофилла (a, b, c и d), содержащиеся в клетках фотосинтезирующих бактерий. В клетках зеленых бактерий имеются бактериохлорофиллы с и d, в клетках пурпурных бактерий — бактериохлорофиллы а и b. Основными пигментами, без которых фотосинтез не идет, являются хлорофилл а для зеленых растений и бактериохлорофиллы для бактерий. Впервые точное представление о пигментах зеленого листа высших растений было получено благодаря работам крупнейшего русского ботаника М.С. Цвета (1872—1919). Он разработал новый хроматографический метод разделения веществ и выделил пигменты листа в чистом виде. Хроматографический метод разделения веществ основан на их различной способности к адсорбции. Метод этот получил широкое применение. М.С. Цвет пропускал вытяжку из листа через стеклянную трубку, заполненную порошком — мелом или сахарозой (хроматографическую колонку). Отдельные компоненты смеси пигментов различались по степени адсорбируемости и передвигались с разной скоростью, в результате чего они концентрировались в разных зонах колонки. Разделяя колонку на отдельные части (зоны) и используя соответствующую систему растворителей, можно было выделить каждый пигмент. Оказалось, что листья высших растений содержат хлорофилл а и хлорофилл b, а также каротиноиды (каротин, ксантофилл и др.). Хлорофиллы, так же как и каротиноиды, нерастворимы в воде, но хорошо растворимы в органических растворителях. Хлорофиллы а и b различаются по цвету: хлорофилл а имеет сине-зеленый оттенок, а хлорофилл b — желто-зеленый. Содержание хлорофилла а в листе примерно в три раза больше по сравнению с хлорофиллом b.
Каротиноиды.Наряду с зелеными пигментами в хлоропластах и хроматофорах содержатся пигменты, относящиеся к группе каротиноидов. Каротиноиды — это желтые и оранжевые пигменты алифатического строения, производные изопрена. Каротиноиды содержатся во всех высших растениях и у многих микроорганизмов. Это самые распространенные пигменты с разнообразными функциями. Каротиноиды, содержащие кислород, получили название ксантофиллы. Основными представителями каротиноидов у высших растений являются два пигмента — каротин (оранжевый) и ксантофилл (желтый). Каротин состоит из 8 изопреновых остатков. При разрыве углеродной цепочки пополам и образовании на конце спиртовой группы каротин превращается в 2 молекулы витамина А. В отличие от хлорофиллов каротиноиды не поглощают красные лучи, а также не обладают способностью к флуоресценции. Подобно хлорофиллу каротиноиды в хлоропластах и хроматофорах находятся в виде нерастворимых в воде комплексов с белками.
В настоящее время установлено, что каротиноиды, поглощая определенные участки солнечного спектра, передают энергию этих лучей на молекулы хлорофилла. Тем самым они способствуют использованию лучей, которые хлорофиллом не поглощаются. Физиологическая роль каротиноидов не ограничивается их участием в передаче энергии на молекулы хлорофилла. Имеются данные, что каротиноиды выполняют защитную функцию, предохраняя различные органические вещества, в первую очередь молекулы хлорофилла, от разрушения на свету в процессе фотоокисления. Опыты, проведенные на мутантах кукурузы и подсолнечника, показали, что они содержат протохлорофиллид (темновой предшественник хлорофилла), который на свету переходит в хлорофилл а, но разрушается. Последнее связано с отсутствием способности исследованных мутантов к образованию каротиноидов. Ряд исследователей указывают, что каротиноиды играют определенную роль в половом процессе у растений. Известно, что в период цветения высших растений содержание каротиноидов в листьях уменьшается. Одновременно оно заметно растет в пыльниках, а также в лепестках цветков.
Фикобилины — красные и синие пигменты, содержащиеся у цианобактерий и некоторых водорослей. Исследования показали, что красные водоросли и цианобактерий наряду с хлорофиллом а содержат фикобилины. В основе химического строения фикобилинов лежат четыре пиррольные группировки. В отличие от хлорофилла у фикобилинов пиррольные группы расположены в виде открытой цепочки. Фикобилины представлены пигментами: фикоцианином, фикоэритрином и аллофикоцианином. Фикоэритрин — это окисленный фикоцианин. Красные водоросли в основном содержат фикоэритрин, а цианобактерий — фикоцианин. Фикобилины образуют прочные соединения с белками (фикобилинпротеиды). Связь между фикобилинами и белками разрушается только кислотой. Предполагается, что карбоксильные группы пигмента связываются с аминогруппами белка. Необходимо отметить, что в отличие от хлорофиллов и каротиноидов, расположенных в мембранах, фикобилины концентрируются в особых гранулах (фикобилисомах), тесно связанных с мембранами тилакоидов.
Фикобилины поглощают лучи в зеленой и желтой частях солнечного спектра. Это та часть спектра, которая находится между двумя основными линиями поглощения хлорофилла. Фикоэритрин поглощает лучи с длиной волны 495— 565 нм, а фикоцианин — 550— 615 нм. Сравнение спектров поглощения фикобилинов со спектральным составом света, в котором проходит фотосинтез у цианобактерий и красных водорослей, показывает, что они очень близки. Это позволяет считать, что фикобилины поглощают энергию света и, подобно каротиноидам, передают ее на молекулу хлорофилла, после чего она используется в процессе фотосинтеза. Наличие фикобилинов у водорослей является примером приспособления организмов в процессе эволюции к использованию участков солнечного спектра, которые проникают сквозь толщу морской воды (хроматическая адаптация). Как известно, красные лучи, соответствующие основной линии поглощения хлорофилла, поглощаются, проходя через толщу воды. Наиболее глубоко проникают зеленые лучи, которые поглощаются не хлорофиллом, а фикобилинами.
Дата добавления: 2015-11-04; просмотров: 423 | Нарушение авторских прав
Фотохимический этап | Цикл Кальвина можно разделить на фазы. | САМ-путь фотосинтеза | Глюкозо-6-фосфат —> фруктозо-6-фосфат | Флавиновые дегидрогеназы. | Пентозофосфатный путь дыхательного обмена | Физиологические функции ауксина. | Физиологические функции гиббереллинов. | Физиологические функции цитокининов. | Физиологические функции абсцизовой кислоты (АБК). |mybiblioteka.su - 2015-2018 год. (0.011 сек.)mybiblioteka.su