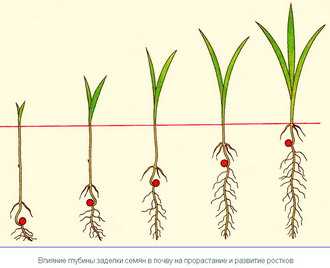
Аппаратура для приготовления гистологических срезов, размельчения тканей и перемешивания. Аппарат для приготовления тонких срезов растений
6. Приготовление срезов.
Срезы с блоков изготовляются на микротоме. Наиболее распространены микротомы санный и замораживающий. В специальных устройствах микротома зажимается парафиновый блок и микротомный нож. Существует механизм, поднимающий объектодержатель с блоком на заданное количество микрометров. Это позволяет при каждом скольжении ножа в плоскости параллельной поверхности блока получать срезы толщиной 5-10 микрометров с парафиновых блоков.
7. Окрашивание.
Изготовленные на микротоме срезы окрашиваются. Перед окраской из парафиновых срезов обязательно удаляют парафин (растворением в ксилоле).
Окрашивание необходимо производить для того, чтобы отчетливо выявить под микроскопом тонкие структуры объекта. В неокрашенных срезах большинство структур одинаково преломляет свет, поэтому рассмотреть их не удается.
Выявление на срезе гистологических структур основано на неодинаковом их отношении к красителям. Одни структуры среза вступают в реакцию с кислыми красителями и ими окрашиваются (ацидофильные, оксифильные структуры), другие реагируют с основными красителями и окрашиваются преимущественно ими (базофильные структуры). Некоторые структуры окрашиваются и кислыми и основными красителями.
По происхождению различают краски естественные, к которым относятся краски растительного и животного происхождения, и краски искусственные. Краской растительного происхождения является гематоксилин, который добывается из кампешевого дерева, растущего в Америке и в Армении.
К краскам животного происхождения относится кармин, который добывается из насекомых кошенили, живущих на кактусовых деревьях в Мексике, Армении и др. В настоящее время большинство красок готовят синтетически (искусственные краски).
По окрашиванию определенных гистологических структур различают краски ядерные (окрашивание ядра), цитоплазматические (окрашивающие цитоплазму), и специальные, окрашивающие избирательно определенные структуры.
Ядерные краски – гематоксилин, кармин, сафранин, метиленовая синь, азур, тионин.
Цитоплазматические краски – эозин, пикрофуксин.
Существуют специальные краски и реактивы: судан Ш (окрашивает жир в оранжевый цвет), осмиевая кислота (импрегнируемый ею жир окрашиватся в черный цвет), резорцинфуксин Вейгерта (дает темно-синюю окраску эластических волокон), орсеин (окрашивает эластические волокна в бурый цвет). Метиленовый синий окрашивает нервные элементы в синий цвет, а при импрегнации серебром они приобретают коричневый цвет.
Чаще всего для окрашивания гистологических срезов применяется окрашивание раствором гематоксилина (приготовленным по методу Бемера) и 1-2% эозином.
8. Заключение среза.
Окрашенные и промытые в воде срезы во избежание помутнения обезвоживают в спиртах (70º, 96º), просветляют в карбол-ксилоле, ксилоле, а затем на предметное стекло, где находится срез, помещают каплю бальзама и срез накрывают покровным стеклом. Бальзам представляет собой растворенную в ксилоле смолу одного из видов сосны, растущей в Канаде (канадский бальзам), смолу пихты (сибирский бальзам) или специальную синтетическую среду.
При исследовании биопсий с целью уточнения диагноза в гистологических лабораториях прибегают к ускоренной обработке материала. Кусочки тканей и органов при этом проходят те же этапы обработки, но за 5-7 дней. Иногда производится так называемая срочная биопсия, когда в течение 15-80 мин. материал фиксирует, получают срезы, окрашивают их и заключают. Быструю фиксацию производят в 10% формалине, подогреваемом пламенем горелки или с использованием СВЧ-печи. Уплотнения добиваются замораживанием (хлорэтилом, углекислотой или с помощью замораживающего микротома).
studfiles.net
Приготовление гистологических срезов
Изучение патологических процессов на клеточном и тканевом уровне производится при помощи микроскопических исследований. Гистологический метод исследования необходим для изучения строения и функции клеток в состоянии нормы, патологии и экспериментальном периоде. Для гистологического исследования берутся элементы тканей и органов. Толщина исследуемого образца не может превышать 1 см3.
Образцы тканей могут браться у человека сразу после смерти (чем быстрее, тем лучше) – аутопсия. Также материал может браться во время операции или непосредственно в диагностических целях при помощи специальных инструментов – биопсия.
Приготовление образцов
Приготовление образцов происходит в несколько этапов:
- Фиксация материала.
- Приготовление среза.
- Процесс окрашивания среза.
Суть фиксации материала заключается в остановке естественных процессов в тканях и клетках. Это необходимо для того, чтобы во время купировать процесс гниения и ферментативные изменения в структуре тканей.
В фиксируемых тканях за счет физико-химических процессов происходит свертывание (коагуляция) белков и липоидной составляющей. Это состояние позволяет тканям долго храниться в неизменном виде, без реакции на различные воздействия. Проще говоря, фиксация тканей проводится с целью сохранения прижизненной структуры биологического материала.
Для фиксации тканей применяются специальные жидкости (фиксаторы). Наиболее популярными фиксаторами можно назвать следующие варианты жидкостей:
- Формальдегид.
- Спирт (96, 100%).
- Осмиевая кислота.
Выше перечислены простые фиксаторы. Также для фиксации тканей применяются более сложные варианты фиксаторов (растворы):
- Спирт-формол.
- Жидкость Ценкера.
- Двухромовоокислый калий.
В списках указаны лишь некоторые виды применяемых фиксаторов. Продолжительность необходимого для фиксации образцов тканей периода может варьироваться от нескольких часов до суток. Длительность зависит от особенностей исследуемых образцов и типа выбранного фиксатора. После того как этап фиксации пройден необходимо произвести промывку материала (в течение нескольких часов) в проточной воде. Это делается для того чтобы освободить образцы от излишков фиксирующей жидкости и осадочной взвеси.

Мутные непрозрачные образцы не подходят для исследования. Такие кусочки материала не позволят получить необходимую информацию. Перед тем как приступить к одному из главных этапов – осуществлению среза, образцы промываются чистой водой в течение нескольких часов. Далее, материал подвергается процессу обезвоживания. Обезвоживание осуществляется при помощи проведения тканевого образца через спирты возрастающей крепости. Этот этап длительный. В каждом спирте кусочки материала находятся от 2-3 часов до суток.
После обезвоживания проводится заливка образцов. Этот этап необходим для уплотнения тканей и получения качественных блоков для исследования. Уплотнение проводится путем замораживания (срочная биопсия) или путем заливки парафином или целлоидином. Заливка парафином - достаточно длительная процедура (от 24 часов и дольше). Такой вариант уплотнения образцов используется для осуществления исследования в обычном режиме. Для лучшей визуализации отдельных структур тканей срезы окрашивают. Для окрашивания применяют специальные гистологические красители (кислые, основные, специальные).
Подготовленные к изучению образцы исследуют при помощи специального микроскопа.
Прежде чем приступить к изучению гистологического препарата необходимо убедиться, что последний полностью соответствует ряду обязательных требований:

- В материале должны быть сохранены прижизненные структуры.
- Срез должен быть тонким и прозрачным.
- Структуры, которые требуется подвергнуть изучению должны быть четко визуализированы за счет окрашивания.
- Препараты должны иметь длительный срок хранения.
При качественном приготовлении препарата достичь соответствия всем перечисленным требованиям достаточно просто. Однако нельзя исключить возможность возникновения небольших погрешностей. Если вовремя распознать некоторые виды неточностей, купировать брак, создать качественный материал вполне возможно.
Самыми распространенными погрешностями при приготовлении срезов можно назвать следующие варианты:
- Крошение среза.
- Выпадение материала из парафиновой массы.
- Невозможность нарезки материала.
- Разрыв материала.
Те или иные погрешности могут возникать по разным причинам. Иногда в основе нарушения качества образца лежат ошибки во время изготовления. Для устранения каждой погрешности предусмотрены определенные алгоритмы действий.
Методы гистологического исследования
Для осуществления микроскопического исследования необходимы тонкие кусочки материала. Ширина таких кусочков измеряется в микрометрах. Для удобства получения таких срезов используются специальные приборы – микротомы. Конструкция этого прибора предусматривает возможность получения срезов толщиной 5-10 микрометров.
Основным методом исследования в гистологии является микроскопия. При помощи микротома можно изготавливать тончайшие срезы, подходящие для проведения микроскопических исследований. Получение среза происходит за счет движения ножа в одном направлении. Толщина среза задается на этапе срабатывания механизма подъема.
Для изготовления срезов из материала, залитого парафином или целлоидином, используют радиальный, ротационный или санный микротом.
Для получения среза с растительных или животных тканей могут применяться специальные замораживающие микротомы. Для микроскопического исследования используется несколько методов приготовления срезов. Для каждого из методов выбираются определенные виды микротомов и применяются определенные четкие алгоритмы действий.
Гистологические срезы бывают:
- Ступенчатые.
- Серийные.
- Горизонтальные.
Могут производиться срезы фиксированного и нефиксированного материала. Все зависит от характера исследуемых тканей и основных целей проведения означенного исследования. Также в гистологии существуют другие методы приготовления срезов.
Микротомы и их применение
Как уже было сказано выше, срезы в гистологии создаются при помощи специального устройства – микротома. В самом названии заложена расшифровка предназначения прибора – micros (маленький), tome (рассечение). Одним из самых используемых можно назвать санный микротом.
Название прибора произошло от принципа работы механизма, который базируется на подаче ножа с зажимом при помощи специальных салазок. Санный микротом предназначен для осуществления парафиновых срезов. Как правило, такой прибор работает с одноразовыми лезвиями или кассетами. Такой высокоточный микротом состоит из станины, механизма микроподачи, подъемного механизма, зажимов для блоков, ножедержателя.
Такой аппарат позволяет изготавливать срезы толщиной от 0,5 до 60 микрометров. Санный микротом отличается высокоточной регулировкой толщины среза. Функция подачи материала может быть механической или ручной. Данный прибор предназначен для осуществления рутинных исследований в области медицины, ботаники и биологии.
Ротационный микротом - прибор с неподвижным ножом и подвижным столиком. В приборе предусмотрена моторизованная подача образца. Этот микротом предназначен для использования в гистологической лаборатории для проведения исследований, направленных на решение гистологических и гистопатологических задач.
Для получения срезов с нефиксированных тканей или в тех случаях, когда необходимо срочное проведение исследования используются замораживающие микротомы. Такие приборы снабжены замораживающим столиком, на котором и закрепляется исследуемый образец. Главным правилом успешного получения гистологического среза при помощи микротома является правильный выбор угла наклона ножа и угла сечения. Наилучшим углом наклона является тот, при котором плоскость лезвия находится параллельно верхней части блока.
Если выбрать угол наклона больший, чем требуется, образуется риск, что срез будет крошиться. При меньшем угле наклона лезвие будет скользить по поверхности материала. Получение требуемого результата при таком положении ножа невозможно. Величина угла сечения зависит от характера исследуемого материала. Чем образец мягче, тем меньше будет угол резания. При обработке мягких блоков неплохим вариантом считается косое расположение ножа.
Резание на микротоме
Для приготовления срезов с парафинированных объектов или образцов, обработанных целлоидином, опять же чаще всего используют ротационный микротом.
Сначала блок подвергают обрезке. Это необходимо для устранения свободного парафина или другого уплотнителя. Если эту процедуру не произвести, срез может получиться неравномерным, морщинистым и, как следствие, малоинформативным. Также сморщивания можно избежать при помощи охлаждения исследуемого материала.
Далее, парафиновый блок прочно закрепляется в зажиме. Предварительно необходимо выверить правильный угол расположения ножа и выбрать необходимый угол резания. После этого нужно используя регулировку механизма подачи, установить блок так, чтобы его поверхность находилась от лезвия ножа на расстоянии 0,5-1 мм.
После осуществления подгонки проводится установка микрометрической шкалы для получения первых толстых срезов. После этого производится моделирование блока (срезка излишков парафина, предание прямоугольной формы). Заключительным этапом является выставление микрометрической шкалы на задуманную толщину и осуществление окончательной резки материала.
www.rumex.ru
Приготовление гистологических срезов — Практика гистолога
(Микроскопическая техника: Руководство / Под редакцией Д.С.Саркисова и Ю.Л.Перова. — М.: Медицина, 1996. ISBN 5-225-02-820-9).
Для получения гистологических срезов применяют специальные микротомные ножи, различающиеся по форме, длине и углу сечения лезвия. По форме они представляют собой сложный стальной клин, у которого режущий край имеет дополнительную клиновидную заточку. Длина ножа может составлять от 8 до 50 см.
По конфигурации лезвия различают три группы микротомных ножей: А, В и С. У микротомных ножей, относящихся к группе А, одна поверхность ровная, а другая вогнутая (их называют плоско-вогнутыми с большой кривизной вогнутой поверхности). Эти ножи чаще всего изготовлены из мягкой или относительно мягкой стали и предназначены для резки объектов, залитых в целлоидин.
Ножи, относящиеся к группе В, называются плоско-вогнутыми, но кривизна вогнутой поверхности у них значительно меньше, чем у ножей группы А. Они изготовлены из более твердой стали, используют их для приготовления целлоидиновых и целлоидин-парафиновых срезов.
У ножей, относящихся к группе С, обе поверхности клинка плоские. Их изготавливают из твердой стали и применяют для резки объектов, залитых в парафин, а также для получения срезов на замораживающем микротоме.
Кроме того, для приготовления парафиновых и полутонких срезов на микротомах и ультратомах используют металлические магнитные лезвия и стеклянные ножи. Металлическое магнитное лезвие (одноразовый нож)позволяет получить срезы с 50-60 парафиновых блоков, затем лезвие меняют.
ЗАТОЧКА МИКРОТОМНЫХ НОЖЕЙ
Получить качественные гистологические срезы при целлоидиновой, целлоидин-парафиновой и парафиновой заливке материала можно с помощью микротомного ножа, толщина лезвия которого должна быть от 3 до 5 мкм. Для работы на замораживающем микротоме необходимо иметь острый нож без зазубрин на лезвии. Нож необходимо своевременно точить, а перед каждой резкой объектов править.
Микротомные ножи затачивают с помощью специальных аппаратов, например «Sakura» (Япония). Однако до сих пор не потеряла актуальности и применяется во многих лабораториях ручная заточка ножей. Вручную микротомные ножи точат на камне, имеющем форму бруска. Желтый, так называемый бельгийский каменьиспользуют для заточки первым, затем продолжают заточку на белом камне (арканзасе), который имеет более мелкую зернистость. Можно использовать природный аспидный камень, который также имеет крупнозернистую и мелкозернистую поверхность.
Перед заточкой на поверхность камня наносят машинное масло или керосин, глицерин, разведенный 70 % спиртом (1:1), мыльную воду. На спинку ножа надевают специальный обушок (желательно постоянно используемый для заточки одних и тех же ножей — это определяет угол заточки), а в стержень или отверстие в торцевой части ножа вкручивают ручку. Затем нож кладут обушком на камень, по которому скользит и лезвие под действием собственной тяжести. Нож проводят по камню с одного конца на другой, а затем, поворачивая через обушок, осуществляют движение в обратном направлении.
Продолжительность процесса зависит от квалификации лаборанта и состояния режущей кромки ножа. В среднем она составляет от 30 мин до 1 ч. Периодически контролируют качество заточки, осторожно укладывая нож на предметный столик микроскопа и перемещая его так, чтобы режущая кромка проходила через поле зрения при малом увеличении. Затем нож правят на широком ремне, натянутом на деревянную колодку. Правку проводят так же, как и заточку (через обушок).
МИКРОТОМЫ И ОСОБЕННОСТИ РАБОТЫ НА НИХ
Микротомы — это приборы, с помощью которых получают срезы тканей, залитых в различные среды, а также замороженных и нефиксированных. Микротомы позволяют получать гистологические срезы различной толщины. По принципу действия различают санные, ротационные, замораживающие микротомы, а такжекриостаты и вибратомы.
Санные микротомы характеризуются горизонтальным движением ножа и вертикальным подъемом блокодержателя. Их с успехом используют для резки объектов, залитых в целлоидин, целлоидин-парафин и парафин. Основные части микротома располагаются на специальных салазках, отсюда происходит его название. Принцип работы санного микротома заключается в том, что при обратном ходе ножа ножевые салазки толкают стержень со шкалой регулятора подачи, вызывая его перемещение. Движение стержня передается на тягу, которая с помощью «собачки» поворачивает храповик. Вращение храповика передается микровинту, который с помощью разъемной гайки перемещает салазки с блоком вверх. С каждым срезом блок поднимается все выше на расстояние, соответствующее толщине среза. После того как блокодержатель достигнет высшей точки, с помощью разъемной гайки надо опустить салазки с механизмом в крайнее нижнее положение. Существуют другие разновидности санных микротомов с различными вариантами способов подачи, зажимов для ножей и т.д.
Ротационные микротомы предназначены для резки парафиновых блоков, с их помощью можно получать серийные срезы. Важнейшая часть ротационного микротома — механизм микроподачи, который включает в себя храповик, дифференциальный механизм, микровинт, лимб, косозубую передачу и кулачок. Приводной механизм при повороте вала с помощью «собачки» поворачивает на заданное количество зубьев храповик, на оси которого находится зубчатое колесо, передающее через шестерню вращение микровинту. Винт перемещает каретку подачи объектодержателя. Толщина срезов устанавливается поворотом лимба.
Объектодержатель ротационного микротома — винтовой зажим, вмонтированный в шаровую оправу каретки подачи. Шарнирный механизм позволяет подать блок под любым углом. Объектодержатель фиксируется в зажиме специальной рукояткой.
Держатель для ножа — массивная подставка с двумя вертикальными стойками, в которые вмонтированы двигающиеся держатели, приспособленные для установки ножа под нужным углом. Фиксация ножа осуществляется винтами. В переднезаднем направлении нож перемещается по специальным направляющим с помощью винта. Постепенно приближая нож к объекту и одновременно поворачивая колесо подачи, подравнивают площадь резания, а затем нож фиксируют.
Ротационные микротомы снабжены специальной транспортной лентой, на которую с ножа попадает полоска (серия) срезов. На ленте их разделяют препаровальными иглами и производят дальнейшие манипуляции. Снимать срезы с ножа ротационного микротома можно кисточкой или препаровальной иглой.
Замораживающие микротомы используют для резки не залитых, но фиксированных объектов, материала, залитого в желатин и водорастворимые пластмассы. Особенно широко применяются замораживающие микротомы для изготовления препаратов при исследовании материала срочных биопсий. По своей конструкции замораживающие микротомы относятся к микротомам санного типа, но в их устройстве есть некоторые особенности. Станина имеет приспособление для крепления к столу. Нож устанавливают под нужным углом в подвижной ручке с помощью одного или двух зажимов. Автоматическая подача осуществляется при каждом размахе ручки с ножом
через систему рычагов. Замораживающий столик снабжен приспособлением для подачи углекислоты или охлаждается термоэлектрически с помощью полупроводниковых элементов.
Криостаты, вибратомы. С развитием гистохимии ферментов и иммуноморфологии возникла необходимость в обработке нефиксированного материала, которая была реализована с помощью специальных приборов — криостатов. Позднее появились криокиты и вибратомы.
Криостат — специализированная холодильная камера с установленным в ней микротомом, в которой имеются отверстия для рук, люминесцентная лампа и смотровое стекло. Надежная изоляция позволяет поддерживать в криостате температуру от -5 до -25 °С. Отрицательными моментами при работе с криостатом являются значительное переохлаждение рук оператора, недостаточная освещенность рабочего поля, а также невозможность ориентировать объект относительно кромки ножа. Эти недостатки практически устранены вкриокитах зарубежного производства, управление которыми вынесено за пределы морозильной камеры. В них можно отдельно регулировать температуру объекта и ножа. Через 3-5 мин после включения прибора достигается низкая температура, причем охлаждение возможно до -65 °С, что предотвращает образование кристаллов в тканях.
Уход за микротомами и микротомными ножами. Все скользящие поверхности микротомов должны быть чистыми и смазаны тонким слоем машинного или вазелинового масла. При постоянной работе на микротоме все скользящие поверхности необходимо один раз в неделю протирать тряпочкой, смоченной бензином или толуолом, и смазывать. После окончания работы на микротоме объектодержатель и станину очищают от остатков парафина, предварительно вынув микротомный нож и убрав его в футляр. Микротомные ножи никогда не оставляют в микротоме или на рабочем столе! Замораживающие микротомы и криостаты через 30 мин после выключения вытирают насухо и винтовую подачу смазывают вазелиновым маслом.
РЕЗАНИЕ ПАРАФИНОВЫХ БЛОКОВ НА САННОМ МИКРОТОМЕ
Парафиновый блок, наклеенный на деревянную колодку или без нее (с большим слоем парафина), зажимают в объектодержатель. Установив нужный угол наклона ножа (оптимальный 13-15°) в зависимости от плотности ткани, медленно подводят нож к блоку, регулируют его высоту до соприкосновения с ножом. Сначала выравнивают поверхность блока, установив микрометрическую шкалу на получение толстых (20-25 мкм) срезов, затем шкалу переводят на б -8 мкм и приступают к резанию материала. Как правило, нож располагается перпендикулярно, но возможно также получение срезов (особенно с более плотных объектов) ножом, который установлен под углом к станине микротома.
Срезы с блока осторожно снимают с помощью сухой или смоченной в спирте кисточки, используют также изогнутую препаровальную иглу или скальпель. Срезы обычно переносят в коробку, дно которой выстлано бумагой черного цвета, и укладывают матовой стороной вверх. После получения нужного количества срезов рядом с ними кладут блок или этикетку с номером. Удобнее сразу обработать 20-30 блоков, а затем приступить к монтированию срезов на предметные стекла.
Часто срезы наклеивают на предметное стекло непосредственно с ножа. Для этого их переносят в склянку с теплой (35-40 °С) дистиллированной или кипяченой водой, а затем вылавливают на предметные стекла, которые предварительно обезжиривают и натирают белком с глицерином. Срезы приклеивают на предметное стекло блестящей, обращенной к ножу стороной. Небольшие складочки на срезе можно расправить, осторожно дотрагиваясь до них углом согнутой препаровальной иглы.
Можно расправлять срезы непосредственно на стекле с помощью специального приспособления для сушки и расправления парафиновых срезов. Для этого на предметное стекло пипеткой наносят каплю воды и в нее опускают срез. Стекло со срезом помещают на нагреваемый столик прибора, где срез постепенно расправляется. После удаления избытка воды пипеткой или фильтровальной бумагой стекло со срезом подсушивают и одновременно срез плотно фиксируется на предметном стекле. На нагреваемом столике прибора помещается одновременно 45 предметных стекол, при его использовании не требуется дальнейшего просушивания стекол со срезами в термостате. Имеются специальные импортные ванночки для расправления срезов и переноса их на стекло. В них постоянно поддерживается оптимальная температура воды 38 °С.
Продолжительность просушивания срезов в термостате при 37 °С 6-12 ч. В случае необходимости проведения срочной окраски срезы можно поместить на 10-15 мин в термостат при 56 °С до начала плавления парафина, что способствует лучшей фиксации среза на предметном стекле. Однако при этом несколько затрудняется депарафинирование: требуется применение дополнительной порции ксилола и увеличение продолжительности депарафинирования.
Существует сухой способ приклеивания срезов к стеклу, который пригоден только для срезов отличного качества. На предметное стекло, смазанное тонким слоем белка с глицерином, помещают срез, аккуратно расправляют его препаровальной иглой или скальпелем и слегка подогревают на спиртовке или нагреваемом столике.
ПРИГОТОВЛЕНИЕ ЦЕЛЛОИДИНОВЫХ СРЕЗОВ
Для приготовления целлоидиновых срезов используют ножи типа А и Б. Целлоидиновые блоки закрепляют так же, как и парафиновые. После установки ножа в микротом к нему пододвигают объектодержатель с укрепленным в нем блоком. Выравнивают поверхность блока до тех пор, пока полностью не обнажится ткань кусочка, а затем приступают к приготовлению срезов желаемой толщины. Во время резания нож и объект обильно смачивают 70 % или 80 % спиртом, пользуясь кисточкой. Нож по салазкам микротома ведут плавно, без давления. Полученный срез расправляют на ноже с помощью кисточки, после чего срез снимают с ножа на подушечку указательного пальца, подложенного под нож. Срезы кладут в склянки с 70 % спиртом.
ПОДГОТОВКА ПРЕДМЕТНЫХ СТЕКОЛ
Предметные стекла, применяемые для получения гистологических препаратов, необходимо предварительно подготовить.Исключение составляют готовые к использованию и специально упакованные импортные предметные стекла.
Предметные стекла моют в теплой мыльной воде или кипятят в 2-3 % растворе гидрокарбоната натрия, затем ополаскивают горячей водой и промывают в течение нескольких часов в проточной воде. Вымытые стекла протирают чистой хлопчатобумажной тканью и на несколько дней помещают в смесь Никифорова: 96 % спирт и эфир (1:1). Обезжиренные стекла извлекают пинцетом из этой смеси, протирают чистой тканью и складывают в коробочку.
Для обезжиривания предметных стекол используют также хромовую смесь, в состав которой входят 100г бихромата калия, концентрированной серной кислоты и 1000 мл горячей воды. Бихромат калия растворяют сначала в горячей воде, затем раствор охлаждают и после этого по стеклянной палочке осторожно по каплям добавляют серную кислоту. Стекла выдерживают в хромовой смеси 2-3 дня, а затем тщательно промывают в проточной воде в течение 1-2 дней.
Предметные стекла также хорошо обезжириваются в крепком растворе соляной кислоты. Через несколько суток их промывают проточной водой и высушивают.
Качество обезжиривания можно проверить, капнув на предметное стекло воду из пипетки: по обезжиренному стеклу вода растекается тонким слоем, а не собирается в каплю.
Для лучшей фиксации срезов на стекле его предварительно смазывают смесью белка с глицерином. Свежий яичный белок взбивают и фильтруют через крупнопористый фильтр, смоченный дистиллированной водой, затем размешивают с равным объемом глицерина и добавляют несколько кристаллов тимола. Смесь хранится в течение нескольких месяцев. Применяют также смесь, в состав которой входят 15 мл сыворотки крови, 5 мл дистиллированной воды и 6 мл 5 % формалина. После фильтрации смесь готова к нанесению на предметные стекла. Ее использование дает лучшие результаты, чем применение яичного белка, так как при окрашивании не образуется фон.
Разработан способ фиксации среза к предметному стеклу без предварительного натирания последнего белком с глицерином. В ванночку с теплой дистиллированной водой капают несколько капель жидкого казеинового клея и перемешивают. В полученную мутноватую жидкость опускают срезы, расправляют препаровальной иглой и вылавливают на чистое обезжиренное стекло. Этот способ дает неизменно хороший эффект и вокруг среза отсутствует окрашенный фон, как это часто бывает при применении белка.
practicagystologa.ru
5. Технологии приготовления временных и постоянных препаратов биологических объектов для проведения световой микроскопии.
1) Временные препараты
Для изучения растительных объектов с помощью светового микроскопа необходимо приготовить микропрепарат. Микропрепараты, не предназначенные для длительного хранения, называются временными. Изучаемый объект помещают на предметное стекло в каплю воды, глицерина, раствора, реактива или красителя и накрывают покровным стеклом. Такие препараты можно хранить в течение нескольких дней, поместив во влажную атмосферу.
2) Постоянные препараты
Постоянные препараты готовятся по специальным методикам, обеспечивающих их хранение в течение десятков лет. К постоянным препаратам относятся мазки, тотальные препараты и срезы. Мазки используются при изучении клеток крови, культур микроорганизмов, изолированных тканевых клеток. Тотальные препараты представляют собой отдельные прозрачные и тонкие объекты Учебные срезы можно сделать вручную, с помощью бритвы. Однако качественные срезы с заданной толщиной 10...22 микрометра обычно изготавливают с помощью специальных приборов – микротомов. Такие срезы часто называют микротомными препаратами. Для получения более тонких срезов (0,01...0,05 мкм, или 10...50 нанометров) используют ультрамикротомы.
Кратко рассмотрим основные этапы приготовления постоянных препаратов.
1.Фиксация материала. Сразу после окончания фиксации производится промывка материала или водой (после водных фиксаторов), или 80%-нымспиртом (после спиртовых фиксаторов). Количество смен промывных жидкостей – не менее 3. Время – до 24 часов.
2.Обезвоживание в спиртах возрастающей концентрации. Параллельно происходит уплотнение материала. Последовательное перемещение материала через ряд растворов называется проводка. После водных фиксаторов используется 8 смен спирта: 20%, 40%, 80%, две смены по 96%, две смены по 100%. После спиртовых фиксаторов – 4 смены спирта : две смены по 96% и две смены по 100%. В каждой смене материал выдерживается по 1 часу.
3.Просветление. Это пропитывание материала растворителем парафина – ксилолом (бензолом, хлороформом). Образец помещается на 1 час последовательно в каждый из последующих растворов: 3 части спирта + 1 часть ксилола, затем 2 части спирта + 2 части ксилола, затем 1 часть спирта + 3 части ксилола, затем две смены ксилола.
4.Заливка в парафин. Это замещение ксилола парафином. Образец помещают в смесь ксилола и парафина при температуре 55...57 градусов и оставляют в термостате при этой температуре до полного испарения ксилола (от нескольких часов до нескольких суток). Затем при температуре 55...57 градусов производится проводка через парафин I (6...12 часов), парафин II (6...12 часов) и заливка в парафин III. Парафины I, II, III отличаются только чистотой: парафин III – это окончательная среда, которая должна обладать наибольшей чистотой. В итоге получаются парафиновые блоки, в которых заключены образцы материала. Эти блоки можно резать в любом направлении.
5.Окрашивание срезов. Парафиновые срезы наклеивают на чистое предметное стекло. В качестве клея можно использовать смесь белка куриного яйца с глицерином (в соотношении 1 : 2) с добавлением антисептика (тимола или фенола). Обычно производят депарафинирование срезов. Для этого стекла с наклеенными срезами проводят через ксилол, спирты убывающей концентрации (100%, 96%, 80%, 70%) и дистиллированную воду. Время нахождения в каждой среде – 2...3 минуты. Далее окрашивают согласно методикам.
6.Обезвоживание и просветление окрашенных срезов. Выполняется путем проводки через спирты возрастающей концентрации, а затем через ксилол.
7.Заключение в среды (заливка). Для длительного хранения препаратов их необходимо заключить в среду, предохраняющую препарат от окисления воздухом и от поражения грибками. Для заливки используются специальные смолы (канадский бальзам, пихтовый бальзам), которые растворяют в ксилоле до консистенции жидкого меда. Каплю такого раствора наносят на срез и покрывают покровным стеклом.
6. Химический состав клеточного вещества. Микро и макроэлементы.
В составе клетки обнаружено более 80 химических элементов, при этом каких-либоспеуиальных элементов, характерных только для живых организмов, не выявлено. Однако, только в отношении 27 элементов известно, какие функции они выполняют. остальные 53 элемента, вероятно, попадают в организм из внешней среды.
По содержанию элементы, входящие в состав клетки, можно разделить на три группы:
1. Макроэлементы
Они составляют основную массу вещества клетки. На их долю приходится около 99% массы всей клетки. Особенно высока концентрация четырех элементов: кислорода (65-75%),углерода(15-18%),азота(1.5-3%)и водорода(8-10%).К макроэлементам относят также элементы, содержание которых в клетке исчисляется десятыми и сотыми долями процента. Это, например, калий, магний, фосфор, сера, железо, хлор, натрий.
2. Микроэлементы К ним относятся преимущественно атомы металлов, входящие в состав ферментов, гормонов и
других жизненно важных веществ. В организме эти элементы содержатся в очень небольших количествах: от 0,001 до 0,000001%; в числе таких элементов бор, кобальт, медь, молибден, цинк, йод, бром и др.
3. Ультрамикроэлементы
Концентрация их не превышает 0,000001%. К ним относят уран, радий, золото, ртуть, бериллий, цезий и другие редкие элементы. Физиологическая роль большинства этих элементов в организмах растений, животных, грибов и бактерий пока не установлена.
studfiles.net
Аппаратура для приготовления гистологических срезов, размельчения тканей и перемешивания
Для приготовления срезов исследуемых под микроскопом образцов тканей служат специальные аппараты — микротомы, диапазон применения которых очень широк. Аппараты этого типа могут использоваться для изготовления срезов с весьма твердых предметов (кость, рог, дерево) и различных мягких тканей растительного и животного происхождения.
В Советском Союзе и зарубежными фирмами выпускаются различные модели микротомов, позволяющие получать срезы различной толщины (вплоть до ультратонких, необходимых для электронной микроскопии) с тканей, залитых в парафин или целлоидин, а также с нативных тканей, подвергнутых замораживанию.
Одним из наиболее распространенных типов микротомов является санный микротом. В большинстве санных микротомов нож, скользящий по направляющим, надвигается на объект. В некоторых моделях имеется неподвижно закрепленный нож, на который надвигается зажим с материалом. Этот тип микротомов наиболее удобен для приготовления серийных срезов.
Как уже упоминалось, для получения срезов часто прибегают к замораживанию образцов. Замораживание осуществляют либо с помощью жидкой углекислоты, подводимой к столику микротома из баллона с углекислотой, либо на замораживающих столиках, охлаждение которых осуществляется полупроводниковым термоэлементом. В некоторых моделях охлаждается также и нож, что в ряде случаев позволяет готовить препараты из нефиксированного материала.
Относительно новыми аппаратами являются ультрамикротомы, позволяющие готовить срезы толщиной 0,05—0,1 мкм, что дает возможность использовать их для изготовления образцов, необходимых при проведении электронномикроскопических исследований.
К большинству микротомов обычно прилагаются ножи, которые по характеру лезвия и направлению действия обозначаются буквами а, в и с. Лезвие ножа а — плосковогнутое, лезвие ножа в тоже плосковогнутое, но вогнутость его менее выражена. Нож с имеет плоское лезвие. Нож а служит для приготовления срезов из сравнительно мягкого материала. Нож c употребляется для резки парафиновых, целлоидинпарафиновых и, в некоторых случаях, целлоидиновых блоков. Нож с используют при работе на замораживающем микротоме и для резки целлоидиновых блоков и плотного материала, залитого в любое вещество. В ультрамикротомах применяются специальные стеклянные или алмазные ножи.
www.medical-enc.ru
§3. Методы получения ультратонких срезов
а) Способы фиксации и заливки биологических объектов
Основная цель фиксации - сохранить объект в таком состоянии, которое правильно бы отражало прижизненное состояние объекта. "В настоящее время в практике электронной микроскопии применяют химические способы фиксации. По способу действия на живые структуры все химические фиксаторы разделяют на две группы:
1) фиксаторы, осаждающие (коагулирующие) белки - спирты, уксусная и пикриновая кислоты, соли тяжелых металлов, которые в основном применяют в световой микроскопии;
2) фиксаторы, стабилизирующие липиды - четырехокись осмия, формалин, перманганат калия.
Для фиксации клеток из культур микроорганизмом, выращенных на плотных и жидких средах, применяют 1%-ный раствор KMnO4 приготовленный на ацетат-вероналовом буфере. При фиксации бактериальных клеток по Ритер-Келленбергер применяют стандартный раствор: 1% OsO4 в ацетат-вероналовом буфере (рН=6,0), в котором фиксатором является осмий.
После фиксации производят обезвоживание. В качестве обезвоживающих веществ используют этиловый спирт, метиловый спирт и ацетон, которые берут в возрастающих концентрациях (30°, 50°, 700 , 96°, 1000).
После обезвоживания объекты заключают в пластмассы или другие среды. Так как оптимальная толщина срезов должна быть не более 250-800 А, то необходимо, чтобы заливочный материал обладал определенной твердостью и другими свойствами. Для этих целей используют пластические массы - метакрилаты, эпоксидные смолы.
В практике электронной микроскопии чаще используют метакрилаты: бутилметакрилат и метилметакрилат. Бутилметакрилат полимеризуется в сравнительно мягкие блоки, поэтому к нему прибавляют 10-20% метилметакрилата. В качестве катализатора применяют 1-2%-ную перекись бензоила. Заливочную смесь (рабочую) заливают в желатиновые капсулы, где происходит полимеризация ее при 600 в течение 48 часов.
б) Приготовление стеклянных ножей
Одним из самых важных этапов при получении ультра тонких срезов является процесс приготовления стеклянного ножа. Стеклянные ножи готовят из полос специального (зеркального) стекла, толщина которого должна быть 5 мм. Из такой полосы приготавливают квадраты размером 3x3 см, для чего стеклорезом вначале делают нарезки и по нарезу обламывают клетки-квадраты. Затем приготовленный квадрат надрезают по диагонали и разламывают.
Насечки стеклорезом производят таким образом, чтобы они не доходили до края стекла на 2-3 мм. После разламывания квадрата по диагонали с помощью лупы просматривают получившиеся лезвия. Обычно нож получается несколько неровным и только небольшая его , часть имеет ровный участок, который и используется в качестве лезвия.
В настоящее время промышленностью выпускается специальный прибор - станок для изготовления стеклянных ножей (ССН-1), который значительно облегчил процесс изготовления ножей. После изготовления ножа на нем укрепляют ванночку из лейкопластыря, и нож с ванночкой устанавливают в микротом.
Демонстрация приготовления стеклянных ножей с помощью прибора ССН-1.
в) Ознакомление с устройством ультрамикротома и получением ультратонких срезов
Незначительная проникающая способность электронов даже при больших ускоряющих -напряжениях требует изготовления сверхтонких срезов. Ультратонкие срезы получают на специальных приборах, называемых ультрамикротомами. В современных микротомах применяется тепловая подача металлического стержня, а через него и блока (объекта) по отношению к ножу. Для подготовки препарата к резанию необходимо, чтобы полушаровидныи конец цилиндрического блока был заточен в виде пирамидки, содержащей объект. Все операции по заточке блока производят под бинокулярной лупой МБС-1 или МБС-2. После подготовки блока к резке , его устанавливают в микротом таким образом, что после включения последнего блок начинает двигаться по отношению к неподвижно закрепленному ножу. Получающиеся при микротомии ультратонкие срезы остаются в ванночке ножа, которая предварительно заполняется дистиллированной водой. Срезы свободно плавают на поверхности жидкости. Когда срезов накапливается достаточное количество, их собирают на сетке (прикосновением к поверхности жидкости).
studfiles.net
Приготовление препаратов для микроскопии в домашних условиях
Приготовление препаратов для микроскопии в домашних условиях Происхождение микропрепаратов берет начало в использовании слоновой кости или обычной кости в качестве подставки под образцы, которые помещались между дисками прозрачной слюды. Подобная конструкция была популярной в викторианской Англии, пока Королевское Микроскопическое Общество не представило стандартизированное предметное стекло для микроскопа.
Термины и определенияГистологический препарат: Тонкий срез биологического объекта, доступный для изучения в проходящем свете микроскопа, окрашенный контрастными красителями для выявления его структур и помещенный на предметное стекло.
Микропрепарата гистологическийПредметное стекло, на котором расположен окрашенный в большинстве случаев, срез ткани, для микроскопического исследования.
Способы приготовления микропрепаратов по биологииМикропрепарат, представляет собой тонкий срез органа живого организма или объекта не живой природы, заключенный в прозрачную среду, чей индекс преломления равен индексу преломления стекла, или близок к этому (показатель преломления предметного стекла n=1,515). Объект исследования, обычно помещается между предметным и покровным стеклами, пространство между которыми заполняется средами с индексом преломления близким к стеклу. Наиболее частой средой, используемой в отечественной практике для заключения и хранения окрашенных гистологических препаратов, являются канадский или пихтовый бальзамы, представляющие собой растворы натуральных смол в ксилоле. А так же полистирол растворенный в ксилоле с добавлением, пластификатора, который после высыхания образует прозрачную пленку. Микропрепараты позволяют демонстрировать внутреннее клеточное строение организмов, что помогает формировать знания о едином клеточном строении организмов.
Микропрепараты можно разделить на две группы: постоянные, изготовленные по смециальной методике, которая позволяет сохранить объект очень продолжительное время, без каких либо видимых изменений в структуре объекта; временные, приготовленные непосредственно перед наблюдением под микроскопом с целью однократного пользования. Постоянные микропрепараты представляют собой тончайшие срезы тканей организмов, их органов. Клетки в большинстве своем не имеют окраски и потому, даже при большом увеличении микроскопа, бывает трудно рассмотреть внутриклеточные структуры, в том числе ядро. В связи с этим микропрепараты тканей окрашивают специальными красителями для придания им большей наглядности. Временные препараты так называются потому, что не сохраняются долго. После ознакомления с микрообъектом временный препарат смывается с предметного стекла. Для изучения живых клеток микроорганизмов применяют препараты “раздавленная капля”, “висячая капля”, “отпечаток”, “агаровая пленка” (“микрокультура”). Препараты живых клеток рассматривают с “сухими системами ” микроскопа. Препараты, работа с которыми уже закончена, прежде чем вымыть, выдерживают в дезинфицирующем растворе, если эти ткани принадлежали животным[4]. Микропрепараты позволяют проводить широкий ряд опытов по биологии Требования к микропрепаратам: Стекла должны быть бесцветными и прозрачными. Покровное стекло должно быть толщиной равной 0,17мм, предметное стекло толщиной в 1,0-1,2 мм которое служит основой изделия. Микроскопические срезы должны быть как можно тоньше, к сожалению, без специального прибора-микротома, изготовить достаточно тонкий срез исследуемого объекта весьма трудно, а иногда и невозможно. В некоторых случаях приготовление препаратов несложно, в других — требует специальной техники. Микропрепараты должны отвечать определенным требованиям, которые необходимо тщательно соблюдать. Для приготовления постоянных микропрепаратов необходимо специальное оборудование.
Оборудование, необходимое для приготовления микропрепаратов Рабочий стол. При отсутствии специального стола с успехом может быть приспособлен любой стол (желательно с ящиками) с площадью рабочей поверхности не менее 60*120см. Если крышка стола не имеет специального покрытия, то его следует сделать из какого-либо влагоустойчивого материала. Однако участок стола, предназначенный для непосредственной работы по приготовлению препаратов, в любом случае необходимо накрыть стеклом и расположить под ним небольшие (9*12см) листы белой или черной бумаги. Этим создается соответствующий фон, облегчающий работу с окрашенными (белый лист) и не окрашенными (черный лист) объектами. Рекомендуется также на оба листа нанести контуры предметного стекла с обозначением места расположения и размеров покровного стекла. Для того, что бы удобнее расположить необходимое оборудование, следует иметь двухъярусную полку для реактивов, растворов и посуды, которая устанавливается либо перед работающим (вдоль заднего края стола), либо сбоку в зависимости от расположения стола относительно источника света.
Лабораторная посуда. Широкогорлые банки с притертыми пробками различной вместимости от 50 до 200 мл – используют для составления гистологических батарей, предназначенных для подготовки кусочков тканей к заливке различными средами. Более крупные банки применяют для фиксации и хранения кусочков тканей в фиксирующих жидкостях, обработки предметных стекол, приготовление нейтрального формалина и пр. В место банок с притертыми пробками можно использовать небольшие хозяйственные банки с жестяными завинчивающимися крышками, разного объема. Бюксы — небольшие круглые стеклянные стаканчики различного диаметра и высоты с шлифованными крышками. Биологические стаканчики — круглые, овальные или четырехугольные (как и высокие бюксы) применяют для проводки гистологических срезов, монтированных на предметных стеклах. Для придания устойчивости и обеспечения порядка в расстановке их помещают в специальные стойки, изготовленные из дерева или пластмассы, по несколько штук в ряд в зависимости от методики обработки. Чашки Петри — широкие, плоские стеклянные чашки с крышками – пригодны для различных манипуляций (окраска свободно плавающих и наклеенных на предметные стекла срезов, использование в качестве подставок под бюксы и т.д.). Мерная посуда – цилиндры и мензурки различной емкости (от 10 до 250-500 мл) воронки различных размеров. Химические стаканчики — круглые стеклянные стаканчики без крышек вместимостью 50-100 мл – находят широкое применение при проведении, окраски срезов наклеенных на стекла и т.д. Колбы (плоскодонные) – вместимостью от 50 мл до 2 л. Малые колбы применяют для приготовления и хранения растворов различных красителей, большие — под дистиллированную воду и прочие жидкости, расходуемые в больших количествах. Пипетки обычные (предназначенные для закапывания лекарств) используют для накапывания на срезы красителей и различных жидкостей, градуированные (вместимостью 0,1-100 мл) применяют для отмеривания малых количеств различных жидкостей. Можно использовать в настоящее время широко используемые автоматические пипетки различной вместительности. Предметные стекла – прямоугольные пластины размером 76*25 мм толщиной 1,0-1,2 мм, предназначенные для размещения срезов в процессе приготовления микропрепаратов. Более толстые стекла не позволяют получить резкое изображение краев диафрагмы осветителя в плоскости препарата, так как оно оказывается в толще стекла, а это нарушает фокусировку конденсора и резко снижает четкость изображения.

Предметное стекло с полосой для записи и шлифованными краями.
Покровные стекла – представляют собой тонкие (0,15-0,17 мм толщины, более толстые стекла ухудшают качество изображения) пластинки различных размеров. Служат для покрытия обработанных срезов, расположенных на предметных стеклах. Размеры покровных стекол выбирают в зависимости от площади объекта.

Покровное стекло
Инструменты. Инструменты, используемые в гистологической лаборатории, включают в себя пинцеты, скальпели, кровоостанавливающие зажимы, корнцанг, бактериологические петли шпатели, препаровальные иглы – прямые и изогнутые, металлические и стеклянные. Стеклянные иглы необходимы при импрегнации серебром, когда металлические иглами пользоваться нельзя. Так же необходимо иметь спиртовку, фильтровальную бумагу, иголки, нитки, плотную бумагу для этикетирования материала, лейкопластырь и карандаш по стеклу.
Подготовка предметных стекол. Предметные стекла, применяемые для получения гистологических препаратов, необходимо предварительно подготовить. Исключение составляют готовые к использованию и специально упакованные импортные предметные стекла. Предметные стекла моют в теплой воде с любым средством для мыться посуды (FAIRY),затем ополаскивают горячей водой и промывают в течение нескольких часов в проточной воде. Другой вариант мытья: разместить стекла в штативе, для окраски,или так что бы они не сопрекасались и обработать их средством для удаления жира например: «Средство для удаления жиров Unicum Gold спрей», затем ополаскивают горячей водой и промывают в течение нескольких часов в проточной воде Вымытые стекла протирают чистой хлопчатобумажной тканью и на несколько дней помещают в 96 % спирт. Обезжиренные стекла извлекают пинцетом из этой смеси, протирают чистой тканью и складывают в коробочку. Качество обезжиривания можно проверить, капнув на предметное стекло воду из пипетки: по обезжиренному стеклу вода растекается тонким слоем, а не собирается в каплю. Для лучшей фиксации срезов на стекле разработан способ фиксации среза к предметному стеклу: ванночку с теплой дистиллированной водой капают несколько капель жидкого казеинового клея и перемешивают. В полученную мутноватую жидкость опускают срезы, расправляют препаровальной иглой и вылавливают на чистое обезжиренное стекло. Этот способ дает неизменно хороший эффект и вокруг среза отсутствует окрашенный фон, как это часто бывает при применении белка [11]. Таким образом, для приготовления микропрепаратов требуется специальное оборудование и инструменты. Основными из них являются предметное и покровное стекла.
Способы приготовления временных микропрепаратов.
|
 Этапы приготовления микропрепарата. Накрывание объекта покровным стеклом. |
| Микропрепарат: Устьиц клеток растения. Приготавливают несколько срезов нижней эпидермы листа и помещают их на 2 часа в 5 %-ный раствор глицерина. Срезы помещают на предметное стекло в том же растворе. Рассматривают препарат. Затем заменяют глицерин на воду, оттягивая его из-под стекла фильтровальной бумагой. Смотрят, что изменилось. После этого воду заменяют 20%-ным раствором глицерина или 1М раствором сахарозы. Наблюдают изменения. Молярная концентрация с – отношение количества вещества (в молях), содержащегося в растворе, к объему раствора. Единицы измерения — моль/м3, (моль /л). Раствор, имеющий концентрацию 1 моль/л, обозначают 1 М; 0,5 моль/л, обозначают 0,5 М. Приготовление 1 М раствора САХАРОЗЫ. Молярная концентрация с – отношение количества вещества (в молях), содержащегося в растворе, к объему раствора. Единицы измерения — моль/м3, (моль /л). Раствор, имеющий концентрацию 1 моль/л, обозначают 1 М; 0,5 моль/л, обозначают 0,5 М. Молярная концентрация C(B) показывает, сколько моль растворённого вещества содержится в 1 литре раствора. C(B) = n(B) / V = m(B) / (M(B) · V),где М(B) — молярная масса растворенного вещества г/моль. Молярная концентрация измеряется в моль/л и обозначается «M». Например, 2 M NaOH — двухмолярный раствор гидроксида натрия. Один литр такого раствора содержит 2 моль вещества или 80 г (M(NaOH) = 40 г/моль). Пример: Какую массу САХАРОЗЫ C12h32O11 нужно взять для приготовления 0,1 литра 1,0 М раствора? Решение: M(C12h32O11) = C(C12h32O11) · V · M(C12h32O11) = 1 моль/л · 0,1 л · 342,29 г/моль » 34,229 г. Таким образом, для приготовления 0,1 литра 1 М раствора нужно взять 34,229 г и растворить в воде, а объём довести до 0,1 литра( довести до 100 мл). Концентрацию раствора можно выразить количеством молей растворённого вещества в 1000 г растворителя. Такое выражение концентрации называют моляльностью раствора. Микропрепарат: Клетки слизистой оболочки полости рта Для работы нужны: микроскоп, предметное и покровное стекла, препаровальная игла, скальпель, пипетка, 0,9-процентный раствор NaCl (физиологический раствор), подкрашенный метиленовой синью или чернилами, спирт, вата. Порядок работы:
|
Методика приготовления постоянных микропрепаратовОбязательным условием для долгосрочного хранения препарата из растительного или животного материала является его фиксация. Фиксирующих жидкостей много, самые доступные из них: этиловый спирт и продающийся в аптеках препарат на основе формалина (Формидрон). Состав: 100 мл препарата содержат 10 г раствора формальдегида в пересчете на 37 % формальдегид; вспомогательные вещества: спирт этиловый 96 %, одеколон, вода очищенная.
Препарат ФОРМИДРОН, может быть использован для создания архива биологических объектов, вспомогательные вещества входящие в аптечный препарат, не сколько не мешают сохранности объекта. ВНИМАНИЕ ФОРМАЛЬДЕГИД ОБЛАДАЕТ РАЗДРАЖАЮЩИМ ДЕЙСТВИЕМ.Если на дне банки с 40 % формалином образовался осадок белого цвета (параформальдегид), то его можно растворить, подогрев до 70-80 °С (в вытяжном шкафу! или на открытом воздухе), и использовать для фиксации. Рассмотрим состав и применение наиболее широко распространенных фиксаторов Спирт-формол по Шафферу — 10% формалин, который готовят из 1 части 40% формалина и 2-3 частей 96 % спирта. Продолжительность фиксации 24-48 ч. Дальнейшая промывка в воде не требуется, и материал сразу же помещают в 96 % спирт. Выпадение белого осадка никак не сказываеться на свойстве фиксатора.
Спирт с формалином. Применяется широко при гистологическом изучении позвоночных животных. Может быть использован и при работах с беспозвоночными. Изготовляется следующим образом: 70° спирт — 100 см3, формалин 40%-ный — 2—3 см3. Продолжительность фиксации 12—24 ч, после чего объекты переводятся в 70° спирт, где и хранятся впредь до дальнейшей обработки. Дает удовлетворительные результаты. Этот фиксатор удобен главным образом в силу своей доступности, так как спирт и формалин имеются в каждой лаборатории.
ПРАВИЛА РАБОТЫ С ФИКСАТОРАМИ Практически все фиксаторы относятся к токсичным веществам поэтому необходимо соблюдать правила техники безопасности при работе с реактивами.
Фиксация необходима с целью остановки (прекращения) жизнедеятельности клеток. Для этого объект помещают в соответствующий фиксатор на время от нескольких минут до нескольких часов.
 Таблица разбавления спиртов (по Гей-Люссаку)
Таблица разбавления спиртов (по Гей-Люссаку) ЗАКЛЮЧЕНИЕ ПРЕПАРАТА ПОД ПОКРОВНОЕ СТЕКЛО Большинство используемых в цитологии и гистологии красителей представляет собой водные растворы. Чтобы сделать временный препарат, срез, вынув из водного раствора красителя, промывают и заключают в глицерин. Приготовить постоянный препарат несколько сложнее: необходимо покрыть срезы покровным стеклом, заключив их в прозрачную затвердевающую среду. Можно, ополоснув срезы дистиллированной водой, капнуть на них разогретый раствор желатины. Но большую сохранность и лучшее качество препаратов можно получить, заключив их в канадский бальзам (прозрачную смолу пихты с показателем преломления n= 1,535). Поскольку канадский бальзам не смешивается с водой, но растворим в ксилоле (толуоле, бензоле), создается необходимость провести препарат по «проводке» для срезов, но в направлении, противоположном тому, в которое стекла велись для удаления парафина и подготовке к окраске. При этом нужно помнить, что даже незначительное присутствие воды в срезе сделает препарат мутным, непригодным для изучения. Поэтому переносить срезы по проводке от воды к толуолу надо медленно, погружая стекло в стаканчик со спиртом или толуолом на 2—3 мин. Схема проведения срезов может быть следующей: дистиллированная вода — ополоснуть, спирт 70%-ный — 2 мин, 96%-ный — 2 мин, 100%-ный —3 мин, Ксилол I — 2 мин, Ксилол II — 3—5 мин. Надо иметь в виду, что некоторые красители легко вымываются из препаратов как в воде, так и в спиртах. Поэтому в некоторых случаях приходится избегать промывки препаратов и проведения через спирты низких концентраций. Чтобы достигнуть обезвоживания, приходится препараты осторожно промокать фильтровальной бумагой, опуская их сразу в 96%- или 100%-ный спирт, можно заменять этиловые спирты ацетоном или изоамиловым спиртом.
Итак, задача, которая стоит при подготовке препарата для монтирования его под покровное стекло, состоит в том, чтобы, не вымыв красителя, добиться полного обезвоживания среза. Достигается это проводкой по спиртам возрастающей крепости, вплоть до 100%. Обработка срезов ксилолом имеет двоякое значение: с одной стороны, в нем достигается просветление препарата, усиливается его прозрачность (краситель при этом из препарата не вымывается), с другой стороны, создаются благоприятные условия для дальнейшего пропитывания среза канадским бальзамом, который растворим в ксилоле. Само заключение среза под покровное стекло осуществляется быстро, пока на препарате не испарился ксилол. Капля бальзама наносится на покровное стекло (оно должно быть чистым и сухим), и покровное стекло быстро перевертывается над срезом. Можно капать бальзам на предметное стекло на поверхность среза и быстро покрывать его покровным стеклом. Канадский бальзам должен иметь консистенцию растительного масла (или гуще). Через 1—2 дня бальзам застывает.
Вместо канадского бальзама можно использовать синтетическую среду на основе полистирола. Для этого берут 25г бесцветного полистирола, 5 мл дибутилфталата (пластификатор может быть любой) и доливают ксилолом до 100 мл. Раствор должен иметь консистенцию меда. Заключение среза под покровное стекло не отличается, от выше описанного. Несомненным плюсом синтетического бальзама это инертность и более лучшая сохранность красителей.
| Этапы приготовления постоянного микропрепарата | |
| 1 | Изучаемый объект помещают в раствор 1части ФОРМИДРОНА с 2 частями воды на несколько дней. Для мазков это время ограничивается 15 минутами и формидрон разводить не следует. В случае использования этилового спирта время фиксации составляет 15-20 мин. |
| 2 | После фиксации объект следует отмыть от фиксатора, для этого его помещают на несколько часов в проточную воду. Для удержания объекта при отмывке удобно поместить его в ситечко-шарик для заваривания чая. Исследуемый объект переносят в батарею спиртов с целью удаления воды. Мазки ополаскивают в проточной воде в течение 3-5 минут. Струя воды должна быть не сильной, мазок сушат. |
| 3 | Далее если необходимо препарат может быть окрашен одним из доступных вам красителей. |
| 4 | После окраски препарат готовят к заключению в монтирующую среду. Приготовить батарею ( ряд флаконов ) растворов спиртов возрастающей крепости для удаления воды. Возможно использовать как этиловый спирт (антисептический раствор) так и Изопропиловый спирт (ИПС) который можно приобрести в магазинах специализирующихся на продаже радиодеталей. Последовательно наливаем в лабораторные стаканчики этанол или изопропанол в концентрациях 50%, 70%, 96%, 99%. Объект помещают в стаканчик, начиная с 50% этанолом на 10 минут. Затем перемещают объект в стаканчики с все более высокой концентрацией спирта, выдерживая в каждом по 10 минут. В процессе такого перемещения этанол будет плавно вытягивать воду из объекта. Помещать объекты сразу в концентрированный этанол нельзя, так как в этом случае, быстро выходящая из клеток вода может повредить клеточные оболочки. Для мазков столь долгое пребывание в спиртах не требуется , достаточно 30-60 секунд, так как некоторые красители могут вымываться из мазка. |
| 5 | Если Вы хотите заключить препарат в канадский бальзам, обезвоженный материал переносят в уайт-спирит или ксилол на 5-6 часов, Канадский бальзам можно заменить на раствор канифоли в уайт-спирите(ксилоле), по консистенции напоминающий сироп. |
| 6 | Если препарат заключается в глицерин-желатиновую смесь, то объект переносят не уайт-спирит, а в глицерин на несколько часов ( глицерин, аптечный) Заключение объекта в глицерин-желатин.Последний приготовляется следующим образом. Чистый желатин (7 г.) размачивают в течение 2—3 ч. в 42 см3 дистиллированной воды, добавляют 50 г. глицерина и 0,5 г. кристаллической карболовой кислоты. Все вместе нагревается при помешивании на водяной бане, фильтруется и охлаждается. При появлении осадка тщательно профильтровать через стекловату. Готовый «глицерин-желатин» хранить в герметичном сосуде. При комнатной температуре глицерин-желатин застывает. Небольшой кусочек глицерин-желатина иглой или скальпелем переносят на предметное стекло. Последнее слегка нагревают на пламени спиртовки, глицерин-желатин расплавляется. В него из глицерина переносится объект и покрывается покровным стеклом. Мазок заключают следующим образом, кусочек глицерин-желатина помещают на покровное стекло Последнее слегка нагревают на спиртовке, глицерин-желатин расплавляется, объект покрывается покровным стеклом. Пространство между предметным и покровным стеклом заполняется монтирующей средой, которая, закрепляет покровное и предметное стекла и консервирует объект. Самым главным требованием к монтирующей среде является соответствие ее коэффициента преломления света к аналогичному показателю стекла. |
| 7 | Заключение объекта в канифоль или канадский бальзамНа покровное стекло по центру наносят каплю или, если стекло длинное, две капли жидкого раствора канифоли. Покровное стекло помещают каплей вниз и слегка прижимают. Края покровного стекла не следует вытирать ватой или марлей, смоченной ксилолом, так как при этом часть смолы может растечься по чистой поверхности покровного стекла. Засыхая, она образует неровности, которые мешают наблюдению под микроскопом и от которых очень трудно избавиться. В результате неполного обезвоживания в окрашенных заключенных препаратах часто образуются непрозрачные или мутные зоны. Под микроскопом в таком участке среза и над ним обнаруживаются многочисленные мелкие капельки воды, окраска сильно выцветает. Чтобы избавиться от этого, снимают покровное стекло, смывают ксилолом синтетическую смолу или бальзам, обезвоживают срез в 100%-ном спирте, ацетоне или изопропиловом спирте, просветляют в смеси ксилола с обезвоживающим агентом и в 2-3 сменах свежего ксилола и вновь заключают. Синтетическая монтирующая среда на основе полистирола.Полистирол (бесцветный)-25г.(можно использовать пищевые стаканчики) Дибутилфталат-5мл (любой доступный пластификатор, если не добавлять, полистирол трескается после высыхания) Ксилол до 100 мл. Растворение происходит в течение нескольких дней, раствор должен иметь консистенцию меда. |
Методика изготовления мазка-отпечатка. Различают «сухие» и «влажные» мазки. Первые имеют ограниченное применение и используются почти исключительно при изучении крови и кровепаразитов. «Влажные» мазки применяются часто главным образом при изучении паразитических простейших, а также и в других случаях. Мазки изготовляются следующим образом. Пинцетом берут тот орган, из которого предполагается сделать мазок, и «намазывают» на покровное стекло. Мазок должен быть совершенно равномерным и одинаковой толщины на всем покровном стекле. Если этого достигнуть сразу не удалось, то при помощи препаровальной иглы можно частично исправить мазок. Не давая подсохнуть мазку, покровное стекло опускают мазком вниз на теплый этиловый спирт, предварительно налитый в часовое стекло или солонку. Происходит быстрая коагуляция тканевых элементов, и мазок плотно пристает к стеклу. Дальнейшая обработка мазка та же, что и тотальных препаратов. После фиксатора следуют промывка в 70° спирте, вторичная промывка в спирте, перенос в воду, окраска, отмывка в воде; спирты возрастающей крепости, ксилол, бальзам (полистирол).
Методика изготовления мазка-отпечатка из печени рыбы: 1. рыбу декапитировать хирургическими ножницами; 2. вскрыть брюшную полость и поместить печень в чашку Петри; 3. печень рассечь лезвием и осторожно осушить поверхность разреза фильтровальной бумагой; 4. обезжиренное стекло слегка нагреть над пламенем спиртовки и коснуться поверхности разреза; 5. мазок высушить на воздухе и окрасить любым доступным красителем.
 Методика изготовления мазка-отпечатка
Методика изготовления мазка-отпечатка 

Мазки крови для исследования лейкоцитарной формулы готовят следующим образом.
| Шаг 1. Поместить небольшую каплю венозной крови на предметное стекло, с помощью стеклянной капиллярной пипетки, (или непосредственно из места укола пальца перенесите выступившую каплю крови на конец стерильного предметного стекла. Избегайте при этом всякого контакта между проколотым участком кожи и стеклом.) Оставляют стекло в горизонтальном положении. | |
| Шаг 2. Размазывают каплю крови по стеклу с помощью чистого шлифованного стекла, помещая его под углом 45°; коротким ребром, подождав, пока вся кровь расплывется по нему | |
| Шаг 3. Как только кровь растеклась по ребру, быстрым движением от капли проводят по предметному стеклу. Не следует сильно нажимать на стекло, так как при этом травмируются форменные элементы крови. | |
| Шаг 4. После приготовления мазки быстро сушат на воздухе до исчезновения влажного блеска. Подсушить мазок можно, подержав его над абажуром лампы или помахав им в воздухе. Хорошо сделанный мазок тонок, имеет желтоватый цвет и оканчивается «метелочкой». Густо-розовые и красноватые мазки непригодны для счета, так как они слишком толсты и клеточные элементы при этом дифференцировать невозможно.При медленном высыхании может изменяться морфология клеток. | |
 Техника мазка — слева направо:Мазок 1 — Идеальный мазокМазок 2 – В момент размазывания мазка произошла остановка.Мазок 3 – Перекос мазка.Мазок 4 — Капля крови слишком большая.Мазок 5 — Мазок слишком короткий. | |
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
microscopist.info