Тяжелые металлы в почве, десять решений одной проблемы. Тяжелые металлы в почве и растениях
Глава 1 Тяжелые металлы в почве
Химический состав почв различных территорий неоднороден и распространение содержащихся в почвах химических элементов по территории неравномерное. Так, например, находясь преимущественно в рассеянном состоянии, тяжелые металлы способны образовывать локальные связи, где их концентрации во многие сотни и тысячи раз превышают кларковые уровни.
Ряд химических элементов необходим для нормального функционирования организма. Их недостаток, избыток или дисбаланс может вызывать болезни, называемые микроэлементозами1, или биогеохимическими эндемиями, которые могут быть как природными так и техногенными. В их распротранении важная роль принадлежит воде, а также пищевым продуктам, в которые химические элементы попадают из почвы по пищевым цепочкам.
Опытным путем установлено, что на процентное содержание ТМ в растениях влияет процентное содержание ТМ в почве, атмосфере, воде (в случае водорослей). Также было замечено, что на почвах с одним и тем же содержанием тяжелых металлов одна и таже культура дает разный урожай, хотя и климатические условия тоже совпадали. Тогда была обнаружена зависимость урожайности от кислотности почв.
Наиболее изученными представляются загрязнения почв кадмием, ртутью, свинцом, мышьяком, медью, цинком и марганцем. Рассмотрим загрязнение почв этими металлами отдельно для каждого.2
Кадмий (Cd)
Содержание кадмия в земной коре составляет примерно 0.15 мг/кг. Кадмий концентрируется в вулканических (в кол-ве от 0.001 до 1.8 мг/кг), метаморфических (в кол-ве от 0.04 до 1.0 мг/кг) и осадочных породах (в кол-ве от 0.1 до 11.0 мг/кг). Почвы, сформированные на основе таких исходных материалов, содержат 0.1‑0.3; 0.1 - 1.0 и 3.0 - 11.0 мг/кг кадмия соответственно.[1]
В кислых почвах кадмий присутствует в форме Cd2+, CdCl+, CdSO4 , а в известковых почвах - в форме Cd2+, CdCl+, CdSO4 , CdHCO3+ . [1]
Поглощение кадмия растениями существенно падает при известковании кислых почв. В этом случае увеличение pH снижает растворимость кадмия в почвенной влаге, равно как и биодоступность почвенного кадмия. Так содержание кадмия в свекольных листьях на известковых почвах было меньше содержания кадмия в таких же растениях на неизвесткованных почвах. Сходный эффект быд показан для риса и пшеницы -->. [10]
Отрицательное влияние увеличения pH на кадмиевую доступность связано с понижением не только растворимости кадмия в фазе почвенного раствора, но и корневой активности, влияющей на абсорбцию.
Кадмий довольно мало подвижен в почвах, и, если добавлять кадмий‑содержащий материал на ее поверхность, основное его количество остается нетронутым.
Методы для удаления загрязнений из почвы включают либо удаление самого загрязненного слоя, либо удаление кадмия из слоя, либо покрытие загрязненного слоя. Кадмий может быть превращен в комплексные нерастворимые соединения доступными хелатообразующими агентами (например, этилендиаминтетрауксусной кислотой). [1,3].
Из-за относительно быстрого поглощения кадмия из почвы растениями и низкого токсического действия обычно встречающихся его концентраций, кадмий может накапливаться в растениях и поступать в звенья пищевой цепи быстрее чем свинец и цинк. Поэтому наибольшую опасность для здоровья человека при внесении в почву отходов представляет кадмий.
Процедура для минимизации количества кадмия, способного входить в пищевую цепь человека из загрязненных почв, - это выращивание на данной почве растений, не используемых в пищу или таких культур, которые абсорбируют малые количества кадмия.
В целом культуры на кислых почвах абсорбируют больше кадмия, чем таковые на нейтральных или щелочных почвах. Поэтому известкование кислых почв - это эффективное средство снижения количества абсорбированного кадмия.
Ртуть (Hg)
Ртуть находится в природе в виде паров металла Hg0 , образующихся при ее испарении из земной коры; в виде неорганических солей Hg(I) и Hg(II), и в виде органического соединения метилртути СН3Hg+ , монометил- и диметил производных СН3Hg+ и (Ch4)2Hg.
Ртуть накапливается в верхнем горизонте (0-40 см) почвы и слабо мигрирут в более глубокие ее слои. Соединения ртути относятся к высокостабильным веществам почвы. Растения, произрастающие на загрязненной ртутью почве, усваивают значительное количество элемента и накапливают его в опасных концентрациях, либо не произрастают.
Свинец (Pb)
По данным опытов, проводимых в условиях песчаной культуры с внесением пороговых для почв концентраций Hg (25 мг/кг) и Pb (25 мг/кг) и превышающие пороговые в 2-20 раз, растения овса до определенного уровня загрязнения растут и развиваются нормально. По мере увеличения концентрации металлов (для Pb начиная с дозы 100 мг/кг) изменяется внешний вид растений. При экстремальных дозах металлов растения погибают через три недели с начала опытов. Содержание металлов в компонентах биомассы в порядке убывания распределено следующим образом: корни - надземная часть - зерно. [3]
Суммарное поступление свинца в атмосферу (а следовательно частично и на почву) от автотранспорта на территории России в 1996 году оценивалось примерно в 4.0 тыс. т, в том числе 2.16 тыс. т. вносил грузовой транспорт. Максимальная нагрузка по свинцу приходилась на Московскую и Самарскую области, за которыми следуют Калужская, Нижегородская, Владимирская области и другие субъекты Российской Федерации, расположенные в центральной части Европейской территории России и Северного Кавказа. Наибольшие абсолютные выбросы свинца отмечались в Уральском (685 т), Поволжском (651 т) и Западно-Сибирском (568 т) регионах. А наиболее неблагоприятное воздействие выбросов свинца отмечалось в Татарстане, Краснодарском и Ставропольском краях, Ростовской, Московской, Ленинградской, Нижегородской, Волгоградской, Воронежской, Саратовской и Самарской областях (газета “Зеленый мир”, специальный выпуск №28, 1997 г.).
Мышьяк (As)
Мышьяк находится в окружающей среде в виде разнообразных химически устойчивых форм. Его два главных состояния окисления: As (III), и As (V). В природе распространен пятивалентный мышьяк в виде разнообразных неорганических соединений, хотя и трехвалентный мышьяк легко обнаруживается в воде, особенно в анаэробных условиях.
Медь (Cu)
Природные медные минералы в почвах включают сульфаты, фосфаты, оксиды и гидроксиды. Медные сульфиды могут образовываться в плохо дренируемых или затопляемых почвах, где реализуются восстановительные условия. Медные минералы обычно слишком растворимы, чтобы оставаться в свободно дренируемых сельскохозяйственных почвах. В загрязненных металлом почвах, однако, химическая среда может контролироваться неравновесными процессами, приводящими к накоплению метастабильных твердых фаз. Предполагается, что и в восстановленных, загрязненных медью почвах могут находиться ковеллин (CuS) или халькопирит (CuFeS2).
Следовые количества меди могут содержаться в виде отдельных сульфидных включений в силикатах и могут изоморфно замещать катионы в филлосиликатах. Несбалансированные по заряду глинистые минералы неспецифически абсорбируют медь, а вот оксиды и гидроксиды железа и марганца показывают очень высокое специфическое сродство к меди. Высокомолекулярные органические соединения способны быть твердыми абсорбентами для меди, а низкомолекулярные органические вещества склонны образовывать растворимые комплексы.
Сложность состава почв ограничивает возможность количественного разделения медных соединений на конкретные химические формы. указывает на -->Наличие большой массы медных конгломератов находится и в органических веществах, и в оксидах Fe и Mn. Внесение медьсодержащих отходов или неорганических солей меди повышает концентрацию соединений меди в почве, способных к экстрагированию сравнительно мягкими реагентами; таким образом, медь может находиться в почве в виде лабильных химических форм. Но легко растворимый и заменяемый элемент - медь - образует малое количество форм, способных к поглощению растениями, обычно менее 5% от общего содержания меди в почве.
Токсичность меди увеличивается с увеличением pH почвы и при низкой катионообменной емкости почвы. Обогащение медью за счет экстракции происходит только в поверхностных слоях почвы, и зерновые культуры с глубокой корневой системой не страдают от этого.
Окружающая среда и питание растений могут повлиять на фитотоксичность меди. Так, например, медная токсичность для риса на равнинных землях отмечалась явно, когда растения поливали холодной, а не теплой водой. Дело в том, что микробиологическая активность подавляется в холодной почве и создает те востановительные условия в почве, которые бы способствовали осаждению меди из раствора.
Фитотоксичность по меди происходит изначально от избытка в почве доступной меди и усиливается кислотностью почвы. Поскольку медь сравнительно малоподвижна в почве, почти вся попадающая в почву медь остается в верхних слоях. Внесение органических веществ в загрязненные медью почвы может снизить токсичность благодаря адсорбции растворимого металла органическим субстратом (при этом ионы Cu2+ превращаются в менее доступные для растения комплексные соединения) либо повышением мобильности ионов Cu2+ и вымыванием их из почвы в виде растворимых медьорганических комплексов.
Цинк (Zn)
Цинк может находиться в почве в виде оксосульфатов, карбонатов, фосфатов, силикатов, оксидов и гидроксидов. Эти неорганические соединения метастабильны в хорощо дренируемых сельскохозяественных угодьях. По-видимому, сфалерит ZnS является термодинамически преобладающей формой как в восстановленных, так и в окисленных почвах. Некоторая ассоциация цинка с фосфором и хлором налицо в восстановленных, загрязненных тяжелыми металлами осадках. Следовательно, сравнительно растворимые соли цинка должны встречаться в богатых металлами почвах.
Цинк изоморфно замещается другими катионами в силикатных минералах, он может быть окклюдирован или соосажден с гидроксидами марганца и железа. Филлосиликаты, карбонаты, гидратированные оксиды металлов, а также органические соединения хорощо абсорбируют цинк, при этом используются и специфические, и неспецифические места связывания.
Растворимочть цинка повышается в кислых почвах, а также при комплексообразовании с низкомолекулярными органическими лигандами. Восстанавливающие условия могут уменьшать растворимость у цинка из-за образования нерастворимого ZnS.
Фитотоксичность цинка обычно проявляется при контакте корней растения с избыточным по цинку раствором в почве. Транспорт цинка через почву происходит посредством обмена и диффузии, причем последний процесс доминирует в почвах с низким содержанием цинка. Обменный транспорт более значителен в высокоцинковых почвах, в которых концентрации растворимого цинка сравнительно стабильны.
Мобильность цинка в почвах повышается в присутствии хелатообразователей (природных или синтетических). Увеличение концентрации растворимого цинка, вызванное образованием растворимых хелатов, компенсирует понижение мобильности, обусловленное увеличением размера молекулы. Концентрации цинка в тканях растений, его общее поглощение и симптомы токсичности положительно коррелируют с концентрацией цинка в растворе, омывающем корни растения.
Свободный ион Zn2+ преимущественно абсорбируется корневой системой растений, поэтому образование растворимых хелатов способствует растворимости данного металла в почвах, а эта реакция компенсирует пониженную доступность цинка в хелатной форме.
Исходная форма металлического загрязнения влияет на потенциал токсичности по цинку: доступность цинка для растения в удобряемых почвах с эквивалентным общим содержанием этого металла уменьшается в ряду ZnSO4>отстой>мусорный компост. [10]
Большинство опытов по загрязнению по почвы Zn-содержащим отстоем не показало падение урожая или явную их фитотоксичность; все же их долговременное внесение с высокой скоростью способно повредить растениям. Простое внесение цинка в виде ZnSO4 вызывает понижение роста культур в кислых почвах, в то время как многолетнее внесение его в почти нейтральные почвы проходит незамеченным.
Токсичность уровней в сельскохозяественных почвах цинк достигает, как правило, из-за поверхностного цинка; он обычно не проникает на глубину более 15-30 см. Глубокие корни определенных культур могут избежать контакта с избыточным цинком благодаря их расположению в незагрязненной подпочве.
Известкование почв, загрязненных цинком, понижает концентрацию последнего в полевых культурах. Добавки NaOH или Ca(OH)2 понижают токсичность цинка в овощных культурах, выращенных на высокоцинковых торфяных почвах, хотя в данных почвах поглощение цинка растениями весьма ограничено. Вызванную же цинком недостаточность по железу можно устранить при помощи внесения хелатов железа или FeSO4 в почву либо прямо на листья. Физическое удаление или захоронение загрязненного цинком верхнего слоя вообще может позволить избежать токсичного воздействия металла на растения.
Марганец
В почве марганец находится в трех состояниях окисления: +2, +3, +4. По большей части этот металл ассоциирован с первичными минералами или со вторичными металлоксидами. В почве общее количество марганца колеблется на уровне 500 - 900 мг/кг.
Растворимость Mn4+ чрезвычайно мала; трехвалентный марганец очень нестоек в почвах. Большая часть марганца в почвах присутствует в виде Mn2+, в то время как в хорошо аэрируемых почвах большая часть его в твердой фазе присутствует в виде оксида, в котором металл находится в степени окисления IV; в плохо же аэрируемых почвах марганец медленно восстанавливается микробной средой и переходит в почвенный раствор, становясь таким образом высокомобильным.
Растворимость Mn2+ увеличивается значительно при низких значениях pH, но при этом поглощение марганца растениями падает.
Марганцевая токсичность часто имеет место там, где общий уровень марганца от среднего до высокого, pH почвы довольно низкий и кислородная доступность для почвы тоже низка (т.е. имеются восстановительные условия). Чтобы устранить действие перечисленных условий, pH почвы следует увеличивать с помощью известкования, потратить усилия на улучшение почвенного дренажа, уменьшить поступление воды, т.е. в целом улучшить структуру данной почвы.
studfiles.net
Загрязнение почвы тяжелыми металлами и способы борьбы с ним
Почва – это поверхность земли, имеющая свойства, которые характеризуют как живую, так и неживую природу.
Почва является индикатором общей техногенной обстановки. Загрязнения поступают в почву с атмосферными осадками, поверхностными отходами. Также они вносятся в почвенный слой почвенными породами и подземными водами.
К группе тяжелых металлов относятся все цветные металлы с плотностью, превышающей плотность железа. Парадокс этих элементов состоит в том, что в определенных количествах они необходимы для обеспечения нормальной жизнедеятельности растений и организмов.
Но их избыток может привести к тяжелым заболеваниям и даже гибели. Пищевой круговорот становится причиной того, что вредные соединения попадают в организм человека и часто наносят огромный вред здоровью.Источники загрязнения тяжелыми металлами — это промышленные предприятия. Существует методика, по которой рассчитывается допустимая норма содержания металлов. При этом учитывается суммарная величина нескольких металлов Zc.
Выделяют 4 категории загрязнения земель металлами, которые учитываются в сельском хозяйстве:
- допустимая;
- умеренно опасная;
- высоко-опасная;
- чрезвычайно опасная.
Очень важна охрана почв. Постоянный контроль и мониторинг не позволяет выращивать сельскохозяйственную продукцию и вести выпас скота на загрязненных землях.
Тяжелые металлы, загрязняющие почву
Существует три класса опасности тяжелых металлов. Всемирная организация здравоохранения самыми опасными считает заражение свинцом, ртутью и кадмием. Но не менее вредна и высокая концентрация остальных элементов.
Ртуть
Загрязнение почвы ртутью происходит с попаданием в нее пестицидов, различных бытовых отходов, например люминесцентных ламп, элементов испорченных измерительных приборов.
По официальным данным годовой выброс ртути составляет более пяти тысяч тонн. Ртуть может поступать в организм человека из загрязненной почвы.
Если это происходит регулярно, могут возникнуть тяжелые расстройства работы многих органов, в том числе страдает и нервная система.
При ненадлежащем лечении отравления ртутью возможен летальный исход.
Свинец
Очень опасным для человека и всех живых организмов является свинец.
Он чрезвычайно токсичен. При добыче одной тонны свинца двадцать пять килограммов попадает в окружающую среду. Большое количество свинца поступает в почву с выделением выхлопных газов.
Зона загрязнения почвы вдоль трасс составляет свыше двухсот метров вокруг. Попадая в почву, свинец поглощается растениями, которые употребляют в пищу человек и животные, в том числе и скот, мясо которого также присутствует в нашем меню. От избытка свинца поражается центральная нервная система, головной мозг, печень и почки. Он опасен своим канцерогенным и мутагенным действием.
Кадмий
Огромной опасностью для организма человека является загрязнение почвы кадмием. Попадая в пищу, он вызывает деформацию скелета, остановку роста у детей и сильные боли в спине.
Медь и цинк
Высокая концентрация в почве этих элементов становится причиной того, что замедляется рост и ухудшается плодоношение растений, что приводит в конечном итоге к резкому уменьшению урожайности. У человека происходят изменения в мозге, печени и поджелудочной железе.
Молибден
Избыток молибдена вызывает подагру и поражения нервной системы.
Опасность тяжелых металлов заключается в том, что они плохо выводятся из организма, накапливаются в нем. Они могут образовывать очень токсичные соединения, легко переходят из одной среды в другую, не разлагаются. При этом они вызывают тяжелейшие заболевания, приводящие часто к необратимым последствиям.Сурьма
 Присутствует в некоторых рудах.
Присутствует в некоторых рудах.
Входит в состав сплавов, используемых в различных производственных сферах.
Ее избыток вызывает тяжелые пищевые расстройства.
Мышьяк
Основным источником загрязнения почвы мышьяком являются вещества, с помощью которых борются с вредителями сельскохозяйственных растений, например гербициды, инсектициды. Мышьяк – это накапливающийся яд, вызывающий хронические отравления. Его соединения провоцируют заболевания нервной системы, мозга, кожных покровов.
Марганец
В почве и растениях наблюдается высокое содержание этого элемента.
При попадании в почву дополнительного количества марганца быстро создается его опасный избыток. На организме человека это сказывается в виде разрушения нервной системы.
Не менее опасен переизбыток и остальных тяжелых элементов.
Из вышесказанного можно сделать вывод, что накопление тяжелых металлов в почве влечет за собой тяжелые последствия для состояния здоровья человека и окружающей среды в целом.
Основные методы борьбы с загрязнением почв тяжелыми металлами
Методы борьбы с загрязнением почвы тяжелыми металлами могут быть физическими, химическими и биологическими. Среди них можно выделить следующие способы:
- Увеличение кислотности почвы повышает возможность загрязнения ее тяжелыми металлами. Поэтому внесение органических веществ и глины, известкование помогают в какой-то мере в борьбе с загрязнением.
- Посев, скашивание и удаление с поверхности почвы некоторых растений, например клевера, существенно снижает концентрацию тяжелых металлов в почве. К тому же данный способ является совершенно экологичным.
- Проведение детоксикации подземных вод, ее откачивание и очистка.
- Прогнозирование и устранение миграции растворимой формы тяжелых металлов.
- В некоторых особо тяжелых случаях требуется полное снятие почвенного слоя и замена его новым.
greenologia.ru
Тяжелые металлы в почве, десять решений одной проблемы | Дача
 Не секрет, что каждому хочется иметь дачу в экологически чистом районе, где нет городской загазованности. Окружающая среда содержит в себе тяжелые металлы (мышьяк, свинец, медь, ртуть, кадмий, марганец и другие), которые исходят даже от выхлопных газов автомобилей. При этом надо понимать, что земля – это природный очиститель атмосферы и грунтовых вод, она накапливает в себе не только тяжелые металлы, но и вредные пестициды с углеводородами. Растения в свою очередь принимают все то, что дает им почва. Металл, оседая в почве, наносит вред не только самой почве, но и растениям, а как следствие и человеку.
Не секрет, что каждому хочется иметь дачу в экологически чистом районе, где нет городской загазованности. Окружающая среда содержит в себе тяжелые металлы (мышьяк, свинец, медь, ртуть, кадмий, марганец и другие), которые исходят даже от выхлопных газов автомобилей. При этом надо понимать, что земля – это природный очиститель атмосферы и грунтовых вод, она накапливает в себе не только тяжелые металлы, но и вредные пестициды с углеводородами. Растения в свою очередь принимают все то, что дает им почва. Металл, оседая в почве, наносит вред не только самой почве, но и растениям, а как следствие и человеку.
Вблизи магистральной дороги много копоти, которая проникает в поверхностные слои почвы и оседает на листьях растений. На таком участке нельзя выращивать корнеплоды, фрукты, ягоды и другие плодородные культуры. Минимальное расстояние от дороги – 50 м.
Почва, наполненная тяжелыми металлами – плохая почва, тяжелые металлы токсичны. На ней вы никогда не увидите муравьев, жужелиц и дождевых червей, но будет большое скопление сосущих насекомых. Растения часто болеют грибковыми болезнями, сохнут и неустойчивы к вредителям.
Самыми опасными являются подвижные соединения тяжелых металлов, которые легко получаются в кислой почве. Доказано, что растения, выращенные на кислой или легкой песчаной почве, содержат в себе больше металлов, чем на нейтральной или известковой почве. Мало того, песчаная почва с кислой реакцией особенно опасна, она легко накапливает и так же легко промывается, попадая в грунтовые воды. Садовый участок, где львиная доля – это глина, тоже легко подвержен накоплению тяжелых металлов, при этом самоочищение происходит долго и медленно. Самой безопасной и устойчивой почвой является чернозем, обогащенный известью и гумусом.
Что делать, если в почве тяжелые металлы? Путей решения проблемы есть несколько.
1. Неудачный участок можно продать.
2. Известкование – хороший способ уменьшить концентрацию тяжелых металлов в почве. Есть разные способы проверки кислотности почвы. Самый простой: горсть земли бросьте в емкость с уксусом, если появится пена, то почва щелочная. Или копните немного землю, если в ней найдете белую прослойку, то кислотность присутствует. Вопрос насколько много. После известкования регулярно проверяйте на кислотность, возможно нужно будет повторить процедуру. Известкуют доломитовой мукой, известью-пушонкой, доменным шлаком, торфяной золой, известняком.
Если тяжелых металлов в земле уже накоплено очень много, то будет полезно верхний слой грунта (20-30 см) снять и заменить черноземом.
 3. Постоянная подкормка органическими удобрениями (навоз, компост). Чем больше гумуса в почве, тем меньше в ней тяжелых металлов, снижается токсичность. Бедная, неплодородная земля не способна защитить растения. Не перенасыщать минеральными удобрениями, особенно азотным. Минеральные удобрения быстро разлагают органику.
3. Постоянная подкормка органическими удобрениями (навоз, компост). Чем больше гумуса в почве, тем меньше в ней тяжелых металлов, снижается токсичность. Бедная, неплодородная земля не способна защитить растения. Не перенасыщать минеральными удобрениями, особенно азотным. Минеральные удобрения быстро разлагают органику.
4. Поверхностное рыхление. После рыхления обязательно провести мульчирование почвы опилками, торфом или компостом. При рыхлении полезно добавить вермикулит, который станет барьером между растениями и токсическими веществами в почве.
5. Промывка земли только при хорошем дренаже. Иначе с водой тяжелые металлы разнесутся по всему участку. Заливают чистой водой так, чтобы промылся слой грунта 30-50 см для овощных культур и до 120 см для плодовых кустарников и деревьев. Промывку проводят весной, когда после зимы влаги в почве достаточно.
6. Верхний слой почвы убрать, сделать хороший дренаж из керамзита или гальки, а сверху засыпать чернозем.
7. Растения выращивать в контейнерах или теплице, где землю легко можно заменить. Соблюдать севооборот культур, не выращивать растение на одном месте длительное время.
8. Если садовый участок у дороги, то в почве с большой вероятностью есть свинец, который выходит с выхлопными газами автомобилей. Проводите вытяжку свинца посадкой гороха между растениями, урожай не собирайте. Осенью горох выкопайте и сожгите вместе с плодами. Улучшат почву растения с мощной глубокой корневой системой, которые перенесут из глубокого слоя в верхний фосфор, калий и кальций.
9. Выращенные на тяжелой почве овощи и фрукты всегда подвергать термической обработке или как минимум мыть под проточной водой, убирая, таким образом, атмосферную пыль.
10. В загрязненных районах или участке при дороге ставят забор сплошной, сетка-рабица не станет барьером от дорожной пыли. За забором обязательно посадить растения-хвойники и лиственные (рябину). Как вариант отличной защитой станут многоярусные посадки, которые сыграют роль защитников от атмосферной пыли и копоти.
Наличие тяжелых металлов в почве – не приговор, главное это своевременно выявить и обезвредить.
Рубрика: Работа с почвойdacha-vprok.ru
Тяжелых металлов в почвах
| Тяжелый металл | Концентрация, мг/кг |
| Ванадий Кадмий Медь Марганец Марганец + Ванадий Мышьяк Никель Ртуть Свинец Цинк Хром | 150 5,0 23,0 1500 1000+100 2,0 35,0 2,1 фон + 20 110 0,05 |
В зависимости от элемента величина ПДК колеблется от 0,05 мг/кг (для хрома) до 1500 мг/кг (для марганца). Учтено значение ПДК при совместном действии марганца и ванадия. ПДК для свинца определяется с учетом его фонового содержания в почве.
Тяжелые металлы поступают в почву в форме различных соединений (карбонатов, оксидов) с ограниченной растворимостью, поэтому только часть из них может быть усвоена растениями. Для растений представляет опасность доступная форма элемента, которая может быть усвоена непосредственно через корневую систему. Доступными считаются те формы соединений тяжелых металлов, которые переходят в вытяжку 2М азотной кислоты или 1 н. раствор соляной кислоты. Именно эти формы тяжелых металлов и поступают из почвы в растения, оказывая на них токсическое действие. Поступление тяжелых металлов в растения и микроорганизмы осуществляется в основном через почвенный раствор. Поэтому он является непосредственным источником тяжелых металлов для высших растений.
Выпадающие на поверхность земли тяжелые металлы аккумулируются в верхнем 2-5 см слое почвы и подразделяются на фиксируемую и мигрирующую часть. Миграционные формы частично или полностью трансформируются. Исходные формы меди и свинца переходят в менее подвижные, а кадмия и цинка – в более подвижные. Миграция тяжелых металлов по почвенному профилю приводит к тому, что с глубиной содержание их снижается, а на глубине 30 – 40 см выходит на фоновый уровень. Содержание в почвенном растворе органических соединений ведет к повышению миграционной способности металлов благодаря образованию органоминеральных комплексов. Содержание в почве в доступных формах кадмия, хрома, никеля и цинка в большей степени зависит от значения рН. Кадмий подвижен в кислых почвах с рН менее 5,5. Для сравнения и дальнейшего анализа приведем валовое содержание тяжелых металлов в пахотном слое различных типах почв России (табл. 5.16). Содержание цинка в пахотном слое почв России колеблется в пределах 5 – 80 мг/кг, содержание кадмия – 0,01 – 2,5 мг/кг.
.
Таблица 5. 16 - Содержание тяжелых металлов в почвах России, мг/кг
| Тип почв | ТЯЖЕЛЫЙ МЕТАЛЛ | |||||||
| Hg | Pb | Cd | Cr | Co | Zn | Ni | Cu | |
| Дерново-подзолистые Серые – лесные Черноземы Каштановые Красноземы Торфяные | 0,01-0,76 0,03-0,80 0,03-0,40 0,01-0,47 0,03-0,08 0,01-0,03 | 3-17 10-25 13-30 10-27 10-38 3-24 | 0,01-2,5 0,1-0,7 0,4-1,7 0,07-0,4 0,12-0,2 0,17-0,2 | 10-181 25-250 20-287 71-330 80-200 3-90 | 3-13 2-12 9-13 5-15 1-2 1-10 | 5-62 20-63 29-63 42-52 47-70 7-62 | 6-25 11-30 20-70 20-45 25-65 2-65 | 4-16 1-48 5-40 13-40 15-140 1-5 |
В незагрязненных районах распределение цинка в пахотном слое почв колеблется в пределах от 5 до 70, а кадмия от 0,01 до 2,5 мг/кг. Увеличение их количества в верхнем горизонте почвы свидетельствует об избыточном поступлении тяжелых металлов из атмосферного воздуха. Содержание ртути колеблется в пределах от 0,01 до 0,8 мг/ кг. Свинца, соответственно, - от 3 до 38, хрома - от 3 до 330, кобальта - от 1 до 15, никеля - от 2 до 70 и меди - от 1 до 140 мг / кг. Решение проблемы получения экологически безопасной продукции на загрязненных территориях невозможно без учета миграции и аккумуляции тяжелых металлов в почвенном профиле. Анализ их содержания в почвах указывает на характерную пространственную и вертикальную неоднородность почв.
Для условного контроля мы брали показатели имеющихся данных по содержанию тяжелых металлов в природных средах (табл. 5.17).
Таблица 5.17- Предельно-допустимые концентрации тяжелых металлов в природных средах
| Металл | Воздух, мг/м3 | Вода, мг/л | Почва, мг/кг | |
| хозяйственно-бытового назначения | подвижная форма | валовая форма | ||
| Pb Cd Cu Zn Ni Co Hg | 0,0003 0,0003 0,001 0,005 0,001 0,001 0,0003 | 0,03 0,001 1,0 1,0 0,1 0,1 0,0001 | 6,0 2,0 3,0 23,0 4,0 5,0 – | 32,0 – 33,0 55,0 20,0 – 2,1 |
Валовое содержание цинка в серых лесных почвах значительно меньше, а в черноземных почвах – больше, чем в пойменных. Особенно существенными являются различия по его содержанию в верхнем двадцати - сантиметровом слое почвы. Подвижность цинка почти в 2 раза больше в верхних слоях почвы (0 – 60 см), чем в нижних слоях. Содержание никеля по профилю серых лесных почв убывает до глубины 80 см, а затем несколько возрастает на глубине от 80 до 100 см. Содержание меди в серых лесных почвах убывает по глубине профиля, а ее подвижность в верхних слоях почвы (0 – 40 см) в 2 раза выше, чем в нижних. Количество хрома в серых лесных почвах повышается на глубине от 0 до 80 см, а затем, в слое 80 – 100 см, выходит на уровень верхнего 20-сантиметрового слоя почвы. Подвижность хрома в серых лесных почвах невысок, в пределах 1,6 – 2 мг/кг.
Для большинства почв характерно наибольшее обогащение ртутью верхней части почвенного профиля (Скрипченко, Золотарева, 1981). Так, в каштановых почвах накопление ртути наблюдается во второй (иллювиальной) полуметровой части профиля. Миграция ртути за пределы почвенного профиля практически не происходит. Скорее происходит аккумуляция ее в верхних горизонтах почв при незначительном содержании в почвообразующих породах, на что необходимо обратить особое внимание. Наибольшее количество ртути накапливается в илистой и мелкопылеватой фракциях почв, что связано с прочным закреплением ртути гумусовыми веществами и глинистыми минералами.
Распределение кадмия по профилю почв хорошо согласуется с особенностями почвообразовательного процесса. В дерново-подзолистых почвах содержание кадмия всегда выше, чем в почвообразующих породах. Наиболее беден кадмием подзолистый горизонт этих почв, тогда как в гумусовом горизонте отчетливо проявляется его аккумуляция. В горизонтах более тяжелых по механическому составу содержание кадмия выше, чем в почвообразующих породах почвы дерново-подзолистой зоны более дифференцированы по профильному распределению кадмия, что связано с образованием ассоциаций с водными оксидами железа и алюминия.
Распределение мышьяка в почвенном профиле зависит от типа почвы. В тяжелосуглинистом черноземе он распределяется равномерно по всему профилю. В подзолистых и бурых горно-лесных почвах его распределение носит элювиально-иллювиальный характер, максимальное содержание находится в иллювиальных горизонтах. Для дерново-подзолистых почв характерно элювиальное распределение мышьяка. Накопление мышьяка в гумусовом горизонте не наблюдается. Характер распределения свинца по профилю почвы аналогичен распределению органического вещества. В кислых дерново-подзолистых почвах происходит перенос свинца в нижние горизонты. В дерново-подзолистых почвах иллювиальный горизонт содержит свинца больше, чем почвообразующие породы или верхние горизонты. Его максимальное содержание в серых лесных почвах отмечается в верхнем слое, что составляет около 40% его валовых запасов. В дерново-глеевых почвах основным барьером на пути передвижения свинца в условиях кислой реакции среды является глиняный горизонт, что связано с высоким содержанием в нем ила (Алексеев 1987).
Повышенное содержание тяжелых металлов в почве нарушает естественные процессы поглощения и передвижения элементов по трофическим цепям. Накопление тяжелых металлов в организмах приводит к развитию многих опасных заболеваний. До последнего времени на нормирование содержания тяжелых металлов в почвах практически не обращали внимания. Если и изучали содержание тяжелых металлов в почве, но не с целью предотвращения чрезмерного накопления, а, наоборот, с целью выявления недостаточности в почвах микроэлементов, таких как цинк, марганец, медь, молибден, кобальт, железо.
Необходимость определения ПДК тяжелых металлов возникла в связи с учащением сообщений об отрицательных последствиях загрязнения почв, проявляющихся в ухудшении гигиенического качества продукции, заболевании животных, и, в конечном счете, ухудшении здоровья человека. Загрязнение почв часто происходит не по вине сельскохозяйственных работников. Из атмосферного воздуха в окрестностях промышленных предприятий и оживленных автомагистралей в почву поступают загрязнители, в том числе и тяжелые металлы. В почвах тяжелые металлы поливалентны, образуют плохо растворимые соединения с фосфатами и гидроокисями, что способствует их постепенному накоплению. В связи с этим необходим постоянный мониторинг состояния почв, так как несущественные, на первый взгляд, количественные изменения, происходящие в результате поступления металлов, могу в определенный момент превысить предельно допустимые его концентрации и, в значительной мере, ухудшить экологическое состояние, особенно, урбанизированных территорий.
studfiles.net
Тяжелых металлов в почвах
| Тяжелый металл | Концентрация, мг/кг |
| Ванадий Кадмий Медь Марганец Марганец + Ванадий Мышьяк Никель Ртуть Свинец Цинк Хром | 150 5,0 23,0 1500 1000+100 2,0 35,0 2,1 фон + 20 110 0,05 |
В зависимости от элемента величина ПДК колеблется от 0,05 мг/кг (для хрома) до 1500 мг/кг (для марганца). Учтено значение ПДК при совместном действии марганца и ванадия. ПДК для свинца определяется с учетом его фонового содержания в почве.
Тяжелые металлы поступают в почву в форме различных соединений (карбонатов, оксидов) с ограниченной растворимостью, поэтому только часть из них может быть усвоена растениями. Для растений представляет опасность доступная форма элемента, которая может быть усвоена непосредственно через корневую систему. Доступными считаются те формы соединений тяжелых металлов, которые переходят в вытяжку 2М азотной кислоты или 1 н. раствор соляной кислоты. Именно эти формы тяжелых металлов и поступают из почвы в растения, оказывая на них токсическое действие. Поступление тяжелых металлов в растения и микроорганизмы осуществляется в основном через почвенный раствор. Поэтому он является непосредственным источником тяжелых металлов для высших растений.
Выпадающие на поверхность земли тяжелые металлы аккумулируются в верхнем 2-5 см слое почвы и подразделяются на фиксируемую и мигрирующую часть. Миграционные формы частично или полностью трансформируются. Исходные формы меди и свинца переходят в менее подвижные, а кадмия и цинка – в более подвижные. Миграция тяжелых металлов по почвенному профилю приводит к тому, что с глубиной содержание их снижается, а на глубине 30 – 40 см выходит на фоновый уровень. Содержание в почвенном растворе органических соединений ведет к повышению миграционной способности металлов благодаря образованию органоминеральных комплексов. Содержание в почве в доступных формах кадмия, хрома, никеля и цинка в большей степени зависит от значения рН. Кадмий подвижен в кислых почвах с рН менее 5,5. Для сравнения и дальнейшего анализа приведем валовое содержание тяжелых металлов в пахотном слое различных типах почв России (табл. 5.16). Содержание цинка в пахотном слое почв России колеблется в пределах 5 – 80 мг/кг, содержание кадмия – 0,01 – 2,5 мг/кг.
.
Таблица 5. 16 - Содержание тяжелых металлов в почвах России, мг/кг
| Тип почв | ТЯЖЕЛЫЙ МЕТАЛЛ | |||||||
| Hg | Pb | Cd | Cr | Co | Zn | Ni | Cu | |
| Дерново-подзолистые Серые – лесные Черноземы Каштановые Красноземы Торфяные | 0,01-0,76 0,03-0,80 0,03-0,40 0,01-0,47 0,03-0,08 0,01-0,03 | 3-17 10-25 13-30 10-27 10-38 3-24 | 0,01-2,5 0,1-0,7 0,4-1,7 0,07-0,4 0,12-0,2 0,17-0,2 | 10-181 25-250 20-287 71-330 80-200 3-90 | 3-13 2-12 9-13 5-15 1-2 1-10 | 5-62 20-63 29-63 42-52 47-70 7-62 | 6-25 11-30 20-70 20-45 25-65 2-65 | 4-16 1-48 5-40 13-40 15-140 1-5 |
В незагрязненных районах распределение цинка в пахотном слое почв колеблется в пределах от 5 до 70, а кадмия от 0,01 до 2,5 мг/кг. Увеличение их количества в верхнем горизонте почвы свидетельствует об избыточном поступлении тяжелых металлов из атмосферного воздуха. Содержание ртути колеблется в пределах от 0,01 до 0,8 мг/ кг. Свинца, соответственно, - от 3 до 38, хрома - от 3 до 330, кобальта - от 1 до 15, никеля - от 2 до 70 и меди - от 1 до 140 мг / кг. Решение проблемы получения экологически безопасной продукции на загрязненных территориях невозможно без учета миграции и аккумуляции тяжелых металлов в почвенном профиле. Анализ их содержания в почвах указывает на характерную пространственную и вертикальную неоднородность почв.
Для условного контроля мы брали показатели имеющихся данных по содержанию тяжелых металлов в природных средах (табл. 5.17).
Таблица 5.17- Предельно-допустимые концентрации тяжелых металлов в природных средах
| Металл | Воздух, мг/м3 | Вода, мг/л | Почва, мг/кг | |
| хозяйственно-бытового назначения | подвижная форма | валовая форма | ||
| Pb Cd Cu Zn Ni Co Hg | 0,0003 0,0003 0,001 0,005 0,001 0,001 0,0003 | 0,03 0,001 1,0 1,0 0,1 0,1 0,0001 | 6,0 2,0 3,0 23,0 4,0 5,0 – | 32,0 – 33,0 55,0 20,0 – 2,1 |
Валовое содержание цинка в серых лесных почвах значительно меньше, а в черноземных почвах – больше, чем в пойменных. Особенно существенными являются различия по его содержанию в верхнем двадцати - сантиметровом слое почвы. Подвижность цинка почти в 2 раза больше в верхних слоях почвы (0 – 60 см), чем в нижних слоях. Содержание никеля по профилю серых лесных почв убывает до глубины 80 см, а затем несколько возрастает на глубине от 80 до 100 см. Содержание меди в серых лесных почвах убывает по глубине профиля, а ее подвижность в верхних слоях почвы (0 – 40 см) в 2 раза выше, чем в нижних. Количество хрома в серых лесных почвах повышается на глубине от 0 до 80 см, а затем, в слое 80 – 100 см, выходит на уровень верхнего 20-сантиметрового слоя почвы. Подвижность хрома в серых лесных почвах невысок, в пределах 1,6 – 2 мг/кг.
Для большинства почв характерно наибольшее обогащение ртутью верхней части почвенного профиля (Скрипченко, Золотарева, 1981). Так, в каштановых почвах накопление ртути наблюдается во второй (иллювиальной) полуметровой части профиля. Миграция ртути за пределы почвенного профиля практически не происходит. Скорее происходит аккумуляция ее в верхних горизонтах почв при незначительном содержании в почвообразующих породах, на что необходимо обратить особое внимание. Наибольшее количество ртути накапливается в илистой и мелкопылеватой фракциях почв, что связано с прочным закреплением ртути гумусовыми веществами и глинистыми минералами.
Распределение кадмия по профилю почв хорошо согласуется с особенностями почвообразовательного процесса. В дерново-подзолистых почвах содержание кадмия всегда выше, чем в почвообразующих породах. Наиболее беден кадмием подзолистый горизонт этих почв, тогда как в гумусовом горизонте отчетливо проявляется его аккумуляция. В горизонтах более тяжелых по механическому составу содержание кадмия выше, чем в почвообразующих породах почвы дерново-подзолистой зоны более дифференцированы по профильному распределению кадмия, что связано с образованием ассоциаций с водными оксидами железа и алюминия.
Распределение мышьяка в почвенном профиле зависит от типа почвы. В тяжелосуглинистом черноземе он распределяется равномерно по всему профилю. В подзолистых и бурых горно-лесных почвах его распределение носит элювиально-иллювиальный характер, максимальное содержание находится в иллювиальных горизонтах. Для дерново-подзолистых почв характерно элювиальное распределение мышьяка. Накопление мышьяка в гумусовом горизонте не наблюдается. Характер распределения свинца по профилю почвы аналогичен распределению органического вещества. В кислых дерново-подзолистых почвах происходит перенос свинца в нижние горизонты. В дерново-подзолистых почвах иллювиальный горизонт содержит свинца больше, чем почвообразующие породы или верхние горизонты. Его максимальное содержание в серых лесных почвах отмечается в верхнем слое, что составляет около 40% его валовых запасов. В дерново-глеевых почвах основным барьером на пути передвижения свинца в условиях кислой реакции среды является глиняный горизонт, что связано с высоким содержанием в нем ила (Алексеев 1987).
Повышенное содержание тяжелых металлов в почве нарушает естественные процессы поглощения и передвижения элементов по трофическим цепям. Накопление тяжелых металлов в организмах приводит к развитию многих опасных заболеваний. До последнего времени на нормирование содержания тяжелых металлов в почвах практически не обращали внимания. Если и изучали содержание тяжелых металлов в почве, но не с целью предотвращения чрезмерного накопления, а, наоборот, с целью выявления недостаточности в почвах микроэлементов, таких как цинк, марганец, медь, молибден, кобальт, железо.
Необходимость определения ПДК тяжелых металлов возникла в связи с учащением сообщений об отрицательных последствиях загрязнения почв, проявляющихся в ухудшении гигиенического качества продукции, заболевании животных, и, в конечном счете, ухудшении здоровья человека. Загрязнение почв часто происходит не по вине сельскохозяйственных работников. Из атмосферного воздуха в окрестностях промышленных предприятий и оживленных автомагистралей в почву поступают загрязнители, в том числе и тяжелые металлы. В почвах тяжелые металлы поливалентны, образуют плохо растворимые соединения с фосфатами и гидроокисями, что способствует их постепенному накоплению. В связи с этим необходим постоянный мониторинг состояния почв, так как несущественные, на первый взгляд, количественные изменения, происходящие в результате поступления металлов, могу в определенный момент превысить предельно допустимые его концентрации и, в значительной мере, ухудшить экологическое состояние, особенно, урбанизированных территорий.
studfiles.net
Тяжелые металлы в почвах
Тяжелые металлы — биохимически активные элементы, входящие в круговорот органических веществ и воздействующие преимущественно на живые организмы. К тяжелым металлам относятся такие элементы, как свинец, медь, цинк, кадмий, никель, кобальт и ряд других.
Миграция тяжёлых металлов в почвах зависит, прежде всего, от щёлочно-кислотных и окислительно-восстановительных условий, определяющих разнообразие почвенно-геохимических обстановок. Важную роль в миграции тяжелых металлов в профиле почв играют геохимические барьеры, в одних случаях усиливающие, в других ослабляющие (в силу способности к консервации) устойчивость почв к загрязнению тяжелыми металлами. На каждом из геохимических барьеров задерживается определённая группа химических элементов, обладающая сходными геохимическими свойствами.
Специфика основных почвообразовательных процессов и тип водного режима обусловливают характер распределения тяжелых металлов в почвах: накопление, консервацию или вынос. Выделены группы почв с накоплением тяжелых металлов в разных частях почвенного профиля: на поверхности, в верхней, в средней части, с двумя максимумами. Кроме того, выделены почвы в зоне вечной мерзлоты, которым присуща концентрация тяжелых металлов за счёт внутрипрофильной криогенной консервации. Особую группу образуют почвы, где в условиях промывного и периодически промывного режимов происходит вынос тяжелых металлов из профиля. Внутрипрофильное распределение тяжелых металлов имеет большое значение для оценки загрязнения почв и прогноза интенсивности аккумуляции в них загрязнителей. Характеристика внутрипрофильного распределения тяжелых металлов дополнена группировкой почв по интенсивности их вовлечения в биологический круговорот. Всего выделено три градации: высокая, умеренная и слабая.
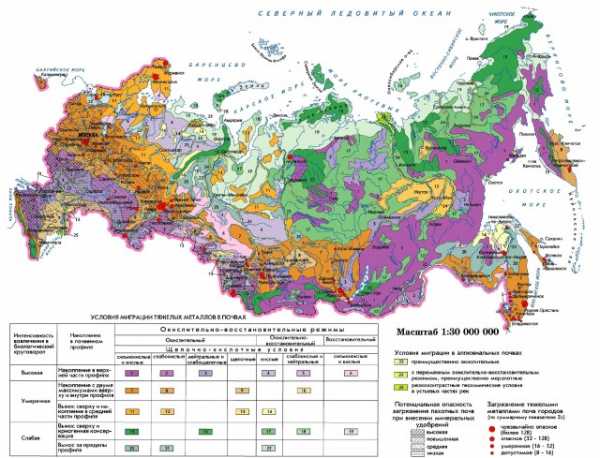
Своеобразна геохимическая обстановка миграции тяжелых металлов в почвах речных пойм, где при повышенной обводнённости значительно возрастает подвижность химических элементов и соединений. Специфика геохимических процессов здесь обусловлена, прежде всего, резко выраженной сезонностью смены окислительно-восстановительных условий. Это связано с особенностями гидрологического режима рек: продолжительностью весенних, наличием или отсутствием осенних паводков, характером меженного периода. Длительность затопления паводковыми водами пойменных террас определяет преобладание либо окислительных (кратковременное затопление поймы), либо окислительно-восстановительных (долгопоёмный режим) условий.
Наибольшим техногенным воздействиям площадного характера подвергаются пахотные почвы. Основной источник загрязнения, с которым в пахотные почвы поступает до 50 % общего количества тяжелых металлов, — фосфорные удобрения. Для определения степени потенциального загрязнения пахотных почв проведен сопряженный анализ свойств почв и свойств загрязнителя: учитывались содержание, состав гумуса и гранулометрический состав почв, а также щелочно-кислотные условия. Данные по концентрации тяжелых металлов в фосфоритах месторождений разного генезиса позволили рассчитать их среднее содержание с учетом приблизительных доз внесения удобрений в пахотные почвы разных районов. Оценка свойств почв соотнесена с величинами агрогенной нагрузки. Совокупная интегральная оценка легла в основу выделения степени потенциального загрязнения почв тяжелыми металлами.
Наиболее опасны по степени загрязнения тяжелыми металлами почвы многогумусовые, глинисто-суглинистые с щелочной реакцией среды: темно-серые лесные, чернозёмы и темно-каштановые — почвы, обладающие высокой аккумулятивной способностью. Повышенной опасностью загрязнения почв тяжелыми металлами характеризуются также Московская и Брянская области. Геохимическая обстановка с дерново-подзолистыми почвами не способствует здесь аккумуляции тяжелых металлов, однако в этих областях техногенная нагрузка велика и почвы не успевают «самоочищаться».
Эколого-токсикологическая оценка почв сельскохозяйственных угодий на содержание тяжелых металлов показала, что 1,7 % земель сельскохозяйственного назначения загрязнено веществами I класса опасности (высокоопасными) и 3,8 % — II класса опасности (умеренно опасными). Загрязнение почв с содержанием тяжелых металльов и мышьяка выше установленных норм выявлено в Республике Бурятия, Республике Дагестан, Республике Карелия, Республике Мордовия, Республике Тыва, в Красноярском и Приморском краях, в Ивановской, Иркутской, Кемеровской, Костромской, Мурманской, Новгородской, Оренбургской, Сахалинской, Читинской областях.
Локальное загрязнение почв тяжелыми металлами связано, прежде всего, с крупными городами и промышленными центрами. Оценка опасности загрязнения почв комплексом тяжелых металлов проводилась по суммарному показателю Zc.
geographyofrussia.com
Изучение тяжёлых металлов в почве
Механизмы поглощения и трансформации ионов тяжёлых металлов в почвах
В системе циклического массообмена металлов особое место занимает почва, в которой сходятся общие миграционные потоки. С одной стороны, в почве мобилизуются металлы, вовлекаемые затем в различные миграционные циклы, с другой – перераспределяются массы металлов, поступающие из почвообразующих пород, с опадом растительности и осаждениями из атмосферы. Регулирование почвой массопотоков металлов обусловлено системой равновесий и взаимопереходов между различными формами нахождения металлов, различающихся прочностью закрепления и способностью включаться в тот или иной вид миграции. Избыточные массы металлов, поступившие в биосферу в силу природных явлений в результате техногенного загрязнения, выводятся из системы миграционных циклов и прочно связываются в твёрдой фазе почвы, откуда они могут постепенно мобилизоваться и пополнять отдельные массопотоки.
Содержание в почве тяжёлых металлов и сопряжённая с этим транслокация их в растения – сложный процесс, на который влияет множество факторов. Чтобы понять механизм воздействия каждого из них, следует изучить влияние отдельных факторов в условиях эксперимента.
О характере связывания свинца и кадмия можно судить по их содержанию в почвах и зависимости профильного распределения от свойств почв. В почвы свинец и кадмий поступают в виде примесей в удобрениях, галогенидов и оксидов этих металлов, которые содержатся в выхлопных газах автомобилей при использовании тетраэтилсвинца в качестве добавки к бензину, в составе отходов, образующихся при добыче и переработке отработанных аккумуляторных батарей.
Исследованиями ряда авторов установлено, что содержание свинца составляет от 2 до 300 мг/кг. Средние значения для антропогенно незагрязнённых ландшафтов оценивается как 15 – 17 мг/кг в почвах лёгкого состава и 17 – 22 мг/кг в почвах тяжёлого состава.
В поверхностном горизонте содержание свинца чаще всего оказывается наиболее высоким. В промышленных и рудодобывающих районах это относят за счёт антропогенного воздействия. Тем не менее, повышенная концентрация свинца в поверхностном слое не обязательно означает загрязнение слоя за счёт атмосферных выпадений. Почти во всех незагрязненных районах содержание элемента существенно больше в лесной подстилке и гумусовых горизонтах, особенно в корнеобитаемой зоне. Можно предположить, что такое распределение формируется из-за перераспределения свинца, содержащегося в почвообразующейся породе, под влияние выноса его растениями и последующем накоплении в лесной подстилке и гумусовом горизонте, в которых концентрации свинца оказываются максимальными. В целом, валовое содержание свинца и его профильное распределение не информативны для понимания характера связывания этого элемента в почвах, доступности растениям и возможности выноса его из почвы с поверхностным или грунтовым стоком. Решающее значение для ответа на эти вопросы, очевидно, должен иметь химический состав и свойства соединений, в составе которых металл находится.
В почве подавляющая часть свинца находится в виде твёрдых соединений. Рекомендуемые в литературе методики , позволяют выделить лишь некоторые условные фракции свинца, которые нельзя отнести к каким-то определенным химическим соединениям.
В целом, они дают всё же основание полагать, что в кислых почвах существует часть свинца, вплоть до 70%, способная действительно обмениваться на другие ионы; в нейтральных почвах преобладают фракции, «связанные с оксидами Fe – Mn» и органическим веществом, а в слабощелочных и щелочных условиях свинец распределён между «карбонатной», «органической» и «остаточной» фракциями. Тем не менее, химический состав и свойства соединений, присутствие которых обусловливает наличие элемента в этих «фракциях», остаются неясными. Таким образом, само по себе «фракционирование» сравнительно малоинформативно.
Твёрдые соединения свинца в почвах находятся во взаимодействии с почвенным раствором, через который происходит как поступление элемента в растения, так и внутрипочвенная миграция, и трансформация его соединений. Характер связывания свинца в твёрдых составляющих, очевидно, и определяет его концентрацию в растворе, которая должна, таким образом, отражать свойства соединений, в которых находится свинец. Чтобы понять причины появления свинца в почвенном растворе, необходимо проанализировать свойства соединений этого элемента, которые могли бы присутствовать в почвах, и возможные механизмы его связывания.
Физико-химические оценки механизмов поглощения Pb (II)
В качестве механизмов связывания свинца авторы называют осаждение его малорастворимых солей и обменное или необменное поглощение гидроксидами металлов, силикатами и органическим веществом почв.
К малорастворимым соединениям свинца относят природные минералы, основными из которых является галенит (PbS), встречающийся во многих районах земного шара, а так же рудные минералы англезит (PbSO4), церуссит (PbCO3), пироморфит (PbCl2 х 3Pb3(PO4)2 ) и милитезит (PbCl2 х 3Pb3(AsJ4)3). Эти соединения, очевидно, и попадают в почвы вблизи разработок рудных месторождений. Металлический свинец сравнительно устойчив к воздействию природных факторов, поскольку под влиянием воздуха и паров воды на его поверхности образуется плёнка оксикарбоната, защищающая металл от дальнейшего окисления. Воздействие воды, содержащей растворённый кислород, приводит к образованию гидроксидов свинца, растворение которых и делает воду токсичной.
Оксид свинца (II) образуется при нагревании металла на воздухе. Другими оксидами являются Pb6O2 и Pb3O4. Первый из них входит в состав пластин свинцовых аккумуляторов, второй используют в качестве пигмента красок. В щелочных растворах образуются гидроксомплексы 4+, 3+, 2+, +, 4+, 0.
Нитрат свинца хорошо растворим в воде, но при его диссоциации в воде образуется стабильный комплекс.
Оксигалиды свинца Pb2 OCl2, Pb3O2CI2, Pb3 OCl4 известны как минералы.
Гидрофосфат (PbHPO4) образует малорастворимый в воде минерал монетит.
Соединения с общей формулой, где X – Сl, Br или OH называют апатитами свинца. Хлорапатит свинца встречается в природе в виде минерала хлоропироморфита (Pb5(PO4)3Сl). Карбонат PbCO3 является одним из наименее растворимых соединений свинца.
В природе он встречается в виде минерала церуссита. Растворимость его заметно возрастает в присутствии растворимого в воде СО2. Ещё менее растворим сульфид свинца – галенит. На воздухе он постепенно окисляется, в результате чего при нахождении сульфидной руды на воздухе галенит постепенно покрывается сначала коркой англезита PbSO4, который затем с поверхности переходит в церуссит.
Растворимость некоторых соединений свинца и их произведения растворимости приведены в таблице 1.
Исходя из этих данных можно сделать вывод о том, что в жидкой фазе почв концентрацию элемента могли бы контролировать только карбонат, сульфид и пироморфит свинца.
Наличие в почвах кальцита, концентрация которого существенно выше, чем у церуссита, приводит к появлению в почвенном растворе ионов карбонатов и гидрокарбанатов в концентрациях, достаточных для осаждения ионов свинца из раствора.
В присутствии кальцита при характерном для многих почв содержанием углекислого газа около 0,3% содержание свинца составляет 31 мкг/л.
Таким образом, в карбонатных почвах связывание ионов свинца происходит за счёт осаждения церуссита.
Таблица 1
Растворимость некоторых соединений Pb (II) в воде.
| соединение | растворимость | -lg (ПР) | t, С | |
| мг/л | моль/л | |||
| Pb(OH)2 | 11,4 | 5,5*10 | 15 | 25 |
| PbCl2 | 5745-12830 | 2,77*10-6,2*10 | 4,67-3,62 | 25 |
| PbCO3 | 0,037 | 1,8*10 | 13,48 | 18 |
| PbHPO4 | 2,3 | 1,8*10 | 9,92 | 25 |
| PbSO4 | 37 | 1,8*10 | 7,8 | 25 |
| PbS | 6*10 | 2,8*10 | 27,1 | 25 |
| Pb5(PO4)3Cl | 1*10 | 5*10 | 83,7 | 25 |
Альтернативным механизмом поглощения свинца является обменное или необменное поглощение Pb (II) оксидами – гидроксидами Fe и Mn, глинистыми минералами и органическим веществом почв. В условиях лабораторного эксперимента исследователи установили, что оксидами – гидроксидами железа в интервале рН от 3,5 до 5,5 практически полностью поглощают ионы свинца из раствора.
Оксиды Mn так же связывают растворённый свинец, рН влияет на этот процесс в существенно меньшей степени. Практически не оказывает на него влияния и изменения поверхности твёрдой фазы. От 20 до 93% свинца, поглощённого свежеосаждёнными оксидами марганца, не удавалось экстрагировать 25% уксусной кислотой, а после «состаривания» в течение 28 недель для доля этой неэкстрагируемой фракции возросла до 37 – 100% поглощения Pd (II). Для свежеосаждённого и «состаренного» гетита доля экстрагируемого такой кислотой свинца составляла, соответственно, 10 – 44 и 19 – 62%. Можно сделать вывод о том, что при взаимодействии свинца даже с простыми сорбентами часть его оказывается более прочно связанной, а часть менее, то есть, проявляется неоднородность «сорбционных центров».
Чтобы заряд поверхности частиц оставался неизменным, поглощение свинца почвами и их составляющими должно сопровождаться вытеснением в раствор каких то других ионов. Связывание 1 моль Pb (II) гидроксидами Mn при рН 4, по данным, приводит к вытеснению H+ в количестве 1 моль для бирнессита и 1,3 моль для криптомелона. Для гидроксидов железа (гематита и петита) это отношение составило соответственно 1,3 и 2 моль. Авторами работы, выдвинуто предположение о том, что поглощение свинца из кислых растворов происходит в соответствии с уравнением:
SOH0 + Pb2+ = + H+, (1)
где SOH0 – незаряженный участок поверхности, а формула в квадратных скобках отражает поглощенную форму катиона свинца.
С ростом рН можно ожидать поглощение моногидроксокомплекса:
SOH0 + Pb 2+ + Н2О = + 2Н+ (2)
С дальнейшим поверхностно - индуцированным межфазным осаждением гидроксида металла в соответствии с выражением:
S + Pb 2+ + 2 Н2О = + 2Н+ (3)
Для оксидов железа резкое увеличение поглощения в узком диапазоне рН автор приписывает достижению уровня рН, при котором становится возможным поглощение PbOH+. Соединения в составе которых есть свинец на поверхности оксидов – гидроксидов, относят к поверхностным внутрисферным комплексам.
Почвы с большим содержанием гумуса не проявляли большей селективности по отношению к Pb 2+. Наиболее селективными сорбентами оказались оксиды железа.
«Сверх – эквивалентное» поглощение обнаружено, согласно, при связывании почвами других катионов, например катионов меди. В соответствии с данными исследований, поглощение катионов почвами принято подразделять на «неспецифическое» и «специфическое». Под «неспецифическим» обычно понимают связывание катионов за счёт действия электростатических сил в двойном электрическом слое, а «специфическое» относят за счёт формирования координационных связей с поверхностью через атомы кислорода или группы – ОН. «Сверх – эквивалентное» поглощение происходит именно за счёт механизма, неселективного поглощения по отношению к ионам Pb 2+.
Об особенностях механизма связывания свинца почвами, подтверждающих гипотезу , можно судить по тому, что его величина не пропорциональна ёмкости катионного обмена.
Предложены и другие гипотезы механизма поглощения свинца в почвах. В частности, другим типом взаимодействия может быть образование комплексов свинца с органическим веществом, сорбированными на поверхности глинистых частиц. Высказывается мнение о том , что роль глинистой фракции в поглощении свинца незначительна по сравнению с ролью органического вещества.
Роль органического вещества неоднозначна и с другой точки зрения : выделенные из почв гуминовые кислоты прочно связывали часть свинца, но 65% удержанного ими свинца оказывались в обменной фракции.
Выделяемая 1н. HNO3 фракция свинца, по мнению авторов , входит в состав комплексных соединений с гуминовыми кислотами. Катионы Pb 2+ могут быть связаны с гуминовыми кислотами либо через карбоксильные, либо через гидроксильные группы.
Недиссоциированные слабокислые ОН – группы сахаров и фенолов также, возможно, участвуют в образовании таких комплексов.
Итак, на основе приведённых данных подтверждённые и гипотетические механизмы поглощения свинца можно представить в виде схемы, показанной в таблице 2.
Таким образом, на современном этапе исследования механизмов поглощения металла можно утверждать, что, во-первых, существуют некоторые условные фракции свинца в почвах, которые нельзя отнести к тем или иным химическим соединениям. Во-вторых, в зависимости от свойств почв металл можно сделать практически полностью недоступным для растений и иммобильным.
Таблица 2
Механизмы поглощения Р b (II) в почвах
| Тип поглощения | На чем происходит связывание | Характер взаимодействия |
| Обменное осаждение | Оксиды-гидроксиды Fe и Мn | -образование поверхностных комплексов по уравнениям (1) и (2) |
| Силикатные материалы |
-электростатическое или полярное с участием Si – О –группы проникновение в межплоскостные
промежутки алюмосиликатов -связывание на цеолитах |
|
| Органическое вещество | -полярное, через карбоксильные группы полярное, через фенольные группы | |
| Необменное осаждение | Оксиды-гидроксиды Fe и Mn, силикатные минералы и органическое вещество |
-выпадение в осадок PbCO3 или пироморфита -связывание ионов или заряженных комплексов на поверхности с изменением заряда поверхности -связывание на цеолитах |
Содержание кадмия в почвенных растворах
В почвы кадмий поступает в составе отходов, образующихся, при добыче и переработке цинковых, свинцово-цинковых, медно-цинковых руд, а также в виде примесей оксидов, сульфидов и иных галогенидов, содержащихся в выхлопных газах автомобилей, попадает с суперфосфатом, как примесь, и входит в состав фунгицидов. Он добавляется для прочности в пластмассу и при её сжигании в мусоре попадает в биосферу. Основной источник загрязнения почвы кадием -–добыча и металлургия цинка, а также производство красок и электротехнической продукции. Распространенность Сd в магматических и осадочных породах не превышает 0,3 мг/кг. Этот элемент, по-видимому, концентрируется в глинистых осадках и сланцах. Геохимия Сd тесно связана с геохимией Zn, но кадмий обнаруживает большую, чем Zn, подвижность в кислых средах. При выветривании Cd легко переходит в раствор, где присутствует в виде Cd2+. Он может образовывать также комплексные ионы (CdCl,+ CdOH,+ CdHCO3,+CdCl3-, CdCl42-,Cd(OH)3-, и Cd(OH)42-) и органические хелаты. Главное валентное состояние Cd+2 в природных средах, и наиболее важные факторы, контролирующие подвижность ионов Cd, - это pH и окислительно-восстановительный потенциал. В сильно окислительных условиях Cd способен образовывать собственные минералы (CdO, CdCO3 ), а также накапливаться в фосфатах и биогенных осадках.
Главный фактор, определяющий содержание Cd в почвах, - это химический состав материнских пород. Среднее содержание кадмия в почвах, по данным, лежат между 0,07 и 1,1 мг/кг. При этом фоновые уровни Cd в почвах, по-видимому, не превосходят 0,5 мг/кг, и все более высокие значения свидетельствуют об антропогенном вкладе в содержание металла в верхнем слое почв.
Кадмий, подобно ванадию и цинку, аккумулируется в гумусовой толще почв. Вынос его за пределы почвенного профиля невелик. Характер распределения в почвенном профиле и ландшафте, видимо, имеет много общего с другими металлами, в частности, с ходом распределения свинца. Однако кадмий закрепляется в почвенном профиле менее прочно, чем свинец. Максимальная адсорбция кадмия свойственна нейтральным и щелочным почвам с высоким содержанием гумуса и высокой ёмкостью поглощения.
В почвах лёгкого механического состава и обеднённых гумусом процессы миграции кадмия усиливаются.
В последние годы широко исследовалась сорбция различных форм Cd компонентами почв. Было установлено, что в связывании кадмия ведящим процессом является конкурирующая адсорбция на глинах. Данные ряда авторов подтверждают мнение, что именно адсорбция, а не осаждение контролируют концентрацию Cd в почвенных растворах до тех пор, пока не будет превышена некоторая предельная величина рН при рН выше 7,5 сорбированный почвой Cd перестаёт быть легкоподвижным, поэтому контролировать его подвижность в почве будут растворимость CdCO3 и, возможно, Cd3 (PO4 )2.
Растворимость Cd, по-видимому, сильно зависит от рН, однако важное значение имеет также природа сорбирующих поверхностей и органических лигандов. Адсорбция Cd на органическом веществе, а также оксидах Fe и Мп была детально изучена рядом исследователей. Все полученные данные приводят к выводу, что в любой почве активность Cd сильно зависит от рН. В кислых почвах органическое вещество и полуторные оксиды могут в значительной степени контролировать растворимость Cd, а в щелочных почвах при рассмотрении равновесий с участием Cd надо, по-видимому, учитывать осаждение кадмиевых соединений.
Концентрация Cd в почвенных растворах относительно низкая и, по имеющимся данным, составляет 0.2-6 мкг/л. Гораздо более высокое значение (300мкг/л) вероятно, указывает на заражение почвы. В почвах, развивающихся в условиях гумидного климата миграция Cd вниз по профилю более вероятна, чем его накопление в поверхностном горизонте почв, поэтому часто наблюдаемое обогащение кадмием поверхностных слоёв должно быть связано с загрязнением. Загрязнение почв кадмием рассматривается как наиболее серьёзная опасность для здоровья и поэтому для охраны окружающей среды было проведено изучение ряда методов, предназначенных для управления режимом обогащенных Cd сельхоз. угодий. Как и в случае цинкового заражения почв, эти методы основаны на повышении рН и катионообменной емкости почв. Известкование в целом рассчитано на ослабление поглощения Cd при увеличении рН почвы, но оно эффективно не для всех почв и растений. Наиболее надежные результаты по снижению биодоступности Cd были получены при насыпке поверх загрязненной почвы слоя незаражённой почвы толщиной до 30 см.
Поглощение соединений Cd (II) и перенос их растениями
Считается, что Cd не входит в число необходимых для растений элементов, однако он эффективно поглощается как корневой системой, так и листьями. Растворимые формы Cd в почве всегда легко доступны растениям. Заметная доля Cd поглощается корнями пассивно, но поглощаться может также и метаболическим путём. Усиление обработки кадмием постепенно снижает его долю, перемещающуюся в поверхностные части молодых листьев. При этом Cd локализуется главным образом в корнях, и, в меньших количествах, - в узлах стеблей, черенках и главных жилках листьев.
Известно, что большая часть Cd аккумулируется в тканях корней, даже если он попадает в растения через листья. Перенос кадмия в растении может иметь ограниченные масштабы из-за того, что он легко захватывает большинство обменных позиций в активных веществах, расположенных на клеточных стенках.
Кадмий считается токсичным элементом для растений, и основная причина токсичности связана с нарушением энзиматической активности. Подавляется образование и хлорофилловых пигментов у растений, обработанных кадмием. Видимые симптомы заражения – это задержка роста, повреждение корневой системы, хлороз листьев, красно-бурая окраска их краёв или прожилков. Фитотоксичность кадмия проявляется в тормозящем действии на фотосинтез, нарушение транспирации и фиксации СО2, изменении проницаемости клеточных мембран.
Содержащийся в растениях кадмий представляет наибольшую опасность, так как может служить источником поступления в организмы человека и животных. Поэтому толерантность и адаптация некоторых растительных видов к повышенным содержаниям кадмия, хотя они и возможны с точки зрения охраны окружающей среды, представляют угрозу для здоровья человека.
Таким образом, представленные в литературе сведения указывают на недостаточную изученность химических форм Cd в почве и почвенном растворе. Предполагается, что доминирующей формой Cd в почвенном растворе в широком диапазоне рН является ионная и гидратированная форма, связанная с минеральными частицами почвы.
Использование почвенных вытяжек при изучении соединений тяжёлых металлов
В настоящее время существует два главных подхода к изучению соединений ТМ и, соответственно, две группы методов, позволяющих оценить их содержание в почвах.
При изучении подвижных соединений тяжёлых металлов в почвах в качестве групповых экстрагентов широко применяют разбавленные (соли) растворы азотной, соляной и серной кислот, ацетатно-аммонийный буферный раствор, раствор ЭДТА и других комплексонов, нейтральные растворы солей. Кислые буферные вытяжки в наилучшей степени удовлетворяют требованиям универсальных экстрагентов подвижных соединений. Однако следует учитывать изменчивость в экстрагируемости тяжёлых металлов, как во времени, так и при смене экстрагентов. В работах Садовниковой наблюдаемая изменчивость реакций тяжёлых металлов в почве на химические экстрагенты вызывала необходимость перехода от единичных экстрагентов к их последовательности, так как это даёт возможность выделить фракции тяжёлых металлов, различающиеся по доступности подвижности растениям, проследить динамику перехода ТМ от одной химической формы к другой в зависимости от изменения почвенных условий. Схемы почвенного фракционирования делятся на две основные группы:
1) фракционирование в зависимости от содержания тяжёлых металлов в почвенных компонентах – органическом веществе, гидроксидах железа, алюминия, марганца, илистой фракции
2) фракционирование с учётом доступности тяжёлых металлов той или иной вытяжке – выделение водорастворимой, обменной, органической минеральной фракций.
Эти схемы, имея разную направленность, принципиально не различаются. Обе имеют определённые недостатки – нельзя полностью разделить почву на компоненты, не вызывая при этом перераспределения тяжёлых металлов. За время экстрагирования определённое количество ТМ может перейти в обменную форму, которая извлекается частично с фракцией органического вещества, при чём наиболее растворимые и наименее устойчивые соединения будут извлечены вместе с органическим веществом. Таким образом, деление почвы на несколько фракций является условным.
Для экспрессной оценки подвижных форм металлов в почвах предложены следующие вытяжки:
1н. (для некарбонатных) и 2н. (для карбонатных) растворов HCl в качестве комплексного экстрагента условно подвижных форм;
1%-ный раствор ЭДТА в ацетатно-аммонийном буферном растворе с рН 4,5 как экстрагент комплексно-связанных форм ацетатно-аммонийный буферный раствор с рН 4,5 как экстрагент водорастворимых и обменных форм.
Каждый экстрагент действует на почву в двух направлениях: по степени агрессивности воздействия и по степени избирательности к определённой фракции. Используют различные схемы экстрагирования, причём большинство из них направлено на извлечение следующих фракций тяжёлых металлов по подвижности:
обменная – извлекается растворами нейтральных солей
органическая – извлекается реагентами, действующими на органическое вещество
оксиды и гидроксиды – извлекаются оксалатным буферным раствором
минеральная – полное разложение смесью сильных кислот остатка почвы.
Очевидно, можно считать установленным наличие в почве следующих соединений ТМ:
растворимые – свободные ионы и растворимые комплексы ТМ с неорганическими анионами или органическими лигандами различной прочности;
обменные – ТМ удерживаются в основном электростатическими силами на глинистых и других минералах, органическом веществе и на аморфных соединениях с низким рН нулевого заряда;
специфически сорбированные – тяжёлые металлы удерживаются в основном ковалентными и координационными связями;
тяжёлые металлы на устойчивом органическом веществе – тяжёлые металлы удерживаются с помощью комплексообразования и хелатизования на собственно органическом веществе или органическом веществе, связанном с катионами железа, алюминия, кальция, с оксидами и гидроксидами железа и алюминия, с глинистыми минералами;
тяжёлые металлы на оксидах-гидроксидах железа, алюминия, магния– окклюдированные катионы внутри аморфных соединений или адсорбированные на их поверхности;
осадки (преципитаты) – соли тяжёлых металлов, представляют собой смешанные кристаллы или смеси кристаллов разных элементов; тяжёлые металлы первичных и глинистых минералов.
При изучении соединений тяжёлых металлов с помощью почвенных вытяжек существенно осложняет исследования фактор переосаждения тяжёлыми металлами. При экстракции реагент, удаляя почвенный компонент путём комплексообразования или разрушения, выделяет в раствор содержащиеся в нём тяжёлые металлы. Параллельно этот процесс порождает образование новых адсорбционных мест на аморфных соединениях, вызывая переосаждение поступивших в раствор ТМ, поскольку нет реагента, действующего сразу на все фазы почвы. Поэтому при выделении одного компонента реагент, по крайней мере, активизирует поверхности других компонентов, вызывая перераспределение поступивших в раствор ТМ.
Значительное влияние на данные последовательных вытяжек оказывает состояние анализируемого образца. Кроме того, экстрагируемость тяжёлых металлов зависит от степени измельчения образца, поскольку измельчение вызывает освобождение глинистых частиц и первичных минералов от органических и оксидных плёнок, увеличивает площадь поверхности, изменяя тем самым характеристики образца в отношении доступности тяжёлых металлов вытяжками.
Таким образом, можно сделать вывод, что достоверные данные о подвижности тяжёлых металлов и формах их связи можно получить лишь в нативном образце, то есть в естественных условиях.
В настоящей работе предпринята попытка с помощью метода последовательных вытяжек оценить относительную подвижность тяжёлых металлов и возможные формы связи с почвенными компонентами в условиях лабораторного эксперимента.
Проявление фитотоксичности тяжёлых металлов в «системе почва – растение»
В связи с возрастающими масштабами техногенного загрязнения почв, особенно в пригородных зонах промышленных центров, необходим постоянный контроль за почвой и гигиеническая оценка производимой на ней продукции.
Растения, будучи чуткими индикаторами геохимической среды, накапливают металлы из загрязненных почв и воздуха и могут аккумулировать самые разные металлы в зависимости от характера промышленного загрязнения.
В условиях земледельческой части Красноярского края эта проблема решается не достаточно полно. Не изучено влияние ТМ при повышенных концентрациях на урожай, качество растениеводческой продукции.
Для исследования этих вопросов Государственный центр агрохимической службы «Красноярский» в 1994-1996 годах провёл мелко-деляночный полевой опыт. В ходе опыта изучали в севообороте на фоне минеральных органических удобрений аккумуляцию свинца и кадмия в почве, продуктивной части растений и их влияние на качество урожая.
Почва опытного участка – тёмноцветная пойменная, среднесуглинистая с содержанием в пахотном слое гумуса 2,6-3,4%, рНсол 6.6-6.8. Исследования проводили в звене овоще – кормового севооборота; капуста белокочанная поздняя – однолетние травы – черный пар, повторность опыта четырёхкратная.
Исследованиями установлено , что при внесении минеральных удобрений отмечалась тенденция к повышению исходного содержания в почве кадмия и свинца. Внесение водорастворимых солей Cd и Pb на фоне минеральных удобрений при выращивании капусты достоверно повышало содержание этих элементов в почве. С увеличением норм внесения концентрация Cd и Pb в пахотном слое почвы возрастала. Совместное внесение минеральных и органических удобрений способствовало снижению содержания Pb в почве.
В отличие от свинца, кадмий - более подвижный элемент, его аккумуляция в варианте с минеральными и при совместном их внесении с органическими удобрениями происходит интенсивнее.
В первый год опыта содержание Cd и Pb в почве достигала значений, превышающих предельно допустимую концентрацию (ПДК).
Внесение солей тяжёлых металлов способствовало повышению содержания подвижных форм Cd и Pb в почве. При этом более высокое их содержание отмечалось в вариантах с внесением повышенных количеств этих элементов. На фоне совместного внесения минеральных и органических удобрений содержание подвижной формы Pb уменьшалось, а количество Cd увеличивалось.
В последействии, при выращивании однолетних трав, также отмечалось высокое содержание в почве свинца и кадмия по сравнению с контролем. Если свинец, внесенный в повышенной форме, накапливается в значениях, не превышающих санитарные нормы, то содержание кадмия превышало ПДК.
На второй год последействия в паровой делянке валовое содержание Cd и Pb продолжало уменьшаться. Свинец аккумулировался в почве в значениях ниже ориентировочно – допустимых концентраций. В то же время содержание Cd в почве оставалось высоким, и в вариантах с внесением повышенных норм превосходило установленные санитарные нормы.
Валовое содержание Pb в кочанах поздней капусты не превышало ПДК, а содержание Cd находилось в пределах гигиенически допустимого количества. В последствии содержание кадмия и свинца в растениях однолетних трав оставалось довольно высоким. Если содержание Pb в зеленой массе трав не превышало нормативного уровня, то содержание Cd было выше санитарных норм.
Загрязнение почв кадмием и свинцом не оказывало существенного влияния на величину урожая поздней капусты, однолетних трав и биохимический состав выращенной продукции.
Таким образом, внесение Cd и Pb способствовало их транслокации в темноцветной пойменной почве. Из-за слабой подвижности свинца и наличия у растений защитных функций аккумуляция этого элемента в продуктивной части растений не отмечалась. Однако кадмий загрязнял растениеводческую продукцию.
biofile.ru