Функции ядерной оболочки: строение мембраны, участие в процессе деления. Растения ядерная оболочка
37. Ядерная оболочка строение,функции,роль ядра при взаимодействии с цитоплазмой.
Роль ядра:Ядро осуществляет две группы общих функций: одну, связанную собственно с хранением генетической информации, другую - с ее реализацией, с обеспечением синтеза белка.
В первую группу входят процессы, связанные с поддержанием наследственной информации в виде неизменной структуры ДНК. Эти процессы связаны с наличием так называемых репарационных ферментов, ликвидирующих спонтанные повреждения молекулы ДНК (разрыв одной из цепей ДНК, часть радиационных повреждений), что сохраняет строение молекул ДНК практически неизменным в ряду поколений клеток или организмов. Далее, в ядре происходит воспроизведение или редупликация молекул ДНК, что дает возможность двум клеткам получить совершенно одинаковые и в качественном и в количественном смысле объемы генетической информации. В ядрах происходят процессы изменения и рекомбинации генетического материала, что наблюдается во время мейоза (кроссинговер). Наконец, ядра непосредственно участвуют в процессах распределения молекул ДНК при делении клеток.
Другой группой клеточных процессов, обеспечивающихся активностью ядра, является создание собственно аппарата белкового синтеза. Это не только синтез, транскрипция на молекулах ДНК разных информационных РНК и рибосомных РНК. В ядре эукариотов происходит также образование субъедениц рибосом путем комплексирования синтезированных в ядрышке рибосомных РНК с рибосомными белками, которые синтезируются в цитоплазме и переносятся в ядро.
Таким образом, ядро представляет собой не только вместилище генетического материала, но и место, где этот материал функционирует и воспроизводится. Поэтому выпадение лил нарушение любой из перечисленных выше функций губительно для клетки в целом. Так нарушение репарационных процессов будет приводить к изменению первичной структуры ДНК и автоматически к изменению структуры белков, что непременно скажется на их специфической активности, которая может просто исчезнуть или измениться так, что не будет обеспечивать клеточные функции, в результате чего клетка погибает. Нарушения редупликации ДНК приведут к остановке размножения клеток или к появлению клеток с неполноценным набором генетической информации, что также губительно для клеток. К такому же результату приведет нарушение процессов распределения генетического материала (молекул ДНК) при делении клеток. Выпадение в результате поражения ядра или в случае нарушений каких-либо регуляторных процессов синтеза любой формы РНК автоматически приведет к остановке синтеза белка в клетке или к грубым его нарушениям.
Значение ядра как хранилища генетического материала и его главная роль в определении фенотипических признаков были установлены давно. Немецкий биолог Хаммерлинг одним из первых продемонстрировал важнейшую роль ядра. Он выбрал в качестве объекта своих экспериментов необычайно крупную одноклеточную (или неклеточную) морскую водоросль Acetabularia .
Хаммерлинг показал, что для нормального развития шляпки необходимо ядро. В дальнейших экспериментах, в которых соединяли нижнюю часть, содержащую ядро одного вида с лишенным ядра стебельком другого вида, у таких химер всегда развивалась шляпка, типичная для того вида, которому принадлежит ядро.
При оценке этой модели ядерного контроля следует, однако, учитывать примитивность организма, использованного в качестве объекта. Метод пересадок был применен позднее в экспериментах, проведенных в 1952 г. двумя американскими исследователями, Бриггсом и Кингом, с клетками лягушки Rana pipenis . Эти авторы удаляли из неоплодотворенных яйцеклеток ядра и заменяли их ядрами из клеток поздней бластулы, уже проявлявших признаки дифференцировки. Во многих случаях из яиц реципиентов развивались нормальные взрослые лягушки.
Говоря о клеточном ядре, мы имеем в виду собственно ядра эукариотических клеток. Их ядра построены сложным образом и довольно резко отличаются от УядерныхФ образований, нуклеоидов, прокариотических организмов. У последних в состав нуклеоидов (ядроподобных структур) входит одиночная кольцевая молекула ДНК, практически лишенная белков. Иногда такую молекулу ДНК бактериальных клеток называют бактериальной хромосомой , или генофором (носителем генов). Бактериальная хромосома не отделена мембранами от основной цитоплазмы, однако собрана в компактную ядерную зону - нуклеоид , который можно видеть в световом микроскопе после специальных окрасок.
Сам термин ядро впервые был применен Броуном в 1833 г. Для обозначения шаровидных постоянных структур в клетках растений. Позднее такую же структуру описали во всех клетках высших организмов.
Клеточное ядро обычно одно на клетку (есть примеры многоядерных клеток), состоит из ядерной оболочки, отделяющей его от цитоплазмы, хроматина, ядрышка, кариоплазмы (или ядерного сока) (рис). Эти четыре основных компонента встречаются практически во всех неделящихся клетках эукариоти-ческих одно- и многоклеточных организмов.
Ядра имеют обычно шаровидную или яйцевидную форму; диаметр первых равен приблизительно 10 мкм, а длина вторых - 20 мкм.
Ядро необходимо для жизни клетки, поскольку именно оно регулирует всю ее активность. Связано это с тем, что ядро несет в себе генетическую (наследственную) информацию, заключенную в ДНК.
Ядерная оболочка
Эта структура характерна для всех эукариотических клеток. Ядерная оболочка состоит из внешней и внутренней мембран, разделенных перинуклеарным пространством шириной от 20 до 60 нм. В состав ядерной оболочки входят ядерные поры.
Мембраны ядерной оболочки в морфологическом отношении не отличаются от остальных внутриклеточных мембран: они имеют толщину около 7 нм и состоят из двух осмиофильных слоев.
В общем виде ядерная оболочка может быть представлена, как полый двухслойный мешок, отделяющий содержимое ядра от цитоплазмы. Из всех внутриклеточных мембранных компонентов таким типом расположения мембран обладают только ядро, митохондрии и пластиды. Однако ядерная оболочка имеет характерную особенность, отличающую ее от других мембранных структур клетки. Это наличие особых пор в оболочке ядра, которые образуются за счет многочисленных зон слияний двух ядерных мембран и представляет собой как бы округлые перфорации всей ядерной оболочки.
Строение ядерной оболочки
Внешняя мембрана ядерной оболочки, непосредственно контактирующая с цитоплазмой клетки, имеет ряд сруктурных особенностей, позволяющих отнести ее к собственно мембранной системе эндоплазматического ретикулума. Так, на внешней ядерной мембране обычно располагается большое количество рибосом. У большинства животных и растительных клеток внешняя мембрана ядерной оболочки не представляет собой идеально ровную поверхность - она может образовывать различной величины выпячивания или выросты в сторону цитоплазмы.
Внутренняя мембрана контактирует с хромосомным материалом ядра (см. Ниже).
Наиболее характерной и бросающейся в глаза структурой в ядерной оболочке является ядерная пора . Поры в оболочке образуются за счет слияния двух ядерных мембран в виде округлых сквозных отверстий или перфораций с диаметром 80-90 нм. Округлое сквозное отверстие в ядерной оболочке заполнено сложноорганизованными глобулярными и фибриллярными структурами. Совокупность мембранных перфораций и этих структур называют комплексом пор ядра. Тем самым подчеркивается, что ядерная пора не просто сквозная дыра в ядерной оболочке, через которую непосредственно вещества ядра и цитоплазмы могут сообщаться.
Сложный комплекс пор имеет октагональную симметрию. По границе округлого отверстия в ядерной оболочке располагаются три ряда гранул, по 8 штук в каждом: один ряд лежит со стороны ядра, другой - со стороны цитоплазмы, третий расположен в центральной части пор. Размер гранул около 25 нм. От этих гранул отходят фибриллярные отростки. Такие фибриллы, отходящие от периферических гранул, могут сходиться в центре и создавать как бы перегородку, диафрагму , поперек поры. В центре отверстия часто можно видеть так называемую центральную гранулу.
Число ядерных пор зависит от метаболической активности клеток: чем выше синтетические процессы в клетках, тем больше пор на единицу поверхности клеточного ядра.
Количество ядерных пор в различных объектах
| Объект | Число ядерных пор на мкм 2 | Число пор на одно ядро |
| Ксенопус, почки | 10,05 | 3417 |
| Ксенопус, ооцит | 51,0 | 37,6*10 6 |
| Крыса, гепатоцит | 16,1 | 3816 |
| Мышь, лимфоцит | 3,3 | 403 |
| Человек, лимфоцит | 4,47 | 713 |
Химия ядерной оболочки
В составе ядерных оболочек обнаруживаются небольшие количества ДНК (0-8%), РНК (3-9%), но основными химическими компонентами являются липиды (13-35%) и белки (50-75%), что для всех клеточных мембран.
Состав липидов сходен с таковым в мембранах микросом или мембранах эндоплазматической сети. Ядерные оболочки характеризуются относительно низким содержанием холестерина и высоким - фосфолипидов, обогащенных насыщенными жирными кислотами.
Белковый состав мембранных фракций очень сложен. Среди белков обнаружен ряд ферментов, общих с ЭР (например, глюкозо-6-фосфатаза, Mg-зависимая АТФаза, глютамат-дегидрогеназа и др.) не обнаружена РНК-полимераза. Тут выявлены активности многих окислительных ферментов (цитохромоксидазы, НАДН-цитохром-с-редуктазы) и различных цитохромов.
Среди белковых фракций ядерных мембран встречаются основные белки типа гистонов, что объясняется связью участков хроматина с ядерной оболочкой.
Ядерная оболочка и ядерно-цитоплазматический обмен
Ядерная оболочка - система, разграничивающая два основных клеточных отсека: цитоплазму и ядро. Ядерные оболочки полностью проницаемы для ионов, для веществ малого молекулярного веса, таких, как сахара, аминокислоты, нуклеотиды. Считается, что белки молекулярного веса до 70 тыс. И размером не больше 4,5 нм могут свободно диффундировать через оболочку.
Известен и обратный процесс - перенос веществ из ядра в цитоплазму. Это в первую очередь касается транспорта РНК синтезируещегося исключительно в ядре.
Еще один путь транспорта веществ из ядра в цитоплазму связан с образованием выростов ядерной оболочки, которые могут отделяться от ядра в виде вакуолей, содержимое их затем изливается или выбрасывается в цитоплазму.
Таким образом, из многочисленных свойств и функциональных нагрузок ядерной оболочки следует подчеркнуть ее роль как барьера, отделяющего содержимое ядра от цитоплазмы, ограничивающего свободный доступ в ядро крупных агрегатов биополимеров, барьера, активно регулирующего транспорт макромолекул между ядром и цитоплазмой.
Одной из основных функций ядерной оболочки следует считать также ее участие в создании внутриядерного порядка, в фиксации хромосомного материала в трехмерном пространстве ядра.
Ядерный матрикс
Этот комплекс не представляет собой какую-то чистую фракцию, сюда входят компоненты и ядерной оболочки, и ядрышка, и кариоплазмы. С ядерным матриксом оказались связаны как гетерогенная РНК, так и часть ДНК. Эти наблюдения дали основание считать, что матрикс ядра играет важную роль не только в поддержании общей структуры интерфазного ядра, но и может участвовать в регуляции синтеза нуклеиновых кислот.
studfiles.net
Биология для студентов - 03. Ядерная оболочка, ее ультраструктура и роль
Структура, ограничивающая параметр клеточного ядра, — ядерная оболочка, разделяет два внутриклеточных компартмента друг от друга — цитоплазму от ядра. Значение такого разделения структур в пространстве очень важно: это приводит к обособлению процессов синтеза белка и процессов синтеза нуклеиновых кислот, что создает дополнительные, по сравнению с прокариотами, возможности для регуляции генной активности и ее реализации в виде синтеза специфических белков. Активная регуляция транспорта из цитоплазмы в ядро и из ядра в цитоплазму через специальные комплексы пор создает систему избирательного транспорта веществ, делая ядерную оболочку «генными воротами» со специальными «привратниками» (контрольными пунктами), регулирующими потоки ядерного импорта и экспорта. Кроме того, ядерная оболочка играет большую роль в организации трехмерной структуры интерфазного ядра, элементы ядерной оболочки являются частью ядерного белкового матрикса.
Ядерная оболочка состоит из двух мембран — внешней и внутренней, между которыми располагается перинуклеарное пространство.

1 — внешняя мембрана ядерной оболочки; 2 — перинуклеарное пространство; 3 — внутренняя мембрана ядерной оболочки; 4 — ядерные поры; 5 — ламины; 6 — хроматин; 7 — мембраны цитоплазмы
Внутренняя мембрана ядерной оболочки структурно связана с ламиной — фиброзным периферическим слоем ядерного белкового матрикса. В общем виде ядерная оболочка может быть представлена как двухслойный мешок, отделяющий содержимое ядра от цитоплазмы. Однако ядерная оболочка имеет характерную особенность, отличающую ее от других двухмембранных структур клетки (митохондрий и пластид). Это наличие особых ядерных пор, которые образуются за счет многочисленных зон слияния двух ядерных мембран и представляют собой как бы округлые, сквозные перфорации всей ядерной оболочки.
Внешняя мембрана ядерной оболочки, непосредственно контактирующая с цитоплазмой клетки, имеет ряд структурных особенностей, позволяющих отнести ее к собственно мембранной системе эндоплазматического ретикулума (ЭПР). Так, на внешней ядерной мембране обычно располагается большое количество рибосом, как и на мембранах эргастоплазмы.
У клеток, бедных эндоплазматическим ретикулумом, внешняя ядерная мембрана может представлять собой «минимальный» объем эндоплазматического ретикулума, который может участвовать в синтезе белкового и липидного компонентов мембран. Состав липидов и белков внешней ядерной мембраны очень схож с таковым ретикулума. Возможно, именно это определяет их общие биохимические функции, что особенно подчеркивается наличием рибосом на поверхности мембран, обращенной в гиалоплазму. Эти рибосомы синтезируют как мембранные, так и секретируемые белки, которые могут транспортироваться в перинуклеарное пространство, а оттуда в полости цистерн ЭПР. У большинства животных и растительных клеток внешняя мембрана ядерной оболочки не представляет собой идеально ровную поверхность, она может образовывать различной величины выпячивания или выросты в сторону цитоплазмы.
Внутренняя мембрана ядерной оболочки рибосом на своей поверхности не имеет, но связана с фиброзным слоем — ядерной ламиной, которая, в свою очередь, заякоривает хроматин на ядерной оболочке. Связь хроматина с внутренней мембраной оболочки является ее характерной особенностью, хотя существуют примеры, когда эти связи нарушаются при сохранении целостности ядерной оболочки. В то же время при делении клеток с так называемым закрытым типом митоза большая часть внутренней ядерной мембраны теряет связь с хроматином.
Фиброзный слой ламины все время перестраивается, особенно в связи с ростом поверхности ядра, во время клеточного цикла. Характерные для внутренней ядерной мембраны белки — ламины А, С и В — относятся к фибриллярным белкам V типа промежуточных филаментов, их фибриллярные мономеры могут образовывать димеры и тетрамеры, а последние образуют фибриллы толщиной около 10 нм. Со стороны кариоплазмы под внутренней ядерной мембраной такие фибриллы образуют ортогональные структуры, чередующиеся с рыхло расположенной сетью этих же фибрилл.
Наиболее характерной и бросающейся в глаза структурой в составе ядерной оболочки является ядерная пора. Поры в оболочке образуются за счет слияния двух ядерных мембран в виде округлых сквозных отверстий, или перфораций, с диаметром около 100 нм. Совокупность мембранных перфораций и этих структур называют комплексом пор ядра. Тем самым подчеркивается, что ядерная пора не просто сквозная дыра в ядерной оболочке, через которую непосредственно вещества ядра и цитоплазмы могут сообщаться. Компоненты комплекса пор имеют белковую природу.
После открытия ядерной оболочки и описания ее строения пришли к заключению, что ядерная оболочка может служить регулятором в ядерно-цитоплазматическом обмене, главная роль в этих процессах отводилась ядерным порам. Обмен продуктами между ядром и цитоплазмой в самом деле очень велик: все ядерные белки поступают в ядро из цитоплазмы и все формы РНК выводятся из ядер. И в этом процессе комплекс поры выступает как супрамолекулярный комплекс, выполняющий роль не только транслокатора — механизма переноса, но и роль сортировщика, узнающего и отбирающего специальным образом переносимые молекулы.
В процессе ядерно-цитоплазматического транспорта ядерные поры функционируют как некоторое молекулярное сито, пропуская частицы определенного размера пассивно, по градиенту концентрации. Так, ионы, сахара, нуклеотиды, АТФ и гормоны свободно поступают в ядра. В то же время ядерные поры осуществляют избирательный транспорт.
vseobiology.ru
Глава 10. Ядерная оболочка
Структура, ограничивающая параметр клеточного ядра, ядерная оболочка, характерна для эукариотических клеток. Она разделяет два внутриклеточных компартмента друг от друга, цитоплазму от ядра. Значение такого разделения структур в пространстве очень важно: это приводит к обособлению процессов синтеза белка и процессов синтеза нуклеиновых кислот, что создает дополнительные, по сравнению с прокариотами, возможности для регуляции генной активности и ее реализации в виде синтеза специфических белков. Активная регуляция транспорта из цитоплазмы в ядро и из ядра в цитоплазму, через специальные комплексы пор создает систему избирательного транспорта веществ, делая ядерную оболочку “генными воротами” со специальными “превратниками” (контрольными пунктами), регулирующими потоки ядерного импорта и экспорта. Кроме того, как уже описывалось, ядерная оболочка играет большую роль в организации трехмерной структуры интерфазного ядра, элементы ядерной оболочки являются частью ядерного белкового матрикса.
Ядерная оболочка состоит из двух мембран, внешней и внутренней, между которыми располагается перинуклеарное пространство (рис. 106). Внутренняя мембрана ядерной оболочки структурно связана с ламиной - фиброзным периферическим слоем ядерного белкового матрикса. В общем виде ядерная оболочка может быть представлена как двухслойный мешок, отделяющий содержимое ядра от цитоплазмы. Однако ядерная оболочка имеет характерную особенность, отличающую ее от других двухмембранных структур клетки (митохондрии и пластиды). Это наличие особых ядерных пор, которые образуются за счет многочисленных зон слияния двух ядерных мембран и представляют собой как бы округлые, сквозные перфорации всей ядерной оболочки.
Компоненты ядерной оболочки
Внешняя мембрана ядерной оболочки, непосредственно контактирующая с цитоплазмой клетки, имеет ряд структурных особенностей, позволяющих отнести ее к собственно мембранной системе эндоплазматического ретикулума (ЭПР). Так, на внешней ядерной мембране обычно располагается большое количество рибосом, как и на мембранах эргастоплазмы. Существуют многочисленные наблюдения о непосредственном переходе внешней ядерной мембраны в систему каналов эндоплазматического ретикулума, что особенно подчеркивает структурную идентичность этих мембран (рис. 106).
Так у клеток, бедных эндоплазматическим ретикулумом, внешняя ядерная мембрана может представлять собой “минимальный” объем эндоплазматического ретикулума, который может участвовать в синтезе белкового и липидного компонентов мембран. Описаны случаи, когда от внешней ядерной мембраны отщепляются мембранные вакуоли, направляющиеся в проксимальный отдел аппарата Гольджи. Состав липидов и белков внешней ядерной мембраны очень схож с таковым ретикулума, что, возможно, и определяет их общие биохимические функции, что особенно подчеркивается наличием рибосом на поверхности мембран, обращенной в гиалоплазму. Эти рибосомы синтезируют, как мембранные, так и секретируемые белки, которые могут транспортироваться в перинуклеарное пространство, а оттуда в полости цистерн ЭПР. Так, например, при стимуляции образования -глобулинов в плазмоцитах первые продукты клеточной активности локализуются в перинуклеарном пространстве, а потом начинают появляться в полостях ЭПР. У большинства животных и растительных клеток внешняя мембрана ядерной оболочки не представляет собой идеально ровную поверхность - она может образовывать различной величины выпячивания или выросты в сторону цитоплазмы.
Внутренняя мембрана ядерной оболочки рибосом на своей поверхности не имеет, но связана с фиброзным слоем, ядерной ламиной (Lamina nucleum limitans), которая, в свою очередь, заякоревает хроматин на ядерной оболочке. Связь хроматина с внутренней мембраной оболочки является ее характерной особенностью, хотя существуют примеры, когда эти связи нарушаются при сохранении целостности ядерной оболочки. Так, например, в ооцитах амфибий на стадии диплотены все хромосомы собираются в центре ядра и полностью теряют связь с ядерной оболочкой. С другой стороны, при делении клеток с т.н. закрытым типом митоза большая часть внутренней ядерной мембраны теряет связь с хроматином.
О специфичности белков ламины уже говорилось в разделе “Ядерный белковый матрикс”, здесь же необходимо еще раз подчеркнуть, что эти фибриллярные белки не образуют неизменную структуру. Фиброзный слой ламины все время перестраивается, особенно в связи с ростом поверхности ядра, во время клеточного цикла. Характерные для внутренней ядерной мембраны белки ламины A, C и B относятся к фибриллярным белкам V типа промежуточных филаментов (см. ниже), их фибриллярные мономеры могут образовывать димеры, тетрамеры, а последние образуют фибриллы толщиной около 10 нм. Со стороны кариоплазмы под внутренней ядерной мембраной такие фибриллы образуют ортогональные структуры, чередующиеся с рыхло расположенной сетью этих же фибрилл.
Белки ламины с мембраной связаны двояким образом. Так ламин B после синтеза модифицируется добавлением гидрофобной изопентильной группы вблизи C-конца. Эта липофильная группа встраивается в слой мембраны и как бы заякоревает ламину на мембране. Кроме того целый ряд интегральных белков внутренней ядерной мембраны (LBR, LAR, эмерин и др.) также закрепляют ламины посредством дополнительных белков, входящих в состав этого фиброзного слоя. Эти же белки участвуют в связывании ядерной мембраны с хроматином.
Наиболее характерной и бросающейся в глаза структурой в составе ядерной оболочки является ядерная пора. Поры в оболочке образуются за счет двух ядерных мембран в виде округлых сквозных отверстий или перфораций с диаметром около 100 нм. При альдегидной фиксации или при использовании метода замораживания и скалывания в электронном микроскопе видно, что округлое сквозное отверстие в ядерной оболочке заполнено сложно организованными глобулярными и фибриллярными структурами (рис. 107). Совокупность мембранных перфораций и этих структур называют комплексом пор ядра. Тем самым подчеркивается, что ядерная пора не просто сквозная дыра в ядерной оболочке, через которую непосредственно вещества ядра и цитоплазмы могут сообщаться. Компоненты комплекса пор имеют белковую природу.
Ядерный поровый комплекс (ЯПК или NPC - nuclear pore complex) представляет собой супрамолекулярную структуру с м.в. более 125 х 106 Да, состоящую из более 1000 белков, масса которых в 30 раз больше чем рибосома. Белки ЯПК носят название нуклеопоринов 50-100 видов. Эти белки собраны примерно в 12 субкомплексов.
В последнее время удалось получить отчетливые изображения ЯПК в электронном микроскопе, что дает возможность понять их структурную организацию. Внешний диаметр порового комплекса составляет около 100 нм, а высота - 75 нм. В целом он представляет собой цилиндрическую фигуру с признаками октогональной симметрии. Несмотря на очень впечатляющие изображения выделенных ЯПК, разные авторы дают разные схемы строения этого сложного комплекса, обладающего симметрией восьмого порядка.
Если посмотреть на ЯПК в плане на ультратонком срезе, то бросается в глаза, что его периферия представлена восьмью глобулами (рис. 108, 109). На выделенных же ЯПК в первую очередь видны кольчатые структуры. От периферических компонентов ЯПК в сторону цитоплазмы простираются фибриллярные выросты. Со стороны ядра тоже фибриллярные выросты образуют корзинкоподобную структуру, связанную терминальным кольцом. В большинстве моделей центр цилиндрической фигуры ЯПК содержит “пробку” (центральную гранулу, или транспортер). По одной из моделей (см. рис. 93) цитоплазматические филаменты отходят от цитоплазматического кольца, состоящего из 8 субъединиц. Между ним и внешней ядерной мембраной располагается тонкое кольцо, а затем звездчатое кольцо. Цитоплазматическое кольцо связано внутренними филаментами с транспортером, который находится в центре и заполняет пространство между внешней и внутренней ядерной мембраной. Сходная структура находится на внутренней мембране: нуклеоплазматическое кольцо поддерживает филаменты “корзины”. Другие варианты моделей показаны на (рис. 110).
Весь ЯПК закрепляется интегральными белками, гликопротеидами gp 210 и РОМ 121 в стенке мембранной перфорации.
По своей сложности организации и, главное, по функциональной значимости комплекс ядерной поры можно было бы отнести к органеллам клетки, т.к. их роль заключается в контроле за ядерно-цитоплазменными связями.
Размер ядерных пор и их структура стандартны не только для данной клетки, но и для всех клеток данного организма, более того для всех эукариот.
Число ядерных пор (см. табл. 13) зависит от метаболической активности клеток: чем выше синтетические процессы в клетках, тем больше пор на единицу поверхности клеточного ядра. Так, у эритробластов (клетки-предшественники ядерных эритроцитов) низших позвоночных животных во время интенсивного синтеза и накопления гемоглобина обнаруживается в ядре около 30 ядерных пор на 1 мкм2. После того как эти процессы заканчиваются, в ядрах зрелых клеток - эритроцитов прекращаются синтезы ДНК и РНК, и количество пор падает до 5 на мкм2. В ядерных оболочках полностью зрелых сперматозоидов поры не обнаруживаются, так же как у микронуклеусов некоторых инфузорий. Количество пор может изменяться в течение клеточного цикла. Первое возрастание числа пор наблюдается при реконструкции и росте ядер после митоза, второй этап увеличения числа пор происходит во время синтеза ДНК.
Таблица 13. Количество ядерных пор в различных объектах
| Объект | Число ядерных пор на мкм2. | Число пор на одно ядро |
| Ксенопус, почки | 10,05 | 3400 |
| Ксенопус, ооцит | 51,0 | 37,6 х 106 |
| Мышь, культура ткани | 10,83 | 5050 |
| Человек, культура ткани | 11,24 | 3930 |
| Крыса, гепатоцит | 16,1 | 3800 |
| Мышь, лимфоцит | 3,3 | 400 |
| Человек, лимфоцит | 4,47 | 700 |
По поверхности ядра поры располагаются более или менее равномерно, но их число резко падает в местах ассоциации с ядерной оболочкой участков гетерохроматина, ядрышкового организатора, теломерных участков.
Поровые комплексы могут встречаться и в других мембранных компонентах клетки, но гораздо реже, чем в ядерной оболочке. Иногда поровые комплексы видны в составе мембран гранулярного эндоплазматического ретикулума. Они обнаруживаются в составе окончатых мембран цитоплазмы, которые представляют собой тесно расположенные пачки замкнутых плоских мембранных мешков, сплошь пронизанных поровыми комплексами, имеющими такую же структуру, как и поры в ядерной оболочке.
Интересные данные были получены при морфометрическом изучении поровых комплексов в ядрах и окончатых мембранах бластодермы эмбрионов дрозофилы. Оказалось, что при переходе от синцитиальной к целлюлярной стадии, количество пор в оболочках ядер остается неизменным, а количество пор в окончатых пластинках вырастает примерно в 10 раз. В дальнейшем окончатые мембраны полностью исчезают. На основании этого было сделано предположение, что на ранней стадии развития в бластодерме дрозофилы происходит “суперпродукция” поровых комплексов (или их компонентов), избыток которых “встраивается” в окончатые мембраны. Т.е. макромолекулярный ансамбль, составляющий комплекс ядерных пор, способен к автономной самосборке и к последующему встраиванию в различные мембранные системы.
Роль ядерной оболочки в ядерно-цитоплазматическом обмене
Со времени открытия ядерной оболочки и описания ее строения делалось заключение о том, что ядерная оболочка может служить регулятором в ядерно-цитоплазматическом обмене и главная роль в этих процессах отводилась ядерным порам. Обмен же продуктами между ядром и цитоплазмой в самом деле очень велик: все ядерные белки поступают в ядро из цитоплазмы и все формы РНК выводятся из ядер. И в этом процессе комплекс поры выступает как супрамолекулярный комплекс, выполняющий роль не только транслокатора, механизма переноса, но и роль сортировщика, узнающего и отбирающего специальным образом переносимые молекулы.
В процессе ядерно-цитоплазматического транспорта ядерные поры функционируют как некоторое молекулярное сито, пропуская частицы определенного размера пассивно, по градиенту концентрации. Так, ионы, сахара, нуклеотиды, АТФ, гормоны - свободно поступают в ядра. С другой стороны ядерные поры осуществляют избирательный транспорт.
Через ядерную оболочку беспрепятственно в обе стороны происходит пассивный транспорт высоко молекулярных соединений, имеющих массу не более 5 х 103 дальтон. Для определения размеров частиц, могущих пройти сквозь пору, используются гранулы декстрана или коллоидного золота, которые путем микроинъекции вводятся в цитоплазму живой клетки. Было обнаружено, что максимальный размер частиц, способных транспортироваться в ядро составляет 8,5-10 нм. При этом сначала частицы собираются в зоне поровых комплексов, а затем оказываются в ядре. Неядерные белки с массой большей, чем 20 000-40 000 дальтон проникают в ядро медленнее, если вообще проникают. Так инъецированные белки с массой 17 кД могут проникнуть в ядро довольно быстро, за 2-3 минуты, белки 40 кД - за 30 минут, белки 60 кД - вообще не проникают в ядра. Считается, что белки с гидродинамическим радиусом больше 3,5 нм (что соответствует глобулярному белку с массой 65 кД), не могут просто механически проходить через ядерную пору. В этих случаях ядерная пора выступает в качестве реального молекулярного сита.
Но дело осложняется тем, что многие белки поступают как в ядро, так и выходят из него против градиента концентраций. Так, например, концентрация гистонов в ядре значительно выше, чем в цитоплазме. Но, несмотря на это, во время синтеза ДНК происходит транспорт огромного количества (106 молекул каждые три минуты, или по 100-500 молекул через одну пору за 1 минуту) гистонов из цитоплазмы в ядро. С другой стороны через ядерные поры реально могут проходить некоторые белки и даже макромолекулярные комплексы с массой значительно большей, чем 60 кД.
Через ядерные поры из цитоплазмы в ядро транспортируются крупные молекулы белков, например, белок нуклеоплазмин, пентамер с молекулярной массой 125 кД. Из ядра через поры выходят в цитоплазму субъединицы рибосом и другие рибонуклеопротеиды, меньшие из которых могут иметь массу 250 кД. Эти данные показывают, что комплексы ядерных пор не представляют собой просто механические сита, которые ограничивают транспорт молекул в зависимости от их размеров.
Работы последнего времени показывают, что многие ядерные белки проходят через ядерные поры с помощью специальных механизмов, включающих узнавание и связывание крупных ядерных белков, а затем только их транслокацию, перенос через поры. Было найдено, что белки, транспортируемые в ядро, имеют определенные последовательности аминокислот - последовательности ядерной локализации (NLS), которые узнаются рецепторами ядерных пор. Такие NLS характерны для кариофильных белков, т.е. для белков ядерной локализации, которые синтезируются на рибосомах в цитоплазме, а затем транспортируются в ядро.
Импорт кариофильных белков
Впервые аминокислотные последовательности ядерной локализации были обнаружены на С-конце субъединиц молекулы нуклеоплазмина (ядерный белок, принимающий участие в структуризации хроматина). Эти эксперименты были проведены на бесклеточной системе, когда выделенные ядра помещались в цитоплазматический экстракт ооцитов ксенопуса, куда добавляли нативные или измененные молекулы нуклеоплазмина. Это крупный белок (125 кД), состоящий из пяти субъединиц, каждая из которых обладает глобулярной и фибриллярной, С-концевой, частями. Если удалит путем протеолиза примерно 50 аминокислот с С-конца, то ни пентамер, ни мономеры в ядро не попадают, в то время как отщепленные фибриллярные участки через поры проходят свободно, так как содержат NLS-участок.
Более того, при смешивании неядерных белков с этими NLS-фрагментами, такие комплексы способны транспортироваться в ядро. Даже крупные частицы декстрана (20 нм), неспособные проникать в ядро, при связывании с ними NLS-последовательностей нуклеоплазмина транспортировались из цитоплазматического экстракта в ядро.
Подробно строение NLS изучено у белка Т антигена вируса SV40. Кариофильный сигнал состоял из последовательности: Pro-Lys-128Lys-Lys-Arg-Lys-Val. Одна лишь аминокислотная замена (128Lys на Thr или Asp) полностью лишают этого фрагмента кариофильных свойств. Оказалось. что можно создавать химерные белки с этим аминокислотным доменом, что позволяет необычные для ядер белки (альбумин плазмы, иммуноглобулин G, и даже ферритин с мол. массой 465 кД) транспортировать через ядерные поры.
Было показано, что белок с NLS проходит в ядро через несколько этапов (рис. 111). Импорт начинается с того, что NLS-белок связывается с гетеродимером рецептора NLS, с белками импортинами и , локализованными в цитоплазме. Возникший белковый комплекс (импортируемый белок с NLS, связанный с импортинами и ) подходит к внешней ядерной мембране и закрепляется на цитоплазматических филаментах порового комплекса. Затем этот комплекс входит в ядерную пору и проходит через “транспортер”. Считается, что транспортер состоит из множества извитых белковых филаментов, обогащенных аланином и глицином (FG-филаменты), представляющих собой барьер для транспорта некариофильных белков. Комплекс же, имеющий NLS как бы разрыхляет эту сеть и проходит через канал транспортера. После перехода комплекса в нуклеоплазму импортин связывается с белком RAN, представляющего собой малую GTP-азу, что приводит к распаду комплекса. Импортируемый белок освобождается и остается в ядре, импортин возвращается в цитоплазму, так же как и импортин , но в связи с RAN-GDP, где последние также диссоциируют. Тем самым только белок с NLS остается в составе ядра (рис. 111).
Экспорт из ядра в цитоплазму
Из ядра в цитоплазму также существует поток как белков, так и ядерных транскриптов в виде рибонуклеопротеидов. В принципе этот экспорт своей организации сходен с процессом импорта кариофильных белков. Так было обнаружено, что гликопротеидные молекулы, связывающие лиганды, локализуются в место поровых комплексов и со стороны ядра. Одна и та же пора может принимать участие как в импорте, так и в экспорте макромолекул. В пользу этого говорит то, что частички коллоидного золота, связанного с нуклеоплазмином, сорбируются на ядерной поре со стороны цитоплазмы, одновременно с сорбцией частичек, связанных с РНК, инъецированных в ядре ооцитов. Подобные эксперименты показали, что многие РНК (тРНК, 5S РНК, поли-У и поли-А), связанные с коллоидным золотом, аккумулируются в зоне ядерных пор, а затем переносятся в цитоплазму. Более того, РНК способствует переносу через ядерную пору крупных частиц золота размером до 20 нм. Обратного переноса не происходит: аналогичные частички, инъецированные в цитоплазму ооцита, в ядро не проникают.
Что касается естественных видов РНП, то комплексы ядерных пор также должны узнавать специфический сигнал на экспорт. Белковые компоненты РНП несут аминокислотные последовательности, сигналы ядерного экспорта (NES), которые дают возможность различным РНП проходить через ядерную оболочку в цитоплазму.
В этом случае также образуется сложный комплекс, состоящий из переносимого белка с NES-последовательностью (связанного с РНК или свободного), ассоциированного с белком экспортином 1, который в свою очередь связан с RAN-GTP. Этот комплекс проходит через центральный канал, создаваемый транспортером, в цитоплазму, где и диссоциирует. При этом освобождается белок с NES-участком (или РНП), который остается в цитоплазме. Экспортин 1 и RAN после гидролиза GTP снова возвращаются в ядро (рис. 112).
В процессе экспорта РНП ядерная пора контролирует не только белковый компонент. Ядерные поры узнают и не экспортируют короткие (100 нуклеотидов) тРНК, если в их структуре есть хоть одна замена. Транспорт незрелых форм иРНК, имеющих интронные участки, не происходит. Вообще в цитоплазме не обнаруживаются незрелые РНК. Вероятно, для экспорта некоторых РНК необходима их связь с особыми белками. Так 5S РНК переносится в цитоплазму вместе с транскрипционным фактором TFIIIA, или с белком L5. Мутантные формы 5S рРНК, которые не связываются с TFIIIA, остаются в ядре.
Мало изучен вопрос о транспорте в цитоплазму крупных РНП-комплексов, таких как субъединицы рибосом, информосомы и малые ядерные РНП. Возможно все они под действием каких-то факторов разворачиваются, меняют свою конформацию и проходят через поровый комплекс. В пользу этого говорят наблюдения гантелевидных РНК-содержащих частиц, в просвете пор ядер гигантских слюнных желез насекомых. Считается, что эта картина отражает момент выхода из ядер РНП-частиц 60 нм в диаметре, относимых к информоферам. Интересно, что состав белков в цитоплазматических информационных РНП иной, это может говорить о том, что в зоне поровых комплексов происходит “переодевание” информационных РНК, связь их с иными белками.
Динамика ядерной оболочки в митозе
Большей частью, но не у всех видов (исключение составляют амебы, эвгленовые, инфузории, динофлагелляты, многие водоросли, некоторые грибы), ядерная оболочка разрушается при митозе и снова возникает после деления клеток. Это так называемый открытый тип митоза (рис. 113). При этом в профазе по мере конденсации хромосом ядерная оболочка теряет с ними связь, а затем в ней появляются разрывы. Она приобретает вид плоских мембранных вакуолей, цистерн. В это время ядерные поры еще видны. Позднее они исчезают. Во время митоза 120 мДа комплекс ядерной поры разбирается на субкомплексы примерно по 1 мДа. Разборка пор начинается с фосфорилирования ряда нуклеопоринов митотической cdc2/циклин B киназой.
Ядерная оболочка превращается в скопление мелких мембранных пузырьков, окружающих зону бывшего интерфазного ядра. Такие пузырьки морфологически нельзя отличить от других мелких вакуолей в цитоплазме, они вероятно сливаются с вакуолями эндоплазматического ретикулума. В метафазе мембранные элементы цитоплазмы оттесняются к периферическим зонам клеток микротрубочками веретена деления.
В конце анафазы, когда прекращается движение хромосом к противоположным полюсам клетки, мембранные пузырьки цитоплазмы, и в первую очередь мембраны гранулярного эндоплазматического ретикулума (см. ниже), начинают контактировать с поверхностью хромосом. Эти контакты происходят сначала в небольшом числе точек, но затем начинается перестройка и рост этих первичных зачатков ядерной оболочки. Они из мелких пузырьков превращаются в плоские вакуоли, которые растут в ширину и обволакивают поверхность деконденсирующихся хромосом. Участки таких растущих плоских мембранных мешков сливаются, замыкая и отгораживая содержимое нового интерфазного ядра. Интересно, что ядерные поры появляются на самых ранних этапах реконструкции ядерной оболочки, когда двойные мембранные цистерны еще не сомкнулись и фактически ничего не разделяют.
При реконструкции ядерной оболочки происходит сборка ядерных пор. Она начинается с образования ямки при слиянии внешней и внутренней ядерной мембраны, которая затем превращается в отверстие. В этом процессе принимают участие интегральные белки gp 210 и POM 121, которые впоследствии будут закреплять ЯПК на мембранах.
За этим следует появление внутренних структур ЯПК: комплекс кольца, спиц, добавление звездчатого кольца и других структур, и, наконец, филаментов.
У некоторых низших организмов в случае закрытого митоза ядерная оболочка не исчезает, она в зоне ядерной перетяжки замыкается, что приводит к образованию двух новых ядер. Здесь участие ядерной оболочки в делении клетки заключается в том, что на ней закреплены хромосомы, и она, по-видимому, принимает участие в индукции образования микротрубочек, необходимых при делении клеток.
По-видимому, для реконструкции ядерной оболочки необходимым условием является деконденсация хромосом. Было показано, что если вызвать преждевременную деконденсацию метафазных хромосом, то они очень быстро контактируют с мембранными пузырьками и одеваются каждая своей отдельно ядерной оболочкой, вследствие чего в клетке возникает множество так называемых микроядер, каждое их которых возникло из одной хромосомы.
С другой стороны, можно экспериментально вызвать разборку ядерной оболочки у интерфазного ядра. Это происходит, если слить в культуре ткани две клетки на разных стадиях клеточного цикла и получить т.н. гетерокарион, где одно из ядер будет находиться в интерфазе, а другое быть в виде митотических хромосом в метафазе. В этом случае в интерфазном ядре начинает конденсироваться хроматин, образуются преждевременно конденсированные хромосомы, а ядерная оболочка исчезнет так же как во время нормального митоза (рис. 114). Эти данные говорят о том, что в цитоплазме митотической клетки существуют какие-то факторы, вызывающие как конденсацию хромосом, так и параллельный этому процесс распада ядерной оболочки.
Сходная динамика совпадения процессов перестройки хромосом и ядерной оболочки наблюдается и в другой системе, в цитоплазме ооцитов или в бесклеточных цитоплазматических экстрактах ооцитов. Так если в цитоплазму ооцита амфибий на стадии метафазы инъецировать выделенные интерфазные ядра, то их ядерная оболочка разбирается, а хроматин конденсируется в виде митотических хромосом. Если же в ооцит на стадии интерфазы ввести митотические хромосомы, то они начинают деконденсироваться, появляются множественные мелкие вакуоли, которые сливаясь друг с другом, образуют ядерные оболочки. Интересно, что в цитоплазму интерфазного ооцита можно ввести даже чужеродную чистую ДНК, которая, связываясь с гистонами в цитоплазме, образует хроматиновые глыбки, которые в свою очередь одеваются ядерными оболочками и превращаются в микроядра.
Эти экспериментальные приемы вместе с методом иммунофлуоресценции позволили проследить судьбу многих белков ядерной оболочки во время митоза. Подробно изучена судьба ламинов. Было найдено, что фиброзный слой ламинов деполимеризуется параллельно распаду ядерных мембран и конденсации хроматина. Этому предшествует обильное (в 7 раз выше, чем в интерфазе) фосфорилирование ламинов. Ламины A и C при этом деполимеризуются до димеров и тетрамеров и, переходя в растворимое состояние, равномерно распределяются в цитоплазме вне связи с другими структурами. Ламин B тоже деполимеризуется до олигомеров, но остается связанным с мембранными пузырьками, возникшими из ядерной оболочки.
При сборке ядерной оболочки в телофазе белки ламины иммунохимически начинают выявляться в центромерных и теломерных участках хромосом, там же обнаруживаются первые признаки образования новой ядерной оболочки. Там же накапливаются антитела к белкам порового комплекса. В бесклеточной системе цитоплазматического экстракта ооцитов было показано, что ассоциация растворимых в митозе ламинов A и C происходит независимо от ламина B. Оказалось, что если систему реконструкции ядерной оболочки лишить ламина B, то ламины A и C связываются с поверхностью хромосом, но сборки ядерной оболочки не происходит. В экстракте, лишенном ламинов A и C, ламин B связывается с хромосомами, но нормальная ядерная оболочка так же не формируется.
studfiles.net
Глава 10. Ядерная оболочка
Структура, ограничивающая параметр клеточного ядра, ядерная оболочка, характерна для эукариотических клеток. Она разделяет два внутриклеточных компартмента друг от друга, цитоплазму от ядра. Значение такого разделения структур в пространстве очень важно: это приводит к обособлению процессов синтеза белка и процессов синтеза нуклеиновых кислот, что создает дополнительные, по сравнению с прокариотами, возможности для регуляции генной активности и ее реализации в виде синтеза специфических белков. Активная регуляция транспорта из цитоплазмы в ядро и из ядра в цитоплазму, через специальные комплексы пор создает систему избирательного транспорта веществ, делая ядерную оболочку “генными воротами” со специальными “превратниками” (контрольными пунктами), регулирующими потоки ядерного импорта и экспорта. Кроме того, как уже описывалось, ядерная оболочка играет большую роль в организации трехмерной структуры интерфазного ядра, элементы ядерной оболочки являются частью ядерного белкового матрикса.
Ядерная оболочка состоит из двух мембран, внешней и внутренней, между которыми располагается перинуклеарное пространство (рис. 106). Внутренняя мембрана ядерной оболочки структурно связана с ламиной - фиброзным периферическим слоем ядерного белкового матрикса. В общем виде ядерная оболочка может быть представлена как двухслойный мешок, отделяющий содержимое ядра от цитоплазмы. Однако ядерная оболочка имеет характерную особенность, отличающую ее от других двухмембранных структур клетки (митохондрии и пластиды). Это наличие особых ядерных пор, которые образуются за счет многочисленных зон слияния двух ядерных мембран и представляют собой как бы округлые, сквозные перфорации всей ядерной оболочки.
Компоненты ядерной оболочки
Внешняя мембрана ядерной оболочки, непосредственно контактирующая с цитоплазмой клетки, имеет ряд структурных особенностей, позволяющих отнести ее к собственно мембранной системе эндоплазматического ретикулума (ЭПР). Так, на внешней ядерной мембране обычно располагается большое количество рибосом, как и на мембранах эргастоплазмы. Существуют многочисленные наблюдения о непосредственном переходе внешней ядерной мембраны в систему каналов эндоплазматического ретикулума, что особенно подчеркивает структурную идентичность этих мембран (рис. 106).
Так у клеток, бедных эндоплазматическим ретикулумом, внешняя ядерная мембрана может представлять собой “минимальный” объем эндоплазматического ретикулума, который может участвовать в синтезе белкового и липидного компонентов мембран. Описаны случаи, когда от внешней ядерной мембраны отщепляются мембранные вакуоли, направляющиеся в проксимальный отдел аппарата Гольджи. Состав липидов и белков внешней ядерной мембраны очень схож с таковым ретикулума, что, возможно, и определяет их общие биохимические функции, что особенно подчеркивается наличием рибосом на поверхности мембран, обращенной в гиалоплазму. Эти рибосомы синтезируют, как мембранные, так и секретируемые белки, которые могут транспортироваться в перинуклеарное пространство, а оттуда в полости цистерн ЭПР. Так, например, при стимуляции образования -глобулинов в плазмоцитах первые продукты клеточной активности локализуются в перинуклеарном пространстве, а потом начинают появляться в полостях ЭПР. У большинства животных и растительных клеток внешняя мембрана ядерной оболочки не представляет собой идеально ровную поверхность - она может образовывать различной величины выпячивания или выросты в сторону цитоплазмы.
Внутренняя мембрана ядерной оболочки рибосом на своей поверхности не имеет, но связана с фиброзным слоем, ядерной ламиной (Lamina nucleum limitans), которая, в свою очередь, заякоревает хроматин на ядерной оболочке. Связь хроматина с внутренней мембраной оболочки является ее характерной особенностью, хотя существуют примеры, когда эти связи нарушаются при сохранении целостности ядерной оболочки. Так, например, в ооцитах амфибий на стадии диплотены все хромосомы собираются в центре ядра и полностью теряют связь с ядерной оболочкой. С другой стороны, при делении клеток с т.н. закрытым типом митоза большая часть внутренней ядерной мембраны теряет связь с хроматином.
О специфичности белков ламины уже говорилось в разделе “Ядерный белковый матрикс”, здесь же необходимо еще раз подчеркнуть, что эти фибриллярные белки не образуют неизменную структуру. Фиброзный слой ламины все время перестраивается, особенно в связи с ростом поверхности ядра, во время клеточного цикла. Характерные для внутренней ядерной мембраны белки ламины A, C и B относятся к фибриллярным белкам V типа промежуточных филаментов (см. ниже), их фибриллярные мономеры могут образовывать димеры, тетрамеры, а последние образуют фибриллы толщиной около 10 нм. Со стороны кариоплазмы под внутренней ядерной мембраной такие фибриллы образуют ортогональные структуры, чередующиеся с рыхло расположенной сетью этих же фибрилл.
Белки ламины с мембраной связаны двояким образом. Так ламин B после синтеза модифицируется добавлением гидрофобной изопентильной группы вблизи C-конца. Эта липофильная группа встраивается в слой мембраны и как бы заякоревает ламину на мембране. Кроме того целый ряд интегральных белков внутренней ядерной мембраны (LBR, LAR, эмерин и др.) также закрепляют ламины посредством дополнительных белков, входящих в состав этого фиброзного слоя. Эти же белки участвуют в связывании ядерной мембраны с хроматином.
Наиболее характерной и бросающейся в глаза структурой в составе ядерной оболочки является ядерная пора. Поры в оболочке образуются за счет двух ядерных мембран в виде округлых сквозных отверстий или перфораций с диаметром около 100 нм. При альдегидной фиксации или при использовании метода замораживания и скалывания в электронном микроскопе видно, что округлое сквозное отверстие в ядерной оболочке заполнено сложно организованными глобулярными и фибриллярными структурами (рис. 107). Совокупность мембранных перфораций и этих структур называют комплексом пор ядра. Тем самым подчеркивается, что ядерная пора не просто сквозная дыра в ядерной оболочке, через которую непосредственно вещества ядра и цитоплазмы могут сообщаться. Компоненты комплекса пор имеют белковую природу.
Ядерный поровый комплекс (ЯПК или NPC - nuclear pore complex) представляет собой супрамолекулярную структуру с м.в. более 125 х 106 Да, состоящую из более 1000 белков, масса которых в 30 раз больше чем рибосома. Белки ЯПК носят название нуклеопоринов 50-100 видов. Эти белки собраны примерно в 12 субкомплексов.
В последнее время удалось получить отчетливые изображения ЯПК в электронном микроскопе, что дает возможность понять их структурную организацию. Внешний диаметр порового комплекса составляет около 100 нм, а высота - 75 нм. В целом он представляет собой цилиндрическую фигуру с признаками октогональной симметрии. Несмотря на очень впечатляющие изображения выделенных ЯПК, разные авторы дают разные схемы строения этого сложного комплекса, обладающего симметрией восьмого порядка.
Если посмотреть на ЯПК в плане на ультратонком срезе, то бросается в глаза, что его периферия представлена восьмью глобулами (рис. 108, 109). На выделенных же ЯПК в первую очередь видны кольчатые структуры. От периферических компонентов ЯПК в сторону цитоплазмы простираются фибриллярные выросты. Со стороны ядра тоже фибриллярные выросты образуют корзинкоподобную структуру, связанную терминальным кольцом. В большинстве моделей центр цилиндрической фигуры ЯПК содержит “пробку” (центральную гранулу, или транспортер). По одной из моделей (см. рис. 93) цитоплазматические филаменты отходят от цитоплазматического кольца, состоящего из 8 субъединиц. Между ним и внешней ядерной мембраной располагается тонкое кольцо, а затем звездчатое кольцо. Цитоплазматическое кольцо связано внутренними филаментами с транспортером, который находится в центре и заполняет пространство между внешней и внутренней ядерной мембраной. Сходная структура находится на внутренней мембране: нуклеоплазматическое кольцо поддерживает филаменты “корзины”. Другие варианты моделей показаны на (рис. 110).
Весь ЯПК закрепляется интегральными белками, гликопротеидами gp 210 и РОМ 121 в стенке мембранной перфорации.
По своей сложности организации и, главное, по функциональной значимости комплекс ядерной поры можно было бы отнести к органеллам клетки, т.к. их роль заключается в контроле за ядерно-цитоплазменными связями.
Размер ядерных пор и их структура стандартны не только для данной клетки, но и для всех клеток данного организма, более того для всех эукариот.
Число ядерных пор (см. табл. 13) зависит от метаболической активности клеток: чем выше синтетические процессы в клетках, тем больше пор на единицу поверхности клеточного ядра. Так, у эритробластов (клетки-предшественники ядерных эритроцитов) низших позвоночных животных во время интенсивного синтеза и накопления гемоглобина обнаруживается в ядре около 30 ядерных пор на 1 мкм2. После того как эти процессы заканчиваются, в ядрах зрелых клеток - эритроцитов прекращаются синтезы ДНК и РНК, и количество пор падает до 5 на мкм2. В ядерных оболочках полностью зрелых сперматозоидов поры не обнаруживаются, так же как у микронуклеусов некоторых инфузорий. Количество пор может изменяться в течение клеточного цикла. Первое возрастание числа пор наблюдается при реконструкции и росте ядер после митоза, второй этап увеличения числа пор происходит во время синтеза ДНК.
Таблица 13. Количество ядерных пор в различных объектах
| Объект | Число ядерных пор на мкм2. | Число пор на одно ядро |
| Ксенопус, почки | 10,05 | 3400 |
| Ксенопус, ооцит | 51,0 | 37,6 х 106 |
| Мышь, культура ткани | 10,83 | 5050 |
| Человек, культура ткани | 11,24 | 3930 |
| Крыса, гепатоцит | 16,1 | 3800 |
| Мышь, лимфоцит | 3,3 | 400 |
| Человек, лимфоцит | 4,47 | 700 |
По поверхности ядра поры располагаются более или менее равномерно, но их число резко падает в местах ассоциации с ядерной оболочкой участков гетерохроматина, ядрышкового организатора, теломерных участков.
Поровые комплексы могут встречаться и в других мембранных компонентах клетки, но гораздо реже, чем в ядерной оболочке. Иногда поровые комплексы видны в составе мембран гранулярного эндоплазматического ретикулума. Они обнаруживаются в составе окончатых мембран цитоплазмы, которые представляют собой тесно расположенные пачки замкнутых плоских мембранных мешков, сплошь пронизанных поровыми комплексами, имеющими такую же структуру, как и поры в ядерной оболочке.
Интересные данные были получены при морфометрическом изучении поровых комплексов в ядрах и окончатых мембранах бластодермы эмбрионов дрозофилы. Оказалось, что при переходе от синцитиальной к целлюлярной стадии, количество пор в оболочках ядер остается неизменным, а количество пор в окончатых пластинках вырастает примерно в 10 раз. В дальнейшем окончатые мембраны полностью исчезают. На основании этого было сделано предположение, что на ранней стадии развития в бластодерме дрозофилы происходит “суперпродукция” поровых комплексов (или их компонентов), избыток которых “встраивается” в окончатые мембраны. Т.е. макромолекулярный ансамбль, составляющий комплекс ядерных пор, способен к автономной самосборке и к последующему встраиванию в различные мембранные системы.
Роль ядерной оболочки в ядерно-цитоплазматическом обмене
Со времени открытия ядерной оболочки и описания ее строения делалось заключение о том, что ядерная оболочка может служить регулятором в ядерно-цитоплазматическом обмене и главная роль в этих процессах отводилась ядерным порам. Обмен же продуктами между ядром и цитоплазмой в самом деле очень велик: все ядерные белки поступают в ядро из цитоплазмы и все формы РНК выводятся из ядер. И в этом процессе комплекс поры выступает как супрамолекулярный комплекс, выполняющий роль не только транслокатора, механизма переноса, но и роль сортировщика, узнающего и отбирающего специальным образом переносимые молекулы.
В процессе ядерно-цитоплазматического транспорта ядерные поры функционируют как некоторое молекулярное сито, пропуская частицы определенного размера пассивно, по градиенту концентрации. Так, ионы, сахара, нуклеотиды, АТФ, гормоны - свободно поступают в ядра. С другой стороны ядерные поры осуществляют избирательный транспорт.
Через ядерную оболочку беспрепятственно в обе стороны происходит пассивный транспорт высоко молекулярных соединений, имеющих массу не более 5 х 103 дальтон. Для определения размеров частиц, могущих пройти сквозь пору, используются гранулы декстрана или коллоидного золота, которые путем микроинъекции вводятся в цитоплазму живой клетки. Было обнаружено, что максимальный размер частиц, способных транспортироваться в ядро составляет 8,5-10 нм. При этом сначала частицы собираются в зоне поровых комплексов, а затем оказываются в ядре. Неядерные белки с массой большей, чем 20 000-40 000 дальтон проникают в ядро медленнее, если вообще проникают. Так инъецированные белки с массой 17 кД могут проникнуть в ядро довольно быстро, за 2-3 минуты, белки 40 кД - за 30 минут, белки 60 кД - вообще не проникают в ядра. Считается, что белки с гидродинамическим радиусом больше 3,5 нм (что соответствует глобулярному белку с массой 65 кД), не могут просто механически проходить через ядерную пору. В этих случаях ядерная пора выступает в качестве реального молекулярного сита.
Но дело осложняется тем, что многие белки поступают как в ядро, так и выходят из него против градиента концентраций. Так, например, концентрация гистонов в ядре значительно выше, чем в цитоплазме. Но, несмотря на это, во время синтеза ДНК происходит транспорт огромного количества (106 молекул каждые три минуты, или по 100-500 молекул через одну пору за 1 минуту) гистонов из цитоплазмы в ядро. С другой стороны через ядерные поры реально могут проходить некоторые белки и даже макромолекулярные комплексы с массой значительно большей, чем 60 кД.
Через ядерные поры из цитоплазмы в ядро транспортируются крупные молекулы белков, например, белок нуклеоплазмин, пентамер с молекулярной массой 125 кД. Из ядра через поры выходят в цитоплазму субъединицы рибосом и другие рибонуклеопротеиды, меньшие из которых могут иметь массу 250 кД. Эти данные показывают, что комплексы ядерных пор не представляют собой просто механические сита, которые ограничивают транспорт молекул в зависимости от их размеров.
Работы последнего времени показывают, что многие ядерные белки проходят через ядерные поры с помощью специальных механизмов, включающих узнавание и связывание крупных ядерных белков, а затем только их транслокацию, перенос через поры. Было найдено, что белки, транспортируемые в ядро, имеют определенные последовательности аминокислот - последовательности ядерной локализации (NLS), которые узнаются рецепторами ядерных пор. Такие NLS характерны для кариофильных белков, т.е. для белков ядерной локализации, которые синтезируются на рибосомах в цитоплазме, а затем транспортируются в ядро.
Импорт кариофильных белков
Впервые аминокислотные последовательности ядерной локализации были обнаружены на С-конце субъединиц молекулы нуклеоплазмина (ядерный белок, принимающий участие в структуризации хроматина). Эти эксперименты были проведены на бесклеточной системе, когда выделенные ядра помещались в цитоплазматический экстракт ооцитов ксенопуса, куда добавляли нативные или измененные молекулы нуклеоплазмина. Это крупный белок (125 кД), состоящий из пяти субъединиц, каждая из которых обладает глобулярной и фибриллярной, С-концевой, частями. Если удалит путем протеолиза примерно 50 аминокислот с С-конца, то ни пентамер, ни мономеры в ядро не попадают, в то время как отщепленные фибриллярные участки через поры проходят свободно, так как содержат NLS-участок.
Более того, при смешивании неядерных белков с этими NLS-фрагментами, такие комплексы способны транспортироваться в ядро. Даже крупные частицы декстрана (20 нм), неспособные проникать в ядро, при связывании с ними NLS-последовательностей нуклеоплазмина транспортировались из цитоплазматического экстракта в ядро.
Подробно строение NLS изучено у белка Т антигена вируса SV40. Кариофильный сигнал состоял из последовательности: Pro-Lys-128Lys-Lys-Arg-Lys-Val. Одна лишь аминокислотная замена (128Lys на Thr или Asp) полностью лишают этого фрагмента кариофильных свойств. Оказалось. что можно создавать химерные белки с этим аминокислотным доменом, что позволяет необычные для ядер белки (альбумин плазмы, иммуноглобулин G, и даже ферритин с мол. массой 465 кД) транспортировать через ядерные поры.
Было показано, что белок с NLS проходит в ядро через несколько этапов (рис. 111). Импорт начинается с того, что NLS-белок связывается с гетеродимером рецептора NLS, с белками импортинами и , локализованными в цитоплазме. Возникший белковый комплекс (импортируемый белок с NLS, связанный с импортинами и ) подходит к внешней ядерной мембране и закрепляется на цитоплазматических филаментах порового комплекса. Затем этот комплекс входит в ядерную пору и проходит через “транспортер”. Считается, что транспортер состоит из множества извитых белковых филаментов, обогащенных аланином и глицином (FG-филаменты), представляющих собой барьер для транспорта некариофильных белков. Комплекс же, имеющий NLS как бы разрыхляет эту сеть и проходит через канал транспортера. После перехода комплекса в нуклеоплазму импортин связывается с белком RAN, представляющего собой малую GTP-азу, что приводит к распаду комплекса. Импортируемый белок освобождается и остается в ядре, импортин возвращается в цитоплазму, так же как и импортин , но в связи с RAN-GDP, где последние также диссоциируют. Тем самым только белок с NLS остается в составе ядра (рис. 111).
Экспорт из ядра в цитоплазму
Из ядра в цитоплазму также существует поток как белков, так и ядерных транскриптов в виде рибонуклеопротеидов. В принципе этот экспорт своей организации сходен с процессом импорта кариофильных белков. Так было обнаружено, что гликопротеидные молекулы, связывающие лиганды, локализуются в место поровых комплексов и со стороны ядра. Одна и та же пора может принимать участие как в импорте, так и в экспорте макромолекул. В пользу этого говорит то, что частички коллоидного золота, связанного с нуклеоплазмином, сорбируются на ядерной поре со стороны цитоплазмы, одновременно с сорбцией частичек, связанных с РНК, инъецированных в ядре ооцитов. Подобные эксперименты показали, что многие РНК (тРНК, 5S РНК, поли-У и поли-А), связанные с коллоидным золотом, аккумулируются в зоне ядерных пор, а затем переносятся в цитоплазму. Более того, РНК способствует переносу через ядерную пору крупных частиц золота размером до 20 нм. Обратного переноса не происходит: аналогичные частички, инъецированные в цитоплазму ооцита, в ядро не проникают.
Что касается естественных видов РНП, то комплексы ядерных пор также должны узнавать специфический сигнал на экспорт. Белковые компоненты РНП несут аминокислотные последовательности, сигналы ядерного экспорта (NES), которые дают возможность различным РНП проходить через ядерную оболочку в цитоплазму.
В этом случае также образуется сложный комплекс, состоящий из переносимого белка с NES-последовательностью (связанного с РНК или свободного), ассоциированного с белком экспортином 1, который в свою очередь связан с RAN-GTP. Этот комплекс проходит через центральный канал, создаваемый транспортером, в цитоплазму, где и диссоциирует. При этом освобождается белок с NES-участком (или РНП), который остается в цитоплазме. Экспортин 1 и RAN после гидролиза GTP снова возвращаются в ядро (рис. 112).
В процессе экспорта РНП ядерная пора контролирует не только белковый компонент. Ядерные поры узнают и не экспортируют короткие (100 нуклеотидов) тРНК, если в их структуре есть хоть одна замена. Транспорт незрелых форм иРНК, имеющих интронные участки, не происходит. Вообще в цитоплазме не обнаруживаются незрелые РНК. Вероятно, для экспорта некоторых РНК необходима их связь с особыми белками. Так 5S РНК переносится в цитоплазму вместе с транскрипционным фактором TFIIIA, или с белком L5. Мутантные формы 5S рРНК, которые не связываются с TFIIIA, остаются в ядре.
Мало изучен вопрос о транспорте в цитоплазму крупных РНП-комплексов, таких как субъединицы рибосом, информосомы и малые ядерные РНП. Возможно все они под действием каких-то факторов разворачиваются, меняют свою конформацию и проходят через поровый комплекс. В пользу этого говорят наблюдения гантелевидных РНК-содержащих частиц, в просвете пор ядер гигантских слюнных желез насекомых. Считается, что эта картина отражает момент выхода из ядер РНП-частиц 60 нм в диаметре, относимых к информоферам. Интересно, что состав белков в цитоплазматических информационных РНП иной, это может говорить о том, что в зоне поровых комплексов происходит “переодевание” информационных РНК, связь их с иными белками.
Динамика ядерной оболочки в митозе
Большей частью, но не у всех видов (исключение составляют амебы, эвгленовые, инфузории, динофлагелляты, многие водоросли, некоторые грибы), ядерная оболочка разрушается при митозе и снова возникает после деления клеток. Это так называемый открытый тип митоза (рис. 113). При этом в профазе по мере конденсации хромосом ядерная оболочка теряет с ними связь, а затем в ней появляются разрывы. Она приобретает вид плоских мембранных вакуолей, цистерн. В это время ядерные поры еще видны. Позднее они исчезают. Во время митоза 120 мДа комплекс ядерной поры разбирается на субкомплексы примерно по 1 мДа. Разборка пор начинается с фосфорилирования ряда нуклеопоринов митотической cdc2/циклин B киназой.
Ядерная оболочка превращается в скопление мелких мембранных пузырьков, окружающих зону бывшего интерфазного ядра. Такие пузырьки морфологически нельзя отличить от других мелких вакуолей в цитоплазме, они вероятно сливаются с вакуолями эндоплазматического ретикулума. В метафазе мембранные элементы цитоплазмы оттесняются к периферическим зонам клеток микротрубочками веретена деления.
В конце анафазы, когда прекращается движение хромосом к противоположным полюсам клетки, мембранные пузырьки цитоплазмы, и в первую очередь мембраны гранулярного эндоплазматического ретикулума (см. ниже), начинают контактировать с поверхностью хромосом. Эти контакты происходят сначала в небольшом числе точек, но затем начинается перестройка и рост этих первичных зачатков ядерной оболочки. Они из мелких пузырьков превращаются в плоские вакуоли, которые растут в ширину и обволакивают поверхность деконденсирующихся хромосом. Участки таких растущих плоских мембранных мешков сливаются, замыкая и отгораживая содержимое нового интерфазного ядра. Интересно, что ядерные поры появляются на самых ранних этапах реконструкции ядерной оболочки, когда двойные мембранные цистерны еще не сомкнулись и фактически ничего не разделяют.
При реконструкции ядерной оболочки происходит сборка ядерных пор. Она начинается с образования ямки при слиянии внешней и внутренней ядерной мембраны, которая затем превращается в отверстие. В этом процессе принимают участие интегральные белки gp 210 и POM 121, которые впоследствии будут закреплять ЯПК на мембранах.
За этим следует появление внутренних структур ЯПК: комплекс кольца, спиц, добавление звездчатого кольца и других структур, и, наконец, филаментов.
У некоторых низших организмов в случае закрытого митоза ядерная оболочка не исчезает, она в зоне ядерной перетяжки замыкается, что приводит к образованию двух новых ядер. Здесь участие ядерной оболочки в делении клетки заключается в том, что на ней закреплены хромосомы, и она, по-видимому, принимает участие в индукции образования микротрубочек, необходимых при делении клеток.
По-видимому, для реконструкции ядерной оболочки необходимым условием является деконденсация хромосом. Было показано, что если вызвать преждевременную деконденсацию метафазных хромосом, то они очень быстро контактируют с мембранными пузырьками и одеваются каждая своей отдельно ядерной оболочкой, вследствие чего в клетке возникает множество так называемых микроядер, каждое их которых возникло из одной хромосомы.
С другой стороны, можно экспериментально вызвать разборку ядерной оболочки у интерфазного ядра. Это происходит, если слить в культуре ткани две клетки на разных стадиях клеточного цикла и получить т.н. гетерокарион, где одно из ядер будет находиться в интерфазе, а другое быть в виде митотических хромосом в метафазе. В этом случае в интерфазном ядре начинает конденсироваться хроматин, образуются преждевременно конденсированные хромосомы, а ядерная оболочка исчезнет так же как во время нормального митоза (рис. 114). Эти данные говорят о том, что в цитоплазме митотической клетки существуют какие-то факторы, вызывающие как конденсацию хромосом, так и параллельный этому процесс распада ядерной оболочки.
Сходная динамика совпадения процессов перестройки хромосом и ядерной оболочки наблюдается и в другой системе, в цитоплазме ооцитов или в бесклеточных цитоплазматических экстрактах ооцитов. Так если в цитоплазму ооцита амфибий на стадии метафазы инъецировать выделенные интерфазные ядра, то их ядерная оболочка разбирается, а хроматин конденсируется в виде митотических хромосом. Если же в ооцит на стадии интерфазы ввести митотические хромосомы, то они начинают деконденсироваться, появляются множественные мелкие вакуоли, которые сливаясь друг с другом, образуют ядерные оболочки. Интересно, что в цитоплазму интерфазного ооцита можно ввести даже чужеродную чистую ДНК, которая, связываясь с гистонами в цитоплазме, образует хроматиновые глыбки, которые в свою очередь одеваются ядерными оболочками и превращаются в микроядра.
Эти экспериментальные приемы вместе с методом иммунофлуоресценции позволили проследить судьбу многих белков ядерной оболочки во время митоза. Подробно изучена судьба ламинов. Было найдено, что фиброзный слой ламинов деполимеризуется параллельно распаду ядерных мембран и конденсации хроматина. Этому предшествует обильное (в 7 раз выше, чем в интерфазе) фосфорилирование ламинов. Ламины A и C при этом деполимеризуются до димеров и тетрамеров и, переходя в растворимое состояние, равномерно распределяются в цитоплазме вне связи с другими структурами. Ламин B тоже деполимеризуется до олигомеров, но остается связанным с мембранными пузырьками, возникшими из ядерной оболочки.
При сборке ядерной оболочки в телофазе белки ламины иммунохимически начинают выявляться в центромерных и теломерных участках хромосом, там же обнаруживаются первые признаки образования новой ядерной оболочки. Там же накапливаются антитела к белкам порового комплекса. В бесклеточной системе цитоплазматического экстракта ооцитов было показано, что ассоциация растворимых в митозе ламинов A и C происходит независимо от ламина B. Оказалось, что если систему реконструкции ядерной оболочки лишить ламина B, то ламины A и C связываются с поверхностью хромосом, но сборки ядерной оболочки не происходит. В экстракте, лишенном ламинов A и C, ламин B связывается с хромосомами, но нормальная ядерная оболочка так же не формируется.
studfiles.net
Глава 10. Ядерная оболочка
Структура, ограничивающая параметр клеточного ядра, ядерная оболочка, характерна для эукариотических клеток. Она разделяет два внутриклеточных компартмента друг от друга, цитоплазму от ядра. Значение такого разделения структур в пространстве очень важно: это приводит к обособлению процессов синтеза белка и процессов синтеза нуклеиновых кислот, что создает дополнительные, по сравнению с прокариотами, возможности для регуляции генной активности и ее реализации в виде синтеза специфических белков. Активная регуляция транспорта из цитоплазмы в ядро и из ядра в цитоплазму, через специальные комплексы пор создает систему избирательного транспорта веществ, делая ядерную оболочку “генными воротами” со специальными “превратниками” (контрольными пунктами), регулирующими потоки ядерного импорта и экспорта. Кроме того, как уже описывалось, ядерная оболочка играет большую роль в организации трехмерной структуры интерфазного ядра, элементы ядерной оболочки являются частью ядерного белкового матрикса.
Ядерная оболочка состоит из двух мембран, внешней и внутренней, между которыми располагается перинуклеарное пространство (рис. 106). Внутренняя мембрана ядерной оболочки структурно связана с ламиной - фиброзным периферическим слоем ядерного белкового матрикса. В общем виде ядерная оболочка может быть представлена как двухслойный мешок, отделяющий содержимое ядра от цитоплазмы. Однако ядерная оболочка имеет характерную особенность, отличающую ее от других двухмембранных структур клетки (митохондрии и пластиды). Это наличие особых ядерных пор, которые образуются за счет многочисленных зон слияния двух ядерных мембран и представляют собой как бы округлые, сквозные перфорации всей ядерной оболочки.
Компоненты ядерной оболочки
Внешняя мембрана ядерной оболочки, непосредственно контактирующая с цитоплазмой клетки, имеет ряд структурных особенностей, позволяющих отнести ее к собственно мембранной системе эндоплазматического ретикулума (ЭПР). Так, на внешней ядерной мембране обычно располагается большое количество рибосом, как и на мембранах эргастоплазмы. Существуют многочисленные наблюдения о непосредственном переходе внешней ядерной мембраны в систему каналов эндоплазматического ретикулума, что особенно подчеркивает структурную идентичность этих мембран (рис. 106).
Так у клеток, бедных эндоплазматическим ретикулумом, внешняя ядерная мембрана может представлять собой “минимальный” объем эндоплазматического ретикулума, который может участвовать в синтезе белкового и липидного компонентов мембран. Описаны случаи, когда от внешней ядерной мембраны отщепляются мембранные вакуоли, направляющиеся в проксимальный отдел аппарата Гольджи. Состав липидов и белков внешней ядерной мембраны очень схож с таковым ретикулума, что, возможно, и определяет их общие биохимические функции, что особенно подчеркивается наличием рибосом на поверхности мембран, обращенной в гиалоплазму. Эти рибосомы синтезируют, как мембранные, так и секретируемые белки, которые могут транспортироваться в перинуклеарное пространство, а оттуда в полости цистерн ЭПР. Так, например, при стимуляции образования -глобулинов в плазмоцитах первые продукты клеточной активности локализуются в перинуклеарном пространстве, а потом начинают появляться в полостях ЭПР. У большинства животных и растительных клеток внешняя мембрана ядерной оболочки не представляет собой идеально ровную поверхность - она может образовывать различной величины выпячивания или выросты в сторону цитоплазмы.
Внутренняя мембрана ядерной оболочки рибосом на своей поверхности не имеет, но связана с фиброзным слоем, ядерной ламиной (Lamina nucleum limitans), которая, в свою очередь, заякоревает хроматин на ядерной оболочке. Связь хроматина с внутренней мембраной оболочки является ее характерной особенностью, хотя существуют примеры, когда эти связи нарушаются при сохранении целостности ядерной оболочки. Так, например, в ооцитах амфибий на стадии диплотены все хромосомы собираются в центре ядра и полностью теряют связь с ядерной оболочкой. С другой стороны, при делении клеток с т.н. закрытым типом митоза большая часть внутренней ядерной мембраны теряет связь с хроматином.
О специфичности белков ламины уже говорилось в разделе “Ядерный белковый матрикс”, здесь же необходимо еще раз подчеркнуть, что эти фибриллярные белки не образуют неизменную структуру. Фиброзный слой ламины все время перестраивается, особенно в связи с ростом поверхности ядра, во время клеточного цикла. Характерные для внутренней ядерной мембраны белки ламины A, C и B относятся к фибриллярным белкам V типа промежуточных филаментов (см. ниже), их фибриллярные мономеры могут образовывать димеры, тетрамеры, а последние образуют фибриллы толщиной около 10 нм. Со стороны кариоплазмы под внутренней ядерной мембраной такие фибриллы образуют ортогональные структуры, чередующиеся с рыхло расположенной сетью этих же фибрилл.
Белки ламины с мембраной связаны двояким образом. Так ламин B после синтеза модифицируется добавлением гидрофобной изопентильной группы вблизи C-конца. Эта липофильная группа встраивается в слой мембраны и как бы заякоревает ламину на мембране. Кроме того целый ряд интегральных белков внутренней ядерной мембраны (LBR, LAR, эмерин и др.) также закрепляют ламины посредством дополнительных белков, входящих в состав этого фиброзного слоя. Эти же белки участвуют в связывании ядерной мембраны с хроматином.
Наиболее характерной и бросающейся в глаза структурой в составе ядерной оболочки является ядерная пора. Поры в оболочке образуются за счет двух ядерных мембран в виде округлых сквозных отверстий или перфораций с диаметром около 100 нм. При альдегидной фиксации или при использовании метода замораживания и скалывания в электронном микроскопе видно, что округлое сквозное отверстие в ядерной оболочке заполнено сложно организованными глобулярными и фибриллярными структурами (рис. 107). Совокупность мембранных перфораций и этих структур называют комплексом пор ядра. Тем самым подчеркивается, что ядерная пора не просто сквозная дыра в ядерной оболочке, через которую непосредственно вещества ядра и цитоплазмы могут сообщаться. Компоненты комплекса пор имеют белковую природу.
Ядерный поровый комплекс (ЯПК или NPC - nuclear pore complex) представляет собой супрамолекулярную структуру с м.в. более 125 х 106 Да, состоящую из более 1000 белков, масса которых в 30 раз больше чем рибосома. Белки ЯПК носят название нуклеопоринов 50-100 видов. Эти белки собраны примерно в 12 субкомплексов.
В последнее время удалось получить отчетливые изображения ЯПК в электронном микроскопе, что дает возможность понять их структурную организацию. Внешний диаметр порового комплекса составляет около 100 нм, а высота - 75 нм. В целом он представляет собой цилиндрическую фигуру с признаками октогональной симметрии. Несмотря на очень впечатляющие изображения выделенных ЯПК, разные авторы дают разные схемы строения этого сложного комплекса, обладающего симметрией восьмого порядка.
Если посмотреть на ЯПК в плане на ультратонком срезе, то бросается в глаза, что его периферия представлена восьмью глобулами (рис. 108, 109). На выделенных же ЯПК в первую очередь видны кольчатые структуры. От периферических компонентов ЯПК в сторону цитоплазмы простираются фибриллярные выросты. Со стороны ядра тоже фибриллярные выросты образуют корзинкоподобную структуру, связанную терминальным кольцом. В большинстве моделей центр цилиндрической фигуры ЯПК содержит “пробку” (центральную гранулу, или транспортер). По одной из моделей (см. рис. 93) цитоплазматические филаменты отходят от цитоплазматического кольца, состоящего из 8 субъединиц. Между ним и внешней ядерной мембраной располагается тонкое кольцо, а затем звездчатое кольцо. Цитоплазматическое кольцо связано внутренними филаментами с транспортером, который находится в центре и заполняет пространство между внешней и внутренней ядерной мембраной. Сходная структура находится на внутренней мембране: нуклеоплазматическое кольцо поддерживает филаменты “корзины”. Другие варианты моделей показаны на (рис. 110).
Весь ЯПК закрепляется интегральными белками, гликопротеидами gp 210 и РОМ 121 в стенке мембранной перфорации.
По своей сложности организации и, главное, по функциональной значимости комплекс ядерной поры можно было бы отнести к органеллам клетки, т.к. их роль заключается в контроле за ядерно-цитоплазменными связями.
Размер ядерных пор и их структура стандартны не только для данной клетки, но и для всех клеток данного организма, более того для всех эукариот.
Число ядерных пор (см. табл. 13) зависит от метаболической активности клеток: чем выше синтетические процессы в клетках, тем больше пор на единицу поверхности клеточного ядра. Так, у эритробластов (клетки-предшественники ядерных эритроцитов) низших позвоночных животных во время интенсивного синтеза и накопления гемоглобина обнаруживается в ядре около 30 ядерных пор на 1 мкм2. После того как эти процессы заканчиваются, в ядрах зрелых клеток - эритроцитов прекращаются синтезы ДНК и РНК, и количество пор падает до 5 на мкм2. В ядерных оболочках полностью зрелых сперматозоидов поры не обнаруживаются, так же как у микронуклеусов некоторых инфузорий. Количество пор может изменяться в течение клеточного цикла. Первое возрастание числа пор наблюдается при реконструкции и росте ядер после митоза, второй этап увеличения числа пор происходит во время синтеза ДНК.
Таблица 13. Количество ядерных пор в различных объектах
| Объект | Число ядерных пор на мкм2. | Число пор на одно ядро |
| Ксенопус, почки | 10,05 | 3400 |
| Ксенопус, ооцит | 51,0 | 37,6 х 106 |
| Мышь, культура ткани | 10,83 | 5050 |
| Человек, культура ткани | 11,24 | 3930 |
| Крыса, гепатоцит | 16,1 | 3800 |
| Мышь, лимфоцит | 3,3 | 400 |
| Человек, лимфоцит | 4,47 | 700 |
По поверхности ядра поры располагаются более или менее равномерно, но их число резко падает в местах ассоциации с ядерной оболочкой участков гетерохроматина, ядрышкового организатора, теломерных участков.
Поровые комплексы могут встречаться и в других мембранных компонентах клетки, но гораздо реже, чем в ядерной оболочке. Иногда поровые комплексы видны в составе мембран гранулярного эндоплазматического ретикулума. Они обнаруживаются в составе окончатых мембран цитоплазмы, которые представляют собой тесно расположенные пачки замкнутых плоских мембранных мешков, сплошь пронизанных поровыми комплексами, имеющими такую же структуру, как и поры в ядерной оболочке.
Интересные данные были получены при морфометрическом изучении поровых комплексов в ядрах и окончатых мембранах бластодермы эмбрионов дрозофилы. Оказалось, что при переходе от синцитиальной к целлюлярной стадии, количество пор в оболочках ядер остается неизменным, а количество пор в окончатых пластинках вырастает примерно в 10 раз. В дальнейшем окончатые мембраны полностью исчезают. На основании этого было сделано предположение, что на ранней стадии развития в бластодерме дрозофилы происходит “суперпродукция” поровых комплексов (или их компонентов), избыток которых “встраивается” в окончатые мембраны. Т.е. макромолекулярный ансамбль, составляющий комплекс ядерных пор, способен к автономной самосборке и к последующему встраиванию в различные мембранные системы.
Роль ядерной оболочки в ядерно-цитоплазматическом обмене
Со времени открытия ядерной оболочки и описания ее строения делалось заключение о том, что ядерная оболочка может служить регулятором в ядерно-цитоплазматическом обмене и главная роль в этих процессах отводилась ядерным порам. Обмен же продуктами между ядром и цитоплазмой в самом деле очень велик: все ядерные белки поступают в ядро из цитоплазмы и все формы РНК выводятся из ядер. И в этом процессе комплекс поры выступает как супрамолекулярный комплекс, выполняющий роль не только транслокатора, механизма переноса, но и роль сортировщика, узнающего и отбирающего специальным образом переносимые молекулы.
В процессе ядерно-цитоплазматического транспорта ядерные поры функционируют как некоторое молекулярное сито, пропуская частицы определенного размера пассивно, по градиенту концентрации. Так, ионы, сахара, нуклеотиды, АТФ, гормоны - свободно поступают в ядра. С другой стороны ядерные поры осуществляют избирательный транспорт.
Через ядерную оболочку беспрепятственно в обе стороны происходит пассивный транспорт высоко молекулярных соединений, имеющих массу не более 5 х 103 дальтон. Для определения размеров частиц, могущих пройти сквозь пору, используются гранулы декстрана или коллоидного золота, которые путем микроинъекции вводятся в цитоплазму живой клетки. Было обнаружено, что максимальный размер частиц, способных транспортироваться в ядро составляет 8,5-10 нм. При этом сначала частицы собираются в зоне поровых комплексов, а затем оказываются в ядре. Неядерные белки с массой большей, чем 20 000-40 000 дальтон проникают в ядро медленнее, если вообще проникают. Так инъецированные белки с массой 17 кД могут проникнуть в ядро довольно быстро, за 2-3 минуты, белки 40 кД - за 30 минут, белки 60 кД - вообще не проникают в ядра. Считается, что белки с гидродинамическим радиусом больше 3,5 нм (что соответствует глобулярному белку с массой 65 кД), не могут просто механически проходить через ядерную пору. В этих случаях ядерная пора выступает в качестве реального молекулярного сита.
Но дело осложняется тем, что многие белки поступают как в ядро, так и выходят из него против градиента концентраций. Так, например, концентрация гистонов в ядре значительно выше, чем в цитоплазме. Но, несмотря на это, во время синтеза ДНК происходит транспорт огромного количества (106 молекул каждые три минуты, или по 100-500 молекул через одну пору за 1 минуту) гистонов из цитоплазмы в ядро. С другой стороны через ядерные поры реально могут проходить некоторые белки и даже макромолекулярные комплексы с массой значительно большей, чем 60 кД.
Через ядерные поры из цитоплазмы в ядро транспортируются крупные молекулы белков, например, белок нуклеоплазмин, пентамер с молекулярной массой 125 кД. Из ядра через поры выходят в цитоплазму субъединицы рибосом и другие рибонуклеопротеиды, меньшие из которых могут иметь массу 250 кД. Эти данные показывают, что комплексы ядерных пор не представляют собой просто механические сита, которые ограничивают транспорт молекул в зависимости от их размеров.
Работы последнего времени показывают, что многие ядерные белки проходят через ядерные поры с помощью специальных механизмов, включающих узнавание и связывание крупных ядерных белков, а затем только их транслокацию, перенос через поры. Было найдено, что белки, транспортируемые в ядро, имеют определенные последовательности аминокислот - последовательности ядерной локализации (NLS), которые узнаются рецепторами ядерных пор. Такие NLS характерны для кариофильных белков, т.е. для белков ядерной локализации, которые синтезируются на рибосомах в цитоплазме, а затем транспортируются в ядро.
Импорт кариофильных белков
Впервые аминокислотные последовательности ядерной локализации были обнаружены на С-конце субъединиц молекулы нуклеоплазмина (ядерный белок, принимающий участие в структуризации хроматина). Эти эксперименты были проведены на бесклеточной системе, когда выделенные ядра помещались в цитоплазматический экстракт ооцитов ксенопуса, куда добавляли нативные или измененные молекулы нуклеоплазмина. Это крупный белок (125 кД), состоящий из пяти субъединиц, каждая из которых обладает глобулярной и фибриллярной, С-концевой, частями. Если удалит путем протеолиза примерно 50 аминокислот с С-конца, то ни пентамер, ни мономеры в ядро не попадают, в то время как отщепленные фибриллярные участки через поры проходят свободно, так как содержат NLS-участок.
Более того, при смешивании неядерных белков с этими NLS-фрагментами, такие комплексы способны транспортироваться в ядро. Даже крупные частицы декстрана (20 нм), неспособные проникать в ядро, при связывании с ними NLS-последовательностей нуклеоплазмина транспортировались из цитоплазматического экстракта в ядро.
Подробно строение NLS изучено у белка Т антигена вируса SV40. Кариофильный сигнал состоял из последовательности: Pro-Lys-128Lys-Lys-Arg-Lys-Val. Одна лишь аминокислотная замена (128Lys на Thr или Asp) полностью лишают этого фрагмента кариофильных свойств. Оказалось. что можно создавать химерные белки с этим аминокислотным доменом, что позволяет необычные для ядер белки (альбумин плазмы, иммуноглобулин G, и даже ферритин с мол. массой 465 кД) транспортировать через ядерные поры.
Было показано, что белок с NLS проходит в ядро через несколько этапов (рис. 111). Импорт начинается с того, что NLS-белок связывается с гетеродимером рецептора NLS, с белками импортинами и , локализованными в цитоплазме. Возникший белковый комплекс (импортируемый белок с NLS, связанный с импортинами и ) подходит к внешней ядерной мембране и закрепляется на цитоплазматических филаментах порового комплекса. Затем этот комплекс входит в ядерную пору и проходит через “транспортер”. Считается, что транспортер состоит из множества извитых белковых филаментов, обогащенных аланином и глицином (FG-филаменты), представляющих собой барьер для транспорта некариофильных белков. Комплекс же, имеющий NLS как бы разрыхляет эту сеть и проходит через канал транспортера. После перехода комплекса в нуклеоплазму импортин связывается с белком RAN, представляющего собой малую GTP-азу, что приводит к распаду комплекса. Импортируемый белок освобождается и остается в ядре, импортин возвращается в цитоплазму, так же как и импортин , но в связи с RAN-GDP, где последние также диссоциируют. Тем самым только белок с NLS остается в составе ядра (рис. 111).
Экспорт из ядра в цитоплазму
Из ядра в цитоплазму также существует поток как белков, так и ядерных транскриптов в виде рибонуклеопротеидов. В принципе этот экспорт своей организации сходен с процессом импорта кариофильных белков. Так было обнаружено, что гликопротеидные молекулы, связывающие лиганды, локализуются в место поровых комплексов и со стороны ядра. Одна и та же пора может принимать участие как в импорте, так и в экспорте макромолекул. В пользу этого говорит то, что частички коллоидного золота, связанного с нуклеоплазмином, сорбируются на ядерной поре со стороны цитоплазмы, одновременно с сорбцией частичек, связанных с РНК, инъецированных в ядре ооцитов. Подобные эксперименты показали, что многие РНК (тРНК, 5S РНК, поли-У и поли-А), связанные с коллоидным золотом, аккумулируются в зоне ядерных пор, а затем переносятся в цитоплазму. Более того, РНК способствует переносу через ядерную пору крупных частиц золота размером до 20 нм. Обратного переноса не происходит: аналогичные частички, инъецированные в цитоплазму ооцита, в ядро не проникают.
Что касается естественных видов РНП, то комплексы ядерных пор также должны узнавать специфический сигнал на экспорт. Белковые компоненты РНП несут аминокислотные последовательности, сигналы ядерного экспорта (NES), которые дают возможность различным РНП проходить через ядерную оболочку в цитоплазму.
В этом случае также образуется сложный комплекс, состоящий из переносимого белка с NES-последовательностью (связанного с РНК или свободного), ассоциированного с белком экспортином 1, который в свою очередь связан с RAN-GTP. Этот комплекс проходит через центральный канал, создаваемый транспортером, в цитоплазму, где и диссоциирует. При этом освобождается белок с NES-участком (или РНП), который остается в цитоплазме. Экспортин 1 и RAN после гидролиза GTP снова возвращаются в ядро (рис. 112).
В процессе экспорта РНП ядерная пора контролирует не только белковый компонент. Ядерные поры узнают и не экспортируют короткие (100 нуклеотидов) тРНК, если в их структуре есть хоть одна замена. Транспорт незрелых форм иРНК, имеющих интронные участки, не происходит. Вообще в цитоплазме не обнаруживаются незрелые РНК. Вероятно, для экспорта некоторых РНК необходима их связь с особыми белками. Так 5S РНК переносится в цитоплазму вместе с транскрипционным фактором TFIIIA, или с белком L5. Мутантные формы 5S рРНК, которые не связываются с TFIIIA, остаются в ядре.
Мало изучен вопрос о транспорте в цитоплазму крупных РНП-комплексов, таких как субъединицы рибосом, информосомы и малые ядерные РНП. Возможно все они под действием каких-то факторов разворачиваются, меняют свою конформацию и проходят через поровый комплекс. В пользу этого говорят наблюдения гантелевидных РНК-содержащих частиц, в просвете пор ядер гигантских слюнных желез насекомых. Считается, что эта картина отражает момент выхода из ядер РНП-частиц 60 нм в диаметре, относимых к информоферам. Интересно, что состав белков в цитоплазматических информационных РНП иной, это может говорить о том, что в зоне поровых комплексов происходит “переодевание” информационных РНК, связь их с иными белками.
Динамика ядерной оболочки в митозе
Большей частью, но не у всех видов (исключение составляют амебы, эвгленовые, инфузории, динофлагелляты, многие водоросли, некоторые грибы), ядерная оболочка разрушается при митозе и снова возникает после деления клеток. Это так называемый открытый тип митоза (рис. 113). При этом в профазе по мере конденсации хромосом ядерная оболочка теряет с ними связь, а затем в ней появляются разрывы. Она приобретает вид плоских мембранных вакуолей, цистерн. В это время ядерные поры еще видны. Позднее они исчезают. Во время митоза 120 мДа комплекс ядерной поры разбирается на субкомплексы примерно по 1 мДа. Разборка пор начинается с фосфорилирования ряда нуклеопоринов митотической cdc2/циклин B киназой.
Ядерная оболочка превращается в скопление мелких мембранных пузырьков, окружающих зону бывшего интерфазного ядра. Такие пузырьки морфологически нельзя отличить от других мелких вакуолей в цитоплазме, они вероятно сливаются с вакуолями эндоплазматического ретикулума. В метафазе мембранные элементы цитоплазмы оттесняются к периферическим зонам клеток микротрубочками веретена деления.
В конце анафазы, когда прекращается движение хромосом к противоположным полюсам клетки, мембранные пузырьки цитоплазмы, и в первую очередь мембраны гранулярного эндоплазматического ретикулума (см. ниже), начинают контактировать с поверхностью хромосом. Эти контакты происходят сначала в небольшом числе точек, но затем начинается перестройка и рост этих первичных зачатков ядерной оболочки. Они из мелких пузырьков превращаются в плоские вакуоли, которые растут в ширину и обволакивают поверхность деконденсирующихся хромосом. Участки таких растущих плоских мембранных мешков сливаются, замыкая и отгораживая содержимое нового интерфазного ядра. Интересно, что ядерные поры появляются на самых ранних этапах реконструкции ядерной оболочки, когда двойные мембранные цистерны еще не сомкнулись и фактически ничего не разделяют.
При реконструкции ядерной оболочки происходит сборка ядерных пор. Она начинается с образования ямки при слиянии внешней и внутренней ядерной мембраны, которая затем превращается в отверстие. В этом процессе принимают участие интегральные белки gp 210 и POM 121, которые впоследствии будут закреплять ЯПК на мембранах.
За этим следует появление внутренних структур ЯПК: комплекс кольца, спиц, добавление звездчатого кольца и других структур, и, наконец, филаментов.
У некоторых низших организмов в случае закрытого митоза ядерная оболочка не исчезает, она в зоне ядерной перетяжки замыкается, что приводит к образованию двух новых ядер. Здесь участие ядерной оболочки в делении клетки заключается в том, что на ней закреплены хромосомы, и она, по-видимому, принимает участие в индукции образования микротрубочек, необходимых при делении клеток.
По-видимому, для реконструкции ядерной оболочки необходимым условием является деконденсация хромосом. Было показано, что если вызвать преждевременную деконденсацию метафазных хромосом, то они очень быстро контактируют с мембранными пузырьками и одеваются каждая своей отдельно ядерной оболочкой, вследствие чего в клетке возникает множество так называемых микроядер, каждое их которых возникло из одной хромосомы.
С другой стороны, можно экспериментально вызвать разборку ядерной оболочки у интерфазного ядра. Это происходит, если слить в культуре ткани две клетки на разных стадиях клеточного цикла и получить т.н. гетерокарион, где одно из ядер будет находиться в интерфазе, а другое быть в виде митотических хромосом в метафазе. В этом случае в интерфазном ядре начинает конденсироваться хроматин, образуются преждевременно конденсированные хромосомы, а ядерная оболочка исчезнет так же как во время нормального митоза (рис. 114). Эти данные говорят о том, что в цитоплазме митотической клетки существуют какие-то факторы, вызывающие как конденсацию хромосом, так и параллельный этому процесс распада ядерной оболочки.
Сходная динамика совпадения процессов перестройки хромосом и ядерной оболочки наблюдается и в другой системе, в цитоплазме ооцитов или в бесклеточных цитоплазматических экстрактах ооцитов. Так если в цитоплазму ооцита амфибий на стадии метафазы инъецировать выделенные интерфазные ядра, то их ядерная оболочка разбирается, а хроматин конденсируется в виде митотических хромосом. Если же в ооцит на стадии интерфазы ввести митотические хромосомы, то они начинают деконденсироваться, появляются множественные мелкие вакуоли, которые сливаясь друг с другом, образуют ядерные оболочки. Интересно, что в цитоплазму интерфазного ооцита можно ввести даже чужеродную чистую ДНК, которая, связываясь с гистонами в цитоплазме, образует хроматиновые глыбки, которые в свою очередь одеваются ядерными оболочками и превращаются в микроядра.
Эти экспериментальные приемы вместе с методом иммунофлуоресценции позволили проследить судьбу многих белков ядерной оболочки во время митоза. Подробно изучена судьба ламинов. Было найдено, что фиброзный слой ламинов деполимеризуется параллельно распаду ядерных мембран и конденсации хроматина. Этому предшествует обильное (в 7 раз выше, чем в интерфазе) фосфорилирование ламинов. Ламины A и C при этом деполимеризуются до димеров и тетрамеров и, переходя в растворимое состояние, равномерно распределяются в цитоплазме вне связи с другими структурами. Ламин B тоже деполимеризуется до олигомеров, но остается связанным с мембранными пузырьками, возникшими из ядерной оболочки.
При сборке ядерной оболочки в телофазе белки ламины иммунохимически начинают выявляться в центромерных и теломерных участках хромосом, там же обнаруживаются первые признаки образования новой ядерной оболочки. Там же накапливаются антитела к белкам порового комплекса. В бесклеточной системе цитоплазматического экстракта ооцитов было показано, что ассоциация растворимых в митозе ламинов A и C происходит независимо от ламина B. Оказалось, что если систему реконструкции ядерной оболочки лишить ламина B, то ламины A и C связываются с поверхностью хромосом, но сборки ядерной оболочки не происходит. В экстракте, лишенном ламинов A и C, ламин B связывается с хромосомами, но нормальная ядерная оболочка так же не формируется.
studfiles.net
строение мембраны, участие в процессе деления
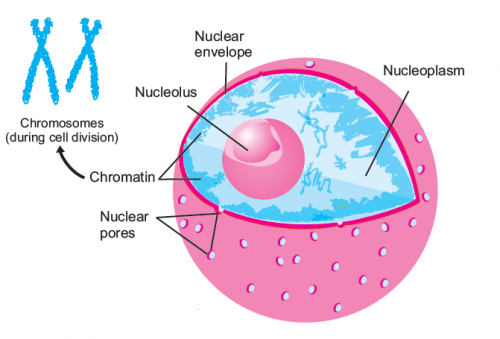
Ядерная оболочка (нуклеолемма) представляет собой сложное образование, отделяющее содержимое ядра от цитоплазмы и других элементов живой клетки. Данная оболочка выполняет ряд важных функций, без которых является невозможным функционирование ядер, полноценное деление клеток. Чтобы определить роль ядерных мембран в жизнедеятельности эукариотных клеток, необходимо узнать не только главные функции, но и особенности строения.
В статье подробно рассматриваются функции ядерной оболочки. Описывается строение, структурные компоненты нуклеолеммы, их взаимосвязь, механизмы транспортировки веществ, процесс деления при митозе.
Содержание:
Строение оболочки
Строение и свойства ЯПК
Виды ядерного транспорта
Импорт и экспорт белков
Ядерная оболочка при делении
Строение оболочки
Главное отличие эукариот заключается в наличии ядра и ряда других органелл, необходимых для его поддержания. Такие клетки входят в состав всех растений, грибов, животных, в то время как клетки-прокариоты представляют собой простейшие безъядерные организмы.
Нуклеолемма состоит из двух структурных элементов – внутренней и наружной мембран. В промежутке между ними существует свободное пространство, называемое перинуклеарным. Ширина перинуклеарного промежутка нуклеолеммы составляет от 20 до 60 нанометров (нм).
Внешняя мембрана нуклеолеммы контактирует с клеточной цитоплазмой. На ее наружной поверхности располагается существенное число рибосом, которые отвечают за синтез белковых соединений из отдельных аминокислот. Внешняя мембрана не содержит рибосом.
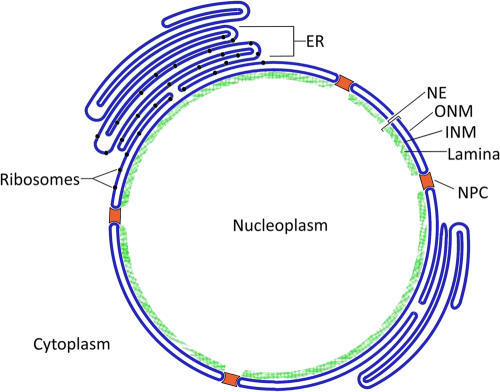
Мембраны, образующие нуклеолемму, состоят из белковых соединений и двойного слоя фосфолипидных веществ. Механическая прочность оболочки обеспечивается сетью филаментов – нитевидных белковых структур. Наличие филаментной сети характерно для большинства эукариот. Они соприкасаются с внутренней мембраной.
Сети филаментов располагаются не только в области нукелолеммах. Такие структуры также располагаются в цитоплазме. Их функция заключается в сохранении целостности клетки, а также в формировании контактов между клетками. При этом, отмечается, что слои, образующие сеть, регулярно перестраиваются. Данный процесс наиболее активен в период роста клеточного ядра перед делением.
Сеть филаментов, которая поддерживает мембраны, называется ядерной ламиной. Она формируется из определенной последовательности белков-полимеров, которые называются ламинами. Она взаимодействует с хроматином – веществом, участвующим в формировании хромосом. Также ламина контактирует с молекулами рибонуклеиновой кислоты, ответственными за хранение генетической информации.
Внешняя мембрана ядра взаимодействует с мембраной, окружающей эндоплазматический ретикулум. В определенных участках оболочки происходит контакт перинуклеарного пространства и внутреннего пространства ретикулума.
Функции эндоплазматического ретикулума:
- Синтез и транспортировка белков
- Хранение продуктов синтеза
- Формирование новой оболочки при митозе
- Хранение минералов кальция, выполняющих функцию медиатора
- Продукция гормонов

Внутри оболочки располагаются ядерные поровые комплексы. Это каналы, посредством которых происходит перенос молекул между клеточным ядром, цитоплазмой и другими клеточными органеллами. На одном квадратном микроне поверхности нуклеолеммы располагает от 10 до 20 поровых комплекса. Исходя из этого, в оболочке 1 соматической клетки может находится всего от 2 до 4 тысяч ЯПК.
Помимо транспорта веществ, оболочка выполняет опорную и защитную функцию. Она отделяет ядро от содержимого цитоплазмы, в том числе продуктов деятельности других органелл. Защитная функция заключается в предохранении генетической информации ядра от негативного воздействия, например, вирусной инфекции.
Считается, что двойная мембрана ядерной оболочки сформировалась в ходе эволюции путем захвата одних клеток другими. Вследствие этого, некоторые поглощенные клетки сохранили собственную активность, но при этом их ядро было окружено двойной мембраной – собственной, и мембраной клетки-хозяина.
Таким образом, ядерная оболочка представляет собой сложную структуру, состоящую из двойной мембраны, содержащей ядерные поры.
Строение и свойства ЯПК
Ядерный поровый комплекс – это симметричный канал, местом локализации которого является сличение наружной и внутренней мембран. ЯПК состоят из набора веществ, включающих около 30 видов белков.
Ядерные поры имеют бочкообразную форму. Образуемый канал не ограничивается ядерными мембранами, а незначительно выступает за их пределы. В результате с двух сторон оболочки возникают кольцеобразные выступы. Размер этих выступов отличается, так как с одной стороны кольцеобразное образование имеет больший диаметр, чем с другой. Элементы ядерных пор, выступающих за пределы мембраны, называются терминальными структурами.
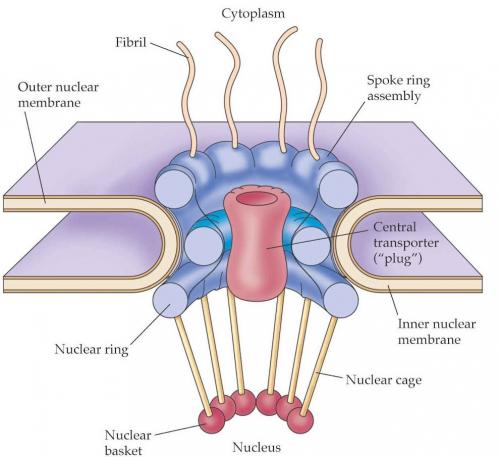
Цитоплазматическая терминальная структура (та что находится на внешней поверхности ядерной мембраны) состоит из восьми коротких фибрилл-нитей. Ядерная терминальная структура также состоит из 8 фибрилл, однако они образуют кольцо, выполняющего функции корзины. Во многих клетках от ядерной корзины исходят дополнительные фибриллы. Терминальные структуры являются местами, где происходит контакт молекул, транспортируемых через ядерные поры.
В месте расположения ЯПК происходит слияние наружной и внутренней ядерной мембраны. Такое слияние объясняется необходимостью обеспечить фиксацию ядерных пор в мембранах с помощью белков, соединяющих их также с ядерной ламиной.
В настоящее время общепринятым считается модульное строение ядерных каналов. Такая модель предусматривает структуру поры, состоящую из нескольких кольцевидных образований.
Внутри ядерной поры постоянно находится плотное вещество. Ее происхождение точно не известно, однако считается, что оно является одним из элементов ЯПК, за счет которого осуществляется транспортировка молекул от цитоплазмы к ядру и наоборот. Благодаря исследованию с использованием электронных микроскопов с высоким разрешением удалось выяснить, что плотная среда внутри ядерного канала способна менять свое месторасположение. Ввиду этого, считается, плотная внутренняя среда ЯПК является карго-рецепторным комплексом.
Транспортные функции ядерной оболочки возможны благодаря наличию ядерных поровых комплексов.
Виды ядерного транспорта
Транспортировка веществ через ядерную оболочку называется ядерно-цитоплазматическим транспортом веществ. Данный процесс предусматривает своеобразный обмен молекулами, синтезируемыми в ядре, и веществами, обеспечивающими жизнедеятельность самого ядра, импортируемыми из цитоплазмы.

Существуют такие виды транспортировки:
- Пассивная. Посредством данного процесса осуществляется перемещение небольших молекул. В частности, через пассивный транспорт происходит передача мононуклеотидов, минеральных компонентов, продуктов метаболического обмена. Процесс называется пассивным, так как протекает путем диффузии. Скорость прохождения через ядерную пору зависит от размера вещества. Чем оно меньше, тем выше скорость транспортировки.
- Активная. Предусматривает перенос через каналы внутри ядерной оболочки крупных молекул или их соединений. При этом, соединения не распадаются на мелкие частицы, что позволило бы увеличить скорость транспортировки. Данный процесс обеспечивает поступление в цитоплазму синтезируемых в ядре рибонуклеиновых молекул. Из внешнего цитоплазматического пространства за счет активного транспорта происходит перенос белков, необходимых для метаболических процессов.
Выделяют пассивный и активный транспорт белков, отличающийся механизмом действия.
Импорт и экспорт белков
Рассматривая функции ядерной оболочки, необходимо напомнить о том, что транспортировка веществ осуществляется в двух направлениях – из цитоплазмы в ядро и наоборот.
Импорт белковых соединений через мембраны к ядру осуществляется за счет наличия особых рецепторов, называемых транспортинами. Эти компоненты содержат запрограммированный сигнал, за счет которого происходит движение в необходимом направлении. Белки и соединения, не обладающие таким сигналом, способны присоединятся к веществам, у которых он есть, и таким образом беспрепятственно перемещаться.
Важно отметить, что сигналы ядерного импорта обеспечивают избирательность поступления веществ в ядро. Многие образования, в числе которых полимеразы ДНК и РНК, а также белки, участвующие в процессах регуляции, не достигают ядра. Таким образом, ядерные поры представляют собой не только механизм транспортировки веществ, но и их своеобразной сортировки.
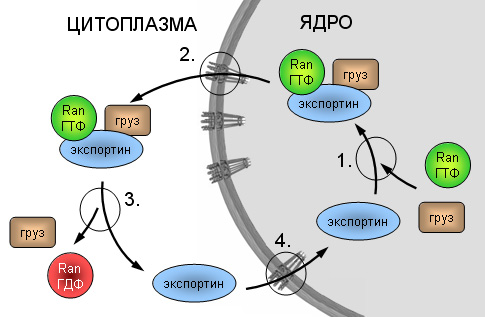
Сигнальные белки отличаются друг от друга. Ввиду этого, существует разница между скоростью перемещения через поры. Также они выполняют функцию источника энергии, так как для перемещения крупных молекул, транспортировка которых не возможна диффузным путем, необходимы дополнительные энергетические затраты.
Первый этап импорта белков заключается в присоединении к импортину (транспортину, обеспечивающему перенос через канал к ядру). Полученное в результате слияния сложное образование проходит через ядерную пору. После этого, с ним связывается другое вещество, за счет которого транспортируемый белок освобождается, а импортин возвращается обратно в цитоплазму. Таким образом, импорт в ядро представляет собой цикличный замкнутый процесс.
Транспорт веществ из ядра через оболочку в цитоплазматическое пространство осуществляется аналогичным образом. Исключением является то, что за перенос вещества-груза отвечают уже сигнальные белки, называемые экспортинами.
На первой стадии процесса белок (в большинстве случаев это молекулы РНК) связываются с экспортином и веществом, отвечающим за высвобождение транспортируемого субстрата. После перехода сквозь оболочку нуклеотид расщепляется, за счет чего переносимый белок высвобождается.
В целом, перенос веществ между ядром и цитоплазмой представляет собой цикличный процесс, осуществляемый за счет белков-транспортинов и веществ, отвечающих за высвобождение груза.
Ядерная оболочка при делении
Большинство клеток-эукариотов размножаются путем непрямого деления, которое называется митозом. Данный процесс предусматривает разделение ядра и других клеточных структур с сохранением одинакового количества хромосом. За счет этого сохраняется генетическая идентичность, полученная в результате деления клеток.

В процессе деления нуклеолемма выполняет еще одну важную функцию. После того как происходит разрушение ядра, внутренняя мембрана не позволяет хромосомам расходится на большие расстояния друг от друга. Хромосомы фиксируются на поверхности мембраны до момента полноценного деления ядер и формирования новой нуклеолеммы.
Ядерная оболочка, несомненно, принимает активное участие в клеточном делении. Процесс состоит из двух последовательных этапов – разрушения и перестройки.
Распад ядерной оболочки происходит в прометафазе. Разрушение мембран происходит стремительно. После распада хромосомы характеризуются хаотичным расположением в области ранее существовавшего ядра. В дальнейшем образуется веретено деления – биполярная структура, между полюсами которой формируются микротрубочки. Веретено обеспечивает деление хромосом и их распределение между двумя дочерними клетками.
Перераспределение хромосом и формирование новых ядерных мембран происходит в период телофазы. Точный механизм восстановления оболочек не известен. Распространенной является теория о том, что слияние частиц разрушенной оболочки происходит под действием везикул – мелких клеточных органелл, функция которых заключается в сборе и хранении питательных веществ.
Также образование новых ядерных мембран связывают с переформировкой эндоплазматического ретикулума. Из разрушенного ЭПР высвобождаются белковые соединения, которые постепенно обволакивают пространство вокруг нового ядра, в результате чего в дальнейшем образуется целостная мембранная поверхность.
Таким образом, нуклеолемма принимает непосредственное участие в процессе деления клетки путем митоза.
Ядерная оболочка – сложный структурный компонент клетки, выполняющий барьерные, защитные, транспортные функции. Полноценное функционирование нуклеолеммы обеспечивается особенностями ее строения, взаимодействием с другими клеточными компонентами и биохимическими процессами, протекающими в них.
plushealth.ru
Ядерная оболочка - это... Что такое Ядерная оболочка?
 Клетки ДНК которых окрашена голубым красителем Хойста. Центральная и правая клетки находятся в интерфазе, поэтому окрашено всё ядро. Клетка слева находится в состоянии митоза (анафаза), поэтому её ядро не видно, а ДНК сконденсирована так, что видны хромосомы.
Клетки ДНК которых окрашена голубым красителем Хойста. Центральная и правая клетки находятся в интерфазе, поэтому окрашено всё ядро. Клетка слева находится в состоянии митоза (анафаза), поэтому её ядро не видно, а ДНК сконденсирована так, что видны хромосомы. Ядро (лат. nucleus), органелла эукариотической клетки, содержащая генетическую информацию в форме молекул ДНК. В ядре происходит репликация — удвоение молекул ДНК, а также транскрипция — синтез молекул РНК на матрице ДНК. В ядре же синтезированные молекулы РНК подвергаются ряду модификаций, после чего выходят в цитоплазму. Сборка рибосом также происходит в ядре, в специальных образованиях, называемых ядрышками.
Тонкая структура клеточного ядра

Схема строения клеточного ядра.
Хроматин
Огромная длина молекул ДНК эукариот предопределила появление специальных механизмов хранения, репликации и реализации генетического материала.
Хроматином называют молекулы хромосомной ДНК в комплексе со специфическими белками, необходимыми для осуществления этих процессов. Основную массу составляют «белки хранения», так называемые гистоны. Из этих белков построены нуклеосомы, структуры на которые намотаны нити молекул ДНК. Нуклеосомы располагаются довольно регулярно, так что образующаяся структура напоминает бусы. Нуклеосома состоит из белков четырех типов: h3A, h3B, h4 и h5. В одну нуклеосому входят по два белка каждого типа — всего восемь белков. Гистон h2, более крупный чем другие гистоны, связывается с ДНК в месте ее входа на нуклеосому. Нуклеосома вместе с h2 называется хроматосомой.
Нить ДНК с нуклеосомами образует нерегулярную соленоид-подобную структуру толщиной около 30 нанометров, так называемую 30 нм фибриллу. Дальнейшая упаковка этой фибриллы может иметь различную плотность. Если хроматин упакован плотно, его называют конденсированным или гетерохроматином, он хорошо видим под микроскопом. ДНК находящаяся в гетерохроматине не транскрибируется, обычно это состояние характерно для незначащих или молчащих участков. В интерфазе гетерохроматин обычно располагается по периферии ядра (пристеночный гетерохроматин). Полная конденсация хромосом происходит перед делением клетки. Если хроматин упакован неплотно, его называют эу- или интерхроматином. Этот вид хроматина гораздо менее плотный при наблюдении под микроскопом и обычно характеризуется наличием транскрипционной активности. Плотность упаковки хроматина во многом определяется модификациями гистонов — ацетилированием и фосфориллированием.
Считается, что в ядре существуют так называемые функциональные домены хроматина(ДНК одного домена содержит приблизительно 30 тысяч пар оснований), то есть каждый участок хромосомы имеет собственную «территорию». К сожалению вопрос пространственного распределения хроматина в ядре изучен пока недостаточно. Известно, что теломерные (концевые) и центромерные (отвечающие за связывание сестринских хроматид в митозе) участки хромосом закреплены на белках ядерной ламины.
Ядерная оболочка, ядерная ламина и ядерные поры
От цитоплазмы ядро отделено ядерной оболочкой, образованной за счёт расширения и слияния друг с другом цистерн эндоплазматической сети таким образом, что у ядра образовались двойные стенки за счёт окружающих его узких компартментов. Полость ядерной оболочки называется люменом или перинуклеарным пространством. Внутренняя поверхность ядерной оболочки подстилается ядерной ламиной, жёсткой белковой структурой, образованной белками-ламинами, к которой прикреплены нити хромосомной ДНК. Ламины прикрепляются к внутренней мембране ядерной оболочки при помощи заякоренных в ней трансмембранных белков — рецепторов ламинов. В некоторых местах внутренняя и внешняя мембраны ядерной оболочки сливаются и образуют так называемые ядерные поры, через которые происходит материальный обмен между ядром и цитоплазмой. Пора не является дыркой в ядре, а имеет сложную структуру, организованную несколькими десятками специализированных белков — нуклеопоринов. Под электронным микроскопом она видна как восемь связанных между собой белковых гранул с внешней и столько же с внутренней стороны ядерной оболочки.

Ядрышко
Ядрышко находится внутри ядра, и не имеет собственной мембранной оболочки, однако хорошо различимо под световым и электронным микроскопом. Основной функцией ядрышка является синтез рибосом. В геноме клетки имеются специльные участки, так называемые ядрышковые организаторы, содержащие гены рибосомной РНК (рРНК), вокруг которых и формируются ядрышки. В ядрышке происходит синтез рРНК РНК полимеразой I, ее созревание, сборка рибосомных субчастиц. В ядрышке локализуются белки, принимающие участие в этих процессах. Некоторые из этих белков имеют специальную последовательность — сигнал ядрышковой локализации (NoLS, от англ. Nucleolus Localization Signal). Следует отметить, самая высокая концентрация белка в клетке наблюдается именно в ядрышке. В этих структурах было локализовано около 600 видов различных белков, причем считается, что лишь небольшая их часть действительно необходима для осуществления ядрышковых функций, а остальные попадают туда неспецифически.
Под электронным микроскопом в ядрышке выделяют несколько субкомпартментов. Так называемые Фибриллярные центры окружены участками плотного фибриллярного компонента, где и происходит синтез рРНК. Снаружи от плотного фибриллярного компонента расположен гранулярный компонент, представляющий собой скопление созревающих рибосомных субчастиц.
Ядерный матрикс
Ядерным матриксом некоторые исследователи называют нерастворимый внутриядерный каркас. Считается, что матрикс построен преимущественно из негистоновых белков, формирущих сложную развлетвленную сеть, сообщающуюся с ядерной ламиной. Возможно, ядерный матрикс принимает участие в формировании функциональных доменов хроматина. В геноме клетки имеются специальные незначащие А-Т-богатые участки прикрепления к ядерному матриксу (англ. S/MAR — Matrix/Scaffold Attachment Regions), служащие, как предполагается, для заякоривания петель хроматина на белках ядерного матрикса. Впрочем, не все исследователи признают существование ядерного матрикса.
 Принципиальная схема реализации генетической информации у про- и эукариот. ПРОКАРИОТЫ. У прокариот синтез белка рибосомой (трансляция) пространственно не отделен от транскрипции и может происходить еще до завершения синтеза мРНК РНК-полимеразой. Прокариотические мРНК часто полицистронные, то есть содержат несколько независимых генов. ЭУКАРИОТЫ. мРНК эукариот синтезируется в виде предшественника, пре-мРНК, претерпевающего затем сложное стадийное созревание - процессинг, включающий присоединение кэп-структуры к 5'-концу молекулы, присоединение нескольких десятков остатков аденина к ее 3'-концу (полиаденилирование), выщепление незначащих участков - интронов и соединение друг с другом значащих участков - экзонов (сплайсинг). При этом соединение экзонов одной и той же пре-мРНК может проходить разными способами, приводя к образованию разных зрелых мРНК, и в конечном итоге разных вариантов белка (альтернативный сплайсинг). Только мРНК, успешно прошедшая процессинг, экспортируется из ядра в цитоплазму и вовлекается в трансляцию.
Принципиальная схема реализации генетической информации у про- и эукариот. ПРОКАРИОТЫ. У прокариот синтез белка рибосомой (трансляция) пространственно не отделен от транскрипции и может происходить еще до завершения синтеза мРНК РНК-полимеразой. Прокариотические мРНК часто полицистронные, то есть содержат несколько независимых генов. ЭУКАРИОТЫ. мРНК эукариот синтезируется в виде предшественника, пре-мРНК, претерпевающего затем сложное стадийное созревание - процессинг, включающий присоединение кэп-структуры к 5'-концу молекулы, присоединение нескольких десятков остатков аденина к ее 3'-концу (полиаденилирование), выщепление незначащих участков - интронов и соединение друг с другом значащих участков - экзонов (сплайсинг). При этом соединение экзонов одной и той же пре-мРНК может проходить разными способами, приводя к образованию разных зрелых мРНК, и в конечном итоге разных вариантов белка (альтернативный сплайсинг). Только мРНК, успешно прошедшая процессинг, экспортируется из ядра в цитоплазму и вовлекается в трансляцию. Эволюционное значение клеточного ядра
Основное функциональное отличие клеток эукариот от клеток прокариот заключается в пространственном разграничении процессов транскрипции (синтеза матричной РНК) и трансляции (синтеза белка рибосомой), что дает в распоряжение эукариотической клетки новые инструменты регуляции биосинтеза и контроля качества мРНК.
В то время, как у прокариот мРНК начинает транслироваться еще до завершения ее синтеза РНК-полимеразой, мРНК эукариот претерпевает значительные модификации (так называемый процессинг), после чего экспортируется через ядерные поры в цитоплазму, и только после этого может вступить в трансляцию. Процессинг мРНК включает несколько элементов.
Из предшественника мРНК (пре-мРНК) в ходе процесса, называемого сплайсингом вырезаются интроны — незначащие участки, а значащие участки — экзоны соединяются друг с другом. Причем экзоны одной и той же пре-мРНК могут быть соединены несколькими разными способами (альтернативный сплайсинг), так что один предшественник может превращаться в зрелые мРНК нескольких разных видов. Таким образом, один ген может кодировать сразу несколько белков.
Кроме того, интрон-экзонная структура генома, практически невозможная у прокариот (т.к. рибосомы смогут транслировать незрелые мРНК), дает эукариотам определенную эволюционную мобильность. Учитывая протяженность интронных участков, рекомбинация между двумя генами зачастую сводится к обмену экзонами. Благодаря тому, что экзоны часто соответствуют функциональным доменам белка, участки получившегося в результате рекомбинации «гибрида», зачастую сохраняют свои функции. В то же время у прокариот рекомбинация между генами невозможна без разрыва в значащей части, что безусловно уменьшает шансы на то, что получившийся белок будет функционален.
Модификациям подвергаются концы молекулы мРНК. К 5' -концу молекулы прикрепляется 7-метилгуанин (так называемый кэп). К 3' -концу нематрично присоединяются несколько десятков остатков аденина (полиаденирование).
Процессинг мРНК тесно сопряжен с синтезом этих молекул и необходим для контроля качества. Непроцессированная или не полностью процессированная мРНК не сможет выйти из ядра в цитоплазму или будет нестабильна и быстро деградирует. У прокариот нет таких механизмов контроля качества, и из-за этого прокариотические мРНК имеют меньший срок жизни - нельзя допустить, чтобы неправильно синтезированная молекула мРНК, если такая появится, транслировалась в течение долгого времени.
Ссылки
Molecular Biology Of The Cell, 4е издание, 2002 г. — учебник по молекулярной биологии на английском языке

Wikimedia Foundation. 2010.
biograf.academic.ru








