Пигменты фотосинтезирующих растений, их физиологическая роль. Фотосинтетические пигменты растений
Биология для студентов - 093. Фотосинтетические пигменты
Фотосинтетические пигменты представлены молекулами, способными поглощать кванты света. Поскольку при этом поглощается свет лишь определенной длины волны, часть световых волн не поглощается, а отражается. В зависимости от спектрального состава отраженного света пигменты приобретают окраску - зеленую, желтую, красную и др. В настоящее время различают три класса фотосинтетических пигментов:
- хлорофиллы,
- каротиноиды,
- фикобилины.
Самым распространенным и наиболее важным фотосинтетическим пигментом является хлорофилл (греч. chloros - зеленоватый, phyllon - лист), который имеется практически у всех фототрофов (фототрофами называются автотрофные организмы, способные к фотосинтезу). Хлорофилл неоднороден, насчитывается свыше десятка зеленых пигментов, отличающихся друг от друга атомными группами, присоединенными к пиррольным структурам порфиринового кольца, а также по некоторым другим характеристикам. Поэтому целесообразно начать с химической характеристики хлорофилла и других фотосинтетических пигментов.
Химически хлорофилл представляет собой сложный эфир дикарбоновой кислоты хлорофиллина с двумя спиртами - фитолом и метанолом. Пространственная структура молекулы определяет свойства хлорофилла. Основой является плоское порфириновое ядро, образованное четырьмя пиррольными кольцами, соединенными между собой метиновыми мостиками, с атомом магния в центре. В порфириновом ядре, кроме собственно пиррола, содержатся также его изомер - пирроленин и продукт неполного восстановления пиррола - пирролин. Поскольку в этих циклических соединениях, помимо атомов углерода, присутствует гетероатом - азот, они называются гетероциклическими. Наличие двойных связей позволяет отнести их к ненасыщенным гетероциклам. Атомы углерода, расположенные в гетероцикле рядом с гетероатомом - азотом, обозначаются как а-атомы, а удаленные от него - d-атомы. Поскольку все связи а-углеродных атомов в молекуле хлорофилла заняты в формировании порфиринового кольца, они не определяют специфику различных видов хлорофилла, эту функцию выполняют d-углеродные атомы. Сами атомы азота взаимодействуют с расположенным в центре ядра атомом металла - магнием (отметим, что у близкого по строению гема, входящего в состав гемоглобина, миоглобина или цитохрома, в центре ядра находится атом железа). Так как в порфириновом ядре имеются многочисленные двойные связи, там присутствуют делокализованные (более подвижные) p-электроны, которых в ядре насчитывается 18.
Фитол относится к дитерпенам, основу которых составляют остатки изопрена.
Такая структура молекулы определяет свойства хлорофилла - гидрофобный фитольный «хвост» надежно удерживает молекулу в гидрофобной части мембраны тилакоида хлоропласта, а гидрофильное порфириновое ядро обращено к строме хлоропласта. При этом само ядро ориентировано параллельно мембране, в которой находится хлорофилл.
Все низшие и высшие растения, а также цианобактерии содержат различные хлорофиллы типа а. У высших растений, зеленых и эвгленовых водорослей имеется хлорофилл b (он образуется из хлорофилла а), который отличается от хлорофилла а присутствием формильной группы -СНО, вместо метильной (-СН3) у третьего атома углерода. Бурые и диатомовые водоросли вместо хлорофилла b содержат хлорофилл с, не имеющий остатка фитола, а красные водоросли - хлорофилл d, который отличается от хлорофилла а тем, что при углеродном атоме 2 порфиринового кольца вместо винильной группы имеется формильный радикал. Хлорофиллы бактерий имеют некоторые специфические особенности и называются бактериохлорофиллами.
Бактериохлорофиллы отличаются от прочих типов хлорофиллов тем, что способны поглощать красный свет гораздо большей длины, чем хлорофиллы растений. Так, бактериохлорофилл зеленых бактерий утилизирует волны длиной 850 нм, бактериохлорофилл а пурпурных бактерий до 900 нм, а бактериохлорофилл b пурпурных бактерий - до 1100 нм. Это обстоятельство позволяет бактериям, особенно пурпурным, активно расти при наличии лишь не видимых человеческим глазом инфракрасных лучей.
Другую обязательную группу фотосинтетических пигментов образуют каротиноиды (лат. carota - морковь). Эти жирорастворимые пигменты имеют различную окраску - от желтой до красной. Они содержатся во всех окрашенных пластидах (хлоропластах и хромопластах) растений. Причем в зеленых частях растений хлорофилл маскирует каротиноиды, делая их незаметными до наступления холодов. Осенью зеленые пигменты разрушаются, и каротиноиды становятся хорошо заметными, определяя окраску осенних листьев. Кроме растений, каротиноиды синтезируют фототрофные бактерии и грибы.
Каротиноиды в растительном организме выполняют ряд функций, среди которых наиболее очевидными являются следующие: участие в фотосинтезе в качестве дополнительных пигментов антенных комплексов. Они способны поглощать свет, не доступный для других пигментов, и передавать его хлорофиллам. Кроме того, каротиноиды ослабляют фотоокисление хлорофилла в присутствии кислорода.
Третьей группой фотосинтетических пигментов являются фикобилины (греч. phykos - водоросль, лат. bilis - желчь), которые присутствуют у некоторых водорослей (красных) и цианобактерий. Отдельными молекулами фикобилины, как правило, не представлены, а образуют комплексы с белками, с которыми они, в отличие от хлорофиллов, связаны прочными ковалентными связями. Комплексы таких пигментов с белками называются фикоби- липротеидами (хромопротеидами).
vseobiology.ru
Фотосинтетические пигменты
У высших растений имеется три группы пигментов: хлорофиллы, каротиноиды и фикобилины.
Основными пигментами, осуществляющими поглощение квантов света в процессе фотосинтеза, являются хлорофиллы, пигменты, содержащие Mg-порфириновый комплекс. Обнаружено несколько форм хлорофиллов, различающихся по химическому строению. Спектр поглощения различных форм хлорофиллов охватывает видимую, ближнюю ультрафиолетовую и ближнюю инфракрасную области спектра (у высших растений от 350 до 700 нм, а у бактерий — от 350 до 900 нм). Хлорофилл а является основным пигментом и характерен для всех организмов, осуществляющих фотосинтез с выделением кислорода (рис 6.5). 
У фотосинтезирующих организмов кроме хлорофилла a имеются хлорофиллы b, с и d, которые расширяют спектр поглощения света.
Рис. 6.5. Строение хлорофилла а
В поглощении световой энергии участвуют каротиноиды (пигменты полиизопреноидной природы) — у фотосинтезирующих эукариот, и фикобилины (пигменты с открытой тетрапиррольной структурой) — у цианобактерий и красных водорослей.
В клетке молекулы хлорофилла вместе с другими пигментами, участвующими в процессах поглощения квантов света и передачи энергии, образуют светособирающие хлорофилл-белковые комплексы (ССК). Молекулы ССК имеют максимум поглощения при разной длине волны и расположены от пигмента с максимумом поглощения при меньшей длине волны к пигменту с большей.
Важнейшим структурно-функциональным звеном фотосинтетического аппарата является фотосистема — совокупность ССК, фотохимического реакционного центра и переносчиков электрона.
В процессе фотосинтеза у растений принимают участие две фотосистемы.
Фотосистема I включает светособирающий комплекс и фотохимический реакционный центр I, в состав которого входит димер хлорофилла, поглощающий свет с длиной волны 700 нм (П700).
Фотосистема II включает светособирающий комплекс и фотохимический реакционный центр II, в состав которого входит димер хлорофилла, поглощающий свет с длиной волны 680 нм (П680).
Свет поглощается двумя фотосистемами раздельно, и нормальное осуществление фотосинтеза требует их одновременного участия.
Световая фаза фотосинтеза
Фотосинтез начинается с поглощения квантов света молекулами хлорофилла и другими связанными с ним пигментами. Энергия поглощенных квантов света стекается от сотен молекул пигментов ССК к молекуле пигмента П700 (Е0 = + 0,43В), которая переходит в возбужденное состояние (Е0 = ‒ 0,80 В) и легко отдает электрон первичному акцептору (фотохимическая реакция). Электрон с первичного акцептора, которым является мономерная форма хлорофилла а, передается на филлохинон (витамин К) – вторичный акцептор и затем на железосерные белки. Следующим переносчиком является железосодержащий белок ферредоксин (Е0 = ‒ 0,43В). Ферредоксин содержит два атома железа в негеминовой форме. От ферредоксина электрон переносится на НАДФ (Е0 = ‒ 0,32В). Этот перенос осуществляется с помощью специфического белка-фермента (ферредоксин-НАДФ-редуктазы), коферментом которого является ФАД.
Последовательность расположения переносчиков определяется величиной окислительно-восстановительного потенциала: электроны спонтанно текут в сторону менее отрицательного окислительно-восстановительного потенциала (рис. 6.6).

Рис 6.6. Электрон-транспортная цепь в мембране тилакоида
Отдав электрон, П700 остается в виде ионизированной молекулы. При этом потенциал П700становится снова + 0,43 В (основное состояние). Благодаря этому он является прекрасным акцептором электронов. Источником электрона, заполняющего эту «дырку», является фотосистема II. Она ответственна за реакции, связанные с разложением воды и выделением кислорода.
В состав реакционного центра фотосистемы II входит хлорофилл а, поглощающий свет с длиной волны 680 нм (П680). Под влиянием поглощенного кванта света возбужденный электрон от П680 (Е0 = ‒ 0,7 В) воспринимается первичным акцептором, которым является молекула феофитина. Затем электрон передается на пластохиноны, переносящие как электроны, так и протоны. От пластохинона электроны поступают на b/f-комплекс и передаются через железосерный белок на цитохром. Цитохром относится к группе цитохромов с (Е0 = +0 ,36 В). Воспринимая электрон, цитохром восстанавливается: Fe3+ + е- —> Fe2+. Следующий переносчик — пластоцианин — это медьсодержащий белок, в котором на каждую молекулу белка приходится два атома меди (Е0 = + 0,37 В), осуществляющих электронный транспорт: Cu2+ + е- —> Сu+. Пластоцианин выполняет роль связующего звена между b/f-комплексом и фотосистемой I. От пластоцианина электрон заполняет электронную «дырку» у П700.
Заполнение электронной вакансии в молекуле П680 происходит за счёт воды. В состав фотосистемы II входит водоокисляющий комплекс, содержащий в активном центре ионы марганца в количестве 4 штук. Для образования одной молекулы кислорода требуется две молекулы воды, дающие 4 электрона. Поэтому процесс проводится в 4 такта и для его полного осуществления требуется 4 кванта света. Водоокисляющий комплекс находится со стороны внутритилакоидного пространства, и полученные 4 протона выбрасываются внутрь тилакоида.
2Мn4+ + 2Н20 —> 2Мn2+ + 4Н+ + 4е- + 02
Таким образом, в результате работы фотосистемы II происходит окисление 2 молекул воды с помощью 4 квантов света с образованием 4 протонов во внутритилакоидном пространстве. Протоны внутрь тилакоида перекачиваются также через b/f-комплекс за счет энергии, которая выделяется в окислительно-восстановительной реакции при транспорте электронов. В результате на мембране тилакоида создается электрохимический потенциал, который является промежуточной формой запасания энергии и используется для синтеза АТФ протонной АТФ-синтазой.
Помимо полного нециклического пути переноса электрона, описанного выше, может протекать и циклический путь. В этом случае ферредоксин вместо НАДФ+ восстанавливает пластохинон, который переносит электрон назад на b/f-комплекс. В результате образуется бóльший протонный градиент и больше АТФ, но не восстанавливается НАДФ+.
Темновая фаза фотосинтеза протекает в строме и не является светозависимой.
С3-фотосинтез (цикл Кальвина, восстановительный пентозофосфатный цикл) состоит из трёх стадий (рис. 6.7):
карбоксилирование;
восстановление;
регенерация акцептора CO2.

Рис. 6.7. Цикл Кальвина
На первой стадии к рибулозо-1,5-бисфосфату присоединяется CO2 под действием фермента рибулозобисфосфаткарбоксилазы.. Этот белок составляет основную фракцию белков хлоропласта и является наиболее распространённым ферментом в природе. В результате образуется промежуточное неустойчивое соединение (С6), распадающееся на две молекулы 3-фосфоглицериновой кислоты (ФГК), которая является первичным продуктом фотосинтеза.
Во второй стадии ФГК фосфорилируется и восстанавливается с образованием глицеральдегид-3-фосфата (ФГА).
В третьей стадии участвуют 5 молекул ФГА, которые через образование 4-, 5-, 6- и 7-углеродных соединений объединяются в 3 молекулы рибулозо-1,5-бисфосфата.
Две молекулы ФГА необходимы для синтеза глюкозы. Таким образом, для синтеза 1 молекулы глюкозы требуется 6 оборотов цикла, 6 CO2, 12 НАДФН∙Н+ и 18 АТФ.
Интенсивность фотосинтеза зависит в первую очередь от интенсивности и спектрального состава света, концентрации СО2 и О2, температуры, водного режима растения, минерального питания и других факторов внешней среды.
studfiles.net
Пигменты фотосинтезирующих растений, их физиологическая роль.
· Хлорофилл – это зелёный пигмент, обуславливающий окраску зелёного цвета растению, при его участии обусловлен процесс фотосинтеза. По химическому строению это Mg-комплекс различных тетрапирролов. Хлорофиллы имеют порфириновое строение, структурно близки к гему.
В пиррольных группировках хлорофилла имеются системы, чередующихся двойных и простых связей. Это и есть хромофорная группа хлорофилла, обуславливающиеся поглощение определённых лучей солнечного спектра и его окраску. D порфировые ядра составляют 10 нм, а длина фитольного остатка 2 нм.
Молекулы хлорофилла полярно, её порфириновое ядро обладает гидрофильными свойствами, а фитольный конец гидрофобными. Это свойство молекулы хлорофилла обуславливают определённое расположение её в мембранах хлоропласта.
Порфириновая часть молекулы связана с белком, а фитольная часть погружена в липидный слой.
Хлорофилл живой интактной клетки обладает способностью к обратимому фотоокислению и фотовосстановлению. Способность к окислительно-восстановительным реакциям связано с наличием в молекуле хлорофилла сопряжённых двойных связей с подвижными п-элктронами и атомами N с неопределёнными электронами.
ФИЗИОЛОГИЧЕСКАЯ РОЛЬ
1) избирательно поглощать энергию света,
2) запасать ее в виде энергии электронного возбуждения,
3) фотохимически преобразовывать энергию возбужденного состояния в химическую энергию первичных фотовосстановленных и фотоокисленных соединений.
· Каротиноиды- этожирорастворимые пигменты желтого, оранжевого, красного цвета — присутствуют в хлоропластах всех растений. Каротиноиды содержатся во всех высших растениях и у многих микроорганизмов. Это самые распространенные пигменты с разнообразными функциями. Каротиноиды имеют максимальное поглощение в фиолетово-синей и синей частях спектра света. Они не способны к флуоресценции в отличие от хлорофилла.
К каротиноидам относятся 3 группы соединения:
- оранжевые, или красные каротины;
- жёлтые ксантофиллы;
- каротиноидные кислоты.
ФИЗИОЛОГИЧЕСКАЯ РОЛЬ
1) Поглощение света в качестве дополнительных пигментов;
2) Защита молекул хлорофилла от необратимого фотоокисления;
3) Тушение активных радикалов;
4) Участвуют в фототропизме, т.к. способствуют направлению роста побега.
· Фикобилины – это красные и синие пигменты, содержащиеся у цианобактерий и некоторых водорослей. Фикобилины состоят из 4-х последовательных пиррольных колец. Фикобилины являются хромофорными группами глобулиновых белков, который называется фикобилинпротеинами. Он делятся на:
-фикоэритрины – белки красного цвета;
-фикоцианин – синеголубые белки;
- алофикоцианин – синие белки.
Все они обладают флуоресценирущей способностью. Фикобилины имею максимальное поглощение в оранжевых, жёлтых и зелёных частях спектра света и позволяют водорослям полнее использовать свет, проникающий в воду.
На глубине 30 м полностью исчезают красные лучи
На глубине 180 м – жёлтые
На глубине 320 м – зелёные
На глубине более 500 м не проникают синие и фиолетовые лучи.
Фикобилины – это дополнительные пигменты примерно 90% энергии света, поглощающего фикобилинами передаётся на хлорофилл.
ФИЗИОЛОГИЧЕСКАЯ РОЛЬ
1) Максимумы поглощения света у фикобилинов находятся между двумя максимумами поглощения у хлорофилла: в оранжевой, желтой и зеленой частях спектр.
2) Фикобилины выполняют у водорослей функции светособирающего комплекса.
3) У растений имеется фикобилин-фитохрм, он не участвет в фотосинтезе, но является фоторецептором красного света и выполняет регуляторную функцию в клетках растений.
Сущность фотофизического этапа. Фотохимический этап. Циклический и нециклический транспорт электронов.
Сущность фотофизического этапа
Фотофизический этап наиболее важный, т.к. осуществляет переход и преобразование энергии одной системы в другую (в живую из неживой).
Фотофизический этап входит в световую фазу фотосинтеза.
Фотофизический этап начинается с поглощения квантов света, электроны атомов входящих в состав пигментов. В первую очередь кванты света будут поглощаться наиболее подвижными электронами в молекуле хлорофилла, т.е. теми, которые слабее удерживаются ядром. Такими подвижными электронами в молекуле хлорофилла являются делокализованные p-электроны двойных связей, орбитали которых обобщены между двумя ядрами и неспаренными электронами атомов N2 и О2 в порфириновом ядре. Именно с этим связано то, что молекулы хлорофилла – две основные линии поглощения (в красной и сине-фиолетовой). Из возбужденного первого синглетного и триплетного состояния, молекула хлорофилла так же может переходить в основное состояние, при этом ее дезактивация (потеря энергии) может проходить:
1) Путем выделения энергии в виде света или тепла
2) Путем переноса энергии на другую молекулу пигмента
3) Путем затрачивания энергии на фотохимические процессы (потеря электрона и присоединение его к акцептору, с образованием АТФ и НАДФН2)
В любом из указанных случаев молекула пигмента дезактивируется и переходит на основной энергетический уровень.
Рассмотрение энергетических сотояний молекулы хлорофилла и различных путей использования энергии электронного возбуждения, указывает, что магнийпорфирин одновременно обладает способностью поглощать и сохранять энергию в виде энергии электронного возбуждения и способностью к окислительно-восстановительным изменениям. Возбужденная молекула хлорофилла – мощный восстановительный агент, играющий решающую роль в образовании высоковосстановленных кофакторов в реакциях фотосинтеза. Хлорофилл имеет две функции: поглощение и передача энергии. Основная часть молекул хлорофилла (свето-собирающий комплекс) только поглощает свет и переносит энергию возбуждения на особые молекулы хлорофилла которые непосредственно учувствуют в фото-химическом процессе. Энергия квантов света улавливается от 200 до 400 молекул антенного хлорофилла свето-собирающего комплекса и как-бы стекается к одной молекуле – ловушке, входящая в реакционный центр.
В улавливании и передачи энергии на молекулу хлорофилла-ловушки могут участвовать не только молекулы хлорофилла но и каратиноиды и фикобилины. Передача энергии между молекулами пигментов идет главным образом резонансным путем без разделения зарядов с большой скоростью, передача энергии происходит от пигментов поглощающих свет с меньшей длинной волны, к пигментам поглощающим свет с большей длинной волны. Потеря энергии приводит к превращению квантов более мелкие с большей длинной волны, поэтому основные формы хлорофилла к которым стекается энергия, является более длинноволновые, обратный перенос энергии невозможен.
Фотофизический этап заключается в том, что кванты света поглощаются и переводят молекулы пигмента в возбужденное состояние, затем эта энергия приносится на хлорофилл-ловушку входящую в реакционный центр, осуществляющий первичные фото-химические реакции – разделение зарядов.
Фотохимический этап
Фото-химически реакции фотосинтеза – это реакции в которых энергия света преобразуется в энергию химических связей в первую очередь в энергию фосфорных связей АТФ. Именно АТФ обеспечивает течение всех процессов, одновременно под действием света происходит разложение воды, образуется восстановленный НАДФ и выделяется О2.
Энергия поглощенных квантов света стекается от сотен молекул пигментов свето-собирающего комплекса к одной молекула-хлорофилла-ловушке отдавая электрон акцептору – окисляется. Электрон поступает в электронно-транспортную цепь, предполагается, что свето-собирающий комплекс состоит из 3-х частей:
· главного антенного компонента
· двух фото фиксирующих систем.
Комплекс антенного хлорофилла погружен в толщу мембраны тилакоидов хлоропластов совокупность антенных молекул пигментов и реакционного центра составляет фотосистему в процессе фотосинтеза принимает участие 2 фотосистемы:
· установленно, что фотосистема 1 включает светофокусирующие пигменты и реакционный центр 1,
· фотосистема 2 включает светофокусирующие пигменты и реакционный центр 2.
Хлорофилл-ловушка фотосистемы 1 поглощает свет с длинной волны700нм. Во второй системе 680нм. Свет поглащается рздельно этими двумя фотосистемами и нормальное осуществление фотосинтеза требует их одновременного участия. Перенос по цепи переносчиков включает ряд окислительно-восстновительных реакций при которых происходит перенос либо атома водорода, либо электронов.
Различают два типа потока электронов:
· циклический
· нециклический.
При циклическом потоке электроны от молекулы хлорофилла передаются к акцептору от молекулы хлорофилла и возвращаются к ней обратно, при нециклическом потоке происходит фотоокисление воды и передача электрона от воды к НАДФ, выделяемая в ходе окислительно-восстановительных реакций энергия частично используется на синтез АТФ. 


Фотосистема I
Светособирающий комплекс I содержит примерно 200 молекул хлорофилла.
В реакционном центре первой фотосистемы находится димер хлорофилла a с максимумом поглощения при 700 нм (П700). После возбуждения квантом света он восстанавливает первичный акцептор — хлорофилл a, тот — вторичный (витамин K1 или филлохинон), после чего электрон передаётся на ферредоксин, который и восстанавливает НАДФ с помощью фермента ферредоксин-НАДФ-редуктазы.
Белок пластоцианин, восстановленный в b6f комплексе, транспортируется к реакционному центру первой фотосистемы со стороны внутритилакоидного пространства и передаёт электрон на окисленный П700.
Фотосистема II
Фотосистема — совокупность ССК, фотохимического реакционного центра и переносчиков электрона. Светособирающий комплекс II содержит 200 молекул хлорофилла a, 100 молекул хлорофилла b, 50 молекул каротиноидов и 2 молекулы феофитина. Реакционный центр фотосистемы II представляет собой пигмент-белковый комплекс, расположенный в тилакоидных мембранах и окружённый ССК. В нём находится димер хлорофилла a с максимумом поглощения при 680 нм (П680). На него в конечном счёте передаётся энергия кванта света из ССК, в результате чего один из электронов переходит на более высокое энергетическое состояние, связь его с ядром ослабляется и возбуждённая молекула П680 становится сильным восстановителем (E0=-0,7 В).
П680 восстанавливает феофитин, в дальнейшем электрон переносится на хиноны, входящие в состав ФС II и далее на пластохиноны, транспортируемые в восстановленной форме к b6f комплексу. Одна молекула пластохинона переносит 2 электрона и 2 протона, которые берутся из стромы.
Заполнение электронной вакансии в молекуле П680 происходит за счёт воды. В состав ФС II входит водоокисляющий комплекс, содержащий в активном центре ионы марганца в количестве 4 штук. Для образования одной молекулы кислорода требуется две молекулы воды, дающие 4 электрона. Поэтому процесс проводится в 4 такта и для его полного осуществления требуется 4 кванта света. Комплекс находится со стороны внутритилакоидного пространства и полученные 4 протона выбрасываются в него.
Таким образом, суммарный результат работы ФС II — это окисление 2 молекул воды с помощью 4 квантов света с образованием 4 протонов во внутритилакоидном пространстве и 2 восстановленных пластохинонов в мембране.
Фотосинтетическое фосфорилирование. Механизм сопряжения электронного транспорта с формированием трансмембранного градиента электрохимического потенциала. Структурно-функциональная организация и механизм работы АТФ-синтетазного комплекса.
Фотосинтетическое фосфорилирование - синтез АТФ из АДФ и неорганического фосфора в хлоропластах, сопряженный с транспортом электронов, индуцируемым светом.
Соответственно двум типам потока электронов различают циклическое и нециклическое фотофосфорилирование.
Перенос электронов по цепи циклического потока сопряжен с синтезом двух макроэргичесих связей АТФ. Вся энергия света, поглощенная пигментом реакционного центра фотосистемы I, расходуется только на синтез АТФ. При циклическом Ф. ф. не образуются восстановительные эквиваленты для углеродного цикла и не выделяется O2. Циклическое Ф. ф. описывается уравнением:

Нециклическое Ф. ф. сопряжено с потоком электронов от воды через переносчики фотосистем I и II НАДФ +. Энергия света в этом процессе запасается в макроэргических связях АТФ, восстановленной форме НАДФН2 и молекулярном кислороде. Суммарное уравнение нециклического Ф. ф. следующее:

__________________________________________________________________________
Механизм сопряжения электронного транспорта с формированием трансмембранного градиента электрохимического потенциала
Хемиосмотическая теория. Переносчики электронов локализованы в мембранах асимметрично. При этом последовательно чередуются переносчики электронов (цитохромы) с переносчиками электрона и протона (пластохиноны). Молекула пластохинона сначала принимает два электрона: ПХ + 2е- —> ПХ-2.
Пластохинон — производное хинона, в полностью окисленном состоянии содержит два атома кислорода, соединенных с углеродным кольцом двойными связями. В полностью восстановленном состоянии атомы кислорода в бензольном кольце соединяются с протонами: с образованием электрически нейтральной формы: ПХ-2 + 2Н+ -> ПХН2. Протоны выделяются в пространство внутри тилакоида. Таким образом, при переносе пары электронов от Хл680 на Хл700 во внутреннем пространстве тилакоидов накапливаются протоны. В результате активного переноса протонов из стромы во внутритилакоидное пространство на мембране создается электрохимический потенциал водорода (ΔμН+), имеющий две составляющие: химическую ΔμН (концентрационную), возникающую в результате неравномерного распределения ионов Н+ по разным сторонам мембраны, и электрическую, обусловленную противоположным зарядом разных сторон мембраны (благодаря накоплению протонов с внутренней стороны мембраны).
__________________________________________________________________________
Структурно-функциональная организация и механизм работы АТФ-синтетазного комплекса
Структурно-функциональная организация. Сопряжение диффузии протонов через мембрану осуществляется макромолекулярным ферментным комплексом, называемым АТФ-синтазой или сопрягающим фактором. Этот комплекс по форме напоминает гриб и состоит из двух частей — факторов сопряжения: круглой шляпки F1, выступающей с наружной стороны мембраны (в ней располагается каталитический центр фермента), и ножки погруженной в мембрану. Мембранная часть состоит из полипептидных субъединиц и формирует в мембране протонный канал, по которому ионы водорода попадают к фактору сопряжения F1. Белок F1 представляет белковый комплекс, который состоит из мембраны, при этом он сохраняет способность катализировать гидролиз АТФ. Изолированный F1 не способен синтезировать АТФ. Способность синтезировать АТФ — это свойство единого комплекса F0—F1, встроенного в мембрану. Связано это с тем, что работа АТФ-синтазы при синтезе АТФ сопряжена с переносом через нее протонов. Направленный транспорт протонов возможен только в том случае, если АТФ-синтаза встроена в мембрану.
Механизм работы. Существуют две гипотезы относительно механизма фосфорилирования (прямой механизм и косвенный). Согласно первой гипотезе фосфатная группа и АДФ связываются с ферментом в активном участке комплекса F1. Два протона перемещаются через канал по градиенту концентрации и соединяются с кислородом фосфата, образуя воду. Согласно второй гипотезе, (косвенный механизм), АДФ и неорганический фосфор соединяются в активном центре фермента спонтанно. Однако образовавшаяся АТФ прочно связана с ферментом, и для ее освобождения требуется энергия. Энергия доставляется протонами, которые, связываясь с ферментом, изменяют его конформацию, после чего АТФ высвобождается.
infopedia.su
Пигменты фотосинтезирующих растений - Справочник химика 21
Условием осуществления фотосинтеза является локализация необходимых пигментных, окислительно-восстановительных и ферментных систем в специальных органоидах фотосинтезирующих клеток. В случае растений и водорослей — это хлоропласты, в случае бактерий — хроматофоры. В них, наряду с фотосинтезом, происходит также синтез белков, нуклеиновых кислот, липидов, пигментов и других физиологически активных веществ фотосинтезирующие органоиды обладают известной автономностью в клетке. [c.7] У всех фотосинтезирующих организмов, включая высшие растения, фотосинтез протекает в мембранных структурах. У пурпурных бактерий поглощающие свет пигменты (бактериальные хлорофиллы и каротины) встроены в мембраны, которые представляют собой складки наружной клеточной мембраны. Эти участки имеют характерную структуру и называются хроматофорами. Они состоят из соединяющихся между собой полых пузырьков, параллельно расположенных трубочек или параллельных пластинок (ламелл) диаметр всей структуры — 50—100 нм. У зеленых бактерий пигменты выстилают внутриклеточные пузырьки. В настоящее время фотосинтезирующие бактерии обитают только в серных источниках и глубоких озерах, но когда-то они были, вероятно, распространены гораздо более широко и являлись единственными фотосинтезирующими организмами на Земле. [c.25]Биосинтез начинается с фотосинтеза [1]. Вся жизнь на Земле зависит от способности некоторых организмов (зеленых растений, водорослей и фотосинтезирующих бактерий), содержащих характерные фотосинтезирующие пигменты, использовать энергию солнечной радиации для синтеза органических молекул из неорганических веществ — диоксида углерода, азота и серы. Продукты фотосинтеза служат затем не только исходными веществами, но и источником химической энергии для всех последующих биосинтетических реакций. Обычно принято описывать фотосинтез только как процесс образования углеводов в некоторых случаях основными продуктами фотосинтеза, действительно, являются исключительно крахмал, целлюлоза и сахароза, однако в других организмах на синтез углеводов идет, быть может, всего лишь третья часть углерода, связываемого и восстанавливаемого в процессе фотосинтеза. При ближайшем рассмотрении оказывается, что нельзя провести четкую границу между образованием продуктов фотосинтеза и другими биосинтетическими реакциями в клетке, в которых могут участвовать промежуточные вещества фотосинтетического цикла восстановления углерода. [c.396]
ПИГМЕНТЫ ФОТОСИНТЕЗИРУЮЩИХ РАСТЕНИИ [c.108]
Важнейшие представители пигментов фотосинтезирующих растений [c.109]
Пигментная система фотосинтезирующих растений — сложная смесь, анализ которой представляет немало трудностей. Экстрагирование разрушает химические единицы, содержащие пигменты пластид в естественном состоянии, разбавляет их пигментами вакуолей и клеточных стенок, не имеющими отношения к фотосинтезу, и приводит их в соприкосновение с клеточными компонентами последние могут оказывать химическое действие на пигменты (например кислоты и энзимы). Разделение экстрагированной смеси на ее компоненты легко может повести к дальнейшей деструкции при соприкосновении с воздухом, растворителем или адсорбентом. Полное разделение затрудняется еще и тем, что смесь пигментов содержит изомеры или другие компоненты, мало отличающиеся друг от друга по растворимости и химическим свойствам. [c.401]
Энергия падающего света поглощается фотосинтезирующими пигментами в органеллах, называемых фоторецепторами (хлоропласты в высших растениях, пластиды в водорослях, хроматофоры в фотосинтезирующих бактериях). Преобладающим пигментом является хлорофилл любой организм, способный осуществлять фотосинтез, содержит по меньшей мере одну разновидность хлоро- [c.396]
В высших растениях фотосинтез протекает наиболее эффективно при поглощении света хлорофиллом а. Роль хлорофилла Ь, каротиноидов и других сопутствующих пигментов не вполне ясна. Хлорофилл а представляет собой единственный пигмент, общий для всех фотосинтезирующих организмов. Поэтому предполагают, что только хлорофилл а способен быть донором энергии непосредственно для фотосинтетической реакции, а все другие пигменты передают поглощенную ими энергию хлорофиллу а. Эта гипотеза согласуется со спектром действия для фотосинтеза и с наблюдением, что сопутствующие пигменты могут сенсибилизировать флуоресценцию [c.258]
ХЛОРОФИЛЛЫ = пигменты фотосинтезирующих растений, являющиеся сенсибилизаторами фотосинтеза (см. Красящие вещества природные, Пигменты биологические, Сенсибилизирующие красители, Фотосинтез). Энергия света, поглощенного X., превращается ими в химич. энергию окислительно-восстановительных реакций, к-рые приводят в движение сложный механизм фотосинтеза растений. Исключительная роль X. в фотосинтезе, являющемся одним пз наиболее важных ироцессов, происходящих на Земле, объясняет интерес, проявляе.мый к изучению X. [c.360]
Наряду с хлорофиллами в комплекс пигментов фотосинтезирующих растений входят каротиноиды и фикобилины. [c.115]
I%I К,френч, 1962). У многих фотосинтезирующих растений установлено наличие пигмента с максимумом поглощения при 700-705 нм ( Кок 956, 1961 Кок, 1962). [c.88]
Во всех фотосинтезирующих растениях обнаружен хлорофилл а, содержание которого превьщ1ает содержание других пигментов. Он является самым важным пигментом, так как образует реакционные центры, участвующие в световой фазе фотосинтеза. Другие формы хлорофиллов, а также каротиноиды рассматриваются как вспомогательные, или сопутствующие, пигменты. Функция каротиноидов не ограничивается ролью светособирающих пигментов. Оки также защищают ткани от окисления кислородом на свету. [c.531]
Самым важным фотосинтетическим пигментом у всех растений является хлорофилл а (Хл а) в бактериях ему соответствует бактериохлорофилл (БХл). Кроме того, фотосинтезирующий аппарат всех клеток содержит ряд пигментов, обычно называемых дополнительными или вспомогательными. Нам теперь ясно, что функции этих компонентов не менее существенны, чем функция обычного хлорофилла а. У всех зеленых растений, включая водоросли, к такого рода пигментам относится также особая форма хлорофилла а (поглощающая в более коротковолновой области спектра) и хлорофилл Ъ. Ряд других вспомогательных пигментов указан в табл. 37. Среди них особенно важную роль играют каротиноиды и фикобилины (фикоцианин и фикоэритрин). На фиг. 93 показано строение некоторых фотосинтетических пигментов. [c.320]
В ранний период истории Земли в восстановленной атмосфере каротиноиды служили в качестве светособирающих пигментов, но постепенно эта функция теряла значение, и по мере изменения свойств атмосферы и эволюции фотосинтезирующих растений фотопротекторная функция каротиноидов стала более значимой, [c.171]
Пигмент, который участвует в фотоокислении воды и показан на схеме, еще не идентифицирован. Арнон считает, что этот пигмент скорее относится к хлорофиллу или добавочным пигментам, находящимся только в высших растениях и водорослях, и не может быть хлорофиллом а, находящимся во всех фотосинтезирующих клетках. [c.332]
Свет, поглощаемый хлорофиллом в листьях растений, используется для фотосинтеза органических веществ из простых неорганических соединений это положение, установленное в работах К. А. Тимирязева, определяет роль хлорофилла как оптического и химического сенсибилизатора процесса. У фотосинтезирующих бактерий ту же роль, что и хлорофилл зеленых растений, выполняет бактериохлорофилл—пигмент, обладающий главным максимумом поглощения в близкой инфракрасной области спектра. [c.92]
Хлорофилл, как известно, принимает непосредственное химическое участие в процессе фотосинтеза, являясь одним из звеньев "в цепи окислительно-восстановительных реакций, приводящих к отнятию водорода от воды и присоединению его к СО2. Роль бактериохлорофилла у фотосинтезирующих бактерий, очевидно, такая же, как хлорофилла а У растений. Эти пигменты в растворе способны также сенсибилизировать реакпию фотохимического переноса водорода, как и хлорофилл (Красновский, Войновская,1951 Красновский, Пакшна, 1959). [c.147]
Зеленые пигменты растений — хлорофиллы, сенсибилизирующие процессы фотосинтеза, — также являются производными порфина, в Которых атомы азота пиррольных групп связаны с магнием. Существуют несколько форм хлорофиллов, различающихся между собой ТОЛЬКО некоторыми радикалами, замещающими водородные атомы в Р-положении пиррольных колец. Основным компонентом фотохимической системы высших растений и водорослей является хлорофилла. В высших растениях и зеленых водорослях содержится и второй фотохимический компонент — хлорофилл Ь, г в бурых и диатомовых водорослях — хлорофилл с, в красных водорослях — хлорофилл й. В фотосинтезирующих бактериях, в синезеленых водорослях и-в других организмах содержатся другие разновидности хлорофиллов и родственных им систем. [c.507]
ХЛОРОФИЛЛЫ м мн. Органические производные порфи-риновых комплексов магния являются пигментами фотосинтезирующих растений, водорослей и бактерий поглощают энергию солнечного света и трансформируют её в ходе синтеза органических соединений в энергию химических связей. [c.483]
Из высших растений, водорослей и фотосинтезирующих бактерий вьщелено и структурно охарактеризовано св. 50 разл. X. Осн. пигменты высших растений и зеленых водорослей - X. а ч Ь. Основа этих X.- ди-гидропорфириновый (хлориновый) цикл, содержащий в качестве эфирных фупп (У) остаток спирта фи-тола (СНз)2СН(СН2)зСН(СНз)(СН2)зСН(СНз)(СН2)зС(СНз) = = СНСНзОН. [c.291]
Зеленые ткани растений своей окраской обязаны фотосинтетическому пигменту хлорофиллу, который в высоких концентрациях содержится в хлоропла-стах. Поглощение света хлорофиллом запускает в хлоропластах процессы переноса электронов, которые сопряжены с переносом протонов через мембраны тилакоидов и, как следствие, с запасанием энергии в биологически полезной форме (в виде молекул АТР) и восстановительных эквивалентов (в виде NADPH). Полученные таким путем АТР и ШОРН в свою очередь используются хлоропластами для превращения СО2 в сахара (см. гл. 9). При этом синтетическая активность хлоропластов такова, что позволяет фотосинтезирующим тканям экспортировать большие количества органических веществ во все остальные части растения. Эти вещества в основном представлены дисахаридом сахарозой, поэтому жидкость, заполняющая ситовидные трубки (флоэмный сок) содержит обычно от 10 до 25% сахарозы [c.178]
Светочувствительные пигменты фотосинтезирующих организмов подразделяются на три класса зеленые липофильные хлорофиллы, желтые липофильные каротиноиды и синие и красные водорастворимые фикобилины. В свою очередь, каротиноиды подразделяются на две подгруппы полиеновые углеводороды, или каротины, и кислородсодержащие пигменты, называемые ксантофиллами (или фитоксантинами ). В хлоропластах авто-трофных растений, принадлежащих к разным таксономическим группам, могут содержаться от одного до нескольких хлорофиллов и от одного до трех каротинов и несколько ксантофиллов. Фикобилиновые пигменты встречаются в форме белковых комплексов, называемых билипротеинами, наряду с хлорофиллами и каротиноидами в красных и сине-зеленых морских водорослях. [c.267]
Фотосинтез зеленых растений протекает в две стадии первая из них объединяет световые реакции, идущие только тогда, когда растение освещено, а вторая-тел новые реакции, которые могут происходить как в темноте, так и на свету. В световых реакциях энергия света поглощается хлорофиллом и другими пигментами фотосинтезирующих клеток и запасается в химической форме в виде двух высокоэнергетических продуктов-АТР и NADPH одновременно выделяется кислород. В темновых реакциях АТР и NADPH, образовавпшеся в световых реакциях, используются для восстановления двуокиси углерода до глюкозы и других органических продуктов (рис. 23-5). Образование кислорода, про- [c.687]
Фотосинтезирующие растения содержат кроме хлорофиллов так называемые дополнительные, вспомогательные, или сопрововдающие пигменты. К ним относятся гсаротиноиды и содержащиеся у некоторых групп водорослей фикобилины. Вопрос о том какова роль этих пигментов в процессе фотосинтеза, участвует ли поглощаемая ими световая энергия в построении органического вещества долгое время оставался неясным. В последние годы изучению роли этих пигментов уделено оольшое внимание и появилось много нового в выяснении их роли в процессе фотосинтеза. [c.136]
Все фотосинтезирующие организмы содержат один или несколько органических пигментов, способных поглощать видимый свет, запуская тем цамым фотохимические реакции фотосинтеза. Из большинства листьев эти пигменты можно экстрагировать спиртом или другими органическими растворителями. Выделить индивидуальные пигменты из спиртового экстракта можно методом хроматографии на колонке с сахарной пудрой. Впервые это сделал русский ботаник М. С. Цвет в 1906 г. В растениях и водорослях встречаются пигменты трех основных классов — хлорофиллы, каротиноиды и фикобилины. Хлорофиллы и каротиноиды нерастворимы в воде, а фикобилины растворимы. Каротиноиды и фикобилины называют вспомогательными, или сопровождающими, пигментами, поскольку энергия квантов света, поглощенных этими пигментами, может передаваться на хлоро-4 илл. В табл. 3.1 приведены характеристики поглощения света этими пигментами. Пигменты фотосинтезирующих бактерий описаны в гл. 7. [c.41]
В фотосинтезирующих клетках активные пигменты расположены внутри ламеллярных мембран в виде функционально-организованных единиц. У фотосинтезирующих эукариот (высших растений и большинства водорослей) несущие пигмент мембраны заключены в специфических органеллах — хлоропластах. У высших растений морфологические различия между хлоропластами невелики, в то время как у водорослей форма и размеры хлоропластов значительно варьируют. hlorella, например, имеет единственный чашевидный хлоропласт, тогда как хлоропласты некоторых видов Spirogyra представляют собой длинные, спирально закрученные образования, лежащие вдоль всей клетки. [c.329]
Фотосинтез — образование зелеными растениями, а также фотосинтезирующими микроорганизмами органических веществ клеток из неорганических при участии и за счет энергии солнечного света. Фотосинтез протекаёт с участием поглощающих сеет пигментов, прежде всего хлорофилла. Первыми стабильными продуктами фотосинтеза являются НАД(ф)Н и АТФ. Далее они используются при ассимиляции СО2 и в других биосинтетических процессах. У вьюших растений донором электронов является нр. При этом фотосинтез сопровождается выделением О2. Суммарный процесс фотосинтеза выражается уравнением [c.333]
Пурпурные серобактерии являются, подобно зеленым растениям, фотосинтезирующими организмами. В клетках этих бактерий содержится особый пигмент — бактериопурвурин, позволяющий использовать солнечную энергию. Эти бактерии могут развиваться в условиях анаэробиоза и окисляют сероводород путем взаимодействия его с углекислотой [c.148]
Светочувствительные пигменты входят в состав фотосинтети-ческого аппарата высших растений, водорослей и фотосинтезирующих бактерий. В эукариотических клетках пигменты находятся в окрашенных пластидах — хлоропластах, у сине-зеленых водорослей — в тилакоидных структурах, у фотосинтезирующих бактерий — в специализированных органеллах мезосомах. Кроме того, эти пигменты встречаются в других структурах, не имеющих отношения к фотосинтезу, например в хромопластах и их предшественниках (этиопластах). [c.267]
Многие жизненно важные природные соединения содержат фрагменты из четырех связанных вместе пиррольных колец, которые иногда могут быть в восстановленной форме. Такие тетрапиррольные фрагменты встречаются в переносящих кислород белках (например, в гемоглобине), в цитохромах (белках, отвечающих за транспорт. электрона в цепи дыхания), в хлорофиллах и бактериохлорофиллах (молекулах, непосредственно участвующих в процессах фотосинтеза в растениях и фотосинтезирующих бактериях), в витамине В12 (витамине, препятствующем возникновению злокачественного малокровия), в-пигментах желчи и в некоторых токсинах морских организмов. На рис. 13.1 в качестве примеров приведены некоторые важные природные тетрапиррольные соединения, а также пример фталоцианина. Фталоцианины не являются природными тетра-пиррольными соединениями они синтезируются в большом масштабе и используются как красители. [c.285]
С водорослями и высшими растениями цианобактерии имеют то общее, что все они осуществляют фотосинтез с выделением кислорода и содержат хлорофилл а, а также ряд других общих с растениями пигментов. Поэтому их и отнесли к водорослям под названием сине-зеленых водорослей. Но уже Ф. Кон, учитывая способ их деления, назвал их S hizophy eae и объединил со S hizomy etes (бактериями сведя в группу высшего порядка S hizophyta. Действительно, если судить по строению клетки, наличию муреиновой клеточной стенки 70 S-рибосомам и другим определяющим признакам, приходится отнести их к грам-отрицательным прокариотам. Цианобактерии-самая обширная, наиболее богатая формами и самая распространенная группа фотосинтезирующих прокариот. Благодаря способности расти в экстремальных условиях и фиксировать молекулярный азот они приобрели большое значение в сложном хозяйстве природы. [c.127]
Вследствие тесной связи, существующей между флуоресценцией и сенсибилизацией (см. т. I, гл. ХУШ и XIX, и т. II, гл. XXIII), исследование флуоресценции хлорофилла в живых растениях может привести к значительным успехам в понимании механизма фотока-талитического действия этого пигмента в фотосинтезе. Флуоресценция является таким свойством хлорофилла, которое может наблюдаться (и уже наблюдалось) одновременно с измерениями фотосинтетической активности. Измеряя выход флуоресценции, можно получить представление об обмене энергии и процессах рассеяния энергии в фотосинтезирующих клетках, без нарушения их жизненных процессов. До сих пор еще никем не изучались изменения, происходящие в спектре флуоресценции (или в спектре поглощения) хлорофилла во время фотосинтеза однако в будущем такого рода исследования могут также оказаться выполнимыми и весьма плодотворными. [c.216]
Хлорофилл а присутствует в хлоропластах или аналогичных структурах у всех фотосинтезирующих организмов. (Исключение составляют фотосинтезирующие бактерии, содержащие бак-териохлорофилл а). Помимо него, всегда имеются также и другие пигменты, у разных организмов различные. Высшие растения и зеленые водоросли содержат хлорофилл Ь, у которого к 3-му атому углерода вместо группы —СНз, имеющейся у хло- [c.20]
К сожалению, в настоящее время отсутствуют какие-либо определенные данные о структуре и организации реакционного центра в фотосинтезирующих системах высших растений и водорослей. Считается, что пигмент П700 представляет собой либо агрегат двух или нескольких молекул хлорофилла а или же агрегат пигмента с белком с сильным межмолекулярным взаимодействием. [c.24]
Итак, мы имеем здесь дело с фотосинтезом без углекислоты Микроскопические исследования представили другие важные данные. В фотосинтезирующих клетках почти всех растений хлорофилл и сопутствующие ему пигменты содержатся в микроскопических тельцах, так называемых хлоропластах. При более детальном изучении было обнаружено, что в хлоропластах пигменты в свою очередь скапливаются в виде мелких зернышек — гранул, почти не различимых в обычный микроскоп, но прекрасно видимых в электронном микроскопе. Анализ взвесей Хилла показал, что содержащиеся в них частицы — это целые или разрушенные хлоропласты или же отдельные гранулы. Таким образом, гранулы являются теми кирпичиками в ферментной системе фотосинтеза, которые обеспечивают высвобождение кислорода из воды на свету, но которые не содержат ферментов, необходимых для поглощения и восстановления углекислоты. Так бьша доказана пространственная раз- [c.52]
Высоконенасыщенные тетратерпены, обнаруженные в высших растениях, грибах, фотосинтезирующих бактериях и водорослях, обычно входят в состав сложных смесей фотосинтезирующих лигментов. Эти так называемые Пигменты хлоропластов представляют собой интенсивно окрашенные соединения, что и послужило главной причиной их выбора в качестве объектов на которых впервые был продемонстрирован принцип хроматографического разделения Фракционирование терпенов этой группы проводилось на самых разнообразных сорбентах, в том числе и таких достаточно распространенных, как силикагель, оксид алюминия, карбонаты цинка и кальция, оксид магния, гидроксид кальция, целлюлоза и сахароза. Элюентами обычно слуЯсили смеси углеводородов, содержащие более полярный растворитель, -например диэтиловый эфир, ацетон, метанол или пропанол. [c.248]
Все фотосинтезирующие организмы содержат хлорофиллы — зеленые магнийпорфириновые пигменты. Известно свыше 10 видов, различающихся природой химических групп, присоединенных к пиррольным структурам порфиринового ядра, окраской, распространением среди живых организмов. У всех зеленых растений содержатся хлорофиллы а и Ь, в диатомовых водорослях — хлорофилл с, в красных водорослях — хлорофилл с1. Все хлорофиллы являются фоторецепторами, так как интенсивно поглощают видимый свет (в спектрах поглощения имеются четыре полосы — три в красно-желтой и одна в синей области). Функции реакционных (фотохимических) центров выполняют особые формы хлорофилла а пигмент Рудр, поглощающий свет с длиной волны около 700 нм, и пигмент Р зд, поглощающий свет с длиной волны 680 нм. На долю этих фотохимически активных форм хлорофилла приходится 1/400 часть общего количества хлорофилла в клетке. [c.195]
chem21.info
Основные фотосинтетические пигменты, спектры поглощения, функции и химическая природа.
Пигменты – это вещества, избирательно поглощающие свет в видимой части спектра. При освещении белым светом их цвет определяется только лучами, которые они отражают или пропускают. Способность пигментов поглощать свет, связано с наличием в их молекулах правильно чередующихся двойных и одинарных связей. Это так называемые сопряженные или коньюгированные связи. Между двумя атомами, связанными двойными связями, находится 4 электрона. Когда система состоит из сопряженных связей, то половина этих электронов может свободно перемещаться вдоль этой системы. Поглотив квант света, такой электрон может оторваться от молекулы пигмента, т. е. становится донором электронов для восстановления веществ. Сейчас известно, что высшие растения содержат две формы зеленых пигментов: хлорофиллы а и b и две формы желтых пигментов (каротиноиды): каротины и ксантофиллы, а так же фикобилины. Главную роль в фотосинтезе играет хлорофилл а. Суммарный химический состав молекулы хлорофилла можно выразить следующей формулой: хлорофилл а С55Н72О5N4Mg, хлорофилл b С55Н70О6 N4Mg. Указанные хлорофиллы отличаются одним атомом кислорода и двумя водорода, а по цвету хлорофилл а – сине-зеленый; b – желто-зеленый. По химической природе хлорофилл а представляет собой сложный эфир дикарбоновой кислоты хлорофиллина, в одном карбоксиле которой водород замещен остатком метанола, а в другом – фитола. Хлорофилл а – самый важный из фотосинтетических пигментов, он присутствует во всех фотосинтезирующих растениях. Существуют и другие формы хлорофиллов (b, с1, с2 и d), которые называются вспомогательными. Каротиноиды – жирорастворимые пигменты желтого, оранжевого и красного цветов. Они входят в состав хлоропластов и хромопластов незеленых частей растений (цветов, плодов, корнеплодов). В зеленых листьях их окраска маскируется хлорофиллом. Каротиноиды являются тетратерпеноидами (8 остатков изопрена) и содержат 40 атомов углерода. Они представляют собой цепи, которые имеют, как и хлорофилл, двойные сопряженные связи. На одном или двух концах цепи находятся иононовые кольца. Каротиноиды делят на две группы: каротины и ксантофиллы. Каротины, например α-каротин (С40Н56) представляет собой чистые углеводороды (тетратерпены). тогда как ксантофиллы: лютеин С40Н56О2 и виолоксантин С40Н56О4 являются окисленными соединениями. Каротины имеют оранжевую или красную окраску, а ксантофиллы – желтую. α-Каротин имеет одно β-иононовое кольцо (двойные связи между С5 и С6), а второе – ε-иононовое (двойные связи между С4 и С5). β-Каротин отличается от α- тем, что имеет два β-иононовых кольца. Относительная распространенность хлорофилла и каротиноидов в высших растениях составляет 4,5:1 (квантосомы содержат 230 молекул хлорофилла и 50 молекул каротиноидов). Интересно отметить, что животные обычно не синтезируют каротиноидов. Поэтому желтая и розовая расцветка птиц (например, канареек, фламинго), так же как и многочисленных беспозвоночных, обусловлена каротиноидами, которые они получают, поедая растения. К пигментам, которые участвуют в световой стадии фотосинтеза, относятся и фикобилины. Все фотосинтетические пигменты (хлорофиллы, каротиноиды и фикобилины) входят в состав пигментных систем в виде хромпротеинов, т. е. пигмент – белковых комплексов. Хлорофиллы и каротиноиды связаны с белками относительно слабо, связь между пигментом и белком не ковалентная. Поскольку такие связи легко нарушаются хлорофиллы и каротиноиды можно экстрагировать с помощью органических растворителей таких как ацетон, спирт. Фикобилины связаны с белком ковалентно, поэтому они находятся в виде молекул – фикобилипротеинов. Фикобилипротеины растворимы в воде и легко вымываются из мацерированных тканей водой или разбавленными растворами солей. Однако, для разрушения молекулы фикобилипротеинов путем расщепления связи между пигментом и белком необходим гидролиз в жестких условиях. По структуре фикобилины – тоже тетрапироллы, но с открытой цепью, которые имеют систему коньюгированных двойных и одинарных связей. Каротиноиды и фикобилины, как и хлорофиллы b, с1, с2 и d, называют вспомогательными или сопутствующими пигментами. Спектр поглощения. Все пигменты поглощают свет избирательно. Так, если пропустить белый свет через раствор хлорофилла, а затем разложить с помощью призмы, то увидим, что отдельные участки спектра будут сильно поглощаться, и на их месте увидим черные полосы. Другие участки спектра будут проходить через раствор хлорофилла в ослабленном виде. . Небольшая разница в строении молекулы хлорофиллов а и b обуславливает некоторую разницу в поглощении ими света. Хлорофилл а более полно поглощает свет с длиною волны 670, 680, 700 и 435 нм, а хлорофилл b – 650 и 480 нм. С наименьшим поглощением проходят через раствор хлорофилла или лист зеленые лучи и часть красных. У хлорофилла b полоса поглощения в красной части спектра смещена в сторону коротковолновых лучей, а в сине-фиолетовой – в сторону длинноволновых. Изучение спектров поглощения показало, что хлорофилл а в живом листе образует 8–10 форм, которые химически одинаковы, но отличаются по поглощению света. Такой результат обусловлен несколькими причинами. Во-первых, молекулы хлорофилла могут взаимодействовать между собой (агрегированная форма). Во-вторых, они взаимодействуют с компонентами мембран хлоропластов, в частности с белком. И, в третьих, это связано с динамическим состоянием молекул хлорофилла в тилакоидах. Хлорофилл беспрерывно разрушается под действием света (фотодесктрукция). На смену разрушенным молекулам в мембраны тилакоидов встраиваются новые.
23. Строение хлорофилла, образование системы двойных связей и свободных π-электронов.
Хлорофиллы. Хлорофилл является сложным органическим веществом. Одной из главных трудностей для выявления точного химического состава хлорофилла является его полная нерастворимость в воде и легкая изменчивость под воздействием солей, кислот и щелочей. Суммарный химический состав молекулы хлорофилла можно выразить следующей формулой: хлорофилл а С55Н72О5N4Mg, хлорофилл b С55Н70О6 N4Mg. Указанные хлорофиллы отличаются одним атомом кислорода и двумя водорода, а по цвету хлорофилл а – сине-зеленый; b – желто-зеленый. По химической природе хлорофилл а представляет собой сложный эфир дикарбоновой кислоты хлорофиллина, в одном карбоксиле которой водород замещен остатком метанола, а в другом – фитола. В основе молекулы лежит порфирин, который состоит из четырех пирольных колец (пронумерованы римскими цифрами), соединенных метиновыми мостиками (–СН=). В центре порфиринового ядра находится атом Mg, связанный с N. Таким образом, хлорофилл относится к Mg-порфиринам. Порфирины входят также в состав гема крови и являются важным компонентом систем, принимающих участие в дыхании; в этом случае вместо магния они содержат железо. Кроме пирольных в состав молекулы хлорофилла входит циклопентановое кольцо (V), которое содержит высокоактивную кетогруппу и участвует в окислении воды. Хлорофилл b отличается от хлорофилла а тем, что ко второму пирольному кольцу присоединена не метильная, а альдегидная группа. Четыре пирольных кольца и метиновые мостики образуют двойные связи. Между двумя атомами, связанными двойными атомами, находится 4 электрона. Когда система состоит из двойных связей, то половина этих π-электронов, как отмечалось, может свободно перемещаться вдоль системы. Молекулу хлорофилла делят на две части: порфириновое ядро и фитольный хвост. Фитольный хвост в два раза длиннее ядра. Порфириновое ядро благодаря наличию атомов кислорода и азота гидрофильно. Фитольный хвост – это углеводородная, а это значит гидрофобная часть молекулы хлорофилла. Поэтому порфириновое ядро размещается в гидрофильной части мембраны тилакоида, а фитольный хвост в гидрофобной. Имея разные свойства, две части молекулы хлорофилла выполняют разную функцию: порфириновое ядро содержащее коньюгированные связи, поглощает свет, а фитольный хвост играет роль якоря, который удерживает молекулу хлорофилла в определенной части мембраны тилакоида. Доказать, что свет поглощается порфириновым ядром молекулы хлорофилла, можно с помощью реакции хлорофилла со щелочью, в результате которой образуются два спирта (метанол и фитол) и соль хлорофилла. Щелочь отсекает от молекулы хлорофилла фитольный хвост, в результате образованная соль теряет способность растворяться в бензине, но сохраняет зеленый цвет хлорофилла. Следовательно, растворимость пигмента в бензине, его гидрофобность обусловлена остатком фитола, а поглощение света связано с порфириновым ядром. Атом магния также влияет на поглощение света молекулой хлорофилла. Если с помощью кислоты заместить магний на водород, то образовавшееся вещество – феофитин – принимает красно-бурый цвет вместо зеленого. В природных условиях образование феофитина происходит осенью, при старении листьев, под воздействием неблагоприятных факторов. В результате листья желтеют. При влиянии различных факторов происходит увеличение проницаемости мембран, и кислый вакуолярный сок, проникая в хлоропласты, преобразует хлорофилл в феофитин. Поскольку избирательная проницаемость мембран нарушается под воздействием разных факторов, то листья желтеют под воздействием низких и высоких температур, дефиците воды и ее избытке и т. д. Хлорофилл а – самый важный из фотосинтетических пигментов, он присутствует во всех фотосинтезирующих растениях. Существуют и другие формы хлорофиллов (b, с1, с2 и d), которые называются вспомогательными.
cyberpedia.su
Пигменты листа
Для того чтобы свет мог оказывать влияние на растительный организм и, в частности, быть использованным в процессе фотосинтеза, необходимо его поглощение фоторецепторами-пигментами. Пигменты — вещества, имеющие окраску. Видимая часть спектра представлена длинами воли от 400 до 800 им. Органические вещества, поглощающие свет с длиной волны менее 400 им, кажутся бесцветными.
Хлорофиллы
Выделенное из листьев зеленое вещество назвали хлорофиллом (от греч. «хлорос» — зеленый и «филлон» — лист). В настоящее время известно около 10 хлорофиллов. Они отличаются по химическому строению, окраске, распространению среди живых организмов. У всех высших зеленых растений содержатся хлорофиллы а и b. Хлорофилл с содержится в диатомовых водорослях, хлорофилл d — в красных водорослях. Кроме того, известны четыре бактериохлорофилла (а, b, сиd), содержащиеся в клетках фотосинтезирующих бактерий., В клетках зеленых бактерий содержатся бактериохлорофиллы с и d. В клетках пурпурных бактерий — бактериохлорофиллы а и b. Основными пигментами, без которых фотосинтез не идет, являются хлорофилл а для зеленых растений и бактериохлорофилл для бактерий. Впервые точное представление о пигментах зеленого листа было получено благодаря работам крупнейшего русского ботаника М. С. Цвета. Он выделил пигменты листа в чистом виде и разработал новый хроматографический метод разделения веществ. Хлорофиллы а и Ъ различаются по цвету. Хлорофилл а имеет сине-зеленый оттенок, а хлорофилл Ъ — желто-зеленый. Содержание хлорофилла а в листе примерно в три раза больше по сравнению с хлорофиллом Ъ.
Химические свойства хлорофилла
По химическому строению хлорофилл — это сложный эфир дикарбоновой органической кислоты — хлорофиллина и двух остатков спиртов — фитола и метилового. Хлорофиллин представляет собой азотсодержащее металлорганическое соединение, относящееся к магний-порфиринам. В центре молекулы хлорофилла расположен атом магния, который соединен с четырьмя азотами пиррольных группировок. В пиррольных группировках хлорофилла имеется система чередующихся двойных и простых связей. Это и есть хромофорная группа хлорофилла, обусловливающая его окраску.
Расстояние между атомами азота пиррольных группировок в ядре хлорофилла составляет 0,25 нм. Интересно, что диаметр атома магния равен 0,24 нм. Таким образом, магний почти полностью заполняет пространство между атомами азота пиррольных группировок. Это придает ядру молекулы хлорофилла дополнительную прочность. Еще К. А. Тимирязев обратил внимание на близость химического строения двух важнейших пигментов: зеленого — хлорофилла листьев и красного — гемина крови. Действительно, если хлорофилл относится к магний-порфиринам, то гемин — к железопорфиринам. Сходство это не случайно и служит еще одним доказательством единства всего органического мира.
Одной из специфических черт строения хлорофилла является наличие в его молекуле, помимо четырех гетероциклов, еще одной циклической группировки из пяти углеродных атомов — циклопентанона. В циклопептанонном кольце содержится кетогруппа, обладающая большой реакционной способностью. Есть данные, что в результате процесса эполизации по месту этой кетогруппы к молекуле хлорофилла присоединяется вода.
Извлеченный из листа хлорофилл легко реагирует как с кислотами, так и со щелочами. При взаимодействии со щелочью происходит омыление хлорофилла, в результате чего образуются два спирта и щелочная соль хлорофиллина. В интактном живом листе от хлорофилла может отщепляться фитол под воздействием фермента хлорофиллазы. При взаимодействии со слабой кислотой извлеченный хлорофилл теряет зеленый цвет, образуется соединение феофитин, у которого атом магния в центре молекулы замещен на два атома водорода.
Хлорофилл в живой интактной клетке обладает способностью к обратимому окислению и восстановлению. Способность к окислительно-восстановительным реакциям связана с наличием в молекуле хло рофилла сопряженных двойных связей. Эти связи фиксированы не прочно, и при их перемещении азот пиррольных ядер может окисляться (отдавать электрон) или присоединять электрон (восстанавливаться).
Молекула хлорофилла полярна, ее порфириновое ядро обладает гидрофильными свойствами, а фитольный конец — гидрофобными. Это свойство молекулы хлорофилла обусловливает определенное расположение ее в мембранах хлоропластов. Исследования показали, что свойства хлорофилла, находящегося в листе и извлеченного из листа, различны, так как в листе он находится в комплексном соединении с белком подобно гемоглобину крови. Это доказывается следующими данными: 1. Спектр поглощения хлорофилла, находящегося в листе, иной по сравнению с извлеченным хлорофиллом. 2. Хлорофилл невозможно извлечь абсолютным спиртом из сухих листьев. Экстракция протекает успешно, только если листья увлажнить или к спирту добавить воды. 3. Выделенный из листа хлорофилл легко подвергается разрушению под влиянием самых разнообразных воздействий (повышенная кислотность, кислород и даже свет). Между тем в листе хлорофилл достаточно устойчив ко всем перечисленным факторам. Следует заметить, что связь между хлорофиллом и белком несколько иного характера, чем между гемином и белком. Установлено, что для гемоглобина характерно постоянное соотношение — на 1 молекулу белка приходится 4 молекулы гемина. Между тем соотношение между хлорофиллом и белком различно (от 3 до 10 молекул хлорофилла на 1 молекулу белка). Это соотношение претерпевает изменения в зависимости от типа растений, фазы их развития, условий среды. Связь между молекулами белка и хлорофиллом осуществляется путем нестойких комплексов, образующихся при взаимодействии кислых групп белковых молекул и азота пиррольных колец. Чем выше содержание дикарбоновых аминокислот в белке, тем лучше идет их комплексирование с хлорофиллом. Блокирование карбоксильных групп в белке сильно уменьшает его способность к связыванию с хлорофиллом. Белки, связанные с хлорофиллом, характеризуются низкой изоэлектрической точкой (3,7—4,9). Молекулярная масса этих белков порядка 68 тыс.
Важным свойством молекул хлорофилла является их способность к взаимодействию друг с другом. В результате этого происходит их переход из мономерной в агрегированную форму, которая может возникнуть в результате взаимодействия двух и более молекул при их близком расположении друг к другу. В процессе образования хлорофилла его состояние в живой клетке закономерно меняется. При этом и происходит его агрегация.
studfiles.net
РАЗДЕЛ I. ПИГМЕНТЫ ФОТОСИНТЕТИЧЕСКОГО АППАРАТА — МегаЛекции
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
Нижегородский государственный университет им. Н.И. Лобачевского
Биологический факультет
Кафедра биохимии и физиологии растений
Ю.В. Синицына
Л.Н. Олюнина
Е.О. Половинкина
Фотосинтез и дыхание растений
Учебно-методическое пособие
Рекомендовано методической комиссией биологического факультета для студентов ННГУ, обучающихся по направлениям подготовки 020200 «Биология» и 020800 «Экология и природопользование» и специальностям 020201 «Биология», 020801 «Экология» и 020207 «Биофизика»
Нижний Новгород
УДК 581.1
ББК Е573
В-57
В-57 Синицына Ю.В., Олюнина Л.Н., Половинкина Е.О. ФОТОСИНТЕЗ И ДЫХАНИЕ РАСТЕНИЙ: Учебно-методическое пособие. – Нижний Новгород: Нижегородский госуниверситет, 2008. – 28с.
Рецензент: доц., канд. биол. наук О.В. Орлова
Учебно-методическое пособие включает описание лабораторных работ по разделам «Фотосинтез» и «Дыхание» курса «Физиология растений». Работы, предлагаемые в разделе I характеризуют основные химические и оптические свойства пигментов и их разделение с помощью тонкослойной хроматографии на пластинках силуфола, что является иллюстрацией раздела соответствующего теоретического курса. В работах, представленных в разделе II, описаны методы определения интенсивности фотосинтеза. Работы, приведенные в разделе III, характеризуют работу ферментов дыхания, а также знакомят с методами анализа интенсивности дыхания. Приводятся методические указания по выполнению работ, перечислены необходимые материалы и оборудование.
Учебно-методическое пособие предназначено для студентов-биологов университетов, а также педагогических и сельскохозяйственных ВУЗов, может быть использовано учителями школ при проведении лабораторных занятий, демонстрации опытов на уроках.
УДК 581.1
ББК Е573
© Нижегородский государственный
Университет им. Н.И. Лобачевского, 2008
СОДЕРЖАНИЕ
РАЗДЕЛ I. ПИГМЕНТЫ ФОТОСИНТЕТИЧЕСКОГО АППАРАТА…………..4
Работа 1. Получение спиртовой вытяжки пигментов и
изучение их химических и оптических свойств…………………….…5
Работа 2. Разделение смеси пигментов с помощью
бумажной хроматографии……………………………………………….8
Работа 3. Сравнение качественного состава пигментов
высших растений разных систематических групп…………………..…9
Работа 4. Определение содержания основных пигментов
фотосинтетического аппарата в листьях высших растений…………..10
РАЗДЕЛ II. ОСНОВНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ ИНТЕНСИВНОСТИ
ФОТОСИНТЕЗА……………………………………………………….13
Работа 5. Определение интенсивности фотосинтеза
высшего водного растения по выделению кислорода………………...13
Работа 6. Обнаружение фотосинтеза методом
крахмальной пробы (по Саксу)…………………………………………14
Работа 7. Определение интенсивности фотосинтеза по поглощению
углекислого газа (по Л.А. Иванову и Л.Н. Коссович)…………….…..15
РАЗДЕЛ III. ДЫХАНИЕ РАСТЕНИЙ…………………………………………….17
Работа 8. Определение интенсивности дыхания по количеству выделенного
диоксида углерода (по Бойсен-Йенсену)………………………….......17
Работа 9. Обнаружение активности ферментов дыхания………………………..20
Работа 10. Определение интенсивности дыхания растений по поглощению
кислорода манометрическим методом Варбурга………………...... ...23
СПИСОК ЛИТЕРАТУРЫ………………………………………………………….27
РАЗДЕЛ I. ПИГМЕНТЫ ФОТОСИНТЕТИЧЕСКОГО АППАРАТА
Пигменты растений – это различные вещества, имеющие окраску и способные к избирательному поглощению части солнечного спектра в области 300–800 нм. К числу пигментов относят разнообразные соединения, участвующие не только в фотохимических, но и энзиматических реакциях, например, флавины, разнообразные хиноны – коферменты биокаталитических систем, близкие к ним цитохромы.
Пигменты фотохимических реакций делят на две группы:
1. Тетрапирролы:
а) хлорофиллы – Mg-порфирины, в основе химического строения которых лежит порфириновое кольцо;
б) фикобилины – тетрапирролы с незамкнутой системой;
2. Полиизопрены – каротиноиды.
Особенно важное значение в реакциях фотосинтеза принадлежит хлорофиллам. Сегодня известно более 10 пигментов, входящих в группу хлорофиллов и различающихся между собой некоторыми структурными особенностями.
Основные хлорофиллы «а» и «b» характерны для высших растений и водорослей, «с» – для бурых и диатомовый водорослей, «а» и «d» – для красных водорослей, бактериохлорофилл – для фотосинтетических бактерий, осуществляющих фоторедукцию.
В основе структуры хлорофилла лежит порфирин – полярная часть молекулы, и фитольный «хвост» (остаток одноатомного непредельного спирта фитола) – гидрофобная часть, заякоривающая молекулу хлорофилла в липидном бислое мембраны тилакоида.
В порфирине выделяют 3 структурных элемента:
1. сопряженная система двойных и одинарных (конъюгированных) связей, обеспечивающая поглощение света;
2. Mg, определяющий физические и химические свойства хлорофилла, способный изменять спектральные и конформационные характеристики молекулы, обеспечивающий связь хлорофилла с белком и пигмент-пигментные взаимодействия;
3. циклопентановое кольцо, содержащее кетогруппу – эта полярная группировка обеспечивает связь хлорофилла с молекулой воды и гидрофильность всей порфириновой структуры.
Фитол (C20h49OH) не участвует в поглощении энергии света, но ориентирует молекулу хлорофилла в структуре хлоропласта.
Хлорофиллы выполняют следующие функции:
а) поглощение энергии света в красной и сине-фиолетовой частях спектра;
б) запасание энергии;
в) преобразование ее в реакционных центрах.
Остальные группы пигментов являются дополнительными (вспомогательными).
Фикобилины – пигменты водорослей, главными из которых являются фикоэритрин и фикоцианин. Они способны активно поглощать энергию света в зеленой части спектра, т.е. области между двумя максимумами поглощения хлорофиллов.
Фикобилины являются хромофорными группами фикобилипротеинов – глобулиновых белков, с которыми, в отличие от хлорофиллов, они связаны прочными ковалентными связями и не способны преобразовывать энергию.
Водорастворимые фикобилипротеины локализованы в клетках водорослей в специальных гранулах – фикобилисомах.
Каротиноиды – жирорастворимые пигменты желтого, оранжевого и красного цвета – присутствуют в хлоропластах всех растений.
Все каротиноиды – полиеновые соединения, состоящие из восьми остатков изопрена, которые образуют цепь конъюгированных связей. Каротиноиды могут быть нециклическими (алифатическими), моно- и бициклическими. Циклы на концах молекул каротиноидов являются производными ионона.
С точки зрения фотосинтеза интересны:
каротины – неполярные соединения;
ксантофиллы – кислородсодержащие производные каротинов.
Каротины локализованы в липидной фракции мембраны, ксантофиллы имеют в своем составе кислород и более полярны. Как и хлорофиллы, каротиноиды нековалентно связаны с белками и липидами мембран.
Каротиноиды выполняют следующие функции:
1. дополнительное поглощение энергии света;
2. защита хлорофилла от фотоокисления;
3. ксантофиллы участвуют в формировании молекулярного кислорода.
Работа 1. Получение спиртовой вытяжки пигментов и изучение их химических и оптических свойств.
Объектом исследования служат листья и зеленые проростки растений различных систематических групп.
Получают спиртовую вытяжку пигментов и исследуют их основные химические свойства.
Ход определения.
Мелко нарезанные листья или проростки (3 – 4г) растирают с СаСО3 и 15 – 20 мл этанола. Вытяжку фильтруют в сухую колбочку через бумажный фильтр. Вытяжка представляет собой смесь пигментов – хлорофиллов “a” и “b”, каротинов, ксантофиллов. Полученную вытяжку используют при исследовании химических свойств пигментов.
А. Разделение пигментов по Краусу.
Метод основан на различной растворимости пигментов в спирте и гептане (бензине). Эти растворители при сливании не смешиваются и образуют две фазы: верхнюю – гептановую (бензиновую), нижнюю – спиртовую, поэтому и происходит разделение компонентов смеси.
Ход определения.
В пробирку наливают 2 – 3 мл спиртовой вытяжки и добавляют 3 – 4 мл гептана (бензина). Содержимое пробирки встряхивают и дают отстояться. При этом происходит разделение слоев:
верхний – зеленый гептановый (бензиновый) слой содержит хлорофиллы
“a” и “b” и каротин;
нижний – желтый спиртовой содержит ксантофиллы.
Б. Омыление хлорофилла щелочью.
Молекула хлорофилла представляет собой эфир двухосновной хлорофиллиновой кислоты с двумя спиртами – фитолом и метанолом. При реакции со щелочью хлорофилл омыляется, давая соответствующие соли и спирты:

 COOCh4 COONa
COOCh4 COONa


 С32h40ON4Mg + 2NaOH C32h40ON4Mg +
С32h40ON4Mg + 2NaOH C32h40ON4Mg +
COOC20h49 COONa
+ Ch4OH + C20h49OH
Образующаяся при этом соль хлорофиллиновой кислоты сохраняет зеленую окраску и оптические свойства хлорофилла.
Ход определения.
В пробирку со спиртовой вытяжкой пигментов приливают 2 – 3 капли 20% раствора КОН или NаОН. Пробирку встряхивают и дают отстояться, затем добавляют равный объем гептана (бензина). При этом происходит разделение слоев:
верхний – желтый гептановый (бензиновый) из-за присутствия каротина;
нижний – зеленый спиртовой, т.к. в нем растворяются продукты омыления хлорофиллов – их щелочные соли. Здесь же находится и ксантофилл.
В. Получение феофитина и обратное замещение водорода на атом металла.
Атом Mg в молекуле хлорофилла легко замещается двумя атомами водорода при воздействии сильных кислот. Это приводит к образованию феофитина бурого цвета:

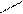 COOCh4 COOCh4
COOCh4 COOCh4
 C32h40ON4Mg + 2HCl C32h42ON4 +MgCl2
C32h40ON4Mg + 2HCl C32h42ON4 +MgCl2

 COOC20h49 COOC20h49
COOC20h49 COOC20h49
Если на феофитин подействовать солями Cu, Zn, Pb, то вместо двух атомов водорода в ядро хлорофилла входит соответствующий металл, и вновь восстанавливается зеленая окраска:

 COOCh4 COOCh4
COOCh4 COOCh4

 C32h42ON4 + Cu(Ch4COO)2 C32h40ON4Cu +
C32h42ON4 + Cu(Ch4COO)2 C32h40ON4Cu +
 COOC20h49 COOC20h49
COOC20h49 COOC20h49
+ 2Ch4COOH
Ход определения.
В две пробирки берут 2 – 3 мл спиртовой вытяжки пигментов и прибавляют 2 – 3 капли 10% HCl. При взбалтывании зеленая окраска хлорофилла переходит в бурую, характерную для феофитина. Далее одну пробирку с феофитином оставляют для контроля, а во вторую вносят несколько кристаллов уксуснокислой меди, раствор нагревают на водяной бане. После нагревания бурый цвет раствора меняется на зеленый вследствие образования хлорофиллоподобного производного меди.
Реактивы и оборудование.
1. CaCO3 сухой,
2. Этанол,
3. Гептан (бензин),
4. 20% NaOH,
5. 10% HCl,
6. Cu(Ch4COO)2 сухой,
7. Ступки,
8. Колбы конические 50 мл,
9. Воронки,
10. Фильтры,
11. Пробирки на 10 мл,
12. Пипетки на 5 и 1 мл,
13. Ланцеты,
14. Водяная баня (кипящая).
Работа 2. Разделение смеси пигментов с помощью бумажной хроматографии.
Хроматографический метод разделения пигментов, впервые предложенный русским ученым М.С. Цветом, заключается в том, что раствор, содержащий смесь пигментов, пропускают через слой адсорбента. Различные пигменты, обладая неодинаковой растворимостью в данном растворителе и разной адсорбируемостью, передвигаются по мере движения растворителя с различной скоростью и располагаются на адсорбенте в разных местах. Чем выше растворимость пигмента в растворителе, тем быстрее он будет передвигаться, и тем дальше от старта будет располагаться зона этого пигмента.
Ход работы.
Измельченные свежие листья помещают в ступку, добавляют немного CaCO3 для нейтрализации органических кислот клеточного сока, а также кварцевого песка или толченого стекла и растирают, постепенно приливая ацетон (на 2 – 3 г листьев примерно 25 мл ацетона). Полученный раствор фильтруют в сухую чистую колбу.
Наливают вытяжку в бюкс и погружают в нее кончик полоски из хроматографической бумаги (3´20 см). Через несколько секунд, когда вытяжка поднимется по бумаге на 1 – 1.5 см, высушивают бумагу на воздухе и снова погружают в раствор пигментов на несколько секунд. Эту операцию повторяют 5–7 раз до тех пор, пока у верхней границы распространения пигментов на бумаге не образуется темно-зеленая полоска. После этого погружают кончик бумажной полоски в ацетон, чтобы все пигменты поднялись на 1 – 1.5 см.
Высушив полоску до полного исчезновения запаха ацетона, ее помещают в вертикальном положении в хроматографическую камеру (цилиндр, на дно которого налита смесь растворителей бензин : бензол в отношении 1:2) и плотно закрывают крышкой.
Через 10 – 15 мин растворитель поднимается по бумаге на 10 – 12 см, при этом пигменты располагаются в виде полос в следующем порядке:
 каротины (поднимаются с фронтом (растворителя)
каротины (поднимаются с фронтом (растворителя)
 ксантофиллы
ксантофиллы
 хл. а
хл. а
 хл. b
хл. b
Рис.1. Распределение пигментов на бумаге.
Вклеивают полученную хроматограмму в отчет, подписывают пигменты и делают вывод о причинах разделения пигментов на бумаге.
Реактивы и оборудование.
1. Ацетоновая вытяжка пигментов,
2. Бензин (гептан),
3. Бензол,
4. Хроматографическая бумага,
5. Хроматографическая камера,
6. Пинцет.
Работа 3. Сравнение качественного состава пигментов высших растений разных систематических групп.
Объектами сравнения служат листья высших растений различных систематических групп. Смесь пигментов разделяют при помощи различных видов хроматографии – например, на бумаге или на пластинках силуфола.
Ход работы.
Разделение пигментов производят на пластинках силуфола (UV-254, Чехословакия) размером 3´15 см. Силуфол– это пластинки для тонкослойной хроматографии на алюминиевой фольге. В качестве сорбента используют силикагель, связывающим веществом является крахмал.
На пластинки силуфола с помощью микропипетки наносят спиртовую вытяжку пигментов полоской 1.5 см на расстоянии 2 см от нижнего края пластинки. Полоску подсушивают струей воздуха (вентилятор), а затем помещают в хроматографическую камеру, предварительно насыщенную смесью растворителей следующего состава:
гептан : ацетон : эфир : гексан
10 : 10 : 3 : 10
На одну пластинку наносят вытяжку пигментов высших растений разных систематических групп. Разгонку пигментов производят в камере с плотно закрытой крышкой и затемненной темной бумагой. Фронт растворителя поднимается вверх до 2 см от верхнего края пластинки. Хроматограмму вынимают и высушивают в токе воздуха.
Полученную хроматограмму вклеивают в отчет с помощью прозрачного скотча, расшифровывают (рис.2) и подписывают.
/\/\/\/\/\/\/\/\ Каротины
/\/\/\/\/\/\/\/\ Феофитин
/\/\/\/\/\/\/\/\ Артероксантин
/\/\/\/\/\/\/\/\ Хл. а
/\/\/\/\/\/\/\/\ Хл. b
/\/\/\/\/\/\/\/\ Лютеин + зеаксантин
/\/\/\/\/\/\/\/\ Виолаксантин
/\/\/\/\/\/\/\/\ Неоксантин
 Старт
Старт
Рис.2. Распределение пигментов на силуфоле.
Реактивы и оборудование.
1. Спиртовая вытяжка пигментов
2. Растворитель (гептан : ацетон : эфир : гексан – 10 : 10 : 3 : 10)
3. Пластинки силуфола
4. Микропипетки
5. Вентиллятор
6. Хроматографическая камера.
Работа 4. Определение содержания основных пигментов фотосинтетического аппарата в листьях высших растений.
Объектом определения служат листья высших растений разных видов или листья разного возраста. Содержание хлорофиллов “a” и “b” определяют спектрофотометрически, рассчитывают соотношение хл. а / хл.b в исследуемом материале.
Работа проводят в два этапа:
- экстракция пигментов;
- определение их концентрации с помощью спектрофотометра или ФЭКа
(фотоэлектроколориметра).
Пигменты могут быть экстрагированы из свежего или фиксированного материала с помощью смеси полярных (спирт, ацетон) и неполярных (эфир, гексан, бензин) растворителей. Полярные растворители расщепляют связь между пигментом и белком и переводят все пигменты в раствор. Поскольку пигменты быстро выцветают на свету, экстрагировать их лучше в затемненном помещении.
Количественное определение пигментов основано на использовании их оптических свойств. В зависимости от природы растворителя для расчетов используют следующие формулы:
а) в 80%-ном ацетоне:
Ca = 12.7´D663 – 2.58´D644 (мг/л)
Cb = 22.9´D644 – 4.66´ D663 (мг/л)
б) в серном эфире:
Ca = 9.93´D660 – 0.78´D642 (мг/л)
Cb = 17.6´D642 – 2.81´D660 (мг/л), где
Сa, Cb – концентрация хлорофилла а, хлорофилла b, соответственно,
D663, D644, … - оптическая плотность раствора при указанной длине волны
Возможно определение концентрации пигментов по заранее построенным калибровочным кривым.
Ход определения.
Навеску растительного материала (500 мг) растирают в присутствии CaCO3 с 4 – 5 мл 80%-ного ацетона. Полученную вытяжку фильтруют в сухую колбочку. Операцию повторяют несколько раз, пока стекающая жидкость не будет прозрачной. Вытяжку помещают в мерную колбу на 25 мл и доводят объем растворителем. Полученная вытяжка содержит сумму зеленых и желтых пигментов.
Концентрацию хлорофилла определяют с помощью ФЭКа. Используя красный светофильтр (650 нм) и кюветы шириной 10 мм, определяют оптическую плотность раствора относительно чистого растворителя (ацетона). Для предотвращения испарения ацетона кюветы лучше закрыть крышечками. Результаты получаются надежными при показаниях ФЭКа от 0.1 до 0.4. Если оптическая плотность выше 0.5, то вытяжку следует разбавить. Если же показания ФЭКа меньше 0.08, работу следует повторить с самого начала, взяв большую навеску.
Измерения повторяют несколько раз, а из полученных отсчетов берут среднее арифметическое, затем определяют концентрацию хлорофилла в вытяжке по калибровочному графику (рис.3).
Содержание хлорофилла в листьях пересчитывают на 1 г сырого веса листьев. Для этого полученное по графику значение умножают на объем вытяжки – находят количество мг хлорофилла в суммарной вытяжке. Эта вытяжка была получена из 500мг сырого веса листьев, следовательно, для расчета на 1 г сырого веса, полученный результат следует умножить на 2.
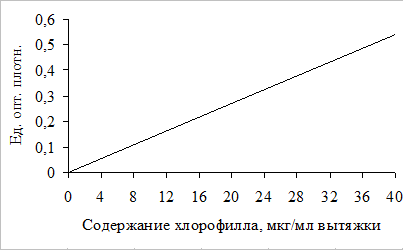 |
Рис.3. Оптическая плотность ацетоновой вытяжки хлорофилла.
Реактивы и оборудование.
1. СаСО3 сухой
2. 80% ацетон
3. Колбы 50 мл
4. Мерные колбы на 25 мл
5. Ступки
6. Ножницы
7. ФЭК, спектрофотометр
8. Кюветы шириной 10 мм
9. Бумажные фильтры
megalektsii.ru











