Содержание
Онлайн урок: Химический состав растений по предмету Биология 6 класс
Lorem ipsum dolor sit amet, consectetur adipisicing elit. Adipisci autem beatae consectetur corporis
dolores ea, eius, esse id illo inventore iste mollitia nemo nesciunt nisi obcaecati optio similique tempore
voluptate!
Adipisci alias assumenda consequatur cupiditate, ex id minima quam rem sint vitae? Animi dolores earum
enim
fugit magni nihil odit provident quaerat. Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Эта информация доступна зарегистрированным пользователям
Растения, как и все живые организмы на нашей планете, состоят в основном из кислорода, углерода, водорода и азота, из которых состоят органические молекулы.
Кроме этих элементов, в их состав входит также фосфор, сера, магний, хлор и, конечно же, натрий и кальций.
Lorem ipsum dolor sit amet, consectetur adipisicing elit. Adipisci autem beatae consectetur corporis
Adipisci autem beatae consectetur corporis
dolores ea, eius, esse id illo inventore iste mollitia nemo nesciunt nisi obcaecati optio similique tempore
voluptate!
Adipisci alias assumenda consequatur cupiditate, ex id minima quam rem sint vitae? Animi dolores earum
enim
fugit magni nihil odit provident quaerat. Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Эта информация доступна зарегистрированным пользователям
Интересно, что некоторые растения способны накапливать разные химические элементы.
Например, вы слышали наверняка от родителей, что нужно есть морскую капусту (научное название ее — ламинария), потому что в ней содержится йод.
Lorem ipsum dolor sit amet, consectetur adipisicing elit. Adipisci autem beatae consectetur corporis
dolores ea, eius, esse id illo inventore iste mollitia nemo nesciunt nisi obcaecati optio similique tempore
voluptate!
Adipisci alias assumenda consequatur cupiditate, ex id minima quam rem sint vitae? Animi dolores earum
enim
fugit magni nihil odit provident quaerat.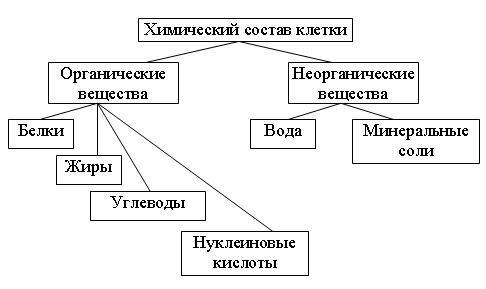 Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Эта информация доступна зарегистрированным пользователям
А вы знаете, что открыть йод ученым помог… котик?
Да, именно обычный домашний кот химика Бернарда Куртуа, который скинул пробирки с реактивами со стола на пол.
Другие водоросли, микроскопические, получившие название «диатомовые», содержат кремний.
Причем этот элемент составляет основную массу водоросли.
Из диоксида кремния (кремнезема) у диатомовых водорослей состоит панцирь, как у черепахи.
Lorem ipsum dolor sit amet, consectetur adipisicing elit. Adipisci autem beatae consectetur corporis
dolores ea, eius, esse id illo inventore iste mollitia nemo nesciunt nisi obcaecati optio similique tempore
voluptate!
Adipisci alias assumenda consequatur cupiditate, ex id minima quam rem sint vitae? Animi dolores earum
enim
fugit magni nihil odit provident quaerat. Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Эта информация доступна зарегистрированным пользователям
В листьях ивы накапливается барий и стронций, причем его содержание в этих зеленых частях растений в 30 раз выше, чем в почве.
А в доннике оседает молибден, и изучать это растение выгоднее, чем почву, ведь в нем такой химический элемент содержится в концентрации, которая превышает грунтовую в 300 раз!
И кора сосны дает такие же рекордные показатели, но она накапливает бериллий.
Еда без вреда
Употребляя растения в пищу, вы получаете все то, что они накопили в себе.
Поэтому медики настоятельно не советуют есть то, что выросло в городской черте.
Ведь растения, впитывая полезные элементы, одновременно поглощают и ядовитые вещества.
Каким бы полезным ни был тот же самый березовый сок, но если он взят из дерева, которое растет у шоссе, то ничего кроме вреда такой напиток не принесет.
Lorem ipsum dolor sit amet, consectetur adipisicing elit. Adipisci autem beatae consectetur corporis
dolores ea, eius, esse id illo inventore iste mollitia nemo nesciunt nisi obcaecati optio similique tempore
voluptate!
Adipisci alias assumenda consequatur cupiditate, ex id minima quam rem sint vitae? Animi dolores earum
enim
fugit magni nihil odit provident quaerat. Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Эта информация доступна зарегистрированным пользователям
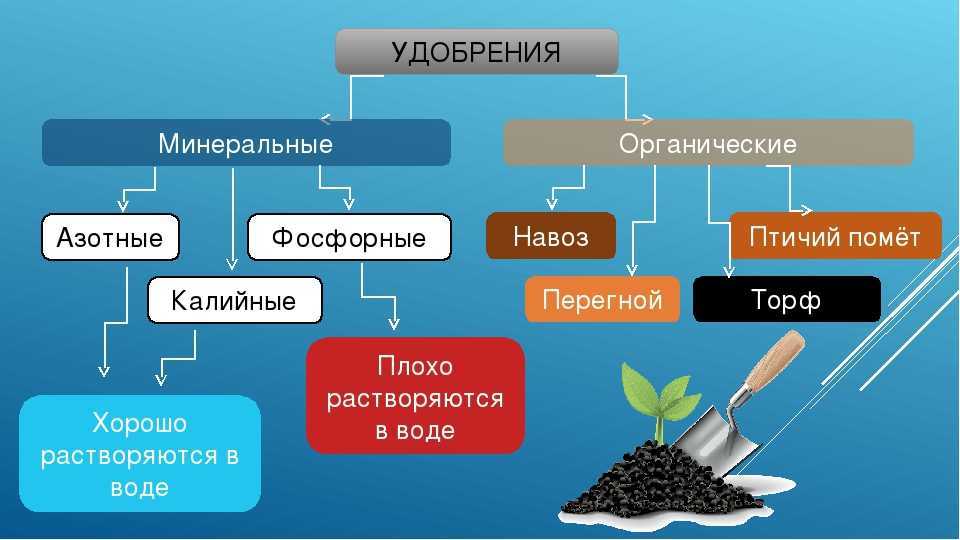
Под словами «минеральное питание» подразумевается, что растение поглощает не органические вещества, а соли в растворенном виде.
Самыми необходимым для жизнедеятельности любой клетки элементами являются, в первую очередь, натрий и хлор.
Эти минеральные вещества составляют основу как межклеточной, так и внутриклеточной жидкости и обеспечивают нормальное давление в клетке.
Другим, не менее важным для растений минералом является магний.
Он необходим для фотосинтеза.
Если магния не хватает, то листья покрываются желтыми пятнами.
Дефицит любого минерала вреден для организма растения так же, как и для человека.
Для того чтобы рост и развитие клеток происходил нормально, без отклонений, в сельском хозяйстве используют удобрения.
Как растения получают минеральные соли?
Корни — это орган растений, который выполняет множество функций.
Он удерживает ствол и крону, не давая им упасть на землю. Он снабжает растение кислородом и водой.
А еще одна задача, которую решает корень — это обеспечение клеток ионами минеральных солей.
Lorem ipsum dolor sit amet, consectetur adipisicing elit. Adipisci autem beatae consectetur corporis
dolores ea, eius, esse id illo inventore iste mollitia nemo nesciunt nisi obcaecati optio similique tempore
voluptate!
Adipisci alias assumenda consequatur cupiditate, ex id minima quam rem sint vitae? Animi dolores earum
enim
fugit magni nihil odit provident quaerat. Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Эта информация доступна зарегистрированным пользователям
Выше мы уже упоминали, что в воде соли растворяются, то есть их молекулы распадаются на составные части — ионы.
И вот такой раствор поглощают корневые волоски.
Они располагаются сразу над зоной роста.
Место, где образуются корневые волоски, называется зоной всасывания.
Lorem ipsum dolor sit amet, consectetur adipisicing elit. Adipisci autem beatae consectetur corporis
dolores ea, eius, esse id illo inventore iste mollitia nemo nesciunt nisi obcaecati optio similique tempore
voluptate!
Adipisci alias assumenda consequatur cupiditate, ex id minima quam rem sint vitae? Animi dolores earum
enim
fugit magni nihil odit provident quaerat. Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Эта информация доступна зарегистрированным пользователям
Наружная оболочка корня состоит из клеток, которые способны удлиняться, врастая в почву.
Их поверхность покрыта слизистым веществом, благодаря которому частицы грунта прилипают к клеточной оболочке.
За счет корневых волосков поверхность всасывания увеличивается в десятки раз, и если повредить эту зону, то растение погибнет.
От корневых волосков вода с ионами поступает в сосуды центрального (по-другому, осевого) цилиндра. Эти сосуды называются по-латыни «ксилема», а по-русски- «древесина».
Поскольку сосуды очень тонкие, вода в них движется наверх благодаря капиллярному восходящему току жидкостей.
Lorem ipsum dolor sit amet, consectetur adipisicing elit. Adipisci autem beatae consectetur corporis
dolores ea, eius, esse id illo inventore iste mollitia nemo nesciunt nisi obcaecati optio similique tempore
voluptate!
Adipisci alias assumenda consequatur cupiditate, ex id minima quam rem sint vitae? Animi dolores earum
enim
fugit magni nihil odit provident quaerat. Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Эта информация доступна зарегистрированным пользователям
Растения поглощают углекислый газ и воду, а под действием солнечного света образуют органические вещества для питания.
Этот процесс называется фотосинтезом.
Под воздействием света в клетках растений происходит образование (синтез) глюкозы — сахара, молекулы которого объединяются в длинные цепочки и образуют в итоге крахмал или используются на нужды развивающегося организма, то есть для роста побегов, образования цветов и плодов.
Побочным продуктом фотосинтеза является кислород, которым дышат животные, человек и даже сами растения.
Если крахмала в избытке, то он откладывается растением «на черный день».
Такие запасы мы можем обнаружить в картофеле, банане, пшенице.
Человек также с удовольствием пользуется этой «энергетической кладовкой», когда ест крахмалистые плоды или зерна, в том числе в виде хлебобулочных изделий и каши.
Lorem ipsum dolor sit amet, consectetur adipisicing elit. Adipisci autem beatae consectetur corporis
dolores ea, eius, esse id illo inventore iste mollitia nemo nesciunt nisi obcaecati optio similique tempore
voluptate!
Adipisci alias assumenda consequatur cupiditate, ex id minima quam rem sint vitae? Animi dolores earum
enim
fugit magni nihil odit provident quaerat. Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Эта информация доступна зарегистрированным пользователям
Как образуется крахмал.
В клетках зеленых частей растений есть так называемые зеленые пластиды — хлоропласты (от греческого «хлорос»- зеленый).
На фотографии под микроскопом они похожи на зеленые пятнышки — горошинки:
Lorem ipsum dolor sit amet, consectetur adipisicing elit. Adipisci autem beatae consectetur corporis
dolores ea, eius, esse id illo inventore iste mollitia nemo nesciunt nisi obcaecati optio similique tempore
voluptate!
Adipisci alias assumenda consequatur cupiditate, ex id minima quam rem sint vitae? Animi dolores earum
enim
fugit magni nihil odit provident quaerat. Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Эта информация доступна зарегистрированным пользователям
А так хлоропласт выглядит в разрезе:
Lorem ipsum dolor sit amet, consectetur adipisicing elit. Adipisci autem beatae consectetur corporis
Adipisci autem beatae consectetur corporis
dolores ea, eius, esse id illo inventore iste mollitia nemo nesciunt nisi obcaecati optio similique tempore
voluptate!
Adipisci alias assumenda consequatur cupiditate, ex id minima quam rem sint vitae? Animi dolores earum
enim
fugit magni nihil odit provident quaerat. Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Эта информация доступна зарегистрированным пользователям
Хлоропласты и есть те самые химические заводы, которые превращают солнечную энергию в питательные вещества.
Солнечный свет включает цепочку химических преобразований, при котором из воды и углекислого газа образуется молекула глюкозы.
А побочным продуктом этого превращения является кислород.
Этот процесс можно записать так, как это делают химики:
углекислый газ (СО2) + вода (Н2О) + солнечный свет = глюкоза (С6H12O6)+ кислород (О2)
Для фотосинтеза хлоропласты не используют зеленую часть спектра солнечного света.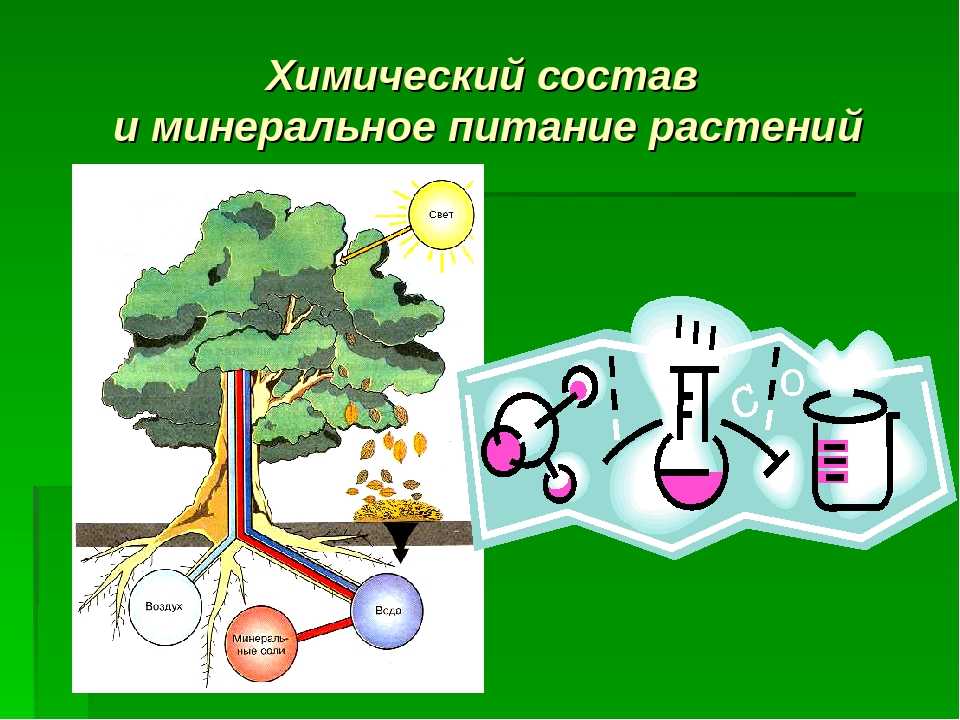
Они ее отражают и именно поэтому кажутся нам зелеными.
Если хлоропласты расходуют большую часть крахмала и накапливают витамин А, то они приобретают оранжево-красный цвет.
Такие пластиды называются хромопластами.
Если же хлорофилл утрачен, то в этом случае бесцветные пластиды называют лейкопластами.
На свету лейкопласты могут превращаться в хлоропласты.
Процесс | Части растения, где осуществляется процесс | Какие вещества поглощаются |
Минеральное питание | Корень с помощью корневых волосков | Ионы минеральных солей |
Фотосинтез | Листья, побеги, плоды, содержащие хлоропласты | Углекислый газ |
Дыхание | Каждая клетка, но наибольший объем циркуляции газов обеспечивают устьица | Кислород |
Lorem ipsum dolor sit amet, consectetur adipisicing elit.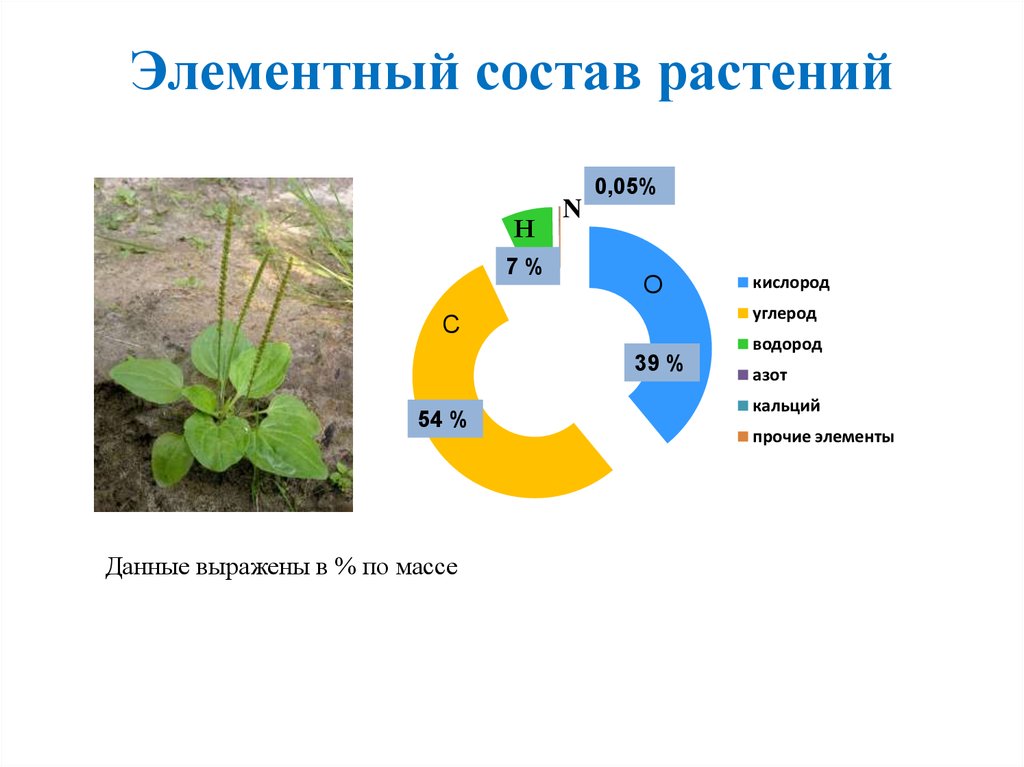 Adipisci autem beatae consectetur corporis
Adipisci autem beatae consectetur corporis
dolores ea, eius, esse id illo inventore iste mollitia nemo nesciunt nisi obcaecati optio similique tempore
voluptate!
Adipisci alias assumenda consequatur cupiditate, ex id minima quam rem sint vitae? Animi dolores earum
enim
fugit magni nihil odit provident quaerat. Aliquid aspernatur eos esse magnam maiores necessitatibus, nulla?
Эта информация доступна зарегистрированным пользователям
Урок биологии в 6 классе «Химический состав растений» | Методическая разработка по биологии (6 класс) на тему:
Тема урока: Химический состав растений
Цели урока:
— изучить химический состав растений на основе изучения состава семян;
— выработать практические умения по обнаружению питательных веществ в семенах;
—
Оборудование: стакан с водой, пробирка, марлевые салфетки, йод, спиртовка, семена пшеницы, подсолнечника, мука, белая бумага, клубни картофеля.
Ход урока:
I. Организационный этап.
1. Приветствие.
2. Проверка подготовленности к учебному занятию.
II. Актуализация субъективного опыта учащихся.
1. Сообщение темы урока: «Химический состав растений» (учащиеся записывают тему урока в тетрадь)
2. Формулировка целей урока: цель нашего урока не просто узнать какие вещества входят в состав растений, но и доказать это опытным путём.
Полученные знания на уроке пригодятся вам при использовании веществ, входящих в состав растений, а также использовать растения по своему назначению.
III. Изучение нового материала.
Вы уже знаете, что все живые организмы имеют сходный химический состав. Они состоят из воды, минеральных и органических веществ (белков, жиров и углеводов). При проведении лабораторной работы, легко убедиться, какие именно вещества входят в состав растений.
Ваша задача внимательно следить за демонстрацией опытов и по ходу заполнять таблицу:
№ п/п | Что брали | Что делали | Что получили |
1. | Пшеница в пробирке | Нагревали на огне | На стенках пробирки появилась вода. |
2. | Семена в тигле | Нагревали на огне | Семена обуглились, осталась зола. |
3. | Тесто в марле | Промывали в стакане с водой. | Вода в стакане помутнела. На марле липкая масса. |
4. | Стакан с мутной водой Срез клубня | Капнули йод Капнули йод | Вода посинела Клубень на срезе посинел |
5. | Семянка подсолнечника | Раздавили на белом листе бумаги | Жирное пятно |
Демонстрация опыта № 1
Семена пшеницы помещаем в пробирку и нагреваем их на слабом огне.
Вопрос: Что вы наблюдаете?
Ответ учащихся: на стенках пробирки появились капельки воды.
Вопрос: А как вы думаете, откуда она взялась?
Ответ: Она была в семенах (из семян)
Вопрос: Какой мы можем сделать вывод?
Учащиеся формируют вывод: В семенах содержится вода.
Какие ещё вещества содержатся в семенах?
Демонстрация опыта № 2
Нагревание семян на металлической пластинке (или тигле). При прокаливании выделяется дым, семена обугливаются. Это сгорают органические вещества. После их сгорания остаётся зола, состоящая из несгорающих минеральных веществ.
Вопрос: Какой вывод мы можем сделать?
Вывод: В состав растений входят минеральные вещества.
Демонстрация опыта № 3
Для проведения этого опыта я приготовила муку.
Вопрос: Из чего делают муку?
Ответ: из зерён пшеницы.
— Значит …. Всё то, что есть в семенах, есть в муке, она имеет такой же химический состав.
(приглашаю ученика для поведения опыта)
Муку помещаем в марлю и хорошо промываем тесто в стакане с водой. Затем смотрим, что осталось в марле. (Белое, тягучее (растянуть) и клейкое (потрогать) вещество (масса)).
Эта тягучая клейкая масса – клейковина. Она сходна по составу с белком куриного яйца и называется растительным белком.
Делаем вывод: в состав растений входит белок.
Демонстрация опыта № 4
Кроме белка в состав растений входит ещё одно вещество.
(приглашаю ученика для проведения опыта)
Добавляем в стакан с мутной водой, в котором промывали тесто, 2-3 капли йода.
Вопрос: что мы наблюдаем?
Ответ: вода посинела.
Йод является индикатором крахмала.
Вывод: следовательно, в состав растений входит крахмал и белок – это органические вещества.
Ещё одно доказательство присутствия крахмала в растениях: на разрез клубня картофеля капнем несколько капель йода. Что происходит? Картофель тоже синеет.
Проведение учащимися опыта № 5
У вас имеются семена подсолнечника и белая бумага. Положите на бумагу семена подсолнечника и раздавите их.
Вопрос: Что вы обнаружили?
Ответ: Масляное пятно (если кто скажет, что вода, можно проверить подсушиванием).
Из семян этих растений, а также из семян льна, конопли добывают масло.
Вывод: в семенах обнаружили ещё одно вещество – жир. Жир – это органическое вещество.
Таким образом, в состав растений входят органические вещества (белки, жиры, углеводы), минеральные вещества и вода.
— Как вы думаете, во всех ли органах растений содержится одинаковое количество воды, органических и минеральных веществ? Найдите ответ на вопрос в тексте параграфа 32, на стр. 155, второй абзац.
В органах растений содержится неодинаковое количество воды, органических и минеральных веществ. В листьях капусты – 90 % воды, в плодах огурцов – 96 % воды, в созревших семенах всего 5-15 % воды. Молодые растения содержат до 95-98 % воды, а одревесневевшие всего около 50 % воды.
Это связано с тем, что вода необходима для всех жизненно важных процессов, происходящих в организме растений. Поэтому клетки, в которых активно протекают процессы жизнедеятельности, всегда содержат много воды.
Содержание минеральных веществ:
— в семенах – 3 %
— в корнях и стеблях – 5 %
— в листьях – 10-15 %
Остальное приходится на органические вещества.
Вопрос: Как вы думаете, одинаковые части растений содержат одинаковое количество веществ? Сравните состав семян пшеницы и подсолнечника по таблице на стр. 155.
Вопрос: Каких веществ больше всего в семенах растений?
Ответ: органических.
Вопрос: В каких семенах больше воды?
Ответ: у зерновок пшеницы
Вопрос: А минеральных веществ?
Ответ: у семянок подсолнечника.
Вывод: В семенах всех растений органических веществ значительно больше, чем воды и минеральных веществ.
Соотношение веществ в органах растений тоже может быть различно:
Семена | Углеводы | Жиры | Белки |
Пшеница | 69 % | 2 % | 13 % |
Подсолнечник | 16 % | 44 % | 26 % |
Зная химический состав растений, человек использует растения по назначению: для получения муки и крупы, содержащие углеводы и белки выращивают одни растения, для получения растительных жиров другие.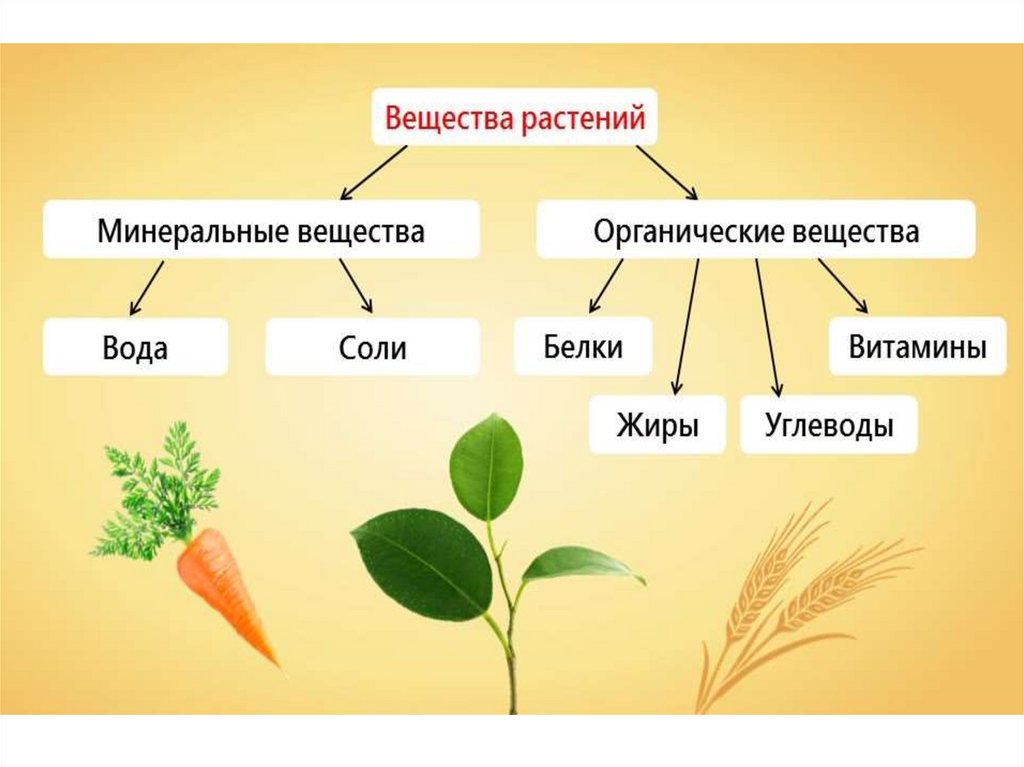 Выпишите в тетрадь, какие растения содержат:
Выпишите в тетрадь, какие растения содержат:
Белки – горох, фасоль, бобы, соя, чечевица
Жиры – подсолнечник, хлопчатник, лён, конопля, арахис, соя
Углеводы – пшеница, рожь, ячмень, кукуруза, рис, просо, овёс, гречиха.
IV. Закрепление изученного материала.
Выполнение задания № 102 в рабочей тетради.
Проверка заполнения таблицы.
V. Итог урока.
VI. Домашнее задание. § 32, задание № 3 на стр. 157, повторить § 20 (зоны корня)
VII. Рефлексия.
Классные ресурсы | Строительные блоки фотосинтеза
ПЛАН УРОКА по химическим изменениям, междисциплинарным, молекулярным формулам, сохранению массы, уравнениям баланса, сохранению массы, обратимым реакциям, химическим изменениям, фотосинтезу.
Последнее обновление: 02 октября 2018 г.
Резюме
На этом уроке учащиеся будут использовать цветные кубики для представления элементов фотосинтеза и иллюстрируют, как они расщепляются и снова собираются для создания глюкозы.
Уровень
Средняя школа
Цели
К концу этого урока учащиеся должны уметь
- Разработайте научное объяснение, основанное на доказательствах роли фотосинтеза в круговороте веществ и потоках энергии в организмы и из них.
Темы по химии
Этот урок помогает учащимся понять следующие темы по химии:
- Реакции
- Фотосинтез
- Сохранение материи
Время
Подготовка учителя : 20 минут
Урок : 45 минут
Материалы
- 6 красных кубиков
- 18 зеленых кубиков
- 12 синих кубиков
- Наклейки Sun’s Energy
(Кубики Unifix или Lego отлично подходят для этой модели. Вы можете использовать любой цвет, который вы хотите, при условии, что количество остается прежним, и вы меняете ключ в Листе активности учащихся.)
Безопасность
Для этого урока не требуется соблюдения особых мер предосторожности.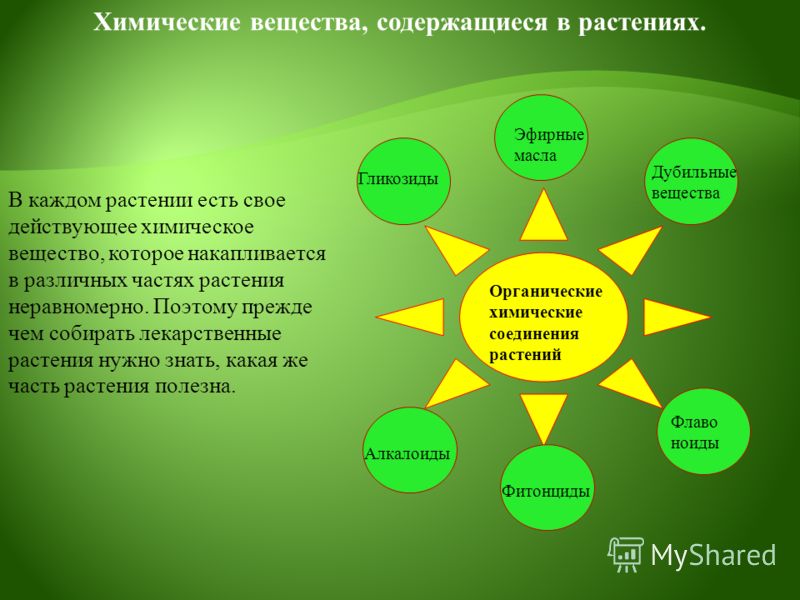
Словарные термины
- Молекулы
- Химическая реакция
- Глюкоза
- Кислород
- Водород
- Углерод
- Фотосинтез
Ключевые слова
Фотосинтез, растения, кислород, углекислый газ, дыхание, глюкоза, выход
Заметки для учителя
- Если блоки цветов, указанных в материалах, недоступны, не стесняйтесь менять цвета по мере необходимости, но не забудьте также изменить ключ.
- Другие возможные заменители блоков включают K-Nex, цветные скрепки, цветные резинки и даже цветную нить, которую можно легко завязать в бантики и растянуть.
- Учащихся с более высоким уровнем успеваемости можно попросить применить эту же модель к дыханию с учетом начальной части формулы.
Задействовать
- Учащиеся будут размышлять в парах и делиться вещами, необходимыми растениям для выживания. Обсуждение в классе должно касаться того, почему некоторые вещи необходимы для роста растений, на основе предварительных знаний и убедительных примеров.
 Если есть некоторые расхождения в том, какие растения должны расти, студентов попросят доказать свои идеи, создав эксперимент для проверки своей теории. Например, если учащиеся не уверены, нужна ли растениям почва для роста, они должны провести эксперимент, исследуя, что происходит с растением, растущим без почвы, и растением, растущим с почвой.
Если есть некоторые расхождения в том, какие растения должны расти, студентов попросят доказать свои идеи, создав эксперимент для проверки своей теории. Например, если учащиеся не уверены, нужна ли растениям почва для роста, они должны провести эксперимент, исследуя, что происходит с растением, растущим без почвы, и растением, растущим с почвой. - Когда класс определит, что растению для роста необходимы вода, углекислый газ и солнечный свет, напишите окончательный список на доске.
Исследовать
- Подготовьте блоки и напишите на доске ключ, объясняющий, что представляет каждый цветной блок:
- Красный = Углерод
- Синий = Кислород
- Зеленый = Водород
- Попросите учащихся самостоятельно составить список того, что нужно растению для роста.
- Спросите учащихся: « Из чего состоит вода? Какие элементы? Вы знаете другие названия воды? Этот вопрос должен привести к мысли, что вода состоит из H 2 O.

- Напишите H 2 O на доске рядом с ключом. Спросите: « Что означает H 2 O? Сможете ли вы составить H 2 O из предоставленных блоков?»
- Предложите учащимся добровольно поделиться своими моделями воды. Обсудите в группе, пока группа не решит, что вода состоит из двух атомов водорода и одного атома кислорода (два зеленых блока и один синий синий).
- Расскажите ученикам; “ Растения поглощают шесть молекул воды за раз. Пожалуйста, сделайте шесть молекул воды».
- Напишите на доске «6 H 2 0 +»
- Спросите студентов, ”Растениям нужна вода, чтобы выжить. Что им еще нужно?» Позвольте учащимся ответить на вопрос о двуокиси углерода.
- Спросите учащихся, «Как вы думаете, как выглядит углекислый газ?» Дайте им время обдумать свою идею, а затем предложите учащимся объяснить свое мнение.
- Когда класс решит, что двуокись углерода состоит из одного атома углерода и двух атомов кислорода (один красный и два синих кубика), попросите их использовать оставшиеся кубики для получения двуокиси углерода.

- Спросите учащихся, «Сколько молекул углекислого газа вы получили?» Когда учащиеся ответят шесть, добавьте к своему уравнению на доске: «6 H 2 O + 6 CO 2 »
- Спросите учащихся, : «Что еще нужно растению, чтобы выжить?» Скорее всего, они ответят солнечным светом. Спроси, «Из чего состоит солнечный свет? Есть ли еще блоки, чтобы сделать больше молекул? Что вы можете сказать о солнечном свете?» С руководством учащиеся должны сделать вывод, что солнечный свет является источником энергии.
- Спросите учащихся, «Какой источник энергии используется в этой модели? Что двигает блоки?» Они ответят, что они являются источником энергии в модели, и они должны понимать, что в этой модели они играют роль солнца.
- Дайте каждому учащемуся наклейку с надписью «Энергия Солнца», чтобы они могли помнить, что они являются энергией в модели.
- Некоторые учащиеся могут не понимать, что они используют энергию.
 Пусть они быстро потирают руки в течение 15 секунд. Когда они говорят, что устали, спросите, почему. Когда они заявляют, что тратят слишком много энергии на потирание рук, подчеркните слово «энергия». Скажите учащимся, : «Вы используете энергию, чтобы двигать вещи. Солнце также излучает энергию в другой форме. Вы потратили много энергии, чтобы потереть руки друг о друга, как они себя сейчас чувствуют? Это потому, что вы использовали энергию для создания этого тепла от трения, точно так же, как солнце использует энергию для перегруппировки молекул в процессе фотосинтеза». В уравнении на доске «6 H 2 O + 6 CO 2 » напишите «Энергия Солнца» и нарисуйте стрелку к уравнению, чтобы показать, что оно способствует протеканию реакции, но не является частью само молекулярное уравнение.
Пусть они быстро потирают руки в течение 15 секунд. Когда они говорят, что устали, спросите, почему. Когда они заявляют, что тратят слишком много энергии на потирание рук, подчеркните слово «энергия». Скажите учащимся, : «Вы используете энергию, чтобы двигать вещи. Солнце также излучает энергию в другой форме. Вы потратили много энергии, чтобы потереть руки друг о друга, как они себя сейчас чувствуют? Это потому, что вы использовали энергию для создания этого тепла от трения, точно так же, как солнце использует энергию для перегруппировки молекул в процессе фотосинтеза». В уравнении на доске «6 H 2 O + 6 CO 2 » напишите «Энергия Солнца» и нарисуйте стрелку к уравнению, чтобы показать, что оно способствует протеканию реакции, но не является частью само молекулярное уравнение. - Добавьте на доске знак урожайности к своему уравнению «6 H 2 O + 6 CO 2 →» Объясните учащимся, что «этот символ ученые используют в уравнении, чтобы сказать «урожайность».
 Это означает, что происходит химическое изменение между реагентами (химикалии с левой стороны стрелки) и продуктами (химикалии с правой стороны стрелки)».
Это означает, что происходит химическое изменение между реагентами (химикалии с левой стороны стрелки) и продуктами (химикалии с правой стороны стрелки)». - Спросите учащихся, «Что выделяет растение в процессе фотосинтеза?» Студенты должны ответить кислородом.
- Скажите учащимся, что «растение выделяет кислород. На самом деле он испускает шесть молекул кислорода в виде O 2 . Сможете ли вы переставить блоки так, чтобы получилось шесть молекул O 2 ?»
- Добавьте кислород к вашему уравнению: «6 H 2 O + 6 CO 2 → 6 O 2
- Скажите учащимся: « Теперь посмотрите на все блоки, которые у вас остались. Что еще может сделать завод? Используйте блоки, чтобы сделать только одну молекулу последнего оставшегося химического вещества, которое растение производит во время этой химической реакции. Придумайте молекулярное уравнение и запишите его самостоятельно из оставшихся блоков».
- Предложите учащимся поделиться химическим уравнением молекулы, которая у них осталась.
 Они должны получить C 6 H 12 O 6 . Добавьте это к уравнению «6 H 2 O + 6 CO 2 → 6 O 2 + C 6 H 12 O 6 ».
Они должны получить C 6 H 12 O 6 . Добавьте это к уравнению «6 H 2 O + 6 CO 2 → 6 O 2 + C 6 H 12 O 6 ». - Спросите учащихся, что они об этом думают. Скажите им, что «эта молекула называется глюкозой. Это действительно разновидность сахара. Растения прошли через процесс, называемый фотосинтезом, чтобы произвести этот сахар. Когда вы едите растения, вы потребляете сахар».
Объяснить
Предложите учащимся объединиться и проиллюстрировать фотосинтез, используя химическое уравнение, которое они только что выучили, и свои собственные иллюстрации того, как он будет выглядеть. Пусть они поделятся своим объяснением с классом.
Примеры для учащихся могут быть такими простыми, как рисование растения, дышащего воздухом, плюс стакан воды и солнечного света, в результате получается мешок с сахаром и человек, дышащий кислородом. На более сложном уровне учитель может предложить учащимся нарисовать молекулы, используя традиционные модели шара и палочки. Это возможность для учащихся разного уровня продемонстрировать разное понимание с помощью собственных иллюстраций.
На более сложном уровне учитель может предложить учащимся нарисовать молекулы, используя традиционные модели шара и палочки. Это возможность для учащихся разного уровня продемонстрировать разное понимание с помощью собственных иллюстраций.
Разработка
Спросите учащихся, что произойдет, если они добавят еще один элемент в процесс фотосинтеза? Например, что, если бы они заменили этанол (C 2 H 5 OH) для воды? Или что, если бы они заменили кофе на воду? Позвольте учащимся выбрать свой собственный заменитель для части уравнения и создать собственное исследование, в котором они могут изучить замены различных ингредиентов и сделать свои собственные выводы.
Оценка
Вопросы с несколькими вариантами ответов
- Что нужно растениям для фотосинтеза?
а. Углерод
б. Кислород
в. Диоксид
д. Углекислый газ* - Что такое C 6 H 12 O 6 ?
а. Глюкоза*
Глюкоза*
б. Калорийность
гр. Сахароза
d. Гидроксид углерода - Что означает стрелка в химическом уравнении?
а. Равно
б. То же, что и
c. Урожайность*
d. Количественно - В какой части клетки происходит фотосинтез?
а. Митохондрии
б. Вакуоли
c. Клеточная мембрана
д. Хлоропласты* - Какие продукты фотосинтеза?
а. Углекислый газ и кислород
b. Кислород и вода
c. Вода и двуокись углерода
d. Кислород и глюкоза*
Вопросы для обсуждения
- Как можно разработать тест, чтобы проверить, действительно ли растение дышит углекислым газом?
- Чем модель похожа и отличается от реальной жизни?
- Что случилось бы с людьми, если бы у нас не было растений?
- Какие еще виды полагаются на растения для получения сахара?
- Какие еще виды полагаются на кислород, который они обеспечивают растениями?
- Как это уравнение иллюстрирует закон сохранения массы?
Открытый вопрос
Для оценки попросите учащихся написать абзац, объясняющий, что происходит при фотосинтезе.
Научные стандарты следующего поколения
Этот урок поддерживает следующее:
Практика науки и техники
- Разработка и использование моделей
- Участие в споре на основании улик
- Использование математического и вычислительного мышления
- Получение, оценка и передача информации
Сквозные концепции
- Энергия и материя: потоки, циклы и сохранение
Основные дисциплинарные идеи, классы 6–8
Науки о жизни
- Растения, водоросли (включая фитопланктон) и многие микроорганизмы используют энергию света для производства сахаров (пищи) из углекислого газа из атмосферы и воды в процессе фотосинтеза, при котором также выделяется кислород. Эти сахара можно использовать сразу или сохранить для роста или последующего использования. (МС-LS1-6)
- Химическая реакция, посредством которой растения производят сложные пищевые молекулы (сахара), требует затрат энергии (т.
 е. солнечного света). В этой реакции углекислый газ и вода объединяются, образуя органические молекулы на основе углерода и выделяя кислород. (вторичный по отношению к MS-LS1-6)
е. солнечного света). В этой реакции углекислый газ и вода объединяются, образуя органические молекулы на основе углерода и выделяя кислород. (вторичный по отношению к MS-LS1-6) - Внутри отдельных организмов пища проходит ряд химических реакций, в ходе которых она расщепляется и перестраивается с образованием новых молекул, поддерживающих рост или высвобождающих энергию. (МС-LS1-7)
Физические науки
- МС-ПС1-5. Разработайте и используйте модель для описания того, как общее число атомов не изменяется в химической реакции и, таким образом, сохраняется масса.
Инженерный проект
- Чем точнее могут быть определены критерии и ограничения задачи проектирования, тем больше вероятность того, что разработанное решение будет успешным. Спецификация ограничений включает рассмотрение научных принципов и других соответствующих знаний, которые могут ограничить возможные решения. (МС-ETS1-1)
- Решение необходимо протестировать, а затем изменить на основе результатов тестирования, чтобы улучшить его.
 (МС-ETS1-4)
(МС-ETS1-4) - Существуют систематические процессы оценки решений с точки зрения того, насколько хорошо они соответствуют критериям и ограничениям проблемы. (МС-ETS1-2), (МС-ETS1-3)
- Иногда части разных решений можно объединить, чтобы создать решение, которое лучше, чем любое из его предшественников. (МС-ETS1-3)
- Модели всех видов важны для тестирования решений. (МС-ETS1-4)
- Хотя один дизайн может не показывать наилучшие результаты во всех тестах, выявление характеристик проекта, который показал наилучшие результаты в каждом тесте, может предоставить полезную информацию для процесса редизайна, т. е. некоторые из этих характеристик могут быть включены в новый дизайн. (МС-ETS1-3)
- Итеративный процесс тестирования наиболее перспективных решений и модификации того, что предлагается на основе результатов тестирования, приводит к большей доработке и, в конечном итоге, к оптимальному решению. (МС-ETS1-4)
Для студента
Исходная информация
В этом упражнении вы будете использовать цветные кубики, чтобы представить молекулы в фотосинтезе и проиллюстрировать, как они расщепляются и снова собираются для создания глюкозы.
Подумай об этом
Что нужно растению для жизни? Укажите как минимум два наблюдения из реальной жизни, которые подтверждают ваши идеи.
_________________________________________________________________________
_________________________________________________________________________
_________________________________________________________________________
Материалы
- 6 красных кубиков
- 18 синих блоков
- 12 зеленых блоков
- Наклейки с изображением солнечной энергии
Процедура
- Сделайте шесть молекул воды (H 2 O).
- Сделайте шесть молекул углекислого газа (CO 2 ).
- Наклейте наклейку «Солнечная энергия».
- Только что произошла реакция. Переставьте блоки из воды и углекислого газа, чтобы построить шесть молекул кислорода (O 2 ).
- Какие еще химические вещества производит завод? Используйте оставшиеся блоки, чтобы построить одну молекулу.
 Запишите химическую формулу.
Запишите химическую формулу.
Данные
Подумайте о количестве и типах молекул в деятельности. Напишите химическое уравнение фотосинтеза в строке ниже. Используйте изображения или символы, чтобы проиллюстрировать молекулы, используемые в уравнении. Не рисуйте блоки. Вместо этого найдите свой собственный способ выразить, как выглядит фотосинтез.
Анализ
- Почему солнечная энергия не указана в уравнении фотосинтеза?
_________________________________________________________________________
_________________________________________________________________________
- Что такое Закон сохранения материи? Как он применяется в фотосинтезе?
_________________________________________________________________________
_________________________________________________________________________
- Проходят ли люди или другие животные фотосинтез? Как люди получают глюкозу?
_________________________________________________________________________
_________________________________________________________________________
- Какие молекулы нужны растениям для фотосинтеза?
- Углерод
- Кислород
- Диоксид
- Углекислый газ
- Что такое C 6 Н 12 О 6 ?
- Глюкоза
- калорий
- Сахароза
- Гидроксид углерода
- Какое слово означает стрелка в химическом уравнении?
- Равен
- То же, что и
- дает
- Количество
- Какие продукты фотосинтеза?
- Углекислый газ и кислород
- Кислород и вода
- Вода и двуокись углерода
- Кислород и глюкоза
Растительные флавоноиды: химические характеристики и биологическая активность
1. De Luna S.L., Ramirez-Garza R.E., Saldívar S.O.S. Экологически безопасные методы извлечения флавоноидов из растительного сырья: влияние условий их эксплуатации на урожайность и антиоксидантные свойства. науч. Мир J. 2020; 2020: 6792069. doi: 10.1155/2020/6792069. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
De Luna S.L., Ramirez-Garza R.E., Saldívar S.O.S. Экологически безопасные методы извлечения флавоноидов из растительного сырья: влияние условий их эксплуатации на урожайность и антиоксидантные свойства. науч. Мир J. 2020; 2020: 6792069. doi: 10.1155/2020/6792069. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2. Фердинандо М.Д., Брунетти К., Фини А., Таттини М. Флавоноиды как антиоксиданты в растениях при абиотических стрессах. В: Ахмад П., Прасад М.Н.В., редакторы. Реакция растений на абиотический стресс: метаболизм, продуктивность и устойчивость. Спрингер; Берлин/Гейдельберг, Германия: 2012. [CrossRef] [Google Scholar]
3. Панче А.Н., Диван А.Д., Чандра С.Р. Флавоноиды: обзор. Дж. Нутр. науч. 2016;5:e47. doi: 10.1017/jns.2016.41. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
4. Диас М.К., Пинто Д.К.Г.А., Фрейтас Х., Сантос К., Сильва А.М.С. Антиоксидантная система Olea europaea к усилению УФ-В излучения также зависит от флавоноидов и секоиридоидов. Фитохимия. 2020;170:112199. doi: 10.1016/j.phytochem.2019.112199. [PubMed] [CrossRef] [Google Scholar]
Фитохимия. 2020;170:112199. doi: 10.1016/j.phytochem.2019.112199. [PubMed] [CrossRef] [Google Scholar]
5. Сайни Н., Гахлават С.К., Латер В. Флавоноиды: нутрицевтики и их роль в качестве противовоспалительных и противораковых средств. В: Гахлават С., Салар Р., Сивах П., Духан Дж., Кумар С., Каур П., редакторы. Биотехнология растений: последние достижения и разработки. Спрингер; Сингапур: 2017. [CrossRef] [Google Scholar]
6. Jucá M.M., Filho F.M.S.C., de Almeida J.C., Mesquita D.S., Barriga J.R.M., Dias K.C.F., Barbosa T.M., Vasconcelos L.C., Leal L.K.A.M., Ribeiro J.R., et al. Флавоноиды: биологическая активность и терапевтический потенциал. Нац. Произв. Рез. 2020;5:692–705. doi: 10.1080/14786419.2018.1493588. [PubMed] [CrossRef] [Google Scholar]
7. Фрага К.Г., Крофт К.Д., Кеннеди Д.О., Томас-Барберан Ф.А. Влияние полифенолов и других биоактивных веществ на здоровье человека. Функция питания 2019;10:514–528. дои: 10.1039/C8FO01997E. [PubMed] [CrossRef] [Google Scholar]
8. Малеки С.Дж., Креспо Дж.Ф., Кабанильяс Б. Противовоспалительные эффекты флавоноидов. Пищевая хим. 2019;299:125124. doi: 10.1016/j.foodchem.2019.125124. [PubMed] [CrossRef] [Google Scholar]
Малеки С.Дж., Креспо Дж.Ф., Кабанильяс Б. Противовоспалительные эффекты флавоноидов. Пищевая хим. 2019;299:125124. doi: 10.1016/j.foodchem.2019.125124. [PubMed] [CrossRef] [Google Scholar]
9. Д’Амелия В., Аверсано Р., Чиайезе П., Карпуто Д. Антиоксидантные свойства растительных флавоноидов: их использование в молекулярной селекции растений. Фитохим. 2018; 17:611–625. doi: 10.1007/s11101-018-9568-y. [Перекрестная ссылка] [Академия Google]
10. Шамец Д., Каралия Э., Шола И., Бок В.В., Салопек-Сонди Б. Роль полифенолов в реакции на абиотический стресс: влияние молекулярной структуры. Растения. 2021;10:118. doi: 10.3390/plants10010118. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
11. Кумар С., Пандей А.К. Химия и биологическая активность флавоноидов: обзор. науч. Мир J. 2013; 2013: 162750. дои: 10.1155/2013/162750. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
12. Набави С.М., Шамец Д., Томчик М., Милелла Л., Руссо Д., Хабтемариам С. , Сунтар И., Растрелли Л., Даглиа М., Сяо Дж. и др. Пути биосинтеза флавоноидов в растениях: универсальные мишени для метаболической инженерии. Биотехнолог. Доп. 2020;38:107316. doi: 10.1016/j.biotechadv.2018.11.005. [PubMed] [CrossRef] [Академия Google]
, Сунтар И., Растрелли Л., Даглиа М., Сяо Дж. и др. Пути биосинтеза флавоноидов в растениях: универсальные мишени для метаболической инженерии. Биотехнолог. Доп. 2020;38:107316. doi: 10.1016/j.biotechadv.2018.11.005. [PubMed] [CrossRef] [Академия Google]
13. Сайто К., Сакакибара К.Ю., Накабаяси Р., Ямадзаки М., Тоге Т., Ферни А.Р. Путь биосинтеза флавоноидов у арабидопсиса: структурное и генетическое разнообразие. Завод Физиол. Биохим. 2013;72:21–34. doi: 10.1016/j.plaphy.2013.02.001. [PubMed] [CrossRef] [Google Scholar]
14. Двиведи М.К., Сонтер С., Мишра С., Патель Д.К., Сингх П.К. Антиоксидантная, антибактериальная активность и фитохимическая характеристика цветов Carica papaya . Университет Бени-Суэф. J. Основное приложение. науч. 2020;9:23. doi: 10.1186/s43088-020-00048-w. [CrossRef] [Google Scholar]
15. Харборн Дж. Б., Бакстер Х. Справочник по природным флавоноидам. Том 1 Джон Вили и сыновья; Чичестер, Великобритания: 1999. [Google Scholar]
16. Cortez R., luna-Vital D.A., Margulis D., Mejia E.G. Натуральные пигменты: методы стабилизации антоцианов для пищевых продуктов. Компр. Преподобный Food Sci. Пищевая безопасность 2017;16:180–198. doi: 10.1111/1541-4337.12244. [PubMed] [CrossRef] [Google Scholar]
Cortez R., luna-Vital D.A., Margulis D., Mejia E.G. Натуральные пигменты: методы стабилизации антоцианов для пищевых продуктов. Компр. Преподобный Food Sci. Пищевая безопасность 2017;16:180–198. doi: 10.1111/1541-4337.12244. [PubMed] [CrossRef] [Google Scholar]
17. Khoo H.E., Azlan A., Tang S.T., Lim S.M. Антоцианидины и антоцианы: окрашенные пигменты в качестве пищевых продуктов, фармацевтических ингредиентов и потенциальной пользы для здоровья. Еда Нутр. Рез. 2017;61:1361779. doi: 10.1080/16546628.2017.1361779. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
18. Брахмачари Г. Встречающиеся в природе флаваноны: обзор. Нац. Произв. Комм. 2008;3:1934578X0800300. doi: 10.1177/1934578X0800300820. [CrossRef] [Google Scholar]
19. Шукла Р., Пандей В., Ваднере Г.П., Лоди С. Роль флавоноидов в лечении воспалительных заболеваний. В: Уотсон Р.Р., Приди В.Р., редакторы. Биоактивная пища как диетическое вмешательство при артрите и связанных с ним воспалительных заболеваниях. Академическая пресса; Кембридж, Массачусетс, США: 2019 г.. стр. 293–322. [CrossRef] [Google Scholar]
Академическая пресса; Кембридж, Массачусетс, США: 2019 г.. стр. 293–322. [CrossRef] [Google Scholar]
20. Вонг Э. Изофлавоноиды. В: Harborne JB, Mabry TJ, Mabry H., редакторы. Флавоноиды. Спрингер; Бостон, Массачусетс, США: 1975. [CrossRef] [Google Scholar]
21. Vitale D.C., Piazza C., Melilli B., Drago F., Salomone S. Изофлавоны: эстрогенная активность, биологический эффект и биодоступность. Евро. J. Drug Metab. Фармакокинетика. 2013; 38:15–25. doi: 10.1007/s13318-012-0112-y. [PubMed] [CrossRef] [Google Scholar]
22. Пинто Д.К.Г.А., Симоес М.А.М., Сильва А.М.С. Genista tridentata L.: Богатый источник флавоноидов с противовоспалительным действием. Лекарства. 2020;7:31. doi: 10.3390/medicines7060031. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
23. Сингх М., Каур М., Силакари О. Флавоны: важная основа для медицинской химии. Евро. Дж. Мед. хим. 2014; 84: 206–239. doi: 10.1016/j.ejmech.2014.07.013. [PubMed] [CrossRef] [Google Scholar]
24. Батиха Г.Е., Бешбиши А.М., Икрам М., Мулла З.С., Эль-Хак М.Е.А.Е., Таха А.Е., Алгаммал А.М., Элева Ю.Х.А. Фармакологическая активность, биохимические свойства и фармакокинетика основного природного полифенольного флавоноида: кверцетина. Еда. 2020;9:374. doi: 10.3390/foods
Батиха Г.Е., Бешбиши А.М., Икрам М., Мулла З.С., Эль-Хак М.Е.А.Е., Таха А.Е., Алгаммал А.М., Элева Ю.Х.А. Фармакологическая активность, биохимические свойства и фармакокинетика основного природного полифенольного флавоноида: кверцетина. Еда. 2020;9:374. doi: 10.3390/foods
74. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
25. Rodríguez-García C., Sánchez-Quesada C., Gaforio J.J. Пищевые флавоноиды как химиопрофилактические средства против рака: обновленный обзор исследований на людях. Антиоксиданты. 2019;8:137. doi: 10.3390/antiox8050137. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
26. Kozłowska A., Szostak-Węgierek D. Флавоноиды — источники пищи, польза для здоровья и задействованные механизмы. В: Mérillon JM, Ramawat K., редакторы. Биоактивные молекулы в продуктах питания. Спрингер; Чам, Швейцария: 2017 г. (серия справочников по фитохимии). [Перекрестная ссылка] [Академия Google]
27. Терахара Н. Флавоноиды в пищевых продуктах: обзор. Нац. Произв. ком. 2015; 10: 521–528. doi: 10.1177/1934578X1501000334. [PubMed] [CrossRef] [Google Scholar]
Нац. Произв. ком. 2015; 10: 521–528. doi: 10.1177/1934578X1501000334. [PubMed] [CrossRef] [Google Scholar]
28. Агравал А.Д. Фармакологическая активность флавоноидов: обзор. Междунар. Дж. Пармацевт. науч. Нано. 2011;4:1394–1398. doi: 10.37285/ijpsn.2011.4.2.3. [CrossRef] [Google Scholar]
29. Basli A., Soulet S., Chaher N., Mérillon J.M., Chibane M., Monti J.P., Richard T. Винные полифенолы: потенциальные агенты нейропротекции. Окислительная Мед. Клетка. Лонгев. 2012;2012:805762. doi: 10.1155/2012/805762. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
30. Bae J., Kim N., Shin Y., Kim S.Y., Kim Y.J. Активность катехинов и их применение. Биомед. Дерматол. 2020;4:8. doi: 10.1186/s41702-020-0057-8. [CrossRef] [Google Scholar]
31. Дуайер Дж. Т., Петерсон Дж. Чай и флавоноиды: где мы находимся, куда двигаться дальше. Являюсь. Дж. Клин. Нутр. 2013;98:1611С–1618С. doi: 10.3945/ajcn.113.059584. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
32. Шарма В., Рамават К.Г. Изофлавоноиды. В: Рамават К., Мериллон Дж. М., редакторы. Натуральные продукты. Спрингер; Берлин/Гейдельберг, Германия: 2013. [CrossRef] [Google Scholar]
Шарма В., Рамават К.Г. Изофлавоноиды. В: Рамават К., Мериллон Дж. М., редакторы. Натуральные продукты. Спрингер; Берлин/Гейдельберг, Германия: 2013. [CrossRef] [Google Scholar]
33. Руис-Крус С., Чапарро-Эрнандес С., Эрнандес-Руис К.Л., Сира-Чавес Л.А., Эстрада-Альварадо М.И., Ортега Л.Е.Г., Орнелас-Пас Л.Л., Мата М.А.Л. Флавоноиды: важные биосоединения в продуктах питания. В: Жустино Г.К., редактор. Флавоноиды — от биосинтеза к здоровью человека. ИнтехОткрытый; Лондон, Великобритания: 2017. [CrossRef] [Google Scholar]
34. Редондо-Бланко С., Фернандес Дж., Лопес-Ибаньес С., Мигелес Э.М., Виллар С.Дж., Ломбо Ф. Фитохимические вещества растений в консервировании пищевых продуктов: противогрибковая биоактивность : Обзор. Дж. Пищевая защита. 2020; 83: 163–171. doi: 10.4315/0362-028X.JFP-19-163. [PubMed] [CrossRef] [Google Scholar]
35. Huvaere K., Skibsted L.H. Флавоноиды, защищающие продукты питания и напитки от света. J. Sci. Фуд Агрик. 2015;95:20–35. doi: 10.1002/jsfa. 6796. [PubMed] [CrossRef] [Google Scholar]
6796. [PubMed] [CrossRef] [Google Scholar]
36. Маркхэм К.Р. Углерод-13 ЯМР-спектроскопия флавоноидов. В: Harborne JB, Mabry TJ, Mabry H., редакторы. Флавоноиды. Спрингер; Бостон, Массачусетс, США: 1982. [CrossRef] [Google Scholar]
37. Stobiecki M., Kachlicki P. Выделение и идентификация флавоноидов. В: Гротевольд Э., редактор. Наука о флавоноидах. Спрингер; Цинциннати, Огайо, США: 2006. Глава 2. [Google Scholar]
38. Цанова М., Атанасов В., Янева З., Иванова Д., Динев Т. Селективность современных методов экстракции флавоноидов из растительного сырья. Процессы. 2020;8:1222. doi: 10.3390/pr8101222. [CrossRef] [Google Scholar]
39. Амир К., Шахбаз Х.М., Квон Дж.Х. Методы зеленой экстракции полифенолов из растительных матриц и их побочных продуктов: обзор. Компр. Преподобный Food Sci. Пищевая безопасность 2017;16:295–315. doi: 10.1111/1541-4337.12253. [PubMed] [CrossRef] [Google Scholar]
40. Soquetta M.B., Tonato D., Quadros M.M., Boeira C.P., Cichoski A. J., Terra L.M., Kuhn R.C. Ультразвуковая экстракция биоактивных соединений из Citrus reticulata кожура с использованием электролизованной воды. J. Food Proc. Сохранить 2019;43:e14236. doi: 10.1111/jfpp.14236. [CrossRef] [Google Scholar]
J., Terra L.M., Kuhn R.C. Ультразвуковая экстракция биоактивных соединений из Citrus reticulata кожура с использованием электролизованной воды. J. Food Proc. Сохранить 2019;43:e14236. doi: 10.1111/jfpp.14236. [CrossRef] [Google Scholar]
Передо А.В., Барберо Г.Ф. и др. Экстракция флавоноидов из природных источников с использованием современных технологий. Фронт. хим. 2020;8:507887. doi: 10.3389/fchem.2020.507887. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
42. Мартинс С., Муссатто С.И., Мартинес-Авила Г., Монтаньес-Санс Х., Агилар С.Н., Тейшейра Х.А. Биоактивные фенольные соединения: производство и экстракция путем ферментации в твердой фазе. Обзор. Биотехнолог. Доп. 2011;29:365–373. doi: 10.1016/j.biotechadv.2011.01.008. [PubMed] [CrossRef] [Google Scholar]
43. Awouafack MD, Tane P., Morita H. Выделение и структурная характеристика флавоноидов. В: Жустино Г.К., редактор. Флавоноиды — от биосинтеза к здоровью человека. ИнтехОткрытый; Лондон, Великобритания: 2017. [CrossRef] [Google Scholar]
[CrossRef] [Google Scholar]
44. Фомо Г., Мадзимбамуто Т.Н., Оджуму Т.В. Применение нетрадиционных технологий зеленой добычи в перерабатывающих отраслях: проблемы, ограничения и перспективы. Устойчивость. 2020;12:5244. doi: 10.3390/su12135244. [CrossRef] [Google Scholar]
45. Розелло-Сото Э., Барба Ф.Дж., Лоренцо Дж.М., Мунеката П.Е.С., Гомес Б., Молто Дж.К. Фенольный профиль масел, полученных из побочных продуктов «орчаты» с помощью сверхкритического CO 2 и его взаимосвязь с параметрами антиоксидантов и окисления липидов: тройная характеристика TOF-LC-MS-MS. Пищевая хим. 2019;274:865–871. doi: 10.1016/j.foodchem.2018.09.055. [PubMed] [CrossRef] [Google Scholar]
46. Пиментель-Мораль С., Боррас-Линарес И., Лосано-Санчес Х., Арраэс-Роман Д., Мартинес-Ферес А., Сегура-Карретеро А. Сверхкритические CO 2 извлечение биологически активных соединений из Hibiscus sabdariffa . Дж. Суперкрит. Жидкости. 2019;147:213–221. doi: 10.1016/j. supflu.2018.11.005. [CrossRef] [Google Scholar]
supflu.2018.11.005. [CrossRef] [Google Scholar]
47. Panja P. Зеленые методы экстракции пищевых полифенолов из растительных материалов. Курс. мнение Пищевая наука. 2017;23:173–182. doi: 10.1016/j.cofs.2017.11.012. [Перекрестная ссылка] [Академия Google]
48. Энрике П., Хелена Д., Рибейро Б., Амадеу Г., Витали Л., Хенсе Х. Экстракция биоактивных соединений из кожуры фейхоа ( Acca sellowiana (O. Berg) Burret) с помощью низких и высоких — техники давления. Дж. Суперкрит. Жидкости. 2019;145:219–227. doi: 10.1016/j.supflu.2018.12.016. [CrossRef] [Google Scholar]
49. Da Silva Francischini D., Lopes A.P., Segatto M.L., Stahl A.M., Zuin V.G. Разработка и применение экологичных и устойчивых аналитических методов извлечения флавоноидов из Пассифлора отходы. BMC хим. 2020;14:56. doi: 10.1186/s13065-020-00710-5. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
50. Октавьянти Н.Д., Картини К., Хадият М.А., Рахмавати Э., Виджая А.С., Хаюн Х. , Муним А. Проект экологически чистой добычи для усиление флавоноидных соединений из цветков Ixora javanica с использованием глубокого эвтектического растворителя. Р. Соц. Открытая наука. 2020;7:201116. doi: 10.1098/rsos.201116. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
, Муним А. Проект экологически чистой добычи для усиление флавоноидных соединений из цветков Ixora javanica с использованием глубокого эвтектического растворителя. Р. Соц. Открытая наука. 2020;7:201116. doi: 10.1098/rsos.201116. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
51. Скарпалезос Д., Деци А. Глубокие эвтектические растворители как среды экстракции ценных флавоноидов из природных источников. заявл. науч. 2019;9:4169. doi: 10.3390/app9194169. [CrossRef] [Google Scholar]
52. Вукикс В., Гуттман А. Структурная характеристика флавоноидных гликозидов с помощью многоступенчатой масс-спектрометрии. Масс-спектр. 2010; 29:1–16. doi: 10.1002/mas.20212. [PubMed] [CrossRef] [Google Scholar]
53. Kang J., Hick L., Price W.E. Исследование фрагментации изофлавона при отрицательной ионизации электрораспылением с помощью масс-спектрометрии с ионной ловушкой MSn и масс-спектрометрии с тройным квадруполем. Быстрое общение. Масс-спектр. 2007; 21: 857–868. doi: 10.1002/rcm.2897. [PubMed] [CrossRef] [Google Scholar]
doi: 10.1002/rcm.2897. [PubMed] [CrossRef] [Google Scholar]
54. Boukhalkhal S., Gourine N., Pinto DCGA, Silva A.M.S., Yousfi M. UHPLC-DAD-ESI-MS n профилирование изменчивости фенольных составляющих Artemisia campestris Популяции L. произрастают в Алжире. Биокатал. Агр. Биотехнолог. 2020;23:101483. doi: 10.1016/j.bcab.2019.101483. [CrossRef] [Google Scholar]
55. Ye M., Yang W.-Z., Liu K.-D., Qiao X., Li B.-J., Cheng J., Feng J., Guo D. .-А., Чжао Ю.-Ю. Характеристика флавоноидов в Millettia nitida вар. hirsutissima по данным ВЭЖХ/DAD/ESI-MS n . Дж. Фармацевт. Анальный. 2012;2:35–42. doi: 10.1016/j.jpha.2011.09.009. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
56. Simões M.A.M., Pinto D.C.G.A., Neves B.M.R., Silva A.M.S. Флавоноидный профиль Genista tridentate L., вида, традиционно используемого для лечения воспалительных процессов. Молекулы. 2020;25:812. doi: 10,3390/молекулы25040812. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
57. Мабри Т.Дж., Маркхэм К.Р., Томас М.Б. Реагенты и методики для ультрафиолетового спектрального анализа флавоноидов. В: Мабри Т.Дж., Маркхэм К.Р., Томас М.Б., редакторы. Систематическая идентификация флавоноидов. Спрингер; Berlin/Heidelberg, Germany: 1970. [Google Scholar]
58. Цанова-Савова С., Денев П., Рибарова Ф. Флавоноиды в пищевых продуктах и их роль в здоровом питании. Диетический микроб. Здоровье. 2018: 165–198. doi: 10.1016/B978-0-12-811440-7.00007-7. [Перекрестная ссылка] [Академия Google]
59. Gonzales G.B., Smaghe G., Grootaert C., Zotti M., Raes K., Van Camp J. Взаимодействие флавоноидов во время пищеварения, всасывания, распределения и метаболизма: последовательный подход, основанный на взаимосвязях структура-активность/свойство в изучение биодоступности и биоактивности. Препарат Метаб. 2015; 47:175–190. doi: 10.3109/03602532.2014.1003649. [PubMed] [CrossRef] [Google Scholar]
60. Сандовал В., Санс-Ламора Х., Ариас Г., Марреро П.Ф., Аро Д., Релат Дж. Метаболическое влияние потребления флавоноидов при ожирении: от центрального к периферическому . Питательные вещества. 2020;12:2393. doi: 10.3390/nu12082393. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Сандовал В., Санс-Ламора Х., Ариас Г., Марреро П.Ф., Аро Д., Релат Дж. Метаболическое влияние потребления флавоноидов при ожирении: от центрального к периферическому . Питательные вещества. 2020;12:2393. doi: 10.3390/nu12082393. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
61. Калим М., Ахмад А. Флавоноиды как нутрицевтики. В: Грумезеску М.А., Холбан А.М., ред. Терапевтические, пробиотические и нетрадиционные продукты. Академическая пресса; Кембридж, Массачусетс, США: 2018. стр. 137–155. [CrossRef] [Google Scholar]
62. Чумарнян Л., Милачу М.В., Рункан О., Веса С.К., Рачис А.Л., Негреан В., Перне М.Г., Донка В.И., Алексеску Т.Г.М., Пара И. и др. Эффекты флавоноидов при сердечно-сосудистых заболеваниях. Молекулы. 2020;25:4320. дои: 10.3390/молекул 25184320. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
63. Ginwala R., Bhavsar R., Chigbu D.G.I., Jain P., Khan Z.K. Потенциальная роль флавоноидов в лечении хронических воспалительных заболеваний с особым акцентом на противовоспалительную активность апигенина. Антиоксиданты. 2019;8:35. doi: 10.3390/antiox8020035. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Антиоксиданты. 2019;8:35. doi: 10.3390/antiox8020035. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
64. Кошик С., Шьям Х., Агарвал С., Шарма Р., Наг Т.С., Двиведи А.К., Балапуре А.К. Генистеин потенцирует центрохроман-индуцированную противоопухолевую активность при раке молочной железы посредством деактивации PI3K/Akt и зависимой от АФК индукции апоптоза. Жизнь наук. 2019;239:117073. doi: 10.1016/j.lfs.2019.117073. [PubMed] [CrossRef] [Google Scholar]
65. Jin S., Zhang Q.Y., Kang X.M., Wang J.X., Zhao W.H. Дайдзеин индуцирует апоптоз клеток рака молочной железы MCF-7 через митохондриальный путь. Энн. Онкол. 2010; 21: 263–268. doi: 10.1093/annonc/mdp499. [PubMed] [CrossRef] [Google Scholar]
66. Zaidun N.H., Thent Z.C., Latiff A.A. Борьба с нарушениями окислительного стресса с помощью цитрусовых флавоноидов: Нарингенин. Жизнь наук. 2018;208:111–122. doi: 10.1016/j.lfs.2018.07.017. [PubMed] [CrossRef] [Академия Google]
67. Pourakbari R., Taher S. M., Mosayyebi B., Ayoubi-Joshaghani M.H., Ahmadi H., Aghebati-Maleki L. Значение гликозилированных соединений и их противораковое действие. Междунар. Дж. Биол. макромол. 2020;163:1323–1332. doi: 10.1016/j.ijbiomac.2020.06.281. [PubMed] [CrossRef] [Google Scholar]
M., Mosayyebi B., Ayoubi-Joshaghani M.H., Ahmadi H., Aghebati-Maleki L. Значение гликозилированных соединений и их противораковое действие. Междунар. Дж. Биол. макромол. 2020;163:1323–1332. doi: 10.1016/j.ijbiomac.2020.06.281. [PubMed] [CrossRef] [Google Scholar]
68. Тавсан З., Каяли Х.А. Флавоноиды продемонстрировали противораковое действие на раковые клетки яичников: участие активных форм кислорода, апоптоз, клеточный цикл и инвазия. Биомед. Фармацевт. 2019;116:109004. doi: 10.1016/j.biopha.2019.109004. [PubMed] [CrossRef] [Google Scholar]
69. Liang T., Guan R., Wang Z., She H., Xia Q., Liu M. Сравнение противораковой и антиоксидантной активности цианидина-3- O -глюкозид липосомы и цианидин-3- O -глюкозид в клетках Caco-2 in vitro. RSC Adv. 2017;7:37359–37368. doi: 10.1039/C7RA06387C. [CrossRef] [Google Scholar]
70. Rolnik A., Zuchowski J., Stochmal A., Olas B. Производные кверцетина и кемпферола, выделенные из надземных частей Lens culinaris Medik в качестве модуляторов функций тромбоцитов. инд. урожая. Произв. 2020;152:112536. doi: 10.1016/j.indcrop.2020.112536. [CrossRef] [Google Scholar]
инд. урожая. Произв. 2020;152:112536. doi: 10.1016/j.indcrop.2020.112536. [CrossRef] [Google Scholar]
71. Zhang Z., Liao P., Zhu M., Li W., Hu D., Chen L., Guan S. модель мышей с перегрузкой. Клетка. Физиол. Биохим. 2017;41:849–864. doi: 10.1159/000459708. [PubMed] [CrossRef] [Google Scholar]
72. Кэссиди А. Берри Потребление антоцианов и здоровье сердечно-сосудистой системы. Мол. Асп. Мед. 2018;61:76–82. doi: 10.1016/j.mam.2017.05.002. [PubMed] [CrossRef] [Академия Google]
73. Гурняк И., Бартошевский Р., Круличевский Дж. Всесторонний обзор антимикробной активности растительных флавоноидов. Фитохим. 2019; 18:241–272. doi: 10.1007/s11101-018-9591-z. [CrossRef] [Google Scholar]
74. Фатима А., Рао Дж. Р. Избирательная токсичность катехина — природного флавоноида по отношению к бактериям. заявл. микробиол. Биотехнолог. 2016; 100:6395–6402. doi: 10.1007/s00253-016-7492-x. [PubMed] [CrossRef] [Google Scholar]
75. Xu X., Zhou X.D., Wu C.D. Галлат эпигаллокатехина чайного катехина ингибирует Streptococcus mutans образование биопленок за счет подавления генов gtf. Арка Оральный биол. 2012; 57: 678–683. doi: 10.1016/j.archoralbio.2011.10.021. [PubMed] [CrossRef] [Google Scholar]
Арка Оральный биол. 2012; 57: 678–683. doi: 10.1016/j.archoralbio.2011.10.021. [PubMed] [CrossRef] [Google Scholar]
76. Al Aboody M.S., Mickymaray S. Противогрибковая эффективность и механизмы действия флавоноидов. Антибиотики. 2020;9:45. doi: 10.3390/антибиотики45. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
77. Tsang P.W.-K., Chau K.-Y., Yang H.-P. Байкалеин проявляет ингибирующее действие на активность энергозависимой эффлюксной помпы в не- albicans Candida грибы. Дж. Чемотер. 2014;27:61–62. doi: 10.1179/1973947814Y.0000000177. [PubMed] [CrossRef] [Google Scholar]
78. Lagrouh F., Dakka N., Bakri Y. Противогрибковая активность марокканских растений и механизм действия вторичных метаболитов растений. Дж. Мед. Микол. 2017;27:303–311. doi: 10.1016/j.mycmed.2017.04.008. [PubMed] [CrossRef] [Google Scholar]
79. Оливейра М.Р.Д., Набави С.Ф., Даглиа М., Растрелли Л., Набави С.М. Галлат эпигаллокатехина и митохондрии — история жизни и смерти. Фармакол. Рез. 2016;104:70–85. doi: 10.1016/j.phrs.2015.12.027. [PubMed] [CrossRef] [Академия Google]
Фармакол. Рез. 2016;104:70–85. doi: 10.1016/j.phrs.2015.12.027. [PubMed] [CrossRef] [Академия Google]
80. Кассетта А., Стоян Дж., Крастанова И., Кристан К., Брунсколе Швегель М., Ламба Д., Ланишник Рижнер Т. Структурные основы ингибирования 17β-гидроксистероидных дегидрогеназ фитоэстрогенами: случай грибкового 17β -HSDкл. Дж. Стероид Биохим. Мол. биол. 2017; 171:80–93. doi: 10.1016/j.jsbmb.2017.02.020. [PubMed] [CrossRef] [Google Scholar]
81. Лалани С., Пох К.Л. Флавоноиды как противовирусные средства для вирусов энтеровируса A71 (EV-A71). 2020;12:184. doi: 10.3390/v12020184. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
82. Хайме М.М.Ф., Редько Ф., Мускетти Л.В., Кампос Р.Х., Мартино В.С., Кавалларо Л.В. Противовирусная активность растительных экстрактов лекарственных растений сложноцветных in vitro. Вирол. Дж. 2013; 10:245. doi: 10.1186/1743-422X-10-245. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
83. Sithisarn P., Michaelis M.

 Если есть некоторые расхождения в том, какие растения должны расти, студентов попросят доказать свои идеи, создав эксперимент для проверки своей теории. Например, если учащиеся не уверены, нужна ли растениям почва для роста, они должны провести эксперимент, исследуя, что происходит с растением, растущим без почвы, и растением, растущим с почвой.
Если есть некоторые расхождения в том, какие растения должны расти, студентов попросят доказать свои идеи, создав эксперимент для проверки своей теории. Например, если учащиеся не уверены, нужна ли растениям почва для роста, они должны провести эксперимент, исследуя, что происходит с растением, растущим без почвы, и растением, растущим с почвой.