Содержание
ИССЛЕДОВАНИЕ ЭФИРНОГО МАСЛА ШИШКОЯГОД JUNIPERUS COMMUNIS L. РАЗЛИЧНОГО ПРОИСХОЖДЕНИЯ В РАМКАХ НАУЧНОГО НАПРАВЛЕНИЯ «ФАРМАЦЕВТИЧЕСКИЙ РЕМЕЙК»
Введение. Доказано, что лекарственные растения и лекарственные продукты на их основе зачастую способны заменить синтетические аптечные препараты. И при этом в значительной степени снижен вред здоровью человека.
Лекарственные растения имеют сложный химический состав, чем объясняется разнообразие их лечебного действия. Биологически активные вещества растений всегда соседствуют с другими, способствующими усвоению первых в организме человека [1].
По-прежнему актуальными остаются научные исследования в области натуроцевтики, проблемы получения и представления на потребительском рынке новых препаратов из лекарственных растений, как признанных официальной медициной, так и используемых в народной.
Наиболее широко используются человечеством эфиромасличные растения, т.к. эфирномасличная флора насчитывает около 3000 видов растений, большая часть которых приходится на сухие субтропики. В списке отечественных фармакопейных растений также достаточно много объектов, у которых действующими являются эфирные масла. Одним из наиболее известных является можжевельник обыкновенный – Juniperuscommunis L.
В списке отечественных фармакопейных растений также достаточно много объектов, у которых действующими являются эфирные масла. Одним из наиболее известных является можжевельник обыкновенный – Juniperuscommunis L.
В доступных изданиях по фармакологии XIX века присутствуют подробные данные о самих растениях и нозологиях, при которых можно использовать можжевельники, а также информация о всквозможных экстемпоральных лекарственных формах на их основе. Так, в книге «Основы фармакологии и рецептуры» профессора Казанского университета И.М. Догеля (рисунок 1) упоминаются водная вытяжка и наливка из плодов можжевельника обыкновенного [2].
Рисунок 1 – Страницы книги И.М. Догеля «Основы фармакологии
и рецептуры» 1900 года издания типографии Карла Риккера
Fig. 1. Book pages from “The Fundamentals of Pharmacology and recipes” by I.M. Dogiel, 1900 edition, Karl Ricker Publishing House
В переводной книге «Фармакология и токсикология» авторского коллектива из Австрии под редакцией академика В. В. Пашутина (рисунок 2) можжевельники обыкновенный рассмотрен очень подробно. Приведены известные на то время ботанические, фитохимические и исторические данные. Последние на наш взгляд, не соответствуют действительности, т.к. сказано, что в древности можжевельники не играли никакой роли как лекарственные растения [3].
В. Пашутина (рисунок 2) можжевельники обыкновенный рассмотрен очень подробно. Приведены известные на то время ботанические, фитохимические и исторические данные. Последние на наш взгляд, не соответствуют действительности, т.к. сказано, что в древности можжевельники не играли никакой роли как лекарственные растения [3].
Рисунок 2 – Страницы книги «Фармакология и токсикология»
под редакцией академика В.В. Пашутина 1895 года издания
Fig. 2. Book pages from “Pharmacology and Toxicology” edited by an academician V.V. Pashutin, 1895 edition
Из лекарственных средств в этой книге описаны сок (жидкий экстракт) можжевеловых ягод, можжевеловый спирт, можжевеловая мазь, масло можжевеловых ягод и пригорелое масло.
В переводных с немецкого сочинениях доктора медицины Ацерсвальда «Целебные травы и растения» можжевельник называется дроздовым деревцом, венце-ягодной тростью и полевой кипариссой (рисунок 3). Здесь, как и в других источниках, дана информация о можжевельнике обыкновенном.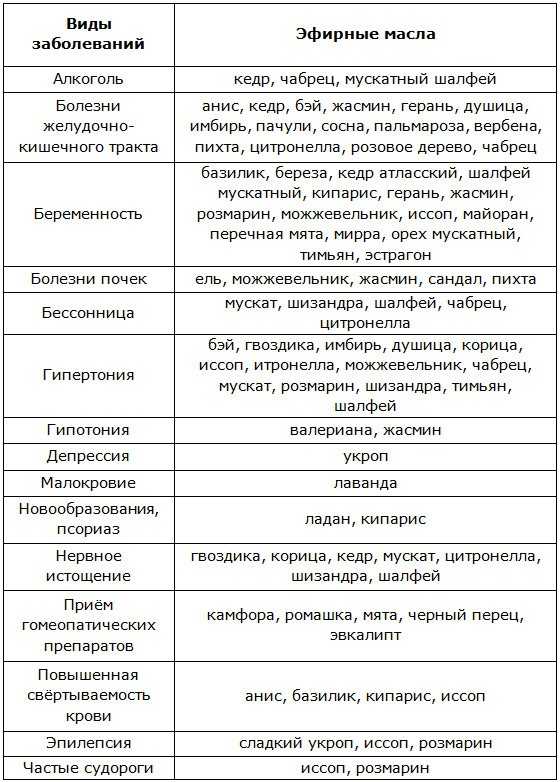 Предлагаемые автором варианты применения растительного сырья ближе к народной рецептуре. Так, предлагается использовать в качестве мочегонного средства холодный чай из ягод можжевельника обыкновенного, а также морс и пиво [4].
Предлагаемые автором варианты применения растительного сырья ближе к народной рецептуре. Так, предлагается использовать в качестве мочегонного средства холодный чай из ягод можжевельника обыкновенного, а также морс и пиво [4].
Рисунок 3 – Фрагменты книги Б. Ауэрсвальда «Целебные травы и растения»
1910 года издания, перевод с 5-го немецкого очень распространенного
и улучшенного издания
Fig. 3. Fragments from B. Auerswald’s book “Healing herbs and plants,”
1910 edition, translated from the 5th German improved edition
Эфирное масло J. communis L. в значительных количествах содержится в надземных частях – шишкоягодах и хвое, меньше – в коре, древесине и корнях. Причем химический состав между различными частями растения характеризуется качественными и количественными различиями. В качестве фармакопейного объекта используются шишкоягоды растения [5].
Биологическая активность шишкоягод J. communis L.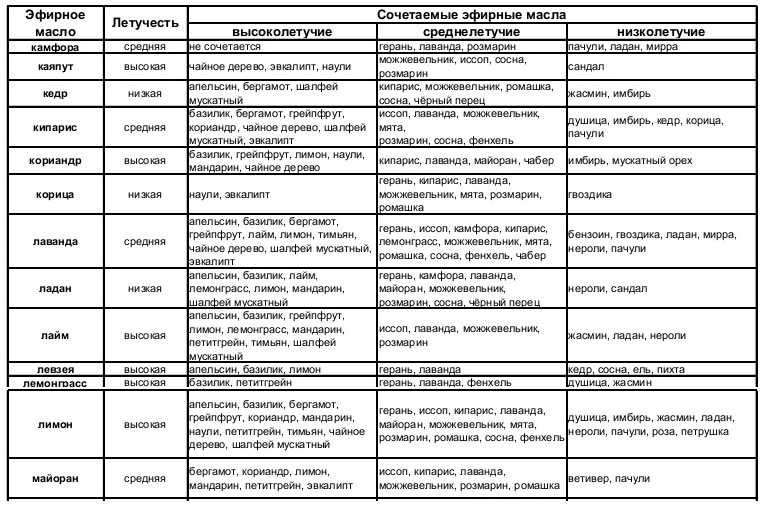 в значительной мере обусловлена эфирным маслом, которое в основном и определяет диуретический, желчегонный, антимикробный и отхаркивающий эффекты растения. Выделяясь через почки, эфирное масло умеренно раздражает их, оказывая диуретическое действие, и одновременно дезинфицирует мочевыводящие пути. Кроме того, оно усиливает секрецию бронхиальных желёз, тем самым, способствуя разжижению секрета, а также облегчает эвакуацию желчи из желчного пузыря [6, 7].
в значительной мере обусловлена эфирным маслом, которое в основном и определяет диуретический, желчегонный, антимикробный и отхаркивающий эффекты растения. Выделяясь через почки, эфирное масло умеренно раздражает их, оказывая диуретическое действие, и одновременно дезинфицирует мочевыводящие пути. Кроме того, оно усиливает секрецию бронхиальных желёз, тем самым, способствуя разжижению секрета, а также облегчает эвакуацию желчи из желчного пузыря [6, 7].
Эфирное масло и дистилляты плодов J. communis L. содержат более 130 компонентов в составе которого преобладают бициклические углеводороды: α-пинен, мирцен, сабинен, лимонен и β-пинен [6, 7,].
В ряде экспериментов, в частности на модели дрожжевых грибов было показано, что эфирное масло J. communis L. обладает сильной антиоксидантной активностью благодаря блокированию окислительных процессов в клетках путем увеличения активности антиоксидантных ферментов супероксиддисмутазы, каталазы и глутатионпероксидазы [8, 9, 10].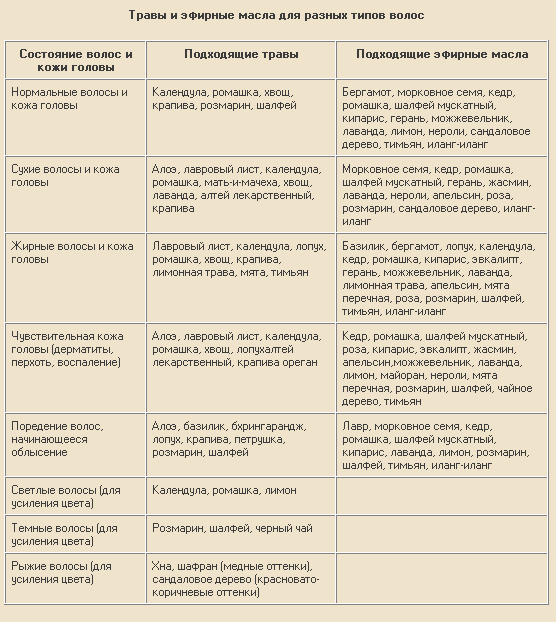
Известно, что состав эфирного масла, даже внутри одного вида подвержен значительной вариабельности, что связано в первую очередь с экологическими особенностями произрастания растения: химический состав почвы, влажность воздуха, освещённость и т.д. [6, 10] Поэтому и состав эфирного масла у разных экотопов может быть не одинаковым. Однако существует ряд маркерных компонентов, которые обусловливают принадлежность эфирного масла к определенному растительному объекту и кроме того характеризуют их качество.
Цель исследования — определение маркерных компонентов эфирного масла плодов J. communis L. для разработки новых норм качества лекарственного растительного сырья и тем самым продолжение дальнейших исследований растений рода Junipers как источника билогически активных соединений в направлении создания новых лекарственных форм.
Материалы и методы. В качестве объектов исследования использованы образцы эфирного масла J. communis L., полученные из сырья, собранного в разных регионах России: Саратовской, Московской, Ленинградской и Новосибирской областей.
communis L., полученные из сырья, собранного в разных регионах России: Саратовской, Московской, Ленинградской и Новосибирской областей.
Для надёжного химического анализа такого сложного объекта как эфирные масла требуются гибридные методы анализа, сочетающие в себе как возможность разделения многокомпонентной системы, так и их достоверную детекцию. Поэтому в качестве аналитического инструмента нами использован метод газовой хроматографии – масс-спектрометрии. Измерение проводили на приборе хромато-масс-спектрометр модели GCMS-QP2010 Ultra, фирма-изготовитель «Shimadzu», Япония, регистрационный номер №46022-10. Тип средств измерений утверждён приказом Федерального агентства по техническому регулированию и метрологии от 28 декабря 2010 г. №5484.
Источник ионов масс-спектрометра работает в режиме электронного удара. Разделение ионов осуществляется квадрупольным масс-фильтром, детектирование – вторичным электронным умножителем с обращённым динодом. Детектирование может быть проведено в режимах селективного ионного детектирования (SIM), или по полному ионному току (SCAN) или в режиме одновременной регистрации SIM/ SCAN.
Детектирование может быть проведено в режимах селективного ионного детектирования (SIM), или по полному ионному току (SCAN) или в режиме одновременной регистрации SIM/ SCAN.
Разделение проводили на колонке:
Zebron ZB-5MS 30 m L × 0,25 mm ID × 0,25 μm df;
Жидкая фаза: 5%-polysilarylene-95 polydimethylsiloxane;
Температурные пределы: от -60 С° до 325/350 С°;
Серийный номер № 238059.
Условия хроматографирования:
Газ-носитель – гелий с постоянным потоком — 0,7 мл/мин;
Анализ осуществлялся в режиме программируемых температур:
Температура колонки программировалась в диапазоне от 70 С° (изотерма 2 мин.) – 230 С° (изотерма 5 мин). Скорость подъёма температуры 3 С°/мин;
Температура испарителя – 240С°;
Температура ионного источника – 250С°;
Температура интерфейса – 250С°;
Режим ввода пробы — с делением потока (Splitratio 1/50) – 1,5 мин;
Напряжение на детекторе – 0,7 — 0,84 кВ;
Поток эмиссии – 60 µА;
Объём вводимой пробы – 1µl.
Детектирование осуществляли в режиме полного ионного тока (SCAN) в диапазоне m/z 70 – 350 Da, со скоростью сканирования 769 и результирующим временем 0,4 сек. Расшифровку компонентного состава эфирных масел J. communis L. проводили с использованием библиотечной базы данных масс-спектров NIST 11.
Результаты исследования и их обсуждение. Результаты хроматографирования эфирных масел можжевельника из разных регионов Российской Федерации представлены на рисунках 4-7.
Рисунок 4 – Хроматограмма образца эфирного масла J. communis L. из Саратовской области
Fig. 4. Chromatogram of the essential oil sample of J. communis L. from Saratov region
Рисунок 6 – Хроматограмма образца эфирного масла J. communis L. из
Ленинградской области
Fig. 6. The chromatogram of the essential oil sample of J. communis L.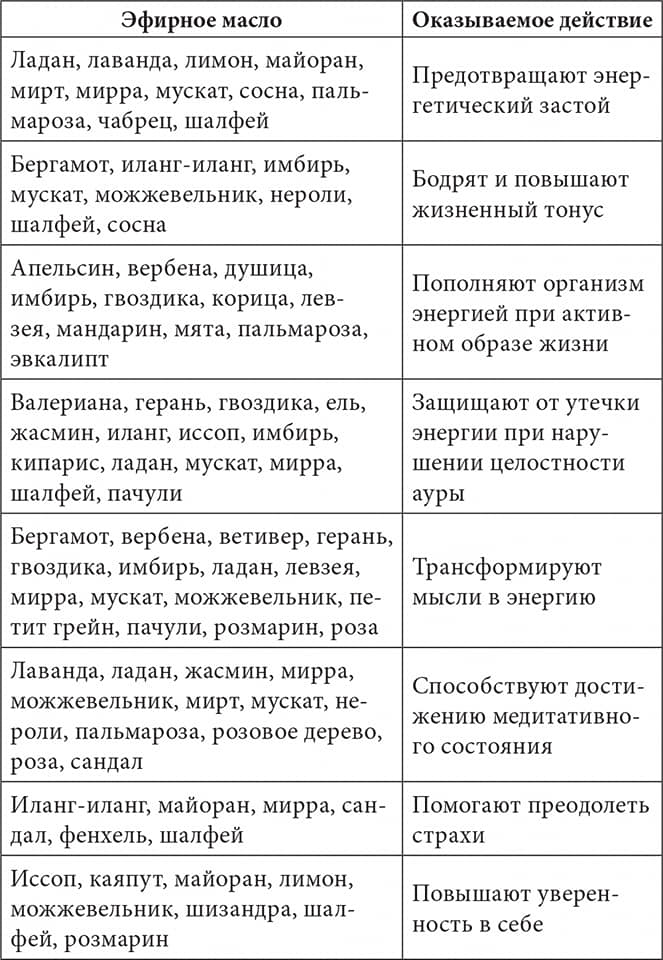 from
from
Leningrad region
Рисунок 7 – Хроматограмма образца эфирного масла J. communis L. из
Новосибирской области
Fig. 7. The chromatogram of the essential oil sample of J. communis L. from
Novosibirsk region
Результаты расшифровки компонентного состава эфирного масла J. communis L. приведены в таблице 1.
Таблица 1
Химический состав эфирного масла шишкоягод J. communis L.
из разных регионов России
Table 1
The essential oil chemical composition of J. communis L. cone
from different regions of Russia
Индекс удерживания, IR | Базовый пик, m/z | Идентифицированный компонент | Содержание компонента, % | |||
Саратовская область | Московская область | Ленинградская область | Новосибирская область | |||
510 | 93 | A-пинен | 33,28 | 57,70 | 41,7 | 59,81 |
550 | 9 | Камфен | 1,12 | 2,0 | 0,83 | 1,70 |
610 | 93 | В-пинен | 8,50 | 15,02 | 12,20 | 14,84 |
650 | 119 | О-цимен | 1,65 | 2,14 | 1,30 | 1,72 |
730 | 68 | А-лимонен | 1,70 | 2,80 | 1,70 | 2,50 |
750 | 43 | Цинеол | 0,88 | — | — | — |
980 | 67 | А-пинен оксид | 0,597 | — | — | — |
1020 | 41 | (α-пинен-4-ол) | 0,42 | — | — | 0,14 |
1050 | 81 | Б-фенхол | 0,19 | — | — | 0,25 |
1080 | 121 | А-терпинолен | — | 1,18 | — | 0,65 |
1130 | 41 | Пинокарвеол | 0,47 | — | — | — |
1270 | 71 | Терпинен-4-ол | 1,38 | 1,41 | 1,41 | 2,0 |
1310 | 59 | А-терпинеол | 1,6 | 1,44 | 1,44 | 1,73 |
1505 | 121 | А-терпенилацетат | 1,73 | — | — | — |
1660 | 95 | Борнилацетат | 32,5 | — | — | 0,40 |
1800 | 93 | Каранол | 0,90 | — | — | — |
1960 | 161 | А-лонгипинен | 0,20 | 0,30 | — | — |
2080 | 41 | Лонгифолен | 0,90 | 1,30 | 1,30 | 1,14 |
2110 | 93 | Б-кариофиллен | 0,80 | 2,0 | 1,44 | 2,20 |
*- жирным выделены специфичные компоненты эфирного масла J. communis L.
communis L.
Результаты, представленные в таблице 1, свидетельствуют о достаточно стабильном компонентном составе эфирного масла J. communis L., однако количественные показатели различных компонентов в разных регионах отличаются. При этом в составе эфирного масла можно выделить 4-х характерные групп терпенов: бициклические монотерпены, моноциклические монетерпены, моноциклические монотерпеновые спирты и бициклические сесквитерепны. Доминирующей группой являются бициклические монотерпены, а именно α- и β-пинены и камфен с значительным превалированием первого. Содержание α-пинена в эфирном масле в зависимости от региона варьирует от 30,0 до 60,0%. Концентрация β-пинена колеблется в диапазоне 8,0 – 15,0%. К минорным компонентам эфирного масла J. communis L. следует отнести моноциклические монотерпены в частности о-цимен и α-лимонен, моноциклические спирты — терпинен-4-ол, α-терпинеол, а также бициклические сесквитерепны – лонгифолен и кариофиллен. Такой компонентый состав эфирного масла J. communis L. можно считать маркерным, что позволит отличить его от любого другого эфирного масла. Остальные компоненты эфирного масла находятся в следовых количествах. Борнилацетат найден только в одном образце эфирного масла, поэтому его не следует относить к специфическим компонентам.
Такой компонентый состав эфирного масла J. communis L. можно считать маркерным, что позволит отличить его от любого другого эфирного масла. Остальные компоненты эфирного масла находятся в следовых количествах. Борнилацетат найден только в одном образце эфирного масла, поэтому его не следует относить к специфическим компонентам.
Полученные результаты могут быть использованы для объективной оценки норм качества фармакопейного лекарственного растительного сырья – шишкоягод (плодов) можжевельника. Дело в том, что в действующей фармакопейной статье на плоды можжевельника в качестве одного из нормируемых качество показателей, является содержание эфирного масла, определяемое весо-объёмным способом, предусматривающим использование метода гидродистилляции. Однако такой подход, учитывая современные мировые тенденции фармацевтической науки, в настоящее время не может быть признан удовлетворительным, поскольку не учитывает состав эфирного масла. Поэтому полученные нами результаты определения качественного и количественного состава эфирного масла плодов J. communis L. могут быть использованы для включения в нормативную документацию на указанное лекарственное растительное сырьё.
communis L. могут быть использованы для включения в нормативную документацию на указанное лекарственное растительное сырьё.
Заключение
Под термином «Фармацевтический ремейк» предложено понимать комплекс традиционных и инновационных технологических, аналитических и фармакологических операций (моделей), приводящих к возрождению ранее известных и ныне не используемых лекарственных составов и форм [1].
Известно, что количество лекарственных растений достигает 20 тысяч, однако официальной медициной пока используется около 300. В последние десятилетия в связи с появлением новой нозологической формы – «лекарственной болезни» – актуальность применения препаратов из растительного сырья возрастает непомерно.
Путь введения в оффицинальную рецептуру лекарственных форм на основе биологически активных соединений ранее известных в официальной и народной медицине лекарственных растений предоставляет в распоряжение разработчиков практически неограниченные возможности. Данный путь расширения номенклатуры лекарственных средств выглядит достаточно рациональным и малозатратным, т.к. нет необходимости заниматься полномасштабным научным поиском.
Данный путь расширения номенклатуры лекарственных средств выглядит достаточно рациональным и малозатратным, т.к. нет необходимости заниматься полномасштабным научным поиском.
Все представленные в данной статье и иные исторические источники рассматривали данный наиболее используемый медициной вид можжевельника – можжевельник обыкновенный – с позиций лекарствоведения значительно шире, нежели это принято сегодня. Причем существующие прописи не оставляют место сомнениям на счет полагаемых фармакологических эффектов. Данные умозаключения дают основу для более широкого изучения можжевельника обыкновенного и всего рода Junirerus с позиций фармакологии, фармацевтической технологии и фитохимического анализа.
Приведенные материалы о химии можжевельника обыкновенного дают дополнительный инструментарий для реализации небольшого фрагмента целевых научных исследований.
ФГБОУ ВО ПГФА Минздрава России
Пермская государственная
фармацевтическая академия
Для слабовидящих
youtube.com/embed/XWLYPhOK6RA»>
Осторожно, грипп!!!
…
Правила здоровья
…
еще …
Наши новости
ПГФА заключила соглашение с группой компаний «Эдвансд»
22 декабря 2022
ПГФА развивает международное сотрудничество
18 ноября 2022
еще …
Наши события
ПГФА и группа российских университетов «РАКУС» наградили иностранных студентов-активистов
30 декабря 2022
Рождественнский вечер сказок и песен на английском языке
29 декабря 2022
еще . ..
..
Конференции, олимпиады, форумы…
Приглашение к участию в Международном литературном конкурсе «Живая латынь»
09 января 2023
I международная научно-практическая Олимпиада по философии для студентов медвузов
15 декабря 2022
Награждение победителей Олимпиады РКИ
15 декабря 2022
еще …
Новости спорта
«Медики тоже играют в игры»
12 декабря 2022
Открытие киберспортивного клуба ПГФА
07 декабря 2022
Документальный фильм об истории Российского студенческого спортивного союза
29 ноября 2022
еще …
Button
Ученый совет
Научный полк
Обращение советов ректоров вызов Пермского края
Мисс Фармация-2019
Галерея новостей
День открытых дверей
Информация об аккредитации специалистов
Видеообзор — введение в профессию
Ректор ПГФА Алексей Юрьевич Турышев рассказывает о перспективах специальности и приёме в 2019 году
В ПГФА имеется 200 бюджетных мест для абитуриентов. Трудоустройство выпускников ПГФА почти 100 %. ПГФА обеспечивает половину кадровой потребности отрасли. Провизоры — аналитики, технологи, организаторы. Обеспечивается полный цикл обучения от создания молекулы до разработки лекарственной формы. Эфир 26 февраля 2019 года
Трудоустройство выпускников ПГФА почти 100 %. ПГФА обеспечивает половину кадровой потребности отрасли. Провизоры — аналитики, технологи, организаторы. Обеспечивается полный цикл обучения от создания молекулы до разработки лекарственной формы. Эфир 26 февраля 2019 года
Смотреть все видеообзоры о професии
Условия проживания студентов в общежитии № 2 (более новое первое общежитие не показано). Съёмка 2016 года.
Имеющиеся у ПГФА два общежития неизменно входят в десятку лучших общежитий образовательных учреждений города Перми. В общежитиях имеются столовая, кухни на каждом этаже, библиотека, спортзал, бытовая, душевая и постирочная комнаты (общежитие № 1 новее).
Первокурсники на лабораторных занятиях по физике в ПГФА. Съёмка 25 февраля 2019 года
На первом курсе студенты изучают биологию, физиологию, математику, физику, неорганическую химию, физическую химию, латинский язык, информатику, экономическую теорию, историю. Основной предмет — химия. За годы учёбы её будет 9 видов.
Впечатления первокурсника
после двух месяцев учёбы в 2018 году.
Ректор
Проректоры
Помощник ректора по воспитательной работе
Ученый совет
Административно — управленческие подразделения
Ведущий юрисконсульт
Учебные подразделения
Кафедры
Научные подразделения
Корпуса и общежития
Отдел качества
Региональный испытательный центр «Фарматест»
Полиграфический отдел
Стоматологическая клиника
Столовая
Здравпункт
Музей
Профком сотрудников
Профком студентов
Социально-психологическая служба
Растительные ароматические вещества — масла, которые необходимы по определенной причине
Предоставлено приглашенным блоггером Риком Селлано
Фундаментальное начало с основами
5
для эфирных масел. Фармакогнозия — это область фармации, изучающая растения, в частности их терапевтическое и медицинское применение. Эти знания привели к тому, что я на всю жизнь увлекся эфирными маслами. 22 апреля я узнал еще больше об этом любимом предмете на занятии Morris Arboretum, которое вел Меган Коппел, преподаватель естественного здоровья.
22 апреля я узнал еще больше об этом любимом предмете на занятии Morris Arboretum, которое вел Меган Коппел, преподаватель естественного здоровья.
Корни эфирных масел
Эфирные масла получили свое название из-за того, что они содержат «эссенцию» растения. Лавандовое масло является хорошим примером. Во время путешествия по Провансу, Франция, мне посчастливилось наблюдать за производством лавандового масла. Полученное эфирное масло, как говорят, обладает всеми свойствами лаванды, включая медицинские (антисептические, противовоспалительные), кулинарные (красители, ароматизаторы), косметические (успокаивающие, ароматизирующие) и ароматерапевтические (успокаивающие, расслабляющие). Эфирное масло лаванды обеспечивает все это, и это много хорошего для цветка, который также приятно видеть в саду или на открытом воздухе.
Цветы в масла
Те, кто занимается производством эфирных масел, собирают сырье (обычно цветы и части растений) с помощью кропотливо медленного процесса. Целые грузовики с цветами — как в случае с лавандой — проходят этапы дистилляции или экстракции, чтобы в конечном итоге получить относительно небольшое количество маслянистой эссенции. Розы представляют подобную проблему. Из-за любви всего мира к аромату розы рынок розового масла силен, а цена настоящего (по сравнению с синтетическим) розового масла высока.
Целые грузовики с цветами — как в случае с лавандой — проходят этапы дистилляции или экстракции, чтобы в конечном итоге получить относительно небольшое количество маслянистой эссенции. Розы представляют подобную проблему. Из-за любви всего мира к аромату розы рынок розового масла силен, а цена настоящего (по сравнению с синтетическим) розового масла высока.
Знакомство с основами из первых рук
В дендрарии Морриса Коппел помог нам принять участие в поучительной и заряжающей энергией программе эфирных масел. Мы взяли каплю или две масла мяты перечной в ладони, а затем добавили каплю или две масла дикого апельсина. Мы смешали их, потирая ладони. Затем мы сложили ладони и вдохнули смесь. Аромат не только открыл чувства, но и вызвал энергичное чувство удовлетворения. Затем мы втирали немного маслянистой смеси в мышцы задней части шеи, что создавало ощущение прохлады и расслабления. Наконец, мы натерли большим пальцем оставшуюся смесь и провели им по нёбу. Результат — чистое дыхание!
Неудивительно, что использование эфирных масел растет. Масла легко доступны, как и аксессуары, в том числе крошечные бутылочки с роллерами для использования на ходу. Диффузоры — это простые электрические приспособления, которые распыляют масло в виде тонкого тумана. Некоторые примечательные эфирные масла: базилик, бергамот, камфора, шалфей, гвоздика, эвкалипт, герань, имбирь, майоран, мускатный орех, апельсин, пачули, масло чайного дерева и иланг-иланг. Эти масла получают из цветов, листьев, кожуры, корней, семян и древесины. Независимо от источника, большинство эфирных масел обладают одинаковыми фундаментальными свойствами. Это вещества на масляной основе, которые плохо растворяются в воде (они гидрофобны) и являются летучими (они диффундируют в воздух, если их контейнер открыть).
Масла легко доступны, как и аксессуары, в том числе крошечные бутылочки с роллерами для использования на ходу. Диффузоры — это простые электрические приспособления, которые распыляют масло в виде тонкого тумана. Некоторые примечательные эфирные масла: базилик, бергамот, камфора, шалфей, гвоздика, эвкалипт, герань, имбирь, майоран, мускатный орех, апельсин, пачули, масло чайного дерева и иланг-иланг. Эти масла получают из цветов, листьев, кожуры, корней, семян и древесины. Независимо от источника, большинство эфирных масел обладают одинаковыми фундаментальными свойствами. Это вещества на масляной основе, которые плохо растворяются в воде (они гидрофобны) и являются летучими (они диффундируют в воздух, если их контейнер открыть).
The Internal Route
Koppel также рассказал о внутреннем использовании эфирных масел. Некоторые люди думают, что при нанесении на кожу эти масла системно всасываются, и этот процесс положительно влияет на внутренние органы и системы — древняя форма медицины, которая до сих пор используется некоторыми. Кроме того, есть очень осторожное использование эфирных масел, используемых в качестве веществ для приема внутрь. Такие масла, как орегано, которое Коппель называет «молотком эфирного масла в вашем ящике с инструментами», могут помочь повысить жизненный тонус. Естественно, вы должны согласовать все, что планируете принимать внутрь, со своим врачом, и что, как и лекарства, эфирные масла следует давать в «уменьшенных дозах» детям и пожилым людям.
Кроме того, есть очень осторожное использование эфирных масел, используемых в качестве веществ для приема внутрь. Такие масла, как орегано, которое Коппель называет «молотком эфирного масла в вашем ящике с инструментами», могут помочь повысить жизненный тонус. Естественно, вы должны согласовать все, что планируете принимать внутрь, со своим врачом, и что, как и лекарства, эфирные масла следует давать в «уменьшенных дозах» детям и пожилым людям.
Использование эфирных масел в домашних условиях
Ароматерапевтические смеси и полностью натуральные духи — не единственные продукты, в которых можно найти эфирные масла. Чистящие и другие товары для дома, особенно простые и безопасные, сделанные дома, прекрасно дополняются эфирными маслами. На самом деле Мэдисон-авеню десятилетиями рекламировала чистящие средства с запахом сосны и лимона; но они часто содержат синтетические ингредиенты. Сегодня, когда опасения по поводу синтетики и частой аллергии становятся все более распространенными, естественные чистящие средства становятся все более востребованными. Коппель объяснил, что мы можем легко приготовить их из таких ингредиентов, как уксус, пищевая сода и простое мыло. Идеальными эфирными маслами для добавления являются сосна, лимон, лайм, апельсин, вечнозеленое растение, огурец, лаванда и розмарин. В некоторых случаях лечебные свойства (например, дезинфекция розмарина) выполняют двойную функцию, добавляя больше, чем просто свежий аромат.
Коппель объяснил, что мы можем легко приготовить их из таких ингредиентов, как уксус, пищевая сода и простое мыло. Идеальными эфирными маслами для добавления являются сосна, лимон, лайм, апельсин, вечнозеленое растение, огурец, лаванда и розмарин. В некоторых случаях лечебные свойства (например, дезинфекция розмарина) выполняют двойную функцию, добавляя больше, чем просто свежий аромат.
Предостережение Emptor
Компания Koppel рассказала, на что обращать внимание при покупке эфирных масел, например на чистоту, эффективность и источник. Масла, одобренные для перорального применения (в дополнение к обычному наружному применению), должны иметь срок годности, хотя эфирные масла, хранящиеся в прохладном темном месте, могут оставаться свежими дольше.
Ценностное предложение
Добавление капельки или большего количества эфирных масел в вашу жизнь — это естественный и приятный способ почувствовать себя лучше и создать более безопасный дом. Тем не менее, наслаждение эфирными маслами, как и многие удовольствия, не самое дешевое занятие. Качественные масла, особенно такие, как ладан, кориандр и кардамон, могут быть дорогими, но, как и в случае с хорошим сыром, шампанским и трюфелями, небольшое количество эфирного масла имеет большое значение. Продолжайте смотреть в Morris Arboretum список образовательных программ для занятий по ряду предметов, чтобы питать свои чувства и расширять свой кругозор. Теперь это важно!
Качественные масла, особенно такие, как ладан, кориандр и кардамон, могут быть дорогими, но, как и в случае с хорошим сыром, шампанским и трюфелями, небольшое количество эфирного масла имеет большое значение. Продолжайте смотреть в Morris Arboretum список образовательных программ для занятий по ряду предметов, чтобы питать свои чувства и расширять свой кругозор. Теперь это важно!
Эфирные масла семи растений Lamiaceae и их антиоксидантная способность
1. Каденбах Б. Введение в митохондриальное окислительное фосфорилирование. В: Каденбах Б., изд. Митохондриальное окислительное фосфорилирование: гены, кодируемые ядром, регуляция ферментов и патофизиология. Спрингер; Нью-Йорк, штат Нью-Йорк, США: 2012. стр. 1–11. Достижения экспериментальной медицины и биологии. [Google Scholar]
2. Хуанг С., Ван Акен О., Шварцлендер М., Белт К., Миллар А.Х. Роль митохондриальных активных форм кислорода в клеточной передаче сигналов и реакции растений на стресс. Завод Физиол. 2016;171:1551–1559. doi: 10.1104/стр.16.00166. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
doi: 10.1104/стр.16.00166. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
3. Вранова Э., Атичартпонгкул С., Вильярроэль Р., Монтегю М.В., Инзе Д., Кэмп В.В. Комплексный анализ экспрессии генов в листьях Nicotiana Tabacum, акклиматизированных к окислительному стрессу. проц. Натл. акад. науч. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 2002;99:10870–10875. doi: 10.1073/pnas.152337999. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
4. Kruk J., Aboul-Enein H.Y., Kładna A., Bowser J.E. Окислительный стресс в биологических системах и его связь с патофизиологическими функциями: влияние физических Деятельность по клеточному окислительно-восстановительному гомеостазу. Свободный Радик. Рез. 2019;53:497–521. doi: 10.1080/10715762.2019.1612059. [PubMed] [CrossRef] [Google Scholar]
5. Sena L.A., Chandel N.S. Физиологические роли митохондриальных активных форм кислорода. Мол. Клетка. 2012; 48: 158–167. doi: 10.1016/j.molcel.2012.09.025. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
6. Фам-Хуи Л.А., Хе Х., Фам-Хуи К. Свободные радикалы, антиоксиданты при заболеваниях и здоровье. Междунар. Дж. Биомед. науч. IJBS. 2008; 4: 89–96. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Фам-Хуи Л.А., Хе Х., Фам-Хуи К. Свободные радикалы, антиоксиданты при заболеваниях и здоровье. Междунар. Дж. Биомед. науч. IJBS. 2008; 4: 89–96. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Рой Дж., Галано Дж.-М., Дюран Т., Геннек Дж.-Ю.Л., Ли Дж.К.-Ю. Физиологическая роль активных форм кислорода как стимуляторов естественной защиты. FASEB J. 2017; 31:3729–3745. doi: 10.1096/fj.201700170R. [PubMed] [CrossRef] [Google Scholar]
8. Fritz K.S., Petersen D.R. Обзор химии и биологии реактивных альдегидов. Свободный Радик. биол. Мед. 2013;59:85–91. doi: 10.1016/j.freeradbiomed.2012.06.025. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
9. Guéraud F., Atalay M., Bresgen N., Cipak A., Eckl P.M., Huc L., Jouanin I., Siems W., Учида К. Химия и биохимия продуктов перекисного окисления липидов. Свободный Радик. Рез. 2010;44:1098–1124. doi: 10.3109/10715762.2010.498477. [PubMed] [CrossRef] [Google Scholar]
10. Cecarini V., Gee J., Fioretti E. , Amici M., Angeletti M., Eleuteri A.M., Keller J.N. Окисление белков и клеточный гомеостаз: акцент на метаболизме. Биохим. Биофиз. Acta BBA мол. Сотовый рез. 2007; 1773: 93–104. doi: 10.1016/j.bbamcr.2006.08.039. [PubMed] [CrossRef] [Google Scholar]
, Amici M., Angeletti M., Eleuteri A.M., Keller J.N. Окисление белков и клеточный гомеостаз: акцент на метаболизме. Биохим. Биофиз. Acta BBA мол. Сотовый рез. 2007; 1773: 93–104. doi: 10.1016/j.bbamcr.2006.08.039. [PubMed] [CrossRef] [Google Scholar]
11. Рейнс Дж.Л., Джейн С.К. Окислительный стресс, передача сигналов инсулина и диабет. Свободный Радик. биол. Мед. 2011; 50: 567–575. doi: 10.1016/j.freeradbiomed.2010.12.006. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12. Senoner T., Dichtl W. Окислительный стресс при сердечно-сосудистых заболеваниях: все еще терапевтическая цель? Питательные вещества. 2019;11:2090. дои: 10.3390/nu11092090. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13. Уттара Б., Сингх А.В., Замбони П., Махаджан Р.Т. Окислительный стресс и нейродегенеративные заболевания: обзор вариантов антиоксидантной терапии выше и ниже по течению. [(по состоянию на 21 февраля 2021 г.)]; Доступно в Интернете: https://www.eurekaselect. com/68874/article [бесплатная статья PMC] [PubMed]
com/68874/article [бесплатная статья PMC] [PubMed]
14. Соса В., Молине Т., Сомоза Р., Пачуччи Р., Кондо Х., Л. Леонарт М. Е. Окислительный стресс и рак: обзор. Старение Res. 2013; 12:376–390. doi: 10.1016/j.arr.2012.10.004. [PubMed] [CrossRef] [Google Scholar]
15. Liguori I., Russo G., Curcio F., Bulli G., Aran L., Della-Morte D., Gargiulo G., Testa G., Cacciatore F. ., Бонадьюс Д. и др. Окислительный стресс, старение и болезни. [(по состоянию на 21 февраля 2021 г.)]; Доступно в Интернете: https://www.dovepress.com/oxidative-stress-aging-and-diseases-peer-reviewed-article-CIA
16. Бирбен Э., Сахинер У.М., Сакесен С., Эрзурум С., Калайчи О. Окислительный стресс и антиоксидантная защита. Всемирный орган аллергии. Дж. 2012; 5:9–19. doi: 10.1097/WOX.0b013e3182439613. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
17. Тан Б.Л., Норхайзан М.Е., Лью В.-П.-П., Сулейман Рахман Х. Антиоксидантный и окислительный стресс: взаимное влияние в возрасте. Сопутствующие заболевания. Фронт. Фармакол. 2018;9 doi: 10.3389/fphar.2018.01162. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Сопутствующие заболевания. Фронт. Фармакол. 2018;9 doi: 10.3389/fphar.2018.01162. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
18. Кринский Н.И., Ландрам Дж.Т., Боун Р.А. Биологические механизмы защитной роли лютеина и зеаксантина в глазах. Анну. Преподобный Нутр. 2003; 23: 171–201. doi: 10.1146/annurev.nutr.23.011702.073307. [PubMed] [CrossRef] [Google Scholar]
19. Лобо В., Патил А., Фатак А., Чандра Н. Свободные радикалы, антиоксиданты и функциональные продукты: влияние на здоровье человека. Фармакогн. 2010; 4:118–126. doi: 10.4103/0973-7847.70902. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
20. Бейкер Д.Д., Чу М., Оза У., Раджгархия В. Значение натуральных продуктов для будущих фармацевтических открытий. Нац. Произв. Отчет 2007; 24: 1225–1244. doi: 10.1039/b602241n. [PubMed] [CrossRef] [Google Scholar]
21. Аморати Р., Фоти М.С., Валгимигли Л. Антиоксидантная активность эфирных масел. Дж. Агрик. Пищевая хим. 2013;61:10835–10847. doi: 10.1021/jf403496k. [PubMed] [CrossRef] [Google Scholar]
doi: 10.1021/jf403496k. [PubMed] [CrossRef] [Google Scholar]
22. Совбхагья Х.Б., Читра В.Н. Ферментная экстракция ароматизаторов и красителей из растительного сырья. крит. Преподобный Food Sci. Нутр. 2010;50:146–161. дои: 10.1080/10408390802248775. [PubMed] [CrossRef] [Google Scholar]
23. Рахими Р., Гиази С., Азими Х., Фахари С., Абдоллахи М. Обзор травяных ингибиторов фосфодиэстеразы; Будущие перспективы новых лекарств. Цитокин. 2010;49:123–129. doi: 10.1016/j.cyto.2009.11.005. [PubMed] [CrossRef] [Google Scholar]
24. Ruberto G., Baratta M.T. Антиоксидантная активность отдельных компонентов эфирных масел в двух модельных системах липидов. Пищевая хим. 2000; 69: 167–174. doi: 10.1016/S0308-8146(99)00247-2. [Перекрестная ссылка] [Академия Google]
25. Аль-Марири А., Сафи М. Антибактериальная активность отдельных эфирных масел губоцветных (Lamiaceae) против Brucella Melitensis. Иран Дж. Мед. науч. 2013; 38:44–50. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Де Мартино Л., Де Фео В., Наззаро Ф. Химический состав и антимикробная и мутагенная активность семи эфирных масел губоцветных in vitro. Молекулы. 2009; 14:4213–4230. doi: 10.3390/молекулы14104213. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Де Мартино Л., Де Фео В., Наззаро Ф. Химический состав и антимикробная и мутагенная активность семи эфирных масел губоцветных in vitro. Молекулы. 2009; 14:4213–4230. doi: 10.3390/молекулы14104213. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
27. Царович-Станко К., Петек М., Грдиша М., Пинтар Й., Бедекович Д., М. Х.Ч., Сатовиц З. Лекарственные растения семейства губоцветных как функциональные пищевые продукты — обзор. Чешский J. Food Sci. 2016; 34: 377–390. doi: 10.17221/504/2015-CJFS. [CrossRef] [Google Scholar]
28. Карпинский Т.М. Эфирные масла растений семейства губоцветных как противогрибковые средства. Биомолекулы. 2020;10:103. doi: 10.3390/biom10010103. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
29. Пракаш О., Чандра М., Пант А.К., Рават Д.С. Глава 64 — Новый ( Mentha spicata L.) Масла. В: Preedy VR, редактор. Эфирные масла в консервации, вкусе и безопасности пищевых продуктов. Академическая пресса; Сан-Диего, Калифорния, США: 2016. стр. 561–572. [Google Scholar]
стр. 561–572. [Google Scholar]
30. Детар Э., Немет Э.З., Госстола Б., Демьян И., Плухар З. Влияние сорта и года роста на свойства эфирных масел лаванды (Lavandula Angustifolia Mill.) и лавандина (Lavandula x Intermedia Emeric Ex Loisel.) Biochem. Сист. Экол. 2020;90:104020. doi: 10.1016/j.bse.2020.104020. [Перекрестная ссылка] [Академия Google]
31. Рехман Р., Ханиф М.А., Муштак З., Аль-Сади А.М. Биосинтез эфирных масел в ароматических растениях: обзор. Food Rev. Int. 2016; 32:117–160. doi: 10.1080/87559129.2015.1057841. [CrossRef] [Google Scholar]
32. Гершензон Дж. Метаболические издержки накопления терпеноидов в высших растениях. Дж. Хим. Экол. 1994; 20:1281–1328. doi: 10.1007/BF02059810. [PubMed] [CrossRef] [Google Scholar]
33. Де Лизи А., Тедоне Л., Монтесано В., Сарли Г., Негро Д. Химическая характеристика популяций тимуса, происходящих из Южной Италии. Пищевая хим. 2011; 125:1284–1286. doi: 10.1016/j.foodchem.2010.10.011. [Перекрестная ссылка] [Академия Google]
34. Kowalski R., Wawrzykowski J. Анализ эфирных масел в высушенных материалах и гранулятах, полученных из Thymus vulgaris L., Salvia officinalis L., Mentha piperita L. и Chamomilla Flavor1 recutita . Дж. 2009; 24:31–35. doi: 10.1002/ffj.1914. [CrossRef] [Google Scholar]
Kowalski R., Wawrzykowski J. Анализ эфирных масел в высушенных материалах и гранулятах, полученных из Thymus vulgaris L., Salvia officinalis L., Mentha piperita L. и Chamomilla Flavor1 recutita . Дж. 2009; 24:31–35. doi: 10.1002/ffj.1914. [CrossRef] [Google Scholar]
35. Нуржинска-Вирдак Р., Завислак Г., Ковальски Р. Содержание и состав эфирного масла Origanum majorana L., выращенного в Польше, в зависимости от времени сбора и способа получения сырья. Подготовка. Дж. Эссент. Масляный медведь. Растения. 2015;18:1482–1489. doi: 10.1080/0972060X.2013.831569. [CrossRef] [Google Scholar]
36. Завислак Г. Урожайность и химический состав эфирного масла из Salvia officinalis L. на третий год выращивания. Герба Пол. 2014; 60 doi: 10.2478/hepo-2014-0012. [CrossRef] [Google Scholar]
37. Кот Б., Вежховска К., Пьехота М., Черневич П., Хшановски Г. Антимикробная активность пяти эфирных масел из Lamiaceae против полирезистентного Staphylococcus aureus .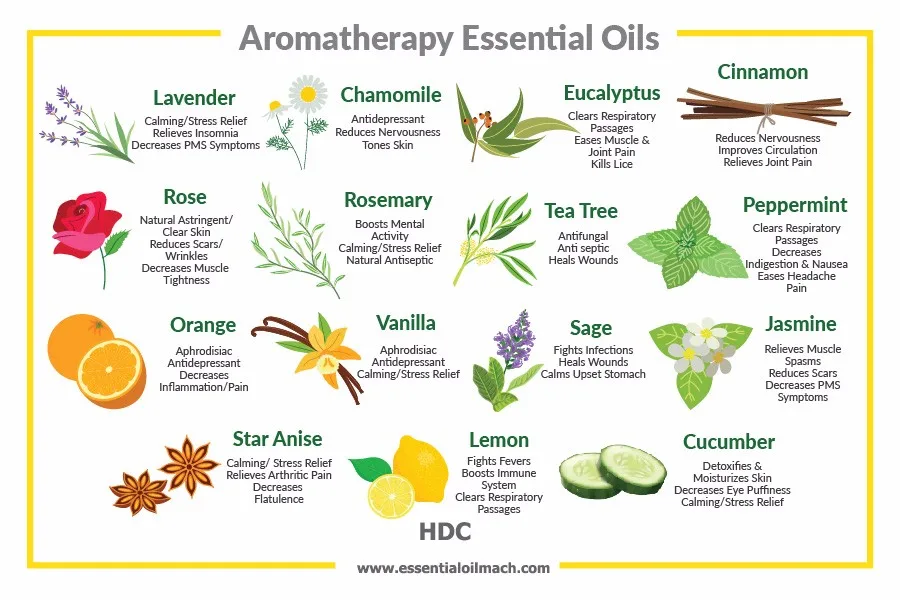 Нац. Произв. Рез. 2018: 1–5. дои: 10.1080/14786419.2018.1486314. [PubMed] [CrossRef] [Google Scholar]
Нац. Произв. Рез. 2018: 1–5. дои: 10.1080/14786419.2018.1486314. [PubMed] [CrossRef] [Google Scholar]
38. Адамс Р.П. Идентификация компонентов эфирных масел с помощью газовой хроматографии/масс-спектроскопии. 4-е изд. Очаровательная издательская корпорация; Кэрол Стрим, Иллинойс, США: 2007. [Google Scholar]
39. Boruga O., Jianu C., Misca C., Golet I., Gruia A., Horhat F. Эфирное масло Thymus Vulgaris: химический состав и антимикробная активность . Дж. Мед. Жизнь. 2014;7:56–60. [Бесплатная статья PMC] [PubMed] [Google Scholar]
40. Бай Т., Корона-Гловняк И., Ковальский Р., Мальм А. Химический состав и микробиологическая оценка эфирного масла из Hyssopus officinalis L. с белыми и розовыми цветками. Откройте хим. 2018;16:317–323. doi: 10.1515/chem-2018-0032. [CrossRef] [Google Scholar]
41. Wesolowska A., Jadczak D., Grzeszczuk M. Состав эфирного масла иссопа [ Hyssopus officinalis L.] Выращивается в Северо-Западной Польше. Герба Пол. 2010;56:57–65. [Google Scholar]
2010;56:57–65. [Google Scholar]
42. Михайлов-Крстев Т., Раднович Д., Китич Д., Златкович Б., Ристич М., Бранкович С. Химический состав и антимикробная активность эфирного масла Satureja Hortensis L. Открытая наука о жизни. 2009 г.;4:411–416. doi: 10.2478/s11535-009-0027-z. [CrossRef] [Google Scholar]
43. Chizzola R., Michitsch H., Franz C. Антиоксидантные свойства листьев тимьяна обыкновенного: сравнение различных экстрактов и хемотипов эфирных масел. Дж. Агрик. Пищевая хим. 2008; 56: 6897–6904. doi: 10.1021/jf800617g. [PubMed] [CrossRef] [Google Scholar]
44. Шалаби Э.А., Шанаб С.М.М. Антиоксидантные соединения, методы определения и механизм действия. фр. Дж. Фарм. Фармакол. 2013;7:528–539. дои: 10,5897/AJPP2013.3474. [CrossRef] [Google Scholar]
45. Schaich K.M., Tian X., Xie J. Reprint of «Hurdles and Pitfalls in Measuring Antioxidant Efficacy: A Critical Evaluation of ABTS, DPPH, and ORAC Assays» J. Funct. Еда. 2015; 18: 782–796. doi: 10.1016/j.jff. 2015.05.024. [CrossRef] [Google Scholar]
2015.05.024. [CrossRef] [Google Scholar]
46. Гил М.И., Томас-Барберан Ф.А., Хесс-Пирс Б., Холкрофт Д.М., Кадер А.А. Антиоксидантная активность гранатового сока и ее связь с фенольным составом и обработкой. Дж. Агрик. Пищевая хим. 2000;48:4581–4589. doi: 10.1021/jf000404a. [PubMed] [CrossRef] [Google Scholar]
47. Саламоне М., ДиЛабио Г.А., Биетти М. Реакции отрыва атома водорода от третичных аминов бензилоксильными и кумилоксильными радикалами: влияние структуры на определяющее скорость образование водород- Связанный предреакционный комплекс. Дж. Орг. хим. 2011;76:6264–6270. doi: 10.1021/jo201025j. [PubMed] [CrossRef] [Google Scholar]
48. Salamone M., Martella R., Bietti M. Извлечение водорода из циклических аминов с помощью кумилоксильных и бензилоксильных радикалов. Роль стереоэлектронных эффектов и водородной связи субстрат/радикал. Дж. Орг. хим. 2012;77:8556–8561. doi: 10.1021/jo3015352. [PubMed] [CrossRef] [Академия Google]
49. Се Дж., Шаич К.М. Повторная оценка анализа свободных радикалов 2,2-дифенил-1-пикрилгидразила (DPPH) на антиоксидантную активность. Дж. Агрик. Пищевая хим. 2014;62:4251–4260. doi: 10.1021/jf500180u. [PubMed] [CrossRef] [Google Scholar]
Дж. Агрик. Пищевая хим. 2014;62:4251–4260. doi: 10.1021/jf500180u. [PubMed] [CrossRef] [Google Scholar]
50. Дорман Х.Дж.Д., Пелтокето А., Хилтунен Р., Тикканен М.Дж. Характеристика антиоксидантных свойств дезодорированных водных экстрактов из выбранных трав Lamiaceae. Пищевая хим. 2003; 83: 255–262. doi: 10.1016/S0308-8146(03)00088-8. [Перекрестная ссылка] [Академия Google]
51. Мигри Х., Хайлауи Х., Акрут А., Наджаа Х., Неффати М. Антимикробная и антиоксидантная активность эфирного масла Artemisia Herba-Alba, выращиваемого в засушливой зоне Туниса. Ч. Р. Чим. 2010;13:380–386. doi: 10.1016/j.crci.2009.09.008. [CrossRef] [Google Scholar]
52. Formisano C., Mignola E., Rigano D., Senatore F., Bellone G., Bruno M., Rosselli S. Химический состав и антимикробная активность эфирного масла из надземных частей Micromeria Fruticulosa (Bertol.) Grande (Lamiaceae), дикорастущей в Южной Италии. Аромат Фрагр. Дж. 2007; 22:289–292. doi: 10.1002/ffj.1795. [CrossRef] [Google Scholar]
53. Brand-Williams W., Cuvelier M.E., Berset C. Использование свободнорадикального метода для оценки антиоксидантной активности. LWT Food Sci. Технол. 1995; 28:25–30. doi: 10.1016/S0023-6438(95)80008-5. [CrossRef] [Google Scholar]
Brand-Williams W., Cuvelier M.E., Berset C. Использование свободнорадикального метода для оценки антиоксидантной активности. LWT Food Sci. Технол. 1995; 28:25–30. doi: 10.1016/S0023-6438(95)80008-5. [CrossRef] [Google Scholar]
54. Re R., Pellegrini N., Proteggente A., Pannala A., Yang M., Rice-Evans C. Антиоксидантная активность с применением улучшенного анализа обесцвечивания катион-радикалов ABTS. Свободный Радик. биол. Мед. 1999; 26:1231–1237. дои: 10.1016/S0891-5849(98)00315-3. [PubMed] [CrossRef] [Google Scholar]
55. TIBCO Software Inc. Statistica (система программного обеспечения для анализа данных), версия 13.3. TIBCO Software Inc.; Пало-Альто, Калифорния, США: 2017. [Google Scholar]
56. Черневич П., Сытыкевич Х., Дурак Р., Боровяк-Собковяк Б., Хшановски Г. Роль фенольных соединений в антиоксидантных реакциях озимого тритикале на тлю и Атака Жуков. Завод Физиол. Биохим. 2017; 118: 529–540. doi: 10.1016/j.plaphy.2017.07.024. [PubMed] [CrossRef] [Академия Google]
57. Марино М., Берсани К., Коми Г. Измерения импеданса для изучения антимикробной активности эфирных масел губоцветных и сложноцветных. Междунар. Дж. Пищевая микробиология. 2001; 67: 187–195. doi: 10.1016/S0168-1605(01)00447-0. [PubMed] [CrossRef] [Google Scholar]
Марино М., Берсани К., Коми Г. Измерения импеданса для изучения антимикробной активности эфирных масел губоцветных и сложноцветных. Междунар. Дж. Пищевая микробиология. 2001; 67: 187–195. doi: 10.1016/S0168-1605(01)00447-0. [PubMed] [CrossRef] [Google Scholar]
58. Мэн А., Сантакроче Л., Джейкоб Р., Маре А., Мэн Л. Антимикробная активность шести эфирных масел против группы патогенов человека: сравнительное исследование. Возбудители. 2019;8:15. doi: 10.3390/pathogens8010015. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
59. Lee J.-H., Kim Y.-G., Lee J. Масло орегано, богатое карвакролом, и красное масло тимьяна, богатое тимолом, ингибируют образование биопленки и вирулентность уропатогенной кишечной палочки. Дж. Заявл. микробиол. 2017; 123:1420–1428. doi: 10.1111/jam.13602. [PubMed] [CrossRef] [Google Scholar]
60. Lambert RJW, Skandamis P.N., Coote P.J., Nychas G.-J.E. Исследование минимальной ингибирующей концентрации и механизма действия эфирного масла орегано, тимола и карвакрола.
